人教版九年级化学溶解度大表
初中化学溶解性表
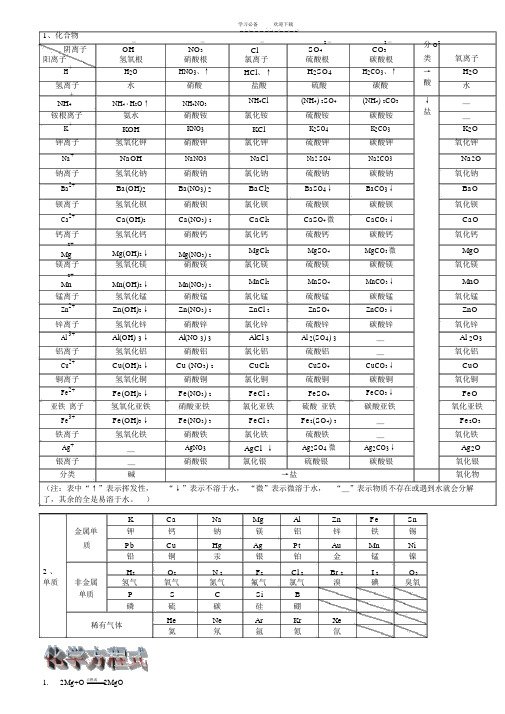
学习必备欢迎下载1、化合物阴离子--OH NO3阳离子氢氧根硝酸根H+H2O HNO3、↑氢离子水硝酸+NH4·H2O↑NH4NO3 NH4铵根离子氨水硝酸铵K+KOH KNO3钾离子氢氧化钾硝酸钾Na+NaOH NaNO3钠离子氢氧化钠硝酸钠Ba2+Ba(OH)2Ba(NO3) 2钡离子氢氧化钡硝酸钡Ca2+Ca(OH)2Ca(NO3) 2钙离子氢氧化钙硝酸钙2+Mg(OH)2↓Mg(NO3) 2 Mg镁离子氢氧化镁硝酸镁2+Mn(OH)2↓Mn(NO3) 2 Mn锰离子氢氧化锰硝酸锰Zn2+Zn(OH)2↓Zn(NO3) 2锌离子氢氧化锌硝酸锌Al 3+Al(OH) 3↓Al(NO 3) 3铝离子氢氧化铝硝酸铝Cu2+Cu(OH)2↓Cu (NO3) 2铜离子氢氧化铜硝酸铜Fe2+Fe(OH)2↓Fe(NO3) 2亚铁离子氢氧化亚铁硝酸亚铁Fe3+Fe(OH)3↓Fe(NO3) 3铁离子氢氧化铁硝酸铁Ag+_AgNO3Cl-2-2-SO4CO3氯离子硫酸根碳酸根HCl、↑H2SO4H2CO3、↑盐酸硫酸碳酸NH4Cl(NH4) 2SO4(NH4) 2CO3氯化铵硫酸铵碳酸铵KCl K2SO4K2CO3氯化钾硫酸钾碳酸钾NaCl Na2 SO4Na2CO3氯化钠硫酸钠碳酸钠BaCl2BaSO4↓BaCO3↓氯化钡硫酸钡碳酸钡CaCl2CaSO4微CaCO3↓氯化钙硫酸钙碳酸钙MgCl2MgSO4MgCO3微氯化镁硫酸镁碳酸镁MnCl2MnSO4MnCO3↓氯化锰硫酸锰碳酸锰ZnCl 2ZnSO4ZnCO3↓氯化锌硫酸锌碳酸锌AlCl 3Al 2(SO4) 3_氯化铝硫酸铝_CuCl2CuSO4CuCO3↓氯化铜硫酸铜碳酸铜FeCl 2FeSO4FeCO3↓氯化亚铁硫酸亚铁碳酸亚铁FeCl 3Fe2(SO4) 3_氯化铁硫酸铁_AgCl ↓Ag2SO4微Ag2CO3↓分O2-类氧离子→H2O酸水↓_盐_K2O氧化钾Na2O氧化钠BaO氧化钡CaO氧化钙MgO氧化镁MnO氧化锰ZnO氧化锌Al 2O3氧化铝CuO氧化铜FeO氧化亚铁Fe2O3氧化铁Ag2O银离子_硝酸银氯化银硫酸银碳酸银氧化银分类碱→盐氧化物(注:表中“↑”表示挥发性,“↓”表示不溶于水,“微”表示微溶于水,“_”表示物质不存在或遇到水就会分解了,其余的全是易溶于水。
溶解度表
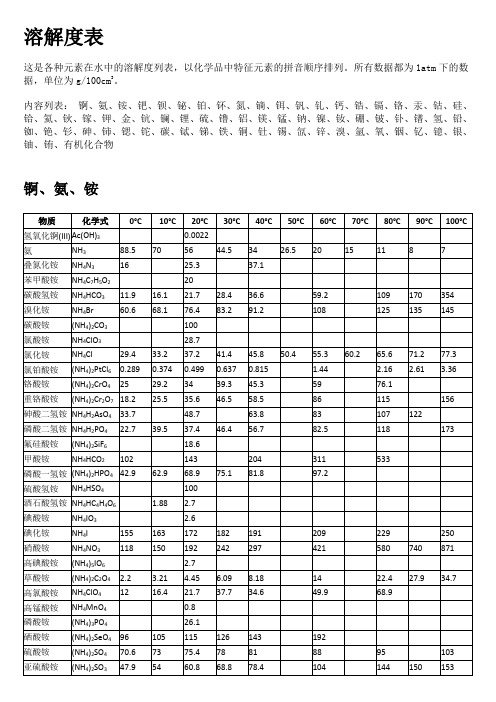
溶解度表
这是各种元素在水中的溶解度列表,以化学品中特征元素的拼音顺序排列。
所有数据都为1atm下的数据,单位为g/100cm3。
内容列表:锕、氨、铵、钯、钡、铋、铂、钚、氮、镝、铒、钒、钆、钙、锆、镉、铬、汞、钴、硅、铪、氦、钬、镓、钾、金、钪、镧、锂、硫、镥、铝、镁、锰、钠、镍、钕、硼、铍、钋、镨、氢、铅、铷、铯、钐、砷、铈、锶、铊、碳、铽、锑、铁、铜、钍、锡、氙、锌、溴、氩、氧、铟、钇、镱、银、铀、铕、有机化合物
锕、氨、铵
钯、钡、铋、铂、钚
氮、镝
铒
钒
钆、钙、锆、镉、铬、汞、钴、硅
铪、氦、钬
镓、钾、金
钪
镧、锂、硫、镥、铝
镁、锰
钠、镍、钕
硼、铍、钋、镨
氢、铅
铷
铯、钐、砷、铈、锶
铊、碳、铽、锑、铁、铜、钍
锡、氙、锌、溴
氩、氧、铟、钇、镱、银、铀、铕
有机化合物。
溶解度大表..doc

内容列表: 锕、氨、铵、钯、钡、铋、铂、钚、氮、镝、铒、钒、钆、钙、锆、镉、铬、 汞、钴、硅、铪、氦、钬、镓、钾、金、钪、镧、锂、硫、镥、铝、镁、锰、钠、镍、钕、 硼、铍、钋、镨、氢、铅、铷、铯、钐、砷、铈、锶、铊、碳、铽、锑、铁、铜、钍、锡、 氙、锌、溴、氩、氧、铟、钇、镱、银、铀、铕、有机化合物
18.6
甲酸 铵
NH4HCO2
102
143
204
311
533
磷酸 一氢
(NH4)2HPO
42.9
62.9
68.9
75.1 81.8
铵4
97.2
硫酸 氢铵
NH4HSO4
100
酒石 酸氢 NH4HC4H4O6 铵
1.88 2.7
碘酸 铵
NH4IO3
2.6
碘化 铵
NH4I
155 163 172 182 191
30°C
40°C
50 °C
60 °C
70 °C
80 °C
90 °C
100 °C
氢
氧
化 钯
Pd(OH)2
(II
)
4.106× 10-10
氢 氧 Pd(OH)4 化
5.247× 10-14
钯 (IV )
乙 酸 钡
Ba(C2H3O2) 58
2
.8
62
72
75 78.5
砷 酸 Ba3(AsO4)2 钡
2.586× 10-9
59
76.1
重铬 (NH4)2Cr2 酸铵 O7
18.2 25.5
溶解度大表.

酒石酸氢铵
NH4HC4H4O6
1.88
2.7
碘酸铵
NH4IO3
2.6
碘化铵
NH4I
155
163
172
182
191
209
229
250
硝酸铵
NH4NO3
118
150
192
242
297
421
580
740
871
高碘酸铵
(NH4)5IO6
2.7
草酸铵
(NH4)2C2O4
2.2
3.21
4.45
6.09
8.18
33.7
48.7
63.8
83
107
122
磷酸二氢铵
NH4H2PO4
22.7
39.5
37.4
46.4
56.7
82.5
118
173
氟硅酸铵
(NH4)2SiF6
18.6
甲酸铵
NH4HCO2
102
143
204
311
533
磷酸一氢铵
(NH4)2HPO4
42.9
62.9
68.9
75.1
81.8
97.2
硫酸氢铵
NH4HSO4
氟化钡
BaF2
0.159
0.16
0.162
氟硅酸钡
BaSiF6
2.8×10-2
甲酸钡
Ba(HCO2)2
26.2
28
31.9
34
38.6
44.2
47.6
51.3
磷酸氢钡
BaHPO4
1.3×10-2
化学人教版九年级下册部分酸碱盐溶解性表

附录1部分酸、碱和盐溶解性表教学目标1.认识酸、碱和盐在室温的溶解性规律2.掌握常见沉淀物质。
3.学会判断复分解反应的发生。
4.通过小组合作,培养学生合作探究精神,以及爱思考的学习精神。
教法实验探究法学法自主学习法教学重点认识酸、碱和盐在室温的溶解性规律教学难点学会判断复分解反应的发生课时安排 1课时实验准备:药品:以下溶液(CuSO4、CaCl2、Ca(OH)2、BaCl2、NaOH、Na2CO3NaCl、AgNO3、FeCl3)盐酸仪器:小试管数支、试管架教学过程温故知新:回顾复分解反应的发生条件是?有沉淀、气体或者水生成。
如何判断生成物中物质为不溶于水的沉淀呢?需要查阅课本114页部分酸、碱、盐的溶解性表,为了更好的判断,我们需要掌握各物质的溶解性规律。
接下来我们大家一起从今天的游戏中体会学习常见的酸碱盐溶解性。
【第一环节】一起玩游戏全体学生分为4个组,学生分配如下:每个同学都有一张属于自己的离子卡片,成为离子代言者。
接下来请各组离子闪亮登场。
游戏1 非常组合游戏规则:第一组和第二组、第一组和第四组的离子分别组合。
说出两种离子构成的物质名称和种类。
第一组和第二组的离子组合构成了常见的酸:例如硝酸、硫酸、盐酸、碳酸。
第一组和第四组的离子组合形成了水,是一种氧化物第三组和第二组、第三组和第四组离子分别组合。
说出两种离子构成的物质名称和种类。
第三组和第二组离子组合构成了盐,如氯化钠、硫酸钡、碳酸钙、硝酸银。
第三组和第四组离子组合构成了碱,如氢氧化钠、氢氧化钙、氢氧化铜、氢氧化铁。
熟悉了各类物质的构成,找出以下各组物质中的不同类物质A. H2O Fe(OH)3NO2B. Ca(OH)2Ba(OH)2Na2CO3C. HNO3 NaHCO3HCl D. BaSO4NaOH MgCl2游戏2 我为离子代言游戏规则:每位同学介绍自己离子的特点,并查阅课本114页附录一谈谈该离子在表中对应物质的溶解性。
(例如:氢离子的介绍,我代表氢离子,对应的物质都属于酸,都是可溶的。
人教版九年级化学溶解度大表

80°C
90°C
100 °C
乙
酸 钆 (II
Gd(C2H3O2) ·4H2O
I)
11.6
碳 酸 氢 Gd(HCO3)3 钆 (II
5.61
I)
溴
酸 钆 (II
Gd(BrO3)3 ·9H2O
50.2
I)
70. 1
95.6
126 166
氢
氧
化 钆
Gd(OH)3
(II
I)
1.882× 10-5
硫
酸 钆 Gd2(SO4)3 (II
0.2 44
0.255
0.2 0.2 64 65
0.2 44
0.234
0.20 5
钨 酸 CaWO4 钙
2.387× 10-3
氟 化 ZrF4 锆
1.32
硫 酸 锆
Zr(SO4)2 ·4H2O
52.5
砷 酸 Cd3(AsO4)2 镉
7.091× 10-6
苯 甲 Cd(C7H5O2) 酸2 镉
2.81
213
278
295
312
钙
霰 CaCO3-霰 石石
7.753× 10-4
方 解 石
CaCO3-方 解石
6.170× 10-4
氯
酸 Ca(ClO3)2
209
钙
铬 酸 CaCrO4 4.5 钙
2.25
1.8 1.4 39
0.8 3
磷
酸 Ca(H2PO4)2
1.8
二
氢 钙
氟 化 CaF2 钙
8.575 ×10-3
氟
硅 酸
CaSiF6
钙
0.518
[精修]初中常见物质溶解度表、初中常见物质化合价表
![[精修]初中常见物质溶解度表、初中常见物质化合价表](https://img.taocdn.com/s3/m/45a7ed2ea300a6c30d229f07.png)
OH-
溶、挥 溶 溶 溶 微 不 不 不 不 不 不 不 -
N03溶、挥
溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶
Cl溶、挥
溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 不
SO42溶 溶 溶 溶 不 微 溶 溶 溶 溶 溶 溶 溶 微
CO32溶、挥
溶 溶 溶 不 不 微 不 不 不 不
制作:化学备课组
初中常见物质化合价表
元素名称 元素符号 常见的化合价
钾
K
+1
钙
Ca
+2
钠
Na
+1
镁
Mg
+2
铝
Al
+3
锌
Zn
+2
铁
Fe
+2 +3
氢
H
+1
铜
Cu
+1 +2
汞
Hg
+1 +2
*银
Ag
+1
元素名称 元素符号 常见的化合价
*锂
Li
+1
碳
C
+2 +4
氮
N
-3 +2 +4 +5
氧
0
-2
*氟
F
-1
硅
Si
+4
磷
P
-3 +3 +5
硫
S
-2 +4 +6
初中溶解性表

NO3
SO4
CO3
PO4
H
hno3
硝酸
溶挥
HCl盐酸溶挥
H2SO4
硫酸溶
H2CO3
碳酸溶挥
H3PO4
磷酸溶
K
KOH
氢氧化钾溶
kno3硝酸钾溶
KCl
氯化钾溶
K2SO4
硫酸钾溶
K2CO3碳酸钾溶
KPO4
磷酸钾溶
Na
NaOH氢氧化钠溶
NaNO3
硝酸钠溶
KCl
氯化钠溶
Na2SO4硫酸钠
溶
Na2CO3
碳酸钠溶
碳酸亚铁
不
Fe3(PO4)2磷酸亚铁不
Fe
+3
Fe(OH)3氢氧化铁
不
Fe(NO3)3硝酸铁
溶
氯化铁溶
Fe2(SO4)3硫酸铁溶
Fe2(CO3)3碳酸铁不
FePO4
磷酸铁不
Cu
+2
Cu(OH)2
氢氧化铜不
CU(NO3)2硝酸铜
溶
CuCl2氯化铜
溶
CuSO4硫酸铜
溶
CuCO3碳酸铜不
CU3(PO4)2磷酸铜不
溶
AlCl3
氯化铝溶
Al2(SO4)3硫酸铝溶
A%磷酸铝不
Z+n
Zn(OH)2
氢氧化锌不
Zn(NO3)2硝酸锌
溶
ZnCl2
氯化锌溶
ZnSO4硫酸锌
溶
ZnCO3
碳酸锌不
Zn3(PO4)2磷酸锌不
Fe
+2
Fe(OH)2
氢氧化亚铁不
Fe(NO3)2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
134
151 166 178
草 酸 CaC2O4 钙
6.7×10
-4
高
氯 酸
Ca(ClO4)2
188
钙
高
锰 酸
Ca(MnO4)2
338
钙
磷 酸 Ca3(PO4)2 钙
2×10-3
硒 酸 钙
CaSeO4·2 H2O
9.73
9.7 7
9.22
8.7 7.1 94
硫 酸 钙
CaSO4·2H 2O
0.223
NH4Cl
29.4 33.2 37.2 41.4 45.8 50.4 55.3 60.2 65.6 71.2 77.3
氯铂 酸铵
(NH4)2PtC l6
0.28 9
0.37 4
0.499
0.63 7
0.81 5
1.44
2.16 2.61 3.36
铬酸 铵
(NH4)2CrO
4
25
29.2 34
39.3 45.3
0.2 44
0.255
0.2 0.2 64 65
0.2 44
0.234
0.20 5
钨 酸 CaWO4 钙
2.387× 10-3
氟 化 ZrF4 锆
1.32
硫 酸 锆
Zr(SO4)2 ·4H2O
52.5
砷 6
苯 甲 Cd(C7H5O2) 酸2 镉
2.81
209
229
250
硝酸 铵
NH4NO3
118 150 192 242 297
421
580 740 871
高碘 酸铵
(NH4)5IO6
2.7
草酸 铵
(NH4)2C2O4
2.2
3.21 4.45
6.09 8.18
14
22.4 27.9 34.7
高氯 酸铵
NH4ClO4
12
16.4 21.7 37.7 34.6
100 °C
一
氧 化
NO
氮
5.6×1 0-3
一 氧 化 N2O 二 氮
0.112
铬
酸 镝 (II
Dy2(CrO4)3·1 0H2O
I)
[编辑]铒
0.663
物质
化学 式
0° 10° CC
20°C
30° 40° 50° 60° 70° 80° 90° 100° CCCCCCC C
氢氧 化铒 Er(OH (III )3 )
653
27. 7
49. 9
67. 3
60.3
氢
氧 化
Bi(OH)3
铋
碘 化 BiI3 铋
磷 酸 BiPO4 铋
硫 化 Bi2S3 铋
氢
氧
化 铂
Pt(OH)2
(II
)
溴 化 铂 PtBr4 (IV )
氟 化 钚 PuF3 (II I)
2.868× 10-7
7.761× 10-4
1.096× 10-10
213
278
295
312
钙
霰 CaCO3-霰 石石
7.753× 10-4
方 解 石
CaCO3-方 解石
6.170× 10-4
氯
酸 Ca(ClO3)2
209
钙
铬 酸 CaCrO4 4.5 钙
2.25
1.8 1.4 39
0.8 3
磷
酸 Ca(H2PO4)2
1.8
二
氢 钙
氟 化 CaF2 钙
8.575 ×10-3
[编辑]钒
1.363×1 0-5
物 质
化 学 0°C 10°C 20°C 30°C 40°C 50°C 60°C 70°C 80°C 90°C 100°C 式
五
氧
化 V2O5
0.8
二
钒
[编辑]钆、钙、锆、镉、铬、汞、钴、硅
物 质
化学式
0°C
10 °C
20°C
30 °C
40 °C
50 °C
60 °C
70 °C
78.7
84.7
87. 92. 91
100
111
125
硝 酸 Cd(NO3)2 122 镉
136
150 194
310
713
草 酸 镉
CdC2O4.3H2 O
6.046× 10-3
高
氯 酸
Cd(ClO4)2
180 188 195 203
221
243
272
镉
磷 酸 Cd3(PO4)2 镉
6.235× 10-6
59
76.1
重铬 (NH4)2Cr2 酸铵 O7
18.2 25.5
35.6
46.5 58.5
86
115
156
砷酸 二氢 NH4H2AsO4 33.7 铵
48.7
63.8
83
107 122
磷酸
二氢 NH4H2PO4 22.7 39.5 37.4 46.4 56.7
82.5
118
173
铵
氟硅 (NH4)2SiF 酸铵 6
49.9
68.9
高锰 酸铵
NH4MnO4
0.8
磷酸 铵
(NH4)3PO4
26.1
硒酸 铵
(NH4)2SeO
4
96
105 115
126 143
192
硫酸 铵
(NH4)2SO4
70.6 73
75.4 78
81
88
95
103
亚硫 酸铵
(NH4)2SO3
47.9 54
60.8 68.8 78.4
104
144 150 153
[编辑]锕、氨、铵
物质
化学式
0°C
10° C
20°C
30° C
40° C
50° C
60° C
70° C
80° C
90° C
100° C
氢氧
化锕 (III
Ac(OH)3
)
0.002 2
氨 NH3
88.5 70 56 44.5 34 26.5 20 15 11 8 7
叠氮 化铵
NH4N3
16
25.3
37.1
苯甲 酸铵
NH4C7H5O2
20
碳酸 氢铵
NH4HCO3
11.9 16.1 21.7 28.4 36.6
59.2
109 170 354
溴化 铵
NH4Br
60.6 68.1 76.4 83.2 91.2
108
125 135 145
碳酸 铵
(NH4)2CO3
100
氯酸 铵
NH4ClO3
28.7
氯化 铵
23 9
336
416
钡
高
锰 酸
Ba(MnO4)2
钡
1.5×10-
2
焦
磷 酸
Ba2P2O7
钡
9×10-3
硒 酸 BaSeO4 钡
5×10-3
硫 酸 BaSO4 钡
2.448× 10-4
硫 化 BaS 钡
2. 88
4.8 9
7.86
10.4 14.9
砷 酸 BiAsO4 铋
7.298× 10-4
495
575
溶解度表以化学品中特征元素的拼音顺序排列。所有数据都为 1atm 下的数据,单 位为 g/100cm3。
内容列表: 锕、氨、铵、钯、钡、铋、铂、钚、氮、镝、铒、钒、钆、钙、锆、镉、铬、 汞、钴、硅、铪、氦、钬、镓、钾、金、钪、镧、锂、硫、镥、铝、镁、锰、钠、镍、钕、 硼、铍、钋、镨、氢、铅、铷、铯、钐、砷、铈、锶、铊、碳、铽、锑、铁、铜、钍、锡、 氙、锌、溴、氩、氧、铟、钇、镱、银、铀、铕、有机化合物
叠
氮 化
Ca(N3)2
45
钙
苯 甲 酸 钙
Ca(C7H5O2)
2
2.32
·3H2O
2.4 5
2.72
3.0 3.4 22
4.7 1
6.87 8.55 8.7
碳
酸 氢
Ca(HCO3)2 16.1
钙
16.6
17. 1
17. 5
17.9
18.4
溴
酸 Ca(BrO3)2
230
钙
溴
化 CaBr2
125
132 143
30°C
40°C
50 °C
60 °C
70 °C
80 °C
90 °C
100 °C
氢
氧
化 钯
Pd(OH)2
(II
)
4.106× 10-10
氢 氧 Pd(OH)4 化
5.247× 10-14
钯 (IV )
乙 酸 钡
Ba(C2H3O2) 58
2
.8
62
72
75 78.5
砷 酸 Ba3(AsO4)2 钡
2.586× 10-9
3.98
3.3 2.6
2.3 2
I)
氯 化 CaCl2 钙
59.5
64. 7
74.5
100 128
137
147 154 159
乙 Ca(C2H3O2)
酸2
37.4
钙 ·2H2O
36 34.7
33. 33. 82
32. 7
33.5 31.1 29.7
砷 酸 Ca3(AsO4)2 钙
