(完整版)初三化学有关溶液的相关计算题及标准答案
【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)

【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)一、选择题1.下列有关溶液的说法符合实际的是()A.将澄清的饱和石灰水加热,无白色浑浊出现B.20℃时氯化钠溶解度是36g,将30g氯化钠放入50g水中充分搅拌,得到80g溶液C.硫酸溶液中存在的阳离子全部是H+D.溶液一定是无色透明的液体【答案】C【解析】A、氢氧化钙的溶解度随温度的升高而减小,升温会使溶质析出出现浑浊,故此选项错误.B、由20℃时氯化钠溶解度可知,30g氯化钠不能都溶解在50g水中,只能溶解18g形成68g溶液,故此选项错误.C、硫酸在水中电离时会出现氢离子与硫酸根离子,除氢离子外再无其他带正电的离子,故此选项正确.D、溶液一定透明但不一定无色,例如硫酸铜的溶液是蓝色的,故此选项错误.故选C2.a,b两种物质的溶解度曲线如下图所示.下列说法不正确的是A.将℃时b的饱和溶液加水可变为不饱和溶液B.将℃时a的饱和溶液降温至℃,溶液质量不变C .℃时,两种物质的饱和溶液中溶质质量分数a bD.将℃时a、b的饱和溶液分别降温至℃,两溶液的溶质质量分数相等【答案】B【解析】试题分析:A、任何物质的饱和溶液加水都可变为不饱和溶液,故将t1℃时b的饱和溶液加水可变为不饱和溶液,正确,B、根据溶解度曲线,物质a的溶解度随温度的升高而增大,故将t2℃时a的饱和溶液降温至t1℃,有晶体析出,故溶液质量变小,错误,C、根据溶解度曲线,t2℃时,物质a的溶解度比物质b的溶解度要更大,故两种物质的饱和溶液中溶质质量分数a>b,正确,D,根据溶解度曲线,t1℃时, a、b种物质的溶解度大小关系是:a=b,将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等,正确,故选B考点:溶解度曲线的意义3.如图是甲乙两种物质的溶解度曲线,下列说法正确的是()A.甲的溶解度大于乙的溶解度B.t℃时,甲乙饱和溶液中溶质的质量分数相等C.升高温度能使接近饱和的甲溶液变为饱和溶液D.10℃时,分别用100g水配制甲乙的饱和溶液,所需甲的质量大于乙的质量【答案】B【解析】【分析】【详解】A、由两种物质的溶解度曲线可以看出,当0~t℃时,乙的溶解度大于甲的溶解度,选项A 错误;B、t℃时,二者的溶解度相等,饱和溶液中溶质的质量分数也相等,选项B正确;C、由甲物质的溶解度曲线可以看出,甲物质的溶解度随着温度的升高而增大,所以升高温度不能使接近饱和的甲溶液变为饱和溶液,选项C错误;D、过10℃作一条垂直于横坐标的垂线,看垂线与曲线的交点高低,从图象可以看出,此时乙的溶解度大于甲的溶解度,选项D错误。
【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)

【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)一、选择题1.NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法错误的是A.乙为NH4Cl B.t3应介于40℃﹣50℃C.55℃时,分别将两饱和溶液蒸发等质量的水,得到固体质量甲>乙 D.等质量的甲、乙饱和溶液从t3降温到t1,析出的晶体质量相等【答案】C【解析】A. 据溶解度表可知,NH4Cl的溶解度随温度升高而增大,故乙是NH4Cl,正确;B、40℃时,Na2SO4的溶解度是48.4g,50℃时,溶解度变小,是47.5g,且t3℃时两种物质的溶解度相等,故t3应介于40℃﹣50℃,正确;C、据溶解度表分析可知,55℃时,NH4Cl的溶解度大于Na2SO4的溶解度,故分别将两饱和溶液蒸发等质量的水,得到固体质量乙>甲,错误;D、两种物质的溶解度从t3降温到t1时,溶解度变化相同,故等质量的甲、乙饱和溶液从t3降温到t1,析出的晶体质量相等,正确。
故选C。
2.如图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法正确的是A.t1℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等B.由t2℃降温到t1℃,甲饱和溶液比乙饱和溶液析出晶体的质量多C.t2℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为90gD.t2℃时,用甲、乙配制等质量的饱和溶液,甲所需要水的质量比乙多【答案】A【解析】A、一定温度下,饱和溶液溶质的质量分数=s100g s×100%。
t1℃时,甲、乙的溶解度相等,甲、乙两种饱和溶液的溶质质量分数相等,正确;B、没有确定溶液的质量无法比较甲、乙饱和溶液析出晶体的质量,错误;C、t2℃时,甲的溶解度为50g,即100g水中最多溶解50g的甲,40g甲加入50g水中,充分溶解后只能溶解25g,所得的溶液质量为75g,错误;D、t2℃时,甲的溶解度大于乙的溶解度,配制等质量饱和溶液,甲所需要水的质量比乙少,错误。
【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)

化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)一、选择题1.下列有关溶液的说法符合实际的是()A.将澄清的饱和石灰水加热,无白色浑浊出现B.20℃时氯化钠溶解度是36g,将30g 氯化钠放入50g 水中充分搅拌,得到80g 溶液C.硫酸溶液中存在的阳离子全部是H+D.溶液一定是无色透明的液体【答案】C【解析】A、氢氧化钙的溶解度随温度的升高而减小,升温会使溶质析出出现浑浊,故此选项错误.B、由20℃时氯化钠溶解度可知,30g 氯化钠不能都溶解在50g 水中,只能溶解18g 形成68g 溶液,故此选项错误.C、硫酸在水中电离时会出现氢离子与硫酸根离子,除氢离子外再无其他带正电的离子,故此选项正确.D、溶液一定透明但不一定无色,例如硫酸铜的溶液是蓝色的,故此选项错误.故选C2.下图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法不正确的是A.10℃时,甲、乙两种物质的饱和溶液浓度相同B.保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液C.30℃时,将40g 甲物质加入50g 水中,充分溶解后溶液的质量为80gD.10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大【答案】D【解析】【分析】【详解】A、根据溶解度曲线,10℃时,甲、乙的溶解度都是20g,故甲、乙两种物质的饱和溶液浓度相同,选项A 正确;B、保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液,选项 B 正确;C、根据溶解度曲线,30℃时,甲物质的溶解度为60g,故将40g 甲物质加入到50g水中并充分搅拌,只能溶解30g,故充分溶解后溶液的质量为80g,选项C 正确;D、根据溶解度曲线,物质甲、乙的溶解度都随温度的升高而增大,故10℃时,将两种饱和溶液升温至30 ℃,都成为30℃时的不饱和溶液,但溶液中的溶质、溶剂质量都不变,故溶质质量分数也不变,选项D 错误。
故选D。
3.交点:两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的。
【化学】初三化学化学计算题专项训练100(附答案)

【化学】初三化学化学计算题专项训练100(附答案)一、中考化学计算题1.现将100 g溶质质量分数为9.8%的稀硫酸与一定质量的氯化钡溶液恰好完全反应后,过滤得到284.7 g滤液。
计算:(1)生成硫酸钡沉淀的质量。
(2)氯化钡溶液中溶质的质量分数。
【答案】(1)生成硫酸钡沉淀的质量为23.3 g。
(2)氯化钡溶液中溶质的质量分数为10%。
【解析】试题分析:解:设生成硫酸钡沉淀的质量为x,反应的氯化钡的质量为y。
H2SO4质量为:10 0g×9.8%=9.8 gBaCl2 + H2SO4 = BaSO4↓ + 2HCl208 98 233y9.8 g x233/98 =x/9.8x=23.3 g208/98 =y/9.8y=20.8 g(2)氯化钡溶液的质量为:284.7 g+23.3 g-100 g=208 g氯化钡溶液的溶质质量分数为:20.8 g/208 g×100%=10%考点:根据化学方程式的计算溶质的质量分数2.有一赤铁矿样品(主要成分为Fe2O3),某学校化学兴趣小组为了测得样品中氧化铁的质量分数,进行了如下探究:小明取10 g赤铁矿样品(杂质不溶于水和酸),不断加入稀盐酸到固体的质量不再减少,加入稀盐酸的量如图所示。
求:(1)赤铁矿中氧化铁的质量分数是________________。
(2)计算所使用的稀盐酸的溶质质量分数____________。
【答案】 80% 10%【解析】氧化铁和稀盐酸反应生成易溶于水的氯化铁和水,所以反应中固体质量减少,最终不溶的固体是杂质,所以氧化铁的质量为:10g-2g=8g,设所使用的稀盐酸的溶质质量为x,Fe2O3+6HCl=2FeCl3+3H2O160 2198g x160/8g=219/xx=10.95g所以所使用的稀盐酸的溶质质量分数为:10.95g÷109.5g×100%=10%;答:略点睛:方程式的计算,关键根据化学反应方程式找出相关物质的质量关系,利用反应中物质的质量比不变进行列比例计算,易错点是,由方程式求质量比算数错误,所以这一步要仔细检查。
【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)

【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)一、选择题1.甲、乙两种不含结晶水的固体的溶解度曲线如图所示.下列说法中正确的是A .t 3℃时,甲的饱和溶液溶质与溶液的质量比为1:2B .t 1℃时,甲的溶解度大于乙的溶解度C .t 2℃时,甲、乙溶液的溶质质量分数都为30%D .t 2℃时,质量相同的甲、乙饱和溶液分别升温至t 3℃,为达饱和状态,需加入甲的质量大于乙的质量【答案】D【解析】A 、t 3℃时,甲物质的溶解度是50g ,所以甲的饱和溶液溶质与溶液的质量比为1:3,故A 错误;B 、通过分析溶解度曲线可知,t 1℃时,甲的溶解度小于乙的溶解度,故B 错误;C 、t 2℃时,甲、乙物质的溶解度是30g ,所以甲、乙饱和溶液的溶质质量分数都为30130g g×100%=23.1%,故C 错误; D 、t 3℃时,甲物质的溶解度大于乙物质的溶解度,所以t 2℃时,质量相同的甲、乙饱和溶液分别升温至t 3℃,为达饱和状态,需加入甲的质量大于乙的质量,故D 正确。
点睛:根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
2.下图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法不正确的是A .10℃时,甲、乙两种物质的饱和溶液浓度相同B .保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液C.30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80gD.10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大【答案】D【解析】【分析】【详解】A、根据溶解度曲线,10℃时,甲、乙的溶解度都是20g,故甲、乙两种物质的饱和溶液浓度相同,选项A正确;B、保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液,选项B正确;C、根据溶解度曲线,30℃时,甲物质的溶解度为60g,故将40g甲物质加入到50g水中并充分搅拌,只能溶解30g,故充分溶解后溶液的质量为80g,选项C正确;D、根据溶解度曲线,物质甲、乙的溶解度都随温度的升高而增大,故10℃时,将两种饱和溶液升温至30℃,都成为30℃时的不饱和溶液,但溶液中的溶质、溶剂质量都不变,故溶质质量分数也不变,选项D错误。
九年级化学有关溶液的计算经典好题汇编(含答案)

九年级化学有关溶液的计算经典好题汇编(含答案)填空与计算题1. (·临沂)工业上常用红锌矿(主要含ZnO)和18%~25%的稀硫酸为原料制取硫酸锌。
(1) 硫酸锌中硫元素和氧元素的质量比是________。
(2) 100 g溶质质量分数为98%的浓硫酸配制成溶质质量分数为20%的稀硫酸,需要水的质量是________。
2. (·绥化)某化学兴趣小组同学在清理实验室时发现一瓶浓盐酸,标签如下。
2题根据标签计算。
(1) HCl中氢元素和氯元素的质量比为________(结果用最简整数比表示)。
(2) 这瓶盐酸的质量为________g。
(3) 现要配制3 800 g溶质质量分数为10%的稀盐酸,需要溶质质量分数为38%的浓盐酸的质量为________g,需要这种浓盐酸________瓶。
3. (·西宁)某兴趣小组用73 g溶质质量分数为20%的盐酸与足量锌粒反应,可制得氢气的质量是多少?4.(·庆阳)某化学兴趣小组同学为回收一块质量为40 g的铜锌合金中的铜,将该合金放入烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸100 g,烧杯内剩余固体27 g。
请完成下列计算:(1) 40 g铜锌合金中锌的质量是________g。
(2) 计算所用稀硫酸中溶质的质量分数。
5.(·郴州)某工厂现有废硫酸9.8 t(H2SO4的质量分数为10%),试计算:(1) 该9.8 t废硫酸中H2SO4的质量为________t。
(2) 如果用该9.8 t废硫酸去中和处理另一工厂的废碱液(主要成分为NaOH),恰好中和废碱液20 t,求废碱液中NaOH的质量分数。
(写出计算过程)6.(·德州)硫酸亚铁在工农业生产中有重要用途,也有较高的医用价值。
工业上用废铁屑和含硫酸的废液来制取硫酸亚铁,变废为宝。
现用5.6 t铁屑与100 t废液恰好完全反应(已知铁屑只和废液中的硫酸反应),请你计算:(1) 可生成硫酸亚铁的质量。
【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)
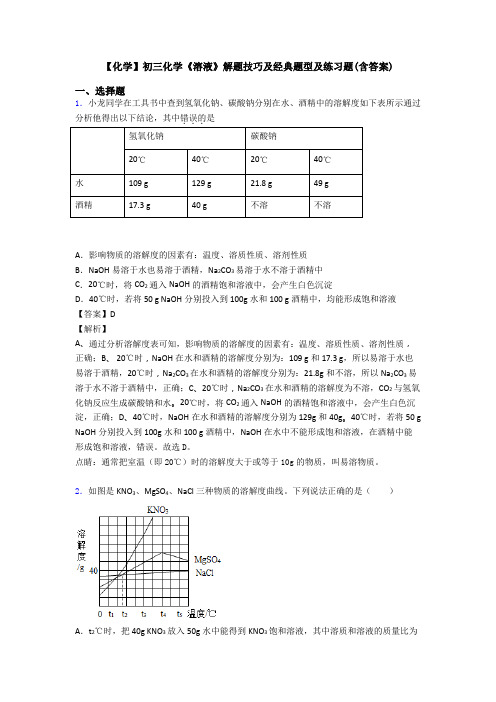
【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)一、选择题1.小龙同学在工具书中查到氢氧化钠、碳酸钠分别在水、酒精中的溶解度如下表所示通过分析他得出以下结论,其中错误的是氢氧化钠碳酸钠20℃40℃20℃40℃水109 g129 g21.8 g49 g酒精17.3 g40 g不溶不溶A.影响物质的溶解度的因素有:温度、溶质性质、溶剂性质B.NaOH易溶于水也易溶于酒精,Na2CO3 易溶于水不溶于酒精中C.20℃时,将CO2通入NaOH的酒精饱和溶液中,会产生白色沉淀D.40℃时,若将50 g NaOH分别投入到100g水和100 g酒精中,均能形成饱和溶液【答案】D【解析】A、通过分析溶解度表可知,影响物质的溶解度的因素有:温度、溶质性质、溶剂性质,正确;B、 20℃时,NaOH在水和酒精的溶解度分别为:109 g和17.3 g,所以易溶于水也易溶于酒精,20℃时,Na2CO3在水和酒精的溶解度分别为:21.8g和不溶,所以Na2CO3 易溶于水不溶于酒精中,正确;C、20℃时,Na2CO3在水和酒精的溶解度为不溶,CO2与氢氧化钠反应生成碳酸钠和水。
20℃时,将CO2通入NaOH的酒精饱和溶液中,会产生白色沉淀,正确;D、40℃时,NaOH在水和酒精的溶解度分别为129g和40g。
40℃时,若将50 g NaOH分别投入到100g水和100 g酒精中,NaOH在水中不能形成饱和溶液,在酒精中能形成饱和溶液,错误。
故选D。
点睛:通常把室温(即20℃)时的溶解度大于或等于10g的物质,叫易溶物质。
2.如图是KNO3、MgSO4、NaCl三种物质的溶解度曲线。
下列说法正确的是()A.t2℃时,把40g KNO3放入50g水中能得到KNO3饱和溶液,其中溶质和溶液的质量比为4:9B.t3℃时,图中三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数大小关系为NaCl>MgSO4>KNO3C.t4℃时,其他条件不变,把MgSO4饱和溶液升温到t5℃,在此操作过程中溶液里无明显现象D.KNO3中含有少量的NaCl杂质,采用蒸发结晶法提纯【答案】B【解析】【详解】A、t2℃时,硝酸钾的溶解度是40g,所以把40g KNO3放入50g水中能得到KNO3饱和溶液,其中溶质和溶液的质量比为20g:70g=2:7,故A错误;B、t1℃时,氯化钠的溶解度最大,硝酸钾的溶解度最小,所以t3℃时,图中三种物质的饱和溶液降温至t1℃,所得溶液中溶质质量分数大小关系为NaCl>MgSO4>KNO3,故B正确;C、t4℃时,其他条件不变,把MgSO4饱和溶液升温到t5℃,溶解度减小,在此操作过程中溶液里会析出晶体,故C错误;D、硝酸钾的溶解度受温度变化影响较大,所以KNO3中含有少量的NaCl杂质,采用降温结晶法提纯,故D错误。
【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)

【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)一、选择题1.A、B、C三种物质的溶解度曲线如图所示。
下列分析正确的是()A.t1℃时,甲、乙两种物质的饱和溶液中溶质的质量相等B.t2℃时,把30g甲放入50g水中能得到80g甲的饱和溶液C.将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是甲=乙D.将t2℃时的乙溶液降温到t1℃时,一定有晶体乙析出【答案】C【解析】【分析】甲、乙两种物质的溶解度随温度增加而增大,交点表示两种物质的溶解度相同。
【详解】A、t1℃时,甲、乙两种物质的溶解度相等,如果甲、乙两物质的饱和溶液的溶液质量相等,则所含的溶质质量相等,但是如果溶液质量不等,则溶质质量不等,故A不正确;B、t2℃时,甲的溶解度为50g,把30g甲放入50g水中能溶解的质量为100g,把30g甲放入50g水中能得到50g+25g=75g甲的饱和溶液,故B不正50g=25g50g确;C、将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃,溶液仍是饱和溶液,甲、乙的溶解度相同,所得溶液的溶质质量分数的大小关系是甲=乙,故C正确;D、t2℃时的乙溶液可能是饱和溶液,也可能不是饱和溶液,如果是饱和溶液,降温到t1℃时,才有晶体乙析出,故D不正确。
故选C。
【点睛】固体物质的溶解度是指在一定的温度下,100g溶剂中溶解溶质达到饱和状态时溶解的溶质的质量,故分析有无晶体析出,要看溶液是否饱和。
2.配制“一定溶质质量分数的氯化钠溶液”的实验常出现以下错误操作,其中不影响所配溶液浓度的是A.氯化钠放在右盘B.氯化钠洒出C.俯视读数D.转移溶液时溅出【答案】D【解析】【分析】【详解】A、氯化钠放在右盘且使用了游码,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小,故选项错误。
B、氯化钠洒出,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小,故选项错误。
C、用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,故选项错误。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1 / 6 初中化学有关溶液的溶质质量分数计算题 一、利用溶质质量分数的定义式及变形式的相关计算题 1.在农业上,有时用10%~20%的食盐溶液来选种。现配制15%的食盐溶液200kg需要食盐和水各多少千克? 2. 将60g20%的食盐溶液和30g5%的食盐溶液相混合,求所得混合溶液的溶质的质量分数 。 3. 向100g溶质的质量分数为10%的KNO3溶液中加入10g水后,所得溶液的溶质质量分数为 ;若加入10gKNO3后,溶质的质量分数为 4.200C时,将一溶质质量分数为20%的氯化钠溶液蒸干,得到20g固体,求该溶液质量 。 5.实验室要配制50g溶质质量分数为20%的硝酸钾溶液。现有25g溶质的质量分数为40%的硝酸钾溶液、20g溶质的质量分数为15%的硝酸钾溶液及足够多的硝酸钾晶体和蒸馏水,请选用上述药品,设计三种配制方案填如下表: 方案 配制时所需药品及用量
方案一 方案二 方案三 二、饱和溶液中溶质质量分数的相关计算 1.已知T 0C时,硝酸钠的溶解度为80g,求这温度时硝酸钠饱和溶液的溶质的质量分数。 2.某种物质的水溶液,加热蒸发掉10g水,冷却到20℃,有晶体析出。此时溶液中溶质的质量分数为26%,求20℃时该物质的溶解度。 3. 在60℃时, 50g水中最多能溶解55g硝酸钾把60℃时210g水中的硝酸钾饱和溶液蒸发掉50g水,再降到60℃,求析出晶体后溶液的溶质的质量分数。 三、溶液的稀释浓缩相关计算: (一)不涉及体积的计算: 1.将200g含水99%的NaOH溶液的含水量变为98%,应蒸发掉多少克水? 2.欲配制50g3%的氯化钠溶液,需6%的氯化钠溶液和水各多少克?, (二)涉及体积的计算 1.用98%的浓硫酸(密度为1.84g/cm3)配制成25%的稀硫酸500g,需浓硫酸和水多少毫升? 2.把5mL溶质的质量分数为62%的浓硝酸(密度为 l.38g/cm3)和20mL水混合,计算稀释后硝酸的溶质的质量分数。 3.用98%(密度为l.84g/cm3)的浓硫酸配制成1∶4的稀硫酸,求稀硫酸的溶质的质量分数。 四、有关溶液的标签型题的计算: 1.实验室有一瓶未开封的浓盐酸,部分标签如右图所示。 (1)这瓶浓盐酸中溶液的质量为多少克? (2)若用这瓶浓盐酸来配制200g溶质质量分数为10%的稀盐酸,需量取浓盐酸多少毫升,水多少毫升?
2. 某校化学实验室有一瓶标签残缺的过氧化氢溶液(如图所2 / 6
示)。该校化学课外兴趣小组的同学为了测定其中溶质的质量分数,他们取出该溶液34g,加入适量催化剂,待完全反应后,共收集到0.32g氧气。试计算该溶液中溶质的质量分数。 五、在溶液中进行化学反应的溶质质量分数的相关计算 (一)基本计算型 1. 6.5g锌跟100g稀硫酸恰好完全反应,求: (1)所用稀硫酸的溶质质量分数; (2)反应后溶液中所得溶液的质量分数 2. 12.5g石灰石与一定量的10%的稀盐酸恰好完全反应(杂质不参加反应),测得生成二氧化碳的质量为4.4g,求: (1)参加反应的稀盐酸质量为多少克? (2)生成物溶液中溶质质量分数为多少? (二)质量守恒型 1.称取12.5g石灰石(主要成分是CaCO3,杂质不参加反应)放人烧杯中,向其中加入50g稀盐酸,二者恰好完全反应。反应结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量,且气体的溶解忽略不计)。试计算 (1)生成二氧化碳的质量; (2)石灰石中CaCO3的质量分数; (3)盐酸中溶质的质量分数; (4)反应后溶液中溶质的质量分数。 2.实验室有一瓶硫酸废液,老师请小红同学设计方案测定该废液中硫酸的质量分数。小红同学先取一干净小烧杯,称其质量为18.2g,然后往其中倒入少量硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸去除铁锈)放入小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为43.9g。请回答下列问题: (1)写出上述反应的化学方程式 (2)反应产生的气体的质量 (3)计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数)。 (4)如果铁钉的铁锈未除净,对(3)计算结果的影响是 (选填“偏大”“偏小”“无影响”),原因是 (三)与体积有关的溶液计算题 1、为测定一瓶敞口放置的浓盐酸的溶质质量分数,某同学量取20mL(密度为1.1g/mL)的该盐酸与大理石充分反应,共用去含碳酸钙85%的大理石7.1g。 (1)浓盐酸需要密封保存的原因是 。 (2)计算该盐酸的溶质质量分数。 2、利用废铁屑与一定质量分数的稀硫酸反应制取硫酸亚铁。现有80g废铁屑与430mL20%的稀硫酸(密度为1.14g/cm3)恰好完全反应(假设废铁屑中除铁以外的物质不溶于水且不与稀硫酸反应)。我能完成下列计算(结果保留整数): (1)稀硫酸中溶质的质量; (2)废铁屑中铁的质量; (3)恰好完全反应时所得溶液中溶质的质量分数。 (四)图像型溶液计算题 1、 某研究性学习小组为测定铜锌合金中铜的质量分数,进行如下实验:取合金10g,向其中不断加入稀硫酸,产生的气体与所 加稀硫酸的质量关系如图所示。求: ①稀硫酸中溶质的质量分数。 ②合金中铜的质量分数。 3 / 6
③反应后,所得溶液中硫酸锌的质量分数 为多少? 2.某化学兴趣小组为了测定当地的石灰石(主要成分是CaCO3)的质量分数,他们做了如下实验:取24克样品放入烧杯中,向其中逐渐加入100克一定质量分数的稀盐酸(杂质不溶于水也不与酸反应),所用盐酸的质量分数与剩余固体的质量关系如图所示,请根据图中的数据进行计算: (1)石灰石样品中CaCO3的质量为 克. (2)24克石灰石样品与盐酸充分反应后最多产生二氧化碳的质量为 克. (3)求所用盐酸的溶质质量分数.(请根据化学方程式写出完整的计算步骤) (五)表格型计算题: 1、化学兴趣小组同学在综合实践活动中了解到,某石灰厂有一批石灰石原料,其中含有的杂质是二氧化硅 ( 二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应 )。为了测定该石灰石的纯度,兴趣小组的同学取用4g 这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸 40g 分 4 次加人,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体是质量见下表。 计算: (1) 该石灰石样品的纯度。 (2) 所用的稀盐酸中溶质的质量分数是多少? (3) 如果该石灰厂锻烧 50t 这种石灰百,最多可得到含杂质的生石灰多少吨? 2、某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 1 2 3 4 加入样品的质量/g 5 10 15 20 生成CO2的质量/g 1.54 3.08 4.4 m (1)哪几项反应中盐酸有剩余_________________________________; (2)上表中m的数值是__________________; (3)试计算这种石灰石矿中碳酸钙的质量分数。 (4)试计算稀盐酸中溶质的质量分数。 (5)试计算充分反应后溶液中溶质的质量分数。 3、沂蒙汽车配件厂新购进了一批黄铜(铜锌合金)。为了测定这批黄铜中铜的质量分数,化验人员将取来的样品先加工成粉末,然后利用该粉末与稀硫酸在烧杯内发生反应。在所进行的三次实验中,只有一次所取用的稀硫酸与黄铜样品是恰好完全反应的。有关实验数据记录如下: 实验次数 1 2 3 所取黄铜样品的质量(g) 10.0 10.0 20.0 加入稀硫酸的质量(g) 100.0 80.0 80.0 反应后烧杯内剩余物质的质量(g) 109.8 89.8 99.8 请分析实验数据,完成下列问题: (1)黄铜样品与稀硫酸恰好完全的是第几组? 4 / 6
(2)求该黄铜样品中铜的质量分数。 (3)求所用稀硫酸中溶质的质量分数。 (4)求恰好完全反应后溶液中溶质的质量分数。 4.某同学探究铁合金中铁的质量分数,先后进行了三次试验,实验数据如下表: 项目 第一次 第二次 第三次 所取合金质量(g) 20 20 40 所加稀硫酸的质量(g) 100 120 80 生成氢气的质量(g) 0.4 0.4 0.4 (1)上表中三次试验中,合金里的铁恰好完全反应时,消耗硫酸溶液的质量为 g; (2)铁合金中铁的质量分数为多少? (3)第三次实验所得溶液溶质质量分数为多少?(结果保留至0.1%) (六)在溶液中中进行的有关差量型计算题 在100g硫酸铜溶液中放入一块铁片,待硫酸铜全部反应后,固体物质的质量增加1g,则原硫酸铜溶液的溶质质量分数为多少? 初中化学有关溶液的溶质质量分数计算题答案: 一、定义式及变形式 1.氯化钠:30Kg 水:170Kg 2. 15% 3. 9.1% 18.2% 4. 100g 5. 10g硝酸钾固体和40g水; 25g40%硝酸钾溶液和25g水 ;20g15%的硝酸钾溶液7g硝酸钾和23g水 二、饱和溶液中溶质质量分数的相关计算 1.44.4% 2. 35.1g 3. 52.4% 三、溶液的稀释浓缩相关计算: (一)不涉及体积的计算: 1. 水100g 2. 6%的氯化钠溶液:25g 水:25g (二)涉及体积的计算 1.浓硫酸:69.3毫升 水:372.4毫升 2. 15.9% 3. 30.9% 四、有关溶液的标签型题的计算: 1.(1)590g (2)浓硫酸45.8毫升 水145.9毫升 2. 2%
五、在溶液中进行化学反应的溶质质量分数的相关计算 (一)基本计算型 1.稀硫酸溶质质量分数98% 所得溶液的质量分数:15.1% 解:设反应生成的H2质量为x,消耗的H2SO4质量为y,生成硫酸锌的质量为z Zn + H2SO4 = ZnSO4 + H2↑ 65 98 161 2 6.5g y Z X 65:2=6.5g:X X=0.2g 65:98=6.5g:y y=9.8g 65:161=6.5g:Z Z=16.1g 稀硫酸溶质质量分数:9.8g/100g*100%=9.8% 所得溶液的质量分数:16.1g /(6.5g+100g-0.2g)*100%=15.1% 答:稀硫酸溶质质量分数9.8% 所得溶液的质量分数15.1% 。 2. 稀盐酸质量73g 生成物溶液中溶质质量分数:14.1% (二)质量守恒型 1. (1)生成二氧化碳的质量:12.5g+50g-58.1g=4.4g(2)石灰石中CaCO3的质量分数:80% (3)盐酸中溶质的质量分数:14.6% (4)反应后溶液中溶质的质量分数:20% 设参加反应的碳酸钙质量为x,消耗的盐酸溶质质量为y,生成CaCl2的质量为z CaCO3+2HCl=CaCl2 + H2O + CO2↑ 100 73 111 44 X y z 4.4g 100:44=x:4.4g x=10g 73:44=y:4.4g y=7.3g 111:44 = z:4.4g z=11.1g 石灰石中CaCO3的质量分数:10g/12.5g*100%=80% 盐酸中溶质的质量分数:7.3g/50g*100%=14.6%
