一种新的有机光致变色及热致变色化合物间氨基苯甲酸缩3
有机光致变色材料汇总-共12页
有机光致变色材料有机光致变色现象发现至今已有100 多年的历史。
1867年Fritzsche 观察到黄色的并四苯在空气和光作用下的褪色现象,所生成的物质受热时重新生成并四苯,变回原来的颜色。
1876 年Meer 首先报道了二硝基甲烷的钾盐经光照发生颜色变化。
Markward 于1899 年研究了1 ,42二氢22 ,3 ,4 ,42四氯萘212酮在光作用下生的可逆的颜色变化行为,并把这种现象称为光色互变。
20 世纪50年代Hirshberg 陆续报道了关于螺吡蝻类化合物受光照变色,在另波长的光照射下或热的作用下又能恢复到原来颜色的现象,并把上述现象称为光致变色现象(photochromism) 。
20 世纪80 年代螺噁嗪类、苯并吡喃类抗疲劳性较好的化合物的发现使得光致变色化合物研究真正兴起。
目前,对光致变色化合物的研究主要集中在俘精酸酐、二芳基乙烯、螺吡喃、螺噁嗪以及相关的杂环化合物上,同时也在探索和发现新的光致变色体系。
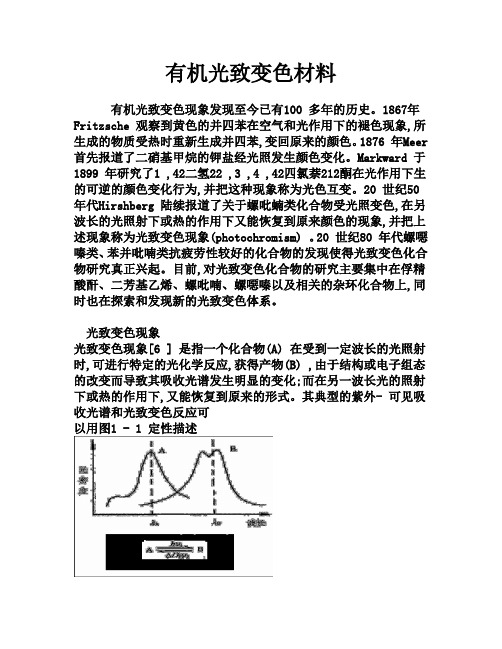
光致变色现象光致变色现象[6 ] 是指一个化合物(A) 在受到一定波长的光照射时,可进行特定的光化学反应,获得产物(B) ,由于结构或电子组态的改变而导致其吸收光谱发生明显的变化;而在另一波长光的照射下或热的作用下,又能恢复到原来的形式。
其典型的紫外- 可见吸收光谱和光致变色反应可以用图1 - 1 定性描述1 有机光致变色化合物的分类1.1 有机光致变色化合物有机光致变色材料种类繁多,反应机理也不尽相同,主要包括:①键的异裂,如螺吡喃、螺嗯嗪等;②键的均裂,如六苯基双咪唑等;③电子转移互变异构,如水杨醛缩苯胺类化合物等;④顺反异构,如周萘靛兰类染料、偶氮化合物等;⑤氧化还原反应,如稠环芳香化合物、噻嗪类等;⑥周环化反应,如俘精酸酐类、二芳基乙烯类等。
下面介绍几种主要的有机类光致变色化合物。
(1)螺吡喃类1. 1螺吡喃( spiropyran) 是最早进行研究且研究得广泛、比较深入的一类有机光致变色化合物。
光致变色与电致变色材料演示文稿

当前41页,共46页,星期一。
五.电致变色器件
电致变色器件(ECD)就是利用物质的 电致变色效应,以电致变色层为基础,
辅以其它相关层和结构而构成的器件。其具
有视角宽、驱动电压低、无功耗记忆等独特 优点 。有固态,半固态,液体三种形式。
目前,已经产业化的电致变色器件有以下几
如:二噻吩乙烯衍生物,以开环异构体为“关”的状态
,闭环异构体为“开”的状态,通过光子调控( 300nm光波和白光),可以可逆实现开环和关环异构 体间转换。
当前26页,共46页,星期一。
当前27页,共46页,星期一。
2.光信息存储
信息存储包括将信息在介质上“写入”和“读出
”这两个功能。同样让双稳态结构分别对应一种功 能,可以实现信息的写入与读出。
四.电致变色材料
电致变色(EO)是指在电场作用下发生稳 定,可逆的氧化还原反应,外观上表现为颜
色或透明度可逆变化的现象。具有电致变色 特性的材料称为电致变色材料,由电致变色 材料制备的器件称为电致变色器件。
电致变色的工作原理:
电致变色材料在外加电场作用下发生电化 学氧化还原反应,得失电子,使材料的颜色 发生变化。
当前14页,共46页,星期一。
稳定性-化合物a<化合物b<化合物c
当前15页,共46页,星期一。
2.3 二芳基乙烯类衍生物
(1)结构特征 二芳基乙烯类衍生物是在乙烯基的1, 2-位上连有芳香 环(Ar)的一类化合物,具有一个共轭6 ∏ 电子的己三烯 母体结构。如图3-7所示,其中芳基(Ar)可为苯环、 五元杂环或稠杂环等,取代基R可为氢原子、烷基、 脂环烃、芳香烃及卤原子等。尤其是,当芳香环(Ar
当前11页,共46页,星期一。
有机光致变色化合物光化学稳定性能研究

在光信息存储 、生物分子活性的光调控 、光计 算 以及防伪鉴伪方面的应用促进 了光致变色材料的 开发和研究 ,但真正具有实 际应用 前景 的光致 J 变色材料还需 以下条件 :1 闭环体和呈色体必须有 足够的热稳定性 ; 2闭环体和呈色体必须有足够长 的循环寿命 ,即高的耐疲劳性;3闭环体 和呈色体
Z HANG He g n ,Y ANG Z u —u,W E a -ig h or IB o qn
( eerhIs tt o hmi l n ier g S h o o hmi l n n ryE gn eig S u hn R sac ntue f e c g ei , c o l f e c dE e n ier , o t C ia i C aE n n C aa g n h
5 l
而且螺唣嗪的光分解产物不干扰螺噫嗪化合物的光 致变色性能,这一点在实际应用 中很重要。而改变 螺嘿嗪的环系或取代基能强烈地改变光稳定性,比 如用苯并嗯唑置换哚啉环时,至少降低光稳定性 1 0 0 倍。在螺嗯嗪的紫外光发色过程中,由于单线态氧
二芳基乙烯类化合物的光化学稳定性要优于螺 吡喃和螺嗯嗪。常见 的两个杂环二芳基 乙烯衍生物 l 一 2 甲基一一 ,2二(一 l 苯并噻吩 ) 全氟环戊烯和 2( ,一 一 12 二 甲基- 吲哚) 3( ,,一 3 一 一 一2 4 5三甲基一一 3噻吩 ) 马来酸 酐 ,在加热到 20 0 ℃也不会发生热致变色 ,并且光 致变色得 到 的闭环产 物在 8  ̄ 保存 3个 多月 , 0 C能
泛的体系之一 ,15 92年 Fs e 和 Hr br 发现 了 i hr c ihe s g 它 的光致 变色 性质 。
热致变色

由三芳甲烷类热致变色色素制成的热致变材料其基本成分有三种: 由三芳甲烷类热致变色色素制成的热致变材料其基本成分有三种: 1.热致变色色素,它决定了材料自身的颜色和变化后的颜色 热致变色色素, 热致变色色素 2.可提供质子的羟基类化合物,如双酚 ,它影响颜色的深度 可提供质子的羟基类化合物, 可提供质子的羟基类化合物 如双酚A, 3.具有极性的有机溶剂,如高级脂肪醇,它控制变色温度 具有极性的有机溶剂,如高级脂肪醇, 具有极性的有机溶剂 由各种醇控制的变色温度 高级醇 正辛醇 正癸醇 月桂醇 肉豆蔻纯 鲸蜡醇 硬脂醇 正二醇 变色温度/ 变色温度 0C -28~-21 -10~-3 7~14 26~31 35~40 39~45 48~57
上述材料主要用于电器设备发热部位的安全界限指示, 上述材料主要用于电器设备发热部位的安全界限指示,机械设备过热部件的 故障指示,转轴等摩擦部件发热的早期发现, 故障指示,转轴等摩擦部件发热的早期发现,加热器件表面温度分布的测定 等。
有机热致变色材料
有机热致变色材料因为其毒性较小且颜色变化明显,受到广泛关注。 有机热致变色材料因为其毒性较小且颜色变化明显,受到广泛关注。 液晶和 两大类。 实用化的有机热致变色材料主要有液晶 荧烷两大类 实用化的有机热致变色材料主要有液晶和荧烷两大类。热致变色液晶 是利用液晶的螺旋状体系受热发生螺距变化而引起颜色变化的性能, 是利用液晶的螺旋状体系受热发生螺距变化而引起颜色变化的性能, 颜色随温度变化产生连续性的改变。荧烷类有机热致变色色素, 颜色随温度变化产生连续性的改变。荧烷类有机热致变色色素,主要 用于热敏记录纸,防伪印刷品,工艺品,玩具等。 用于热敏记录纸,防伪印刷品,工艺品,玩具等。 具有热致变色性能的有机化合物主要有三芳甲烷类 荧烷类, 三芳甲烷类, 具有热致变色性能的有机化合物主要有三芳甲烷类,荧烷类,螺吡喃 席夫碱类,由于所处介质的酸碱变化而引起分子结构变化, 类,席夫碱类,由于所处介质的酸碱变化而引起分子结构变化,以致 发生了颜色变化,也有受热产生结构变化的。 发生了颜色变化,也有受热产生结构变化的。前三类化合物变色的化 学原理是分子体系中的一个碳原子由sp 杂化态转为sp 杂化态, 学原理是分子体系中的一个碳原子由 3杂化态转为 2杂化态,使原 先被隔离开的π体系转变为完整的大 体系, 体系转变为完整的大π体系 先被隔离开的 体系转变为完整的大 体系,进而使化合物从无色变 为有色。含邻羟基的席夫碱类热致变色物质, 为有色。含邻羟基的席夫碱类热致变色物质,其化学结构存在烯醇式 和酮式两个构造, 和酮式两个构造,它们的变色是由于这两个互变异构体之间存在一个 对温度敏感的平衡。 对温度敏感的平衡。
新型含氮杂环螺吡喃化合物的合成及性能研究

2010年第68卷化学学报V ol. 68, 2010第18期, 1895~1902 ACTA CHIMICA SINICA No. 18, 1895~1902* E-mail: pangmeili@; mengjiben@Received January 4, 2010; revised April 18, 2010; accepted May 17, 2010.国家自然科学基金(Nos. 20971071, 20602020)资助项目.1896化 学 学 报 V ol. 68, 2010一类令人感兴趣的光致变色化合物. 螺吡喃类光致变色材料具有灵敏度高、反应速度快、对紫外光敏感、电子转移速度快等特点, 在高技术领域, 如分子开关, 高密度数据存储等方面, 有着十分广泛的应用前景. 在紫外光照射下, 螺吡喃的螺C —O 键发生异裂, 生成在长波区域有吸收的开环部花菁化合物, 实现了光致变色, 其变色过程如Scheme 1所示.图式1 螺吡喃的光致变色机理Scheme 1 Photochromic mechanism of spiropyran由于螺吡喃染料自身结构的影响, 目前还存在耐疲劳度差, 室温下寿命比较短以及热稳定性较差的缺点, 使其应用受到一定的限制, 这些不足和螺吡喃分子的自身结构, 以及在各种分散介质中的聚集形态有着密不可分的关系. 为了改进螺吡喃化合物的热稳定性和耐疲劳度, 人们进行了不懈的探索. 研究表明, 取代基的性质和位置对吲哚啉螺吡喃的光致变色性能有着决定性的影响[7~9]. 对螺吡喃的修饰主要集中在以下几个方面: (1)变化螺环体系. 改变与吲哚或吡喃环稠合的芳环结构, 从而增大或减小共轭体系[8,10]; (2)在螺环上或吲哚啉的氮杂原子上导入适当的取代基[9]; (3)向目标分子中引入某些特定的杂环结构, 进而通过生成金属配合物等途径, 改善呈色体的稳定性. 为了提高开环呈色体的稳定性, 常在部花菁的氧原子附近引入适当的取代基, 使之形成分子内氢键, 或者选择适当的分散介质, 或者与金属离子鳌合等[11~14]. 在螺吡喃吲哚啉环的氮原子上引入合适的取代基, 合成相对方便, 可修饰性较好, 可根据合成的目的引入不同性质的取代基. 本文设计在螺吡喃的吲哚啉氮原子上, 通过短碳链引入含氮杂环, 合成一系列含氮杂环取代的螺吡喃化合物, 并研究其在不同溶剂和高分子膜中的光致变色性能, 拟合计算消色过程动力学常数, 研究其开环体的稳定性和耐疲劳度. 通过短碳链引入含氮杂环是基于以下两点考虑: (1)连接杂环的碳链较短, 引入含氮杂环后, 可以增加开环体自发热恢复到闭环体的位阻效应, 从而增加开环体的稳定性; (2)含氮杂环中的氮原子距离吲哚啉环上的氮原子和吡喃环上的氧原子距离较近, 开环异构之后可通过分子内氢键的生成或空间静电相互作用, 增加开环体的稳定性. 该修饰不仅可以影响到该类化合物的聚集状态, 增加开环体的稳定性, 而且有望提高其耐疲劳度, 为螺吡喃光致变色材料的结构与性能研究提供新思路. 目标化合物的合成路线如Scheme 2所示.图式2 化合物4a ~4f 的合成路线Scheme 2 Synthetic routes of compound 4a ~4f合成目标化合物之后, 我们对化合物4a ~4f 在不同有机溶剂及高分子膜中的光致变色性质进行研究, 对光照后在可见光区新出现的属于开环部花菁结构的吸收峰进行消色过程动力学拟合, 研究改变取代基团以后, 对光致变色性能产生的影响.1 实验部分1.1 试剂与仪器核磁共振谱仪: Bruker Avance 300型和Bruker Avance 400型; 质谱仪: 7070E-HE 型; 红外光谱仪: Nicolet 380 FT-IR 型; 元素分析仪: YANACO CHN CORDER MT-3型; 紫外-可见光谱仪: Varian Cary 300No. 18 庞美丽等:新型含氮杂环螺吡喃化合物的合成及性能研究1897conc. UV-Visible Spectrophotometer.除聚乙烯醇缩丁醛(PVB)为天津燕化新材料有限公司生产外, 其余试剂均为国产分析纯试剂, 用通用方法进行无水处理.1.2 1-(3-碘丙基)-2,3,3-三甲基吲哚啉碘化物1的合成参照文献[15]方法合成了1-(3-碘丙基)-2,3,3-三甲基吲哚啉碘化物1.1.3 1-(3-碘丙基)-3,3-二甲基-2-甲叉基吲哚啉(2)的制备参照文献[16]的方法合成了1-(3-碘丙基)-3,3-二甲基-2-甲叉基吲哚啉2.1.4 1'-(3-碘丙基)-3',3'-二甲基-6-硝基螺[吲哚啉-2,2' [2H]苯并吡喃](3)的合成在N2保护下, 向100 mL三口瓶中, 加入401 mg (2.4 mmol) 5-硝基水杨醛, 10 mL无水乙醇, 加热回流,回流状态下缓慢滴加654 mg (2 mmol)新制得的化合物2在10 mL无水乙醇中的溶液, 反应液由淡黄色变为红棕色. 滴毕, 继续回流4 h, 反应期间用TLC监测. 反应结束, 停止加热, 室温冷却, 有黄色固体析出, 抽滤, 固体用少量乙醇洗涤, 无水乙醇重结晶, 得淡黄色固体[17],产率为70%. m.p. 108~110 ℃.1H NMR (CDCl3, 300 MHz) δ: 1.17 (s, 3H, CH3), 1.28 (s, 3H, CH3), 2.02~2.27 (m, 2H, CH2), 3.12~3.35 (m, 4H, NCH2, ICH2), 5.87 (d,J=10.4 Hz, 1H, C H=CH), 6.61~8.03 (m, 8H, ArH, CH=C H); 13C NMR (CDCl3, 75 MHz) δ: 3.1, 16.0, 19.9, 32.6, 44.1, 52.6, 106.6, 106.8, 115.6, 118.5, 119.8, 121.8, 122.8, 126.0, 127.8, 128.5, 136.0, 141.2, 146.8, 159.4; IR (KBr) ν: 3054, 2963, 1652, 1515, 1482, 1283, 1088, 951, 748, 499 cm-1; MS (ESI) m/z: 477.1 [M+H]+.1.5 目标化合物4a~4f的合成在N2保护下, 向100 mL的圆底烧瓶中加入 3.5 mmol含氮杂环, 10 mL THF, 166 mg (1.2 mmol)充分研细的K2CO3, 加热回流, 在回流条件下缓慢滴加含有476 mg (1 mmol)化合物3的THF溶液(约10 mL). 滴毕,继续回流过夜, 用TLC监测, 待反应结束后, 冷却, 旋蒸除去THF, 水洗, 乙醚萃取, 收集醚层, 无水Na2SO4干燥, 脱溶后用二氯甲烷-石油醚(60~90 ℃)重结晶得目标化合物4a~4f.4a: 暗紫色固体, 产率61%. m.p. 160~162 ℃; 1H NMR (CDCl3, 300 MHz) δ: 1.17 (s, 3H, CH3), 1.28 (s, 3H, CH3), 1.41~1.45 (m, 2H, CH2), 1.50~1.59 (m, 4H, CH2), 1.69~1.88 (m, 2H, CH2), 2.27~2.31 (m, 6H, 3×NCH2), 3.12~3.28 (m, 2H, NCH2), 5.87 (d,J=10.4 Hz, 1H, C H=CH), 6.61~8.02 (m, 8H, ArH, CH=CH); 13C NMR (CDCl3, 75 MHz) δ: 19.8, 24.5, 26.0, 26.3, 45.7, 52.7, 54.6, 56.7, 106.8, 115.5, 118.6, 119.3, 121.6, 122.1, 122.7, 125.8, 127.7, 128.0, 135.9, 141.0, 147.1, 159.7, 162.4; IR (KBr) ν: 3066, 2929, 1611, 1337, 1275, 1092, 1017, 951, 752 cm-1; MS (ESI) m/z: 434.5 [M+H]+. Anal. calcd for C26H31N3O3: C 72.03, H 7.21, N 9.69; found C 72.08, H 7.23, N 9.65.4b: 黄绿色固体, 产率58.5%. m.p. 174~175 ℃; 1H NMR (CDCl3, 400 MHz) δ: 1.18 (s, 3H, CH3), 1.28 (s, 3H, CH3), 1.74~1.87 (m, 2H, CH2), 2.35~2.39 (m, 6H, 3×NCH2), 3.17~3.32 (m, 2H, NCH2), 3.62~3.77 (m, 4H, 2×OCH2), 5.86 (d, J=10.4 Hz, 1H, C H=CH), 6.62~8.03 (m, 8H, ArH, CH=C H); 13C NMR (CDCl3, 100 MHz) δ: 19.9, 25.9, 26.0, 41.5, 52.7, 53.7, 56.3, 67.0, 106.8, 115.6, 118.5, 119.4, 121.7, 122.1, 122.7, 125.9, 127.8, 128.1, 135.9, 140.9, 147.1, 159.7; IR (KBr) ν: 3068, 2954, 2806, 1609, 1336, 1117, 950, 805, 748 cm-1; MS (ESI) m/z: 435 [M+H]+. Anal. calcd for C25H29N3O4: C 68.95, H 6.71, N 9.65; found C 68.98, H 6.65, N 9.71.4c: 黄色固体, 产率39.5%. m.p. 158~160 ℃;1H NMR (CDCl3, 400 MHz) δ: 1.20 (s, 3H, CH3), 1.28 (s, 3H, CH3), 2.04~2.06 (m, 2H, CH2), 2.90~2.94 (m, 2H, ArCH2), 3.04~3.11 (m, 2H, NCH2), 3.23~3.38 (m, 4H, 2×NCH2), 5.85 (d, J=10.4 Hz, 1H, C H=CH), 6.39~8.02 (m, 12H, ArH, CH=C H); 13C NMR (CDCl3, 100 MHz): δ 19.8, 26.0, 26.6, 28.5, 41.4, 46.9, 52.6, 53.0, 106.7, 106.9, 115.5, 117.7, 118.4, 119.5, 121.7, 121.9, 122.7, 124.4, 125.8, 127.2, 127.8, 128.1, 130.0, 136.0, 140.9, 147.0, 152.4, 159.5; IR (KBr) ν: 3051, 2964, 2810, 1610, 1481, 1335, 1278, 954, 918, 808, 748 cm-1; MS (ESI) m/z: 468 [M+H]+. Anal. calcd for C29H29N3O3: C 74.50, H 6.25, N 8.99; found C 74.48, H 6.28, N 8.91.4d: 黄色固体, 产率30.6%. m.p. 124~125 ℃;1H NMR (CDCl3, 400 MHz) δ: 1.18~1.22 (m, 6H, CH3, CHCH3), 1.28 (s, 3H, CH3), 1.77~2.01 (m, 4H, ArCH2, C H2), 3.01~3.65 (m, 5H, 2×NCH2, NC H CH3), 5.86 (d, J=10.4 Hz, 1H, C H=CH), 6.25~8.04 (m, 12H, ArH, CH=C H); 13C NMR (CDCl3, 100 MHz) δ: 19.9, 21.5, 26.5, 26.8, 28.5, 41.4, 46.9, 52.6, 53.0, 106.7, 106.9, 115.5, 117.7, 118.4, 119.5, 121.7, 121.9, 122.7, 124.4, 125.8, 127.2, 127.8, 128.1, 131.2, 133.9, 137.0, 141.9, 147.0, 151.9, 159.8; IR (KBr): 3050, 2866, 1607, 1511, 1482, 1123, 807, 751 cm-1; MS (ESI) m/z: 481 [M]+. Anal. calcd for C30H31N3O3: C 74.82, H 6.49, N 8.73; found C 74.79,1898化学学报V ol. 68, 2010H 6.51, N 8.71.4e: 亮黄色固体, 产率36.6%. m.p. 177~179 ℃; 1H NMR (CDCl3, 400 MHz) δ: 1.18 (s, 3H, CH3), 1.28 (s, 3H, CH3), 1.93~1.94 (m, 2H, CH2), 2.55~2.88 (m, 6H, 2×NCH2, ArCH2), 3.19~3.36 (m, 2H, NCH2), 3.60 (m, 2H, NCH2), 5.88 (d, J=10.4 Hz, 1H, C H=CH), 6.63~8.03 (m, 12H, ArH,CH=C H); 13C NMR (CDCl3, 100 MHz) δ: 19.9, 26.1, 26.6, 29.2, 41.6, 50.9, 52.7, 55.7, 56.2, 106.8, 115.6, 118.6, 119.4, 121.7, 122.0, 122.7, 125.7, 125.9, 126.2, 126.5, 127.8, 128.1, 128.7, 134.3, 134.8, 135.9, 140.9, 147.2, 159.7, 162.3; IR (KBr) ν: 3050, 2963, 2905, 1613, 1484, 1333, 1175, 746 cm-1; MS (ESI) m/z: 481 [M]+. Anal. calcd for C30H31N3O3: C 74.82, H 6.49, N 8.73; found C 74.85, H 6.45, N 8.76.4f: 暗红色固体, 产率28.3%. m.p. 122~123 ℃; 1H NMR (CDCl3, 400 MHz) δ: 0.97 (t, J=7.1 Hz, 6H, 2×CH3), 1.18 (s, 3H, CH3), 1.28 (s, 3H, CH3), 1.65~1.85 (m, 2H, CH2), 2.41~2.51 (m, 6H, 3×NCH2), 3.13~3.26 (m, 2H, NCH2), 5.86 (d, J=10.4 Hz, 1H, C H=CH), 6.59~8.03 (m, 8H, ArH,CH=C H); 13C NMR (CDCl3, 100 MHz) δ: 19.9, 25.9, 26.0, 41.5, 52.7, 53.7, 56.3, 67.0, 106.8, 112.8, 115.6, 118.5, 119.4, 121.7, 122.1, 122.7, 125.9, 127.8, 128.1, 135.9, 140.9, 147.1, 159.7; IR (KBr) ν: 3059, 2967, 2806, 1608, 1487, 1379, 1180, 1105, 952, 744 cm-1; MS (ESI) m/z: 421 [M]+. Anal. calcd for C25H31N3O3: C 71.23, H 7.41, N 9.97; found C 71.20, H 7.43, N 9.95.2 结果与讨论2.1 螺吡喃化合物在溶液中的紫外光谱性质本文合成的螺吡喃类化合物4a~4f在乙醇、二氯甲烷和环己烷中都表现出良好的光致变色性能. 我们配制一定浓度的乙醇、二氯甲烷和环己烷溶液(约10-5 mol/L), 用365 nm的紫外灯照射1 min后, 测试其紫外可见光吸收, 得化合物光照后的最大吸收波长(表1).由表1的测试结果可知, 随着溶剂极性的增强, 螺吡喃类化合物4a~4f在紫外光谱中可见光区的吸收逐渐蓝移, 显示负的溶剂化显色效应. 溶剂化显色效应可能有两种机理: (1)从一种溶剂变成另一种溶剂时, 螺吡喃类化合物两种异构体在溶液中的平衡混合物的浓度发生变化, 该平衡位置主要与溶剂的极性、取代基的性质和溶液的浓度有关; (2)螺吡喃类化合物与不同极性的溶剂间的相互作用不同. 螺吡喃化合物4a~4f显示负的溶剂化显色效应, 主要可能是由于开环体的电子跃迁表1化合物3和4a~4f在不同溶液中的最大吸收波长Table 1The maximum absorption wavelength of 3 and 4a~4fin different mediaλmax /nmCompd.Ethanol DichloromethaneCyclohex-ane3 551 585 6184a 549 580 618 4b 548 582 617 4c 554 579 623 4d 556 580 622 4e 546 580 615 4f 547 578 618 与分子内给电子部位与受电子部位之间的电荷迁移有关. 激发态的偶极矩明显不同于基态的偶极矩, 当基态的极性大于激发态时, 随着溶剂极性的加大, 基态能量的降低大于激发态能量的降低, 因而基态与激发态之间的能量差别加大, 跃迁所需能量加大, 吸收光谱发生蓝移[18]; 反之, 随着溶剂极性的减小, 吸收光谱发生红移.另外极性溶剂有利于稳定极性较大的有色开环体, 而非极性溶剂又有利于稳定极性较小的无色闭环体, 因此大多数螺吡喃类化合物表现为负的溶剂显色效应.2.2 螺吡喃化合物在溶液中的动力学性质的研究以化合物4a为例研究该类化合物的光致变色动力学, 对螺吡喃化合物的热消色过程进行了记录, 并绘制了热消色A-λ曲线(图1)和热消色A-t曲线(图2)(均为375W高压汞灯照射1 min后测得).图1 化合物4a在二氯甲烷中的热消色曲线图Figure 1 Decay curves of compound 4a (c=2.0×10-5 mol/L)in dichloromethane我们对化合物4a的热消色过程进行了动力学拟合,拟合结果表明, 该类化合物在乙醇、二氯甲烷和环己烷中的热消色过程均基本符合单级指数方程[19].动力学方程: ln [(A t-A e)/(A o-A e)]=-kt在上式中A o为光化学反应初始的吸光度值, A t为tNo. 18 庞美丽等:新型含氮杂环螺吡喃化合物的合成及性能研究1899图2 4a在乙醇、二氯甲烷及环己烷中的A-t热消色曲线Figure 2 Decay rate of 4a in ethanol (a), dichloromethane (b) and cyclohexane (c)时刻的吸光度值, A e为光化学反应完全时的吸光度值, k 为热消色速率常数. 以ln [(A t-A e)/(A o-A e)]对t作图, 得到4a的动力学拟合曲线如下图(图3)所示.由图3可以看出, 化合物4a在溶液中的光致变色反应动力学基本符合直线关系, 说明此化合物在溶液中的光致变色反应更符合一级动力学反应方程. 根据一级动力学方程式, 计算得4a在乙醇溶液中的热消色速率常数k1=1.87×10-3 s-1; 在二氯甲烷溶液中的热消色速率常数k2=8.40×10-3 s-1; 在环己烷溶液中的热消色速率常数k3=7.13×10-3s-1. 比较4a在不同溶剂中的热消色速率常数: k2>k3>k1. 我们推测是由于乙醇的极性最图3 4a在乙醇、二氯甲烷及环己烷中的一级动力学拟合Figure 3 A kinetic fitting curve of 4a in ethanol (a), dichloro-methane (b), and in cyclohexane (c)大, 有利于开环体的稳定存在, 所以在乙醇中的热消色速率最慢. k3<k2的原因可能是环己烷中开环体部花菁结构存在着多种不同的聚集状态, 通过它们之间的相互转化, 使得消色速率常数小于在二氯甲烷中的消色速率常数[20]. 用同样的方法对化合物4e在环己烷中的消色曲线进行测量, 并用一级动力学方程对消色过程动力学进行拟合分析, 测得化合物4e在环己烷中的热消色速率常数k4=6.98×10-3 s-1. 我们推测k4<k3的原因是由于化合物4e中四氢异喹啉取代基的位阻效应要略大于4a中的哌啶取代基, 阻碍了开环体的闭环消色过程, 因而化合物4e开环体稳定性要略大于4a, 消色速率减慢.1900化 学 学 报 V ol. 68, 20102.3 螺吡喃化合物在PMMA 膜和PVB 膜中的紫外光谱性质2.3.1 螺吡喃化合物PMMA 膜和PVB 膜的制备在30 mL 三氯甲烷中溶解5 g PMMA, 加热搅拌至固体完全溶解成无色透明溶液. 然后再按一定百分比将制备好的螺吡喃光致变色化合物加入到PMMA 的三氯甲烷溶液中, 搅拌至完全混合均匀. 最后将含有光致变色化合物的溶液均匀铺在载玻片上, 置于暗处晾干, 待溶剂完全挥发后, 即制得螺吡喃光致变色PMMA 膜.螺吡喃化合物PVB 膜的制备同PMMA 膜的方法相同. 2.3.2 测试将制得的螺吡喃化合物PMMA 膜、PVB 膜于365 W 高压汞灯下2 cm 处照射1 min, 然后用紫外分光光度计测定其紫外吸收光谱. 化合物4a ~4f 在PMMA 膜和PVB 膜中的最大吸收波长如表2所示.表2 化合物4a ~4f 在PMMA 膜和PVB 膜中的最大吸收波长Table 2 Maximum absorption wavelength of 4a ~4f in PMMA and in PVB filmλmax /nmCompd. PMMA filmPVB film4a 582 583 4b 580 578 4c 580 582 4d 583 585 4e 582 5784f574 576 2.4 典型螺吡喃化合物4a 在PMMA 膜和PVB 膜中的热消色动力学研究以化合物4a 为代表, 对该类化合物在PMMA 膜和PVB 膜中的热消色A -t 曲线进行了测试, 并分别进行了一级动力学拟合和双指数衰减拟合, 拟合方程见下式:一级动力学拟合方程: ln [(A t -A e )/(A o -A e )]=-kt 双指数衰减拟合方程:A (t )=A 1exp(-t /t 1)+A 2exp(-t /t 2)+A 3化合物4a 在PMMA 膜(左)和PVB 膜(右)中的一级动力学拟合曲线如图4所示.化合物4a 在PMMA 膜和PVB 膜中的A -t 消色曲线以及双指数衰减拟合曲线如图5所示, 图中A 为测得的A -t 曲线, B 为双指数衰减拟合曲线.图4 4a 在PMMA 膜(a)和PVB 膜(b)中的一级动力学拟合曲线 Figure 4 Kinetic fitting curve of 4a in PMMA (a) and in PVB (b) 对热消色曲线进行动力学拟合后发现, 螺吡喃化合物在PMMA 膜和PVB 膜中的热消色过程偏离一级动力学规律, 更加符合双指数衰减规律, 有一个快过程和一个慢过程. 原因可能是, 螺吡喃化合物受紫外光激发后, 形成的呈色态PMC 是多种异构体平衡的混合物, 由于高分子介质空间位阻大, 使开环体的消色过程减缓, 相对稳定的异构体和相对不稳定的异构体的消色速度被区分开来, 所以呈现出一个快过程和一个慢过程[21]. 2.5 典型螺吡喃化合物4a 和4e 在环己烷中的耐疲劳度研究和螺噁嗪类化合物相比, 螺吡喃化合物本身结构在极性较大的溶剂中和在高分子介质中的消色过程较为缓慢. 我们将该类化合物配成一定浓度的环己烷溶液, 测定其耐疲劳度, 并与不连含氮杂环的母体化合物(1',3',3'-三甲基-6-硝基螺[吲哚啉-2,2'-[2H ]苯并吡喃], 化合物5)的耐疲劳度进行对比实验, 结果如图6所示.No. 18 庞美丽等:新型含氮杂环螺吡喃化合物的合成及性能研究1901图54a在PMMA膜(a)和PVB膜(b)中的A-t消色曲线以及双指数衰减拟合曲线Figure 5The experimental data (dots) of A-t achromatic curve according to 4a in PMMA (a) and in PVB (b)The inset is the experimental data (dots) of double-exponential decay fitting curve according to 4a其中, N为相对循环次数, 而不是真实的循环次数; A0为起始开环体在λmax处的光密度值; A为第N次光照时开环体在λmax处的光密度值; A/A0为归一化密度值.数据测试结果显示, 经过8次消色循环后, 母体5在环己烷中的光密度降为原来的26.2%, 而4a在环己烷中的光密度值降为原来的52.7%, 4e在环己烷中的光密度值降为原来的60.1%. 虽然耐疲劳度还不是很好, 但是在螺吡喃的吲哚啉氮上引入含氮杂环的新化合物, 其耐疲劳度比母体化合物5有了新的提高. 化合物4e与化合物4a相比较, 化合物4e中的四氢异喹啉取代基位阻略大于化合物4a中的哌啶取代基, 从测试结果上看, 位阻增加, 使化合物的耐疲劳度略有增加. 经过进一步的改进, 辅助添加一定的抗氧化剂和紫外吸收剂等改善其变色性能, 有望达到实用性的要求.3 结论在螺吡喃氮原子上, 通过短碳链引入含氮杂环结图6螺吡喃母体化合物5 (a)及含氮杂环取代螺吡喃化合物4a (b)和4e (c)在环己烷溶液(c=1.0×10-5 mol/L)中开环体的A/A0随循环次数N的变化Figure 6 Change of A/A0 with N (cycle times) in cyclohexane for compound 5 (a), 4a (b) and 4e (c)构, 合成得到一系列的含氮杂环取代的新化合物4a~4f, 对化合物的结构进行了充分的表征. 利用紫外光谱法测试了化合物在乙醇、二氯甲烷、环己烷溶液中, 以及PMMA和PVB膜中的光致变色性能, 结果表明, 化合物在各种介质中均具有良好的光致变色性能, 在溶液中体现负的显色效应. 测试并拟合分析了化合物在各种介质中的消色过程动力学, 结果表明化合物在不同溶剂中的消色速度为: 二氯甲烷>环己烷>乙醇; 在溶液中的消色过程基本符合一级动力学方程, 在高分子膜中的消色过程更符合双指数衰减动力学方程. 测试并比较了1902化学学报V ol. 68, 2010化合物4a, 4e和不带含氮杂环的母体螺吡喃化合物在环己烷中的耐疲劳度, 结果表明通过短碳链在螺吡喃吲哚啉环氮原子上引入含氮杂环结构, 化合物的耐疲劳度有了明显的提高.References1Kopelman, R. A.; Snyder, S. M.; Frank, N. L. J. Am. Chem.Soc. 2003, 125(45), 13684.2Feng, C.-G.; Wang, J.-Y. Chin. J. Org. Chem. 2006, 26(7), 1012 (in Chinese).(冯长根, 王建营, 有机化学, 2006, 26(7), 1012.)3Bertelson, R. C. Mol. Cryst. Liq. Cryst. 1994, 246, 1.4Kurihara, M.; Hirooka, A.; Kume, S.; Sugimoto, M.;Nishihara, H. J. Am. Chem. Soc. 2002, 124(30), 8800.5Hampp, N. Chem. Rev. 2000, 100, 1755.6Chen, Y.; Pang, M.-L.; Cheng, K.-G.; Wang, Y.; Han, J.;Meng, J.-B. Acta Chim. Sinica2008, 66(9), 1091 (in Chinese).(陈勇, 庞美丽, 程凯歌, 王英, 韩杰, 孟继本, 化学学报, 2008, 66(9), 1091.)7Görner, H. Phys. Chem. Chem. Phys. 2001, 3, 416.8Li, Y.; Xie, M.-G. Funct. Mater. 1998, 29(2), 113 (in Chinese).(李瑛, 谢明贵, 功能材料, 1998, 29(2), 113.)9Huang, Y.; Liu, Z.-J. J. Org. Chem. 1994, 14, 499 (in Chi-nese).(黄怡, 刘仲杰, 有机化学, 1994, 14, 499.) 10Querol, M.; Bozic, B.; Salluce, N.; Belser, P. Polyhedron 2003, 22, 655.11Sakata, T.; Yan, Y.-L.; Marriott, G. J. Org. Chem. 2005, 70, 2009.12Jukes, R. T. F.; Bozic, B.; Belser, P.; Cola, L. D.; Hartl, F.Inorg. Chem. 2006, 45, 8326.13Jukes, R. T. F.; Bozic, B.; Belser, P.; Cola, L. D.; Hartl, F.Inorg. Chem. 2009, 48, 1711.14Tu, C.-Q.; Louie, A. Y. Chem. Commun. 2007, 48, 1331.15Randall, M. H.; Buzby, P. R.; Erickson, T. J. US 6114350, 2000 [Chem. Abstr. 2000, 133, 224250].16Inouye, M.; Ueno, M.; Tsuchiya, K.; Nakayama, N.; Kon-ishi, T.; Kitao, T. J. Org. Chem. 1992, 57(20), 5377.17Vandewyer, P. H.; Smets, G. J. Polym. Sci. Part A-1, Po-lym. Chem.1970, 8(9), 2361.18Zhu, W.-H.; Yang, X.-Y.; Li, J. Organic Spectral Analysis and Performance, Chemical Industry Press, Beijing, 2007, pp. 5~6 (in Chinese).(朱为宏, 杨雪艳, 李晶, 有机波谱及性能分析法, 化学工业出版社, 北京, 2007, pp. 5~6.)19Li, Y.-T.; Zhou, J.-W.; Wang, Y.-Q.; Zhang, F.-S.; Song, X.-Q. J. Photochem. Photobiol. A: Chem. 1998, 113, 65.20Frade, V. H. J.; Gonçalves, M. S. T.; Coutinho, P. J. G.;Moura, J. C. V. P. J. Photochem. Photobiol. A: Chem. 2007, 185(2~3), 220.21Liu, P.; Ming, Y.-F.; Fan, M.-G. Sci. China, Ser. B1999, 29(4), 327 (in Chinese).(刘平, 明阳福, 樊美公, 中国科学B辑, 1999, 29(4), 327.)(A1001042 Qin, X.; Dong, H.)。
均苯三甲酸摩尔质量

均苯三甲酸:从分子到应用
均苯三甲酸是一种有机化合物,摩尔质量为480.4 g/mol,具有极高的透明度和热稳定性,被广泛应用于光电子、电子材料等领域。
本文将从分子结构、性质到应用领域等方面全面介绍均苯三甲酸。
1. 分子结构与性质
均苯三甲酸(tris(4-carboxyphenyl)amine,TCTPA)化学式为
C33H24O6,其分子结构由三个苯环通过中心的氨基相连,周围还固定了三个羧基。
这种分子链的结构保证了均苯三甲酸的优良物理化学性质,如高度透明性、电子亲和力强、空穴传输能力好等。
2. 应用领域
2.1 光电子材料
均苯三甲酸在光电子材料领域的应用广泛。
由于其具有优异的空穴传输性能,可作为半导体内部层的材料,提高光电子器件的效率。
使用均苯三甲酸作为阴离子,可以提高有机发光二极管的效率和稳定性。
2.2 光伏材料
均苯三甲酸可以作为一种新型的高分子无机杂化材料,应用于太阳能电池领域。
这种材料可以同时具有高的载流子传输速度和长的载流子寿命,从而提高太阳能电池的效率和稳定性。
2.3 光致变色材料
均苯三甲酸还可以作为一种优秀的光致变色材料,其化学结构使其能够通过外界光的激发发生电荷转移,产生不同颜色的发光,可应用于智能窗等领域。
3. 总结
均苯三甲酸具有优良物理化学性质,应用广泛。
在光电子、电子材料等领域得到了广泛应用。
未来,随着对均苯三甲酸的深入研究,相信将会有更多优秀的应用出现。
热致变色色素 电致变色色素
由水杨醛类化合物与吲哚啉类化合物在极性溶剂,如醇类 溶剂中加热回流,经缩合反应得到各种螺吡喃类热致变色 化合物,反应机理(P241) 利用上述方法,还可以得到一系列各种色谱的螺吡喃类化 合物,如:(P243)
H3C
CH3
H3C
CH3
N O CH3 O 2N
N O CH3 NO2
4-硝 基 -1, 3, 3-三 甲 基 螺 黄 棕 色
H N H OCH3
5.2.2.5 吩噁嗪和吩噻嗪类色素
这类化合物实际上也是酸碱变色的色素。(P238)
CH3N
S
2
N C O
NCH3
2
CH3N
S
2
N H C O
N CH3
+
5.2.3 热致变色色素的合成
5.2.3.1 三芳甲烷类热致变色化合物的合成 (1)结晶紫内酯(CVL)的合成(P239)
5.2.2有机热致变色材料
某些荧烷类,三芳甲烷类,螺吡喃类等有机化合 物也具有热致变现象,它们的色变温度比较宽 (-100—100度),颜色变化丰富。 已经实用化的有机热致变色材料主要有液晶和荧 烷两大类 5.2.2.1 三芳甲烷类热致变色色素 最早使用的热致变色色素是结晶紫内酯,简称 CVL,结构式如下(P235)
+
NH
O O
Cl NH COO-
5.2.3.3 螺吡喃类热致变色化合物的合成
螺吡喃类热致变色化合物的一般合成步骤是先合成中间体 水杨醛类化合物,然后再与吲哚啉类化合物缩合得到各种 目标产物。中间体水杨醛类化合物可以有酚类化合物用氯 仿来甲酰化合成,也可以由六亚甲基四胺和多聚甲醛来甲 酰化合成,这两种甲酰化方法机理如下: 1)氯仿法(P241) 2)六亚甲基四胺-多聚甲醛法(P241)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第 1 期 1
发 光 学 报
CH I NES OURNAL OF L EJ UM I NES CENCE
Vo 2 N . 1 L3 o 1
No v.,2 011
21 0 1年 1 月 1
文 章 编 号 :10 - 3 ( 0 1 1—150 0 07 2 2 1 ) 11 1 -5 0
E— i :lg a g u 1 2 3 ma l iu n h a 9 9 9@ 1 3 c l 6 . oa
:通讯联系人 ; - al igh le eu cl E m i ng @gt.d .r :d i
发
光
学
报
第3 2卷
3 5二氯水杨醛( ,一 化学纯 , 江阴新星化工厂) , 间氨基 苯 甲酸 ( 析纯 , 海 晶纯 试 剂有 限公 分 上 司) 乙醇 、 , 甲醇、 乙醚和 N, - 甲基 甲酰胺 ( N二 分
目 前有机光致变色化合物的类型主要是质子 转移 互变 异构 型 _ ( 杨 醛缩 苯 胺 类 希夫 碱 化 合 6 水 物)顺一 、 反异构 型l ( 氮苯类化合物 ) 键 的异 偶 、 裂型_ ( 8 螺吡喃 、 螺嗯嗪类化合物 ) 周 环反 应体 、
转蒸发器 ( 上海亚荣生化仪器厂 ) D F62 , Z - 0型真 0 空干燥箱( 上海恒科学仪器有限公司) 。
关 键 词: 希夫碱 ; 光致变色 ; 热致 变色 P S: 2 5 . i AC 3 .0 F P C: 2 0 AC 35 F 文献标识码 : A
中图分类号 : 42 3 0 8 .
DOI 0. 7 8 fx 2 1 2 1 1 1 :1 3 8 / g b 01 3 1 . 1 5
一
种新 的有机光致变色 及热致变色化合物 问氨基 苯 甲酸缩 35二氯水杨醛希夫碱 ,一
李光华 ,丁国华
( 桂林理工大学化学与生物工程学院 有色金属及材料加工新技术教育部重点实验室 , 广西 桂林 5 10 ) 4 04
摘要 : 制备了间氨基苯甲酸缩 35-氯水杨醛希夫碱, ,-" 利用红外(R 、 I )核磁(H N R 、 M )质谱( s 和元素分 M)
2 实
验
2 1 实验仪 器与试 剂 .
P 20 朊 素分析仪 ( E40 美国 P E公 司, 测定 c 、 H、 )NC C T47型红外光谱仪 ( N ,IO E 0 美国, B 压 Kr
片法 ) P r a o dT / T —p c u n T R ,yi D i n G D A Set m O eF I s m r
物 中研究最广泛 的主要是二芳乙烯 、 俘精酸酐 、 螺 吡喃 、 偶氮苯、 螺嗯嗪等几类化合物 , 对有机热致
变 色化 合物 的报 道还 相 对较 少
一
。本 文合 成 了
种新 的 同时具 有光 致变 色和 热致变 色性 能 的化
合物间氨基苯 甲酸缩 3 5二氯水杨醛希夫碱 , ,一 有
对光或热的特殊变色效应使这方面的研究一度成为 热点。自 从发现光( 致变色现象以后 , 热) 人们已寻 找或合成出许 多不 同类 型的此类物质 。有些物 质 固
态下就具有很强 的光 ( ) 热 致变 色性质 , 的则必 须 有 在合适 的溶剂 中才呈现 出光 ( 致变色 。 热)
热重仪 ( 国 P 美 E公 司 , 温 速率 1 / i, , 升 0K r n N 气 a
收稿 日期 : 0 10 ;修订 1期 : 0 10 -3 2 1_ 4 3 2 1 -60 基金项 目: 广西科学研究 与技术 开发计划项 目( 桂科能 04 0 33 ) 广西教育厅科研项 目( 6 0 3 资助 82 0 - ; 8 0 70 ) 作者简介 : 李光华( 94一) 男 , 18 , 吉林 四平人 , 主要从事 功能有机材料 的研究 。
氛)u 一 5 型紫外光谱仪( 本岛津) I - ,V2 0 4 日 , 5 5 5型 荧光光谱仪( 美国 P 公司)A A C V 0 核磁 E ,V N EA 50
共 振谱仪 ( 士布鲁克 )B U E T质谱仪 ( 瑞 ,R K RHC 美 国布鲁克 道 尔顿 公 司 ) D - I 热式 恒 温加 热 , F1 S急 0 磁 力搅拌器 ( 河南 予华仪 器有 限公 司 )R 5.9旋 ,E 29
析对化合物结构进行 了表征。研究 了它的荧光性质和热稳定性 。对化 合物 的紫外可见 ( V Vs 光谱 和荧光 u - i) 光谱 的研究 表明 , 该化合物在 D F溶液中具有较好 的光致 变色和 热致 变色性 能。化合物 的吸光度值 和最大 M 发射波 长与时间或温度呈线性关系 , 进一步说明该化合物是性能 良好 的光致变 色及 热致 变色材料 。
望 应用 到光 ( ) 热 致变 色器 件 当中 。
相材料、 伪装及 防伪材料及装饰材料等_ l 刮领域都
有广 阔的应用 前景 。光 致变 色 现象 最早 发 现在 1 9 世纪 的 , 尤 其 是含 有 F¨ 或 Mo 的氧 化 物 的 一些 物 质 。 随 e 着 时代 的变 迁 , 们 不 仅 发 现 了更 多 的 光致 变 色 人 化 合物 , 而且 还 发 现 了热 致 变 色 现 象 。这些 物 质
1 引
言
系( 俘精酸酐类 , 苯并二甲基二氢芘 , 二芳基 乙烯
类 化合 物 ) 。 目前 , 众 多 有 机 光 致 变 色 化 合 等 在
光 ( ) 变 色 材 料 随 着 各 种 光 电技 术 的 发 热 致 展, 正不 断渗 透到人类社 会生活 的各个 领域 。有机 光 ( ) 变 色 材料 是 一 种新 型功 能 性 材料 , 分 热 致 在 子 开关 、 学记忆 、 光计 、 子传感 器 、 光 露 分 纺织 纤维 、 非 线性光学 、 录和显示 材料 、 记 防护材料 、 自显 影照
