8第八章立体化学(重点难点)
《高分子化学增强版》第八章 立体化学

S
口诀:竖顺 ,横顺S 口诀:竖顺R,横顺
S
S
S
最小基团在上或下即竖向位置为“ 最小基团在上或下即竖向位置为“竖”,剩余基团从大到小排列 为顺时针方向的,就是 构型 口诀中任改两字,仍旧正确。 构型, 为顺时针方向的,就是R构型,口诀中任改两字,仍旧正确。
中
COOH CH3 OH 大
小
视线
视线
中 COOH 小 H3C OH 大
S-乳酸 乳酸
H
H
R-乳酸 乳酸
3) 构型的 R、S 表示方法 、 手性碳的构型:与手性碳相连的四个不同基团的空间排列, 手性碳的构型 与手性碳相连的四个不同基团的空间排列, 与手性碳相连的四个不同基团的空间排列 将最小基团放在离眼睛最远的地方,从大到小, 将最小基团放在离眼睛最远的地方,从大到小,顺R逆S。 逆 。
乳酸的分子模型图
两个乳酸模型不能叠合
• 乳酸的两个模型的关系象左手和右手一样 它们 乳酸的两个模型的关系象左手和右手一样,它们
不能相互叠合,但却互为镜像. 不能相互叠合 但却互为镜像 但却互为镜像
•在立体化学中 不能与镜象叠合的分子叫手性分子 而能叠 在立体化学中,不能与镜象叠合的分子叫手性分子,而能叠 在立体化学中 不能与镜象叠合的分子叫手性分子 合的叫非手性分子.乳酸是手性分子 乳酸是手性分子。 合的叫非手性分子 乳酸是手性分子。
分子的手性和对称因素(了解) 一. 分子的手性和对称因素(了解) 1. 手性 手性(Chirality) 2. 对称因素 1) 平面对称因素 σ) 平面对称因素(σ
chapt 08 立体化学[1]
![chapt 08 立体化学[1]](https://img.taocdn.com/s3/m/193f970eeff9aef8941e0615.png)
四、 e.e.值(对映体过量值):合成中研究重点
[ R] [S ] %e.e. * 100% % R % S [ R] [ S ]
8.3、含一个手性碳原子的化合物
含一个手性碳原子的化合物,在空间有两种不同的排布,
它们互为实物与镜像的关系→对映体。
一、表示手性分子的空间形象 Fischer 投影式
可以固定一个基团,其他基团按顺时针( 或逆时针)方向
COOH H OH CH3
翻 转
转动→ 得到的化合物构型不变
COOH HO H CH3
翻 转
CO O H H OH C H3
旋 转180
C H3 。 HO H CO O H
旋转180 。
CO O H H OH C H3
旋 转90 。
H C H3 CO O H OH
R
(1)只适用于
H R'
Y
型的化合物
(2)同一化合物通过不同的推导路线,结论有时不一致 氨基酸标准 不统一 D 如: (+)-酒石酸 造成混乱 甘油醛标准 L (3)有许多化合物无法与甘油醛联系
D / L命名法主要在碳水化合物和氨基酸中使用。
二、 R / S标记法:
1970年,IUPAC建议采用R/S命名法
能使偏振光振动面旋转的物质,叫旋光性物质。 使偏振光旋转的角度,称为旋光度,以 表示。
亮
α 丙 酸
暗 亮
乳酸
旋光方向:右旋(+); 左旋(-)
因旋光度受温度、光源、浓度、管长等因素的影响, 为了便于比较,常用比旋光度[]来表示:
α
t
λ
= cⅩl
α
式中: α 为试样的旋光度;
有机化学 第八章 对映异构

4)交替对称因素(Sn) ——了解
Cl H3C H H H Cl H CH3
旋转180o
H H3C H H Cl Cl CH3 H
Cl H3C H H H Cl H CH3
具有旋转反映对称因素的分子是对称分子。非手性分子。 一般情况下,不具有对称面和对称中心的分子, 其实物与镜影不能重叠,该分子称为不对称分子 或手性分子。Br* *来自* OH * * COOH
8.4 构型的表示法、构型的确定和构型的标记
8.4.1 构型的表示法
(1)透视式(三维结构)
COOH C CH3 H OH COOH H C CH3 HO
(2)Fischer 投影式:
[投影规则]
投影时,与手性碳相连横向两个键朝
前,竖向两个键向后,交叉点为手性碳。(横前竖后)
凡具有对称面、对称中心、交替对称轴(极少数
情况)其中一种对称因素的分子,都能与其镜像
分子叠合,都是非手性分子。反之,都不具有上
述对称因素的分子,是手性分子。是否有对称轴
对分子是否有手性没有决定作用。
只要能判断一个分子既没有称面,也没有
对称中心,一般能初步断定它是一个手性分
子。 凡是手性分子,实物与其镜象不能重叠,互
左旋体与右旋体,旋光度相同、旋光方向相反。 对映体之间的异同点
(1)物理性质和化学性质一般都相同,比旋光度的数 值相等,仅旋光方向相反。 (2)在手性环境条件下,对映体会表现出某些不同的 性质,如反应速度有差异,生理作用的不同等。
等量的左旋体和右旋体的混合物称为外消旋体,一 般用(±)来表示。
( + ) CH3CHCOOH OH ( ) CH3CHCOOH OH ( + ) CH3CHCOOH OH
第八章 立体化学
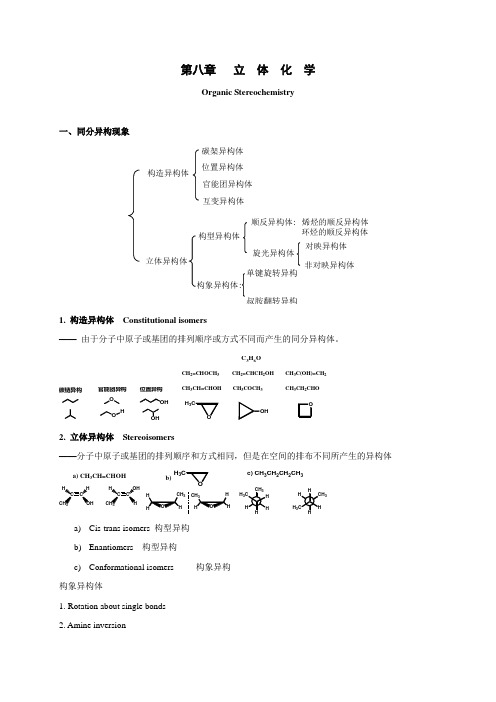
第八章 立 体 化 学Organic Stereochemistry一、同分异构现象构造异构体碳架异构体位置异构体官能团异构体互变异构体立体异构体构型异构体构象异构体:顺反异构体:烯烃的顺反异构体环烃的顺反异构体旋光异构体对映异构体非对映异构体单键旋转异构叔胺翻转异构1. 构造异构体Constitutional isomers—— 由于分子中原子或基团的排列顺序或方式不同而产生的同分异构体。
碳链异构O O官能团异构OH 位置异构C 3H 6OCH 2=CHOCH 3 CH 2=CHCH 2OH CH 3C(OH)=CH 2CH 3CH=CHOH CH3COCH 3 CH 3CH 2CHOH 32. 立体异构体 Stereoisomers——分子中原子或基团的排列顺序和方式相同,但是在空间的排布不同所产生的异构体C C HHCCOHHa) CH 3CH=CHOH3H 3b)H 33H 3c) CH 3CH 2CH 2CH 3a) Cis-trans isomers 构型异构 b) Enantiomers 构型异构c) Conformational isomers 构象异构 构象异构体1. Rotation about single bonds2. Amine inversionNonbonding electron pair is requiredInversion energy ~ 25 kJ/molcan rapidly interconvert at RT构型异构体——顺反异构——对映异构与非对映异构(旋光异构)3. 同分异构的多层次性构造异构、构型异构和构象异构是不同层次上的异构。
其中构造异构属较低层次的异构形式,其次为构型异构,而构象异构是较高层次的异构形式。
其中低层次异构形式通常包含有较高层次的异构形式。
C7H14Oconstitutionalconformational二、构型异构中的顺反异构Cis–trans isomers result from restricted rotation that can be caused either by a double bond or by a cyclic structure。
chapt08立体化学(6)

chapt08立体化学(6)第八章立体化学大纲要求:旋光性、手性、分子的手性与对称性;对映异构现象和对映异构体,非对映异构体,对映异构体的命名和表示方法;手性碳原子及其命名;含有一个以上手性碳原子的立体异构体;外消旋体和内消旋体;外消旋体的拆分;化学反应的立体选择性;不对称合成。
引言: 同分异构体的分类1、碳干异构构造异构同分异构2、官能团异构3、官能团位置异构4、互变异构顺反异构构型异构立体异构构象异构对映异构本章重点:几个概念(对映体、非对映体、内消旋体、外消旋体)C*的构型表示式C*的R/S命名烯烃加溴反应的立体化学。
课时安排:4课时镜象与手性的概念§8.1 手性和对映体8.1.1 对映异构现象的发现A D CB BC A D左手和右手不能叠合左右手互为镜象1 对映异构:如一个化合物分子与其镜象不能重合,两者关系相当于自己左右手一样,即相互对映,这种异构体称为对映异构体。
CH3 CH3 H OH COOH一个物体若与自身镜象不能叠合,叫具有手性. ?在立体化学中,不能与镜象叠合的分子叫手性分子, 而能叠合的叫非手性分子.HO HOOCH2 不对称碳原子:与四个原子或原子相连的碳原子称为不对称碳原子,通常用“C*”标记。
8.1.2 手性与对称因素练习:找出不对称碳原子一对称因素物质分子能否与其镜象完全重叠(是否有手性),可从分子中有无对称因素来判断,最常见的分子对称因素有对称面和对称中心。
CH3CH2 CH CH3 Cl*Ph CH CH3 D*1 对称面(m)假设分子中有一平面能把分子切成互为镜象的两半,该平面就是分子的对称面,例如:* * OHClHOOCCH CH OH OH**COOH12 对称中心(σ)若分子中有一点P,通过P点画任何直线,如果在离P等距离直线两端有相同的原子或基团,则点P称为分子的对称中心。
例如:H H Br P Br COOH H H Br H H H CH3 CH3 H H BrCH3 HCH3 HCH3 HCH3 HCH3 CH3 H HCH3 CH3 H H物像PH H具有对称面的分子无手性。
有机化学---第8章 立体化学
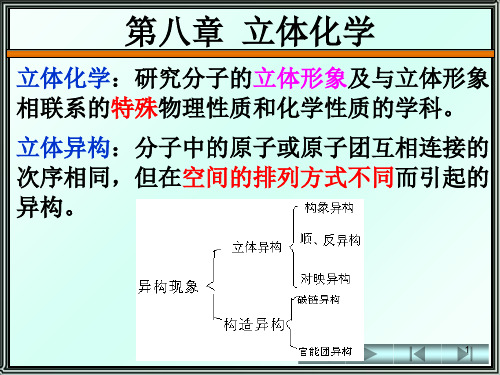
① 对称面 ② 对称中心 ③ 对称轴
④ 交替对称轴(旋转反映轴)* 对称操作:旋转+ 反射 手性判断:有交替对称轴,分子无手性。
凡物质分子在结构上不具有对称面、对称
中心或四重交替对称轴,这个物质就具有手性,
从而具有对映异构现象。
h
6
8-2 旋光性和比旋光度
旋光性:能使偏振光振动平面旋转的性质。
Nicol 棱镜
COOH
H
OH
D-(-)- 乳酸
C H3
COOH
HO
H
L-(+)-乳酸
C H3
注意:该标记法只能表示出分子中含有
一个手性碳原子的构型。
h
17
构型的标记
R-S标记法
根据化合物的实际构 型或投影式而命名的
含有一个手性碳化合物C-abcd的命名步骤:
① 将手性碳原子所连的四个基团(a,b,c,d)根据 “次序规则”先后排列, 如a > b > c > d;
绝对构型: 能真实代表某一光活性化合物的构型.
实验证实, 任意指定的甘油醛的构型正是其绝
对构型, 因此由甘油醛关联而得到的各旋光性化
合物的相对构型就是他们的绝对构型。
h
15
构型的标记
D-L标记法
以甘油醛的构型为对 照标准来进行标记
标记规则:右旋甘油醛的构型为D型; 左旋甘油醛的构型为L型。
凡构型与D-甘油醛相同的化合物, 命名时标以 “D”; 凡构型与L-甘油醛相同的化合物, 命名时标以“L” 注 意:旋光方向用(+)(-h )表示 , 不用“d”或“1l6” 。
外消旋体
由等量的左旋体和右旋体混合而成的没有 旋光性的混合物。 一般用(±)表示。
ch8立体化学2019

一 偏振光和旋光性 光电磁波,它的振动方向与其前进方向 垂直(图a).普通光的光波可在垂直于它前 进方向的任何可能的平面上振动(图b).
光束前进方向
(a)前进方向与振动方向垂直 (b)普通光线的振动平面
a Nicol
(a) 水等不旋光物质
A为盛液体 或溶液的管子
(b) 乳酸等旋光物质
右旋:面对光源顺时针旋转,以“+”或“d”表示 左旋:反时针旋转,以“-”或“l”表示
投影式相互转化规则:
*投影式不可离开平面翻转。
*可在平面内旋转180度;不可在平面内旋转90 度;
*允许保持一个原子(团)不动,其余三个依 次换位;
*允许偶次交换同碳上的原子(团)。
CH3 HO H
COOH (Ⅱ)
OH
H3C
COOH
H
(Ⅲ)
H
HOOC CH3 OH (Ⅳ)
二 锯架投影式
H H
HH HH
酒 石
CO2H (1)
酸 (2S,3S)-
[α]D-12°
mp: 170 ℃
CO2H (2)
(2R,3R)-
[α]D+12 °
170 ℃
CO2H (3)
(2S,3R)-
[α]D 0°
140 ℃
CO2H (4)
(2R,3S)-
[α]D0 °
140 ℃
对映体
非对映异构体
对映体 ?
(3)为具有手性中心的非手性分子,称为内消旋体。
第八章 立体化学
• 学习要求: • 1.掌握偏振光、旋光性、比旋光度。
2.掌握手性、对映性、非对映性,内消旋体、外消旋体 和不对称性等概念。 3.掌握fischer投影的规则,和使用该投影式的规定,以 及fischer投影式和Newman式,楔形式的转换。 4.掌握含有一个和二个手性碳原子的手性分子的R/S标定 法。 5.理解对称元素和对称操作,识别指定结构的对称元素。 6.理解对映异构体理化性质差异及外消旋体的化学拆分 原理。 7.了解构型的D、L标记法及手性在自然界的意义。 • 8.了解手性合成、环状化合物的立体异构。 9.能运用立体化学知识解释烯烃亲电加成反应历程。
第八章 对映异构

COO H
HO
H
CH 3
COOH HO C H
CH3
COOH HO H
CH3
含有两个手性碳的手性分子的投影
CH3
HO CH3 H
C
HO CH3 H
C
HO
H
HO
H
CH3
C H H3C
OH HO
C CH3
H
(2)注意事项 ① 可以沿纸面旋转180;
COOH
H
OH
CH3
旋 转180 。
CH3
HO
H
COOH
a CC
b
c
C d
c
a
C CC
d
b
2、 一个双键与一个环相连(1909年拆分)
H
COOH
H3C
H
三、联苯型的旋光异构体
a
c
a
b
c
d
d b
4 COOH -
1COOH HO 2 H
H 3 Cl 4COOH
(2R,3S)
差向异构体:在C*≧2立体异构体中,只有一个C*构 型不同,其他都相同的立体异构体。
CHO
H
OH
H
OH
H
OH
CH2 OH
CHO H OH H OH HO H
CH2OH
二、含两个相同C*化合物的对映异构
OHC-CH(OH)-CH(OH)-CHO
CH3
CH3
反-1,2-二甲基环丁烷 (1R,2R)-1,2-二甲基环丁烷
H
CH3
H3C
H
(1S,2S)-1,2-二甲基环丙烷
H3C
H
H
CH3
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第八章立体化学
第八章立体化学
【重点难点】
1. 理解以下基本概念:
平面偏振光、旋光性、旋光性物质、右旋体、左旋体、旋光度、比旋光度、对映体、非对映体、内消旋体、外消旋体。
2. 掌握含一个、两个手性碳原子化合物的对映异构;掌握含有两个手性碳原子化合物的立体异构;掌握环状化合物的立体异构。
3. 熟练掌握Fischer投影式规则,应做到:
(1)根据化合物的名称写出其Fischer投影式。
(2)根据化合物的其它立体结构式写出其Fischer投影式。
4.熟练掌握R/S标记法,应做到:
(1)用R/S标记法,标记任何一种立体结构式(如Fische r投影式、楔型式等)中手性碳的构型。
(2)对于给出的立体结构式,能判断哪些具有旋光性。
(3)对于给出的立体结构式,能判断哪些是对映体、非对映体、相同构型。
1。
