第七章 多环芳烃和非苯芳烃
07多环芳烃和稠环芳烃

+
X2
CCl4 低温
(B) 氧 化 反 应
O O
工业 :在 V2O5下加 热 300-500制 备 O
O O 9,10-蒽 醌 O
+
AlCl3 F-C反应 COOH O SO3H
H2SO4 - H2O
O
发烟硫 酸 加 热
O
7.2.3 菲
菲是白色片状晶体,熔点100 ℃,沸点340 ℃,易溶于苯和乙醚,溶液呈蓝色荧光。菲的结 构比蒽稳定,反应主要发生在9,10位。
联苯为无色晶体,熔 点70 ℃ ,沸点254 ℃。 不溶于水,而易溶于有 机溶剂。 它的性质与苯相似, 两个苯环上均可发生磺 化、硝化等反应(主要 为对位产物,邻位较 少)。
I + Cu
+
CuI
HNO3 H2SO4 O2N
HNO3 H2SO4 O2N NO2
NO2
Zn NaOH
N N H H
HCl
H2N
振)。
返回
6 5 0.139 0.142 4 0.137
3
0.140
(2) 萘的性质
A、取代反应(主要在α 位Cl )
Cl2 Fe Cl
+ Br
CCl4 (72%-75%) NO2 NH2 Zn + HCl (79%) SO3H
+
Br2
+ HNO3
H2SO4
100% H2SO4 (80)
(96%)
H2SO4(165) 95% H2SO4 (165) NaOH (300) H+ OH SO3H (85%) 容 易 得到
3
92% H2SO4
3
SO3H
第七章 芳 烃

上一内容
下一内容
回主目录
返回
苯中的P轨道
P轨道的重叠
2、 分子轨道理论解释 、 分子轨道理论认为, 分子中六个P轨道线 分子轨道理论认为 , 分子中六个 轨道线 形组合成六个π分子轨道 , 其中三个成键规定, 形组合成六个 分子轨道, 其中三个成键规定 , 分子轨道 三个反键轨道。 在基态时, 苯分子的六个π电 三个反键轨道 。 在基态时 , 苯分子的六个 电 子成对填入三个成键轨道, 子成对填入三个成键轨道,其能量比原子轨道 所以苯分子稳定, 低,所以苯分子稳定,体系能量 较低 。
CH3 CH CH3 NO2 Cl
异丙基苯
叔丁基苯
硝基苯
氯苯
上一内容
下一内容
回主目录
返回
当苯环上连有 -COOH、 -SO3H、-NH2、-OH、-CHO、 、 、 、 、 较复杂时, -CH=CH2或R较复杂时,则把苯环作为取代基。例如: 较复杂时 则把苯环作为取代基。例如:
COOH SO3H CHO OH NH2
上一内容 下一内容 回主目录 返回
反键轨道 E 原子轨道 成键 轨道 苯的分子轨道能级示意图
上一内容
下一内容
回主目录
返回
三个节面 ψ6
ψ4
二个节面
ψ5
E
ψ2 一个节面 无节面 ψ1 苯 的 π电 子 分 子 轨 道 重 叠 情 况 ψ3
苯分子的大π键是三个成键轨道叠加的结果,由于 电子都是离域的 电子都是离域的, 苯分子的大 键是三个成键轨道叠加的结果,由于π电子都是离域的, 键是三个成键轨道叠加的结果 所以碳碳键长完全相同。 所以碳碳键长完全相同。
一、 苯的凯库勒式 1865年凯库勒从苯的分子式 6H6出发 根据苯 年凯库勒从苯的分子式C 出发,根据苯 年凯库勒从苯的分子式 的一元取代物只有一种( 的一元取代物只有一种(说明六个氢原子是等同 的事实),提出了苯的环状构造式 ),提出了苯的环状构造式。 的事实),提出了苯的环状构造式。
7 第七章 芳烃
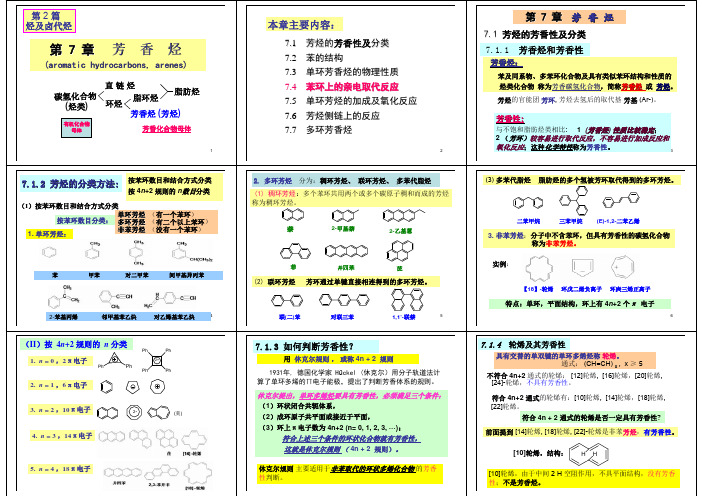
本章主要内容:
第 7 章 芳 香 烃
7.1 芳烃的芳香性及分类 7.1.1 芳香烃和 和芳香性
芳香烃:
苯及同系物、多苯环化合物及具有类似苯环结构和性质的 烃类化合物 称为芳 芳香碳氢化合物,简称芳香烃 芳香烃 或 芳烃。 碳氢化合物 芳烃 芳烃的官能团 芳环, 芳烃去氢后的取代基 芳基 (Ar-)。
二苯甲烷
三苯甲烷
(E)-1,2-二苯乙烯
萘
2-甲基萘
2-乙基蒽
3. 非苯芳烃:分子中不含苯环,但具有芳香性的碳氢化合物 称为非苯芳烃。 实例:
菲
并四苯
芘
苯
甲苯
对二甲苯
间甲基异丙苯
(2) 联环芳烃
芳环通过单键直接相连得到的多环芳烃。
【18】-轮烯 环戊二烯负离子 环庚三烯正离子
特点:单环,平面结构,环上有 4n+2 个π 电子
思考:二甲苯三种异构体中, 邻二甲苯的沸点最高,对二甲苯对熔点最高?
17
7.3.2
沸点 熔点
苯的同系物中每增加一个 -CH2-单位,沸点平均 增高约 20-30 ℃。
16
沸 点
如: 苯、甲苯、乙苯、正丙苯和正丁苯的沸点分别 为 80.1 ℃, 110.6 ℃,136 ℃,159.2 ℃和 183 ℃。
+ Cl2
FeCl3
Cl
Cl
+
Cl
24
在卤化反应中,铁粉也能起到催化剂的作用。
X
苯与卤素的反应的活性顺序:
氟>氯>溴>碘
苯与氟的反应过于激烈,很难控制,一般不用; 苯与碘的反应太慢, 需要在氧化剂(HNO3)存在下进行, 一般也不用。 氯的反应活性大于溴的反应活性,但溴化产物的选择性 比氯化产物高。取代苯的溴化产物,以对位产物为主。
第七章芳香烃资料.

§7.1 芳香族化合物的分类
芳烃
单环 芳烃
分子中含一个苯环
联苯 苯环各以环上 一个碳原子直 接相连。
CH3
联苯 mp.70.5
多环 芳烃
多苯代 脂肪烃
CH2
二苯甲烷 mp.27
芴 CmHp2.116
苯环共用相 稠环芳烃 邻两个以上
碳原子稠合 而成。
萘 mp.80.2
蒽 mp.218
单环芳烃
§7.2 苯的结构
道
E
节面
反键轨道
节面
成键轨道
苯的分子轨道模型
▪ 由于苯的大体系结构是封闭成环的,所以其电子 具有完全的离域性,分子内能进一步降低,因此具 有特殊的稳定性,即所谓的“芳香性”。
§7.3 单环芳烃的异构现象及命名
单环芳烃可看作是苯环上的氢原子被烃基取 代所得的衍生物,分为一烃基苯、二烃基苯、三烃 基苯等等。
一、一烃基苯
例:
只有一种,而无异 构体。命名时,以 苯环作母体,烃基 作取代基,称为某 烃(基)苯。
CH3
甲苯 methylbenzene
Bp. 111
CH2CH3
乙苯 ethylbenzene Bp. 136.2
二、二烃基苯
二烃基苯有三种异构体, 用数字或邻、间、对 (o-, m-, p-)表示取代基位置。 例如:
CH3 CH3
CH3
CH3
1,2-二甲苯 邻-二甲苯
o-二甲苯
CH3
1,3-二甲苯 间-二甲苯
m-二甲苯
CH3
1,4-二甲苯
对-二甲苯
p-二甲苯
o– orther
m– meta
p- para
三、三烃基苯 若三个相同烃基的三烃基苯也有三种异构体,例如:
有机化学第七章 芳烃

1
一、教学目的和要求 通过对本章的学习,掌握芳烃的定义、分类、苯的结构、 闭合共轭体系、芳香性及苯的同系物的命名,掌握苯环上 的亲电取代反应及定位规则,侧链卤代和氧化反应,掌握 萘的结构及命名,萘的亲电取代反应、氧化反应;熟悉休 克尔规则及非苯芳烃的芳香性判断;了解联苯、蒽、菲的 结构及命名以及苯及其同系物的主要物理性质(易燃性)。 二、教学重点内容 芳烃的结构、闭合共轭体系、命名、亲电取代反应及其定 位规律、侧链氧化、萘的结构、命名及亲电取代反应、非 苯芳烃芳香性的判断是本章的重点。
CH3 CH3 CH3
(1)单环芳烃
苯 甲苯 间二甲苯
(2)多环芳烃
连 苯 三
C H 苯 甲
烷
(3)稠环芳烃
萘 蒽 菲
4
5.1
芳烃的构造异构和命名
5.1.1 构造异构
苯及其同系物的通式为:CnH2n-6。 例如苯有六个碳和六个氢,其六个碳和六个氢是等同的; 结构异构: 一元取代:只有一种
CH3 CH CH2 H3C CH CH3
(a)
(b) (c) (d) (e)
卤化
硝化 磺化 Friedel-Crafts反应 氯甲基化
17
(1)亲电取代反应
(a) 卤化
苯环上和卤代反应较困难,常用FeX3(Lewis酸)作催化剂。
+ Cl2
FeCl3,25oC 90%
Cl + HCl
控制苯过量,不要太激烈,避免二卤代。 因是亲电反应,所以苯的同系物(甲苯)比苯更易反应。 Cl 卤代活性: F2>Cl2>Br2>ICH CH3 CH3 CH3 2。 3
14
5.3
单环芳烃的物理性质
第七章 芳香烃(2)
定位效应包括两方面:(1)基团所进入的位置; (2)反应的速度快慢。
42
CH3
H2SO4+ HNO3
30 ℃
CH3 NO2
( O + P = 96.5 %)
56.5 %
CH3
NO2
40 %
NO2
H2SO4+ HNO3
90~100 ℃
(O + P = 6.7%)
NO2
NO2
93.2%
NO2 NO2
6.4%
结构特点:与苯环直接相连的原子多数含有未共用 电子对。
44
2. 间位定位基—第二类定位基(钝化 苯环)
强致钝基:-N+R3, -NO2, -CX3 中等致钝基: -CN, -SO3H, -COR(H), -CO2H, -CCl3 弱致钝基:-COOR,-CONHCH3, -CONH2, -NH3, etc.
H
O
X
CR
卤代反应 NO2
SO3H
R 酰基化 反应
硝化反应
20
磺化反应 烷基化反应
反应机理: 亲电取代反应
sp2 + E+
E+ 慢
sp3
H -H+
+
E
sp2 E
亲电试剂 络合物
络合物
产物
用极限式表示中间体 络合物 :
H
H
E
E
+
+
21
+H E
1.卤代反应
卤 素:Cl2 、Br2 催化剂:FeX3 AlCl3 ZnCl2或 Fe
具有三个相同烃基的取代苯也有三种异构体。如:
CH3 CH3
有机化学第七章 芳烃
119.5 119.5
239.0 231.6
358.5 208.2
原因:存在共轭体系,π电子高度离域使苯环特别稳定。
离域能:358.5-208.2 = 150.3 kJ·mol-1
6
Kekulè用迅速互变异构解释苯的邻位二元取代物只有一种。
Br
Br
Br
Br
但无法解释难发生加成、氧化反应;并把这些异常的性质 称为芳香性,原因归结为环状交替单双键结构。
15
1-丁烯的共振式:
-+
C H 2 C HC H 2 C H 3 C H 2 C HC H 2 C H 3
+
CH2
-
CH CH2CH3
×
-
CH2
CH2
+
CHCH3
碳酸根的共振式:
原子排列不同
· ·
O· ·
· · · O · · · -
· · · O · · · -
- · · · · O · ·C · · O · · · · -
C · · · O ·
· · O · · · · -
- · · · · O · ·C · O · · ·
16
(3) 对共振杂化体中不同经典结构式的贡献 越稳定的经典结构式在共振杂化体中占的分量越大。 经典结构式稳定性的确定: 共价键数目最多的经典结构式最稳定; 经典结构式的正负电荷越分散越稳定,即电荷分离的经 典结构式稳定性差; 经典结构式中所有原子都具有完整的价电子层的较稳定; 负电荷在电负性大的原子上的经典结构式较稳定。
B r 相同
Br
Br
Br
苯为高度不饱和的分子,却不容易发生加成反应而容易 发生取代反应;
07第7章_芳烃
+
R
C X
注意:
每类反应的特点; 比较苯、甲苯和硝基苯的反应活性; 反应机理。
总目录
1. 硝化反应
注意1:反应 温度、试剂浓 度的差别!
注意2: 引入取代基的位置!
总目录
两个取代基定位作用一致
两个取代基定位作用不一 致,致活基团起主导作用
总目录
思考
(1)浓硫酸起什么作用? (2) 从反应条件(试剂浓度、反应温度),看几种 单环芳烃的硝化活性。
6个Csp2— Csp2键 6个C—H键
Csp2杂化(垂直的p 轨道未画出)
总目录
(2)6个p 轨道平行重叠形成大π键
碳原子的p轨道
苯分子的大π 键
总目录
苯环所有键示意图
总目录
2. 分子轨道理论解释
(1)苯的骨架结构(同上) (2)6个p 原子轨道线性组合成6个分子轨道:
反键轨道 原子轨道 成键轨道
第四节 苯环的亲电取代定 位效应 一、定位效应 二、定位效应的解释 三、定位效应的应用 第五节 多环芳烃 一、联苯 二、稠环芳烃 第六节 非苯系芳烃 一、芳香性的几个特征 二、休克尔规则 三、非苯芳烃 四、大环芳烃 第七节 富勒烯与C60
ห้องสมุดไป่ตู้
总目录
脂肪烃
aliphatics
烃
芳香烃
aromatic hydrocarbons
+
总目录
(2)反应机理—— 亲电加成-消除反应历程
σ 络合物 (该中间体亲电取代都经历) 亲电加成 消除
说明σ 配合物的生成决速步骤
总目录
σ 配合物: 碳原子杂化态从sp2转化为sp3,大π
键被破坏,4个π电子离域于环上5 个碳原子上,使苯环呈正电荷。
有机化学第七章 芳烃
苯甲醛 benzaldehyde
COOH
苯甲酸 benzoic acid
SO3H
苯磺酸 benzenesulfonic acid
29
有两种以上取代基时,选择母体的顺序为:
—OR,—R,—NH2,—OH,—COR,—CHO, —CN,—CONH2,—COCl,—COOR,—SO3H, —COOH,正离子等。
NH2
对氨基苯磺酸 4-aminobenzenesulfonic acid
SO3H
31
苯环上连有三个及三个以上取代基时,只能用阿拉伯数 字编号。
COOH
O2N
NO2
3,5-二硝基苯甲酸 3,5-dinitrobenzoic acid
NH2 CH3
2-甲基-4-氯苯胺 4-chloro-2-methylaniline
16
(3) 对共振杂化体中不同经典结构式的贡献 越稳定的经典结构式在共振杂化体中占的分量越大。 经典结构式稳定性的确定: 共价键数目最多的经典结构式最稳定; 经典结构式的正负电荷越分散越稳定,即电荷分离的经 典结构式稳定性差; 经典结构式中所有原子都具有完整的价电子层的较稳定; 负电荷在电负性大的原子上的经典结构式较稳定。
CH3
CH2CH3
CH(CH3)2
甲苯 methylbenzene
乙苯
异丙苯
ethylbenzene propan-2-ylbenzene
23
烃基较复杂或有不饱和键时,把链烃当作母体,苯环 作为取代基。
苯基的英文名称为 phenyl。
CH2CH CH2
CH3CH2CHCH(CH3)2
3-苯基-1-丙烯 3-phenylprop-1-ene prop-2-en-1-ylbenzene
第七讲 芳烃
第七讲 芳 烃芳烃,也叫芳香烃,一般是指分子中含苯环结构的碳氢化合物。
芳香二字的来由最初是指从天然树脂(香精油)中提取而得、具有芳香气的物质。
现代芳烃的概念是指具有芳香性的一类环状化合物,它们不一定具有香味,也不一定含有苯环结构。
芳香烃具有其特征性质——芳香性(易取代,难加成,难氧化)。
芳烃按其结构可分类如下:§7—1 苯的结构一、 苯的凯库勒式1865年凯库勒从苯的分子式C 6H 6出发,根据苯的一元取代物只有一种(说明六个氢原子是等同的事实,提出了苯的环状构造式。
苯的凯库勒式结构 二、苯分子结构的价键观点现代物理方法(射线法、光谱法、偶极距的测定)表明,苯分子是一个平面正六边形构型,键角都是120°,碳碳键长都是0.1397nm 。
图示如下:2CH 3CHCH 32CH 3CH 2苯系芳烃非苯芳烃单环芳烃多环芳烃联苯稠环芳烃多苯代脂烃苯乙苯异丙苯苯乙烯联苯对三联苯萘 蒽二苯甲烷环戊二烯负离子环庚三烯正离子薁简写为所有的原子共平面键长均为键长均为所有键角都为C-C C-H 0.1397nm0.110nm 120°0.1397nm正六边形结构理论解释:1. 杂化轨道理论解释苯分子中的碳原子都是以sp 2杂化轨道成键的,故键角均为120°,所有原子均在同一平面上。
未参与杂化的P 轨道都垂直与碳环平面,彼此侧面重叠,形成一个封闭的共轭体系,由于共轭效应使π电子高度离域,电子云完全平均化,故无单双键之分。
2. 分子轨道理论解释分子轨道理论认为,分子中六个P 轨道线形组合成六个π分子轨道,其中三个成键规定,三个反键轨道。
在基态时,苯分子的六个π电子成对填入三个成键轨道,其能量比原子轨道低,所以苯分子稳定,体系能量 较低 。
苯分子的大π键是三个成键轨道叠加的结果,由于π电子都是离域的,所以碳碳键长完全相同。
二、 从氢化热看苯的稳定性苯中的P 轨道P轨道的重叠E 原子轨道反键轨道成键 轨道苯的分子轨道能级示意图H 22H 23H 2H=_120KJ / mol H=_232KJ / molH=_208KJ / mol H 苯实=208 KJ / molH 苯理=3x120=360KJ / molE ψψ351三个节面苯的π电子分子轨道重叠情况苯的稳定化能(离域能或共振能)=360-208=152KJ/mol三、苯的共振式和共振论的简介 (自学)§7—2 单环芳烃的异构和命名一、 异构现象1.烃基苯有烃基的异构例如:2.二烃基苯有三中位置异构例如: 3. 三取代苯有三中位置异构 例如:二、 命名 1.基的概念芳烃分子去掉一个氢原子所剩下的基团称为芳基(Aryl )用Ar 表示。
