有机化学---第7章 多环芳烃和非苯芳烃
有机化学第七章(多)
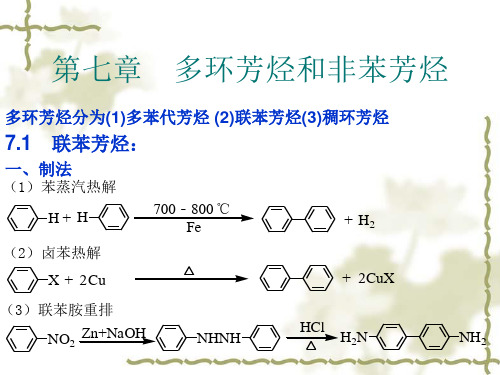
4 3 2 1
1
α-甲基萘 β-甲基萘 1-甲基萘 2-甲基萘
SO3H
5 4 NO2
SO3H 2 3
4 3 2 1 OH
CH3 5
4-甲基-1-萘磺酸 5-硝基-2-萘磺酸
5-甲基-1质: (1)性状:无色片状晶体,mp:80.2℃,bp:218 ℃,有特殊气味。 性状: 有特殊气味。 性状 无色片状晶体, ℃ 有特殊气味 (2)易升华,蒸气有杀菌作用。用于做卫生球,用于杀菌防虫。 易升华, 易升华 蒸气有杀菌作用。用于做卫生球,用于杀菌防虫。 萘的化学性质与苯相似,但由于离域的不太好, 萘的化学性质与苯相似,但由于离域的不太好,π电子云不是均匀 分布,所以反应活性与苯相比,不仅比苯易进行亲电取代反应, 分布,所以反应活性与苯相比,不仅比苯易进行亲电取代反应, 而且也较易进行加成和氧化反应。 而且也较易进行加成和氧化反应。 1.亲电取代反应 亲电取代反应 萘环上的π电子云不是均匀分布,据测定,它的α 萘环上的π电子云不是均匀分布,据测定,它的α位上电子云密度 最高, 位次之, 位最低, 最高,β位次之,γ位最低,所以萘的亲电取代反应一般发生在 特殊情况下也能在β位反应。 α位。特殊情况下也能在β位反应。
CH3
(2)原来取代基为第二类定位基时,则钝化芳环,主要发生异环α 原来取代基为第二类定位基时,则钝化芳环,主要发生异环α 原来取代基为第二类定位基时 位取代。 -位取代。如: NO
2
NO2
萘亲电取代的定位规律
但是,萘的亲电取代反应有的不遵循定位规律, 但是,萘的亲电取代反应有的不遵循定位规律,如:
H2 SO4 H2O
9,10-蒽醌和它的衍生物是蒽醌类染料的主要原料。 -蒽醌和它的衍生物是蒽醌类染料的主要原料。
有机化学 徐寿昌 第二版

(C6H5)3COH (C6H5)3CBr (C6H5)3C-Na+ + NH3
(C6H5)3CH + Na+NH2
CH3CH3 pka ~50 C6H5CH3 41 NH3 34-35
(C6H5)2CH2 34
(C6H5)3CH 31.5
CH ≡ CH 25
7.2 联苯
4HC≡CH
Ni(CN)2 15-20 atm, 50oC
(70%)
无芳香性
- 2K
乙醚
=
≡
有芳香性
C-C键键长平均 化,均为1.40A。 八个碳原子共平 面。
*K给出二个电子。
7.4.2轮烯芳香性的判别
1 定义: 分子式符合(CH)n的环多次甲基化合物称为轮烯。 (n≥10) 2 命名: 轮烯是根据碳氢的数目来命名的。
COOH
电子云密度高的环易被氧化。
(2) 萘的还原
H2 / 弱催化剂 H2 / pt 高温高压 H2 / Ni (pd) Na C2H5OH 152oC Na (or Li) NH3-C2H5OH (2mol) Na C2H5OH 78oC 高温高压
Na (or Li) NH3-C2H5OH (4mol)
NO2
O2N
NO2
Br
NH2
Br2
NH2 Br
7.3 稠环化合物
1 定义:
两个或多个苯环公用两个邻位碳原子的化合物 称为稠环芳烃。
2 重要稠环化合物的名称和结构
8 7 6 5 4 1 2 3
8 9 10 1 2 3 5 4
6
5
4
3 2
萘
7 6
蒽
徐寿昌《有机化学》(第2版)名校考研真题(多环芳烃和非苯芳烃)【圣才出品】

第7章多环芳烃和非苯芳烃一、选择题1.下列化合物有芳香性的是()。
[华中科技大学2000研]【答案】(B),(C)【解析】(B)项分子中有6个π电子,符合休克尔规则;(C)项中的七元环带一个单位正电荷,五元环带一个单位负电荷,这样七元环和五元环的π电子数都为6个,且在同一平面内,都符合休克尔规则。
2.下列化合物中有芳香性的是()。
[中国科学院-中国科学技术大学2001研]【答案】(A)【解析】(A)中有10个π电子数,符合休克尔规则。
3.薁的亲核取代反应容易发生在哪些位置上?()[上海大学2004研]A.1、2和3位B.1和3位C.5和7位D.4、6和8位【答案】D【解析】薁的七元环带一单位正电荷,五元环带一单位负电荷,是典型的非苯芳烃,有芳香性。
七元环显正电性,易受亲核试剂的进攻,同时亲核反应发生在4、6和8位时,活性中间体中五元环带一单位负电荷,较稳定。
4.如果薁进行亲电取代反应,那么容易发生在哪些位置上呢?()[上海大学2004研]A.1、2和3位B.1和3位C.5和7位D.4、6和8位【答案】B【解析】薁的五元环带负电荷,易受亲电试剂进攻,故亲电反应发生在五元环,同时亲电反应发生在1和3位时,活性中间体碳正离子较稳定。
二、填空题1.命名:。
[武汉理工大学2004研]【答案】β-5-硝基萘乙酸(或5-硝基-2-羧甲基萘)【解析】以羧酸作为主体命名或以萘作为主体命名都可。
2.用系统命名法命名:。
[华中科技大学2002研]【答案】5-硝基-1-溴萘【解析】以萘作为主体进行命名,取代基的列出顺序按顺序规则,将小基团优先列出。
3.写出化合物9,10-二溴菲的结构式。
[华东理工大学2004研]【答案】【解析】要熟悉菲的取代基编号顺序:三、简答题1.杯烯具有较大的偶极矩(5.8D),为何?[上海大学2004研]答:杯烯中电子离域,五元环带一个单位负电荷,三元环带一个单位正电荷,这样五元环电子数为6,三元环电子数为2,都符合休克尔规则,为稳定的芳香结构。
有机化学课件-多环芳烃

§7.1.1 命名
a.联苯及衍生物
3 2 2' 3'
3 2 2' 3' 2" 3"
4
1 1'
4' 4
1 1'
4' 1"
4"
5 6 6' 5'
联苯
5 6 6' 5' 6" 5"
对联三苯
Cl Cl
32
2' 3'
4
1 1'
4'
5 6 6' 5'
3 2 NO2 2' 3'
4
1 1'
4' NO2
5 6 6' 5'
与苯环不同处:键长不均等 (但与普通的单双键不同)
§7.3 稠环芳烃 §7.3.1 萘、蒽的结构
b. 蒽的结构
表达式
sp2杂化, 平面结构, 键长不均等(与普通的单双键不同)
§7.3 稠环芳烃 §7.3.2 萘、蒽的化学性质
具有芳香性,易发生亲电取代, 但比苯易发生氧化及加成反应。
a. 萘的化学性质 1. 亲电取代反应
萘
稠环共用原子不编号,与螺环化合物区别(螺碳编号)。
蒽
菲
8 7
6 5
1 2 3
4
1,4,5,8 称为位 2,3,6,7 称为位
SO3H
- 萘磺酸
8 91
7
2
6
3
5 10 4
1,4,5,8 称为位 2,3,6,7 称为位 9,10称为γ位
6 54 3
7
2
8
有机化学第七章 芳烃

H
H
H
H
H
H
可以解释:为什么苯分子特别稳定? 为什么苯分子中碳碳键长完全等同? 为什么邻位二取代物只有一种?
(b)分子轨道理论 分子轨道理论认为:苯分子形成σ键后,苯的
六个碳原子上的六个P 轨道经线性组合可以形成六 个分子轨道,其中ψ1 、ψ2 和ψ3 是成键轨道,ψ4、 ψ5和 ψ6是反键轨道。当苯分子处于基态时六个电 子填满三个成键轨道,反键轨道则是空的。
-络合物
(b)硝化反应
2 H2SO4 HNO3
NO2
HNO3 H2SO4,45℃
CH3
HNO3 H2SO4,30℃
NO2
CH3 NO2
CH3
NO2
HNO3 H2SO4,95℃
NO2
NO2
NO2
H3O 2 HSO4
反应比苯容易 反应比苯困难
硝化反应机理
硝化反应中进攻试剂是NO2+,浓硫酸的作 用促进NO2+的生成:
苯环的特殊稳定性可以从它具有较低的氢化热 得到证明:
环己三烯氢化热=360kj/mol(假想值) 苯环氢化热=208kj/mol 相差152kj/mol
氢化热简图:
环己三烯+3H2
环己二烯+2H2
苯+3H2
环己烯+H2
231kj/mol
120kj/mol
208kj/mol
360kj/mol
环己烷
苯分子的近代概念
ቤተ መጻሕፍቲ ባይዱ
(1)煤的干馏
煤隔绝空气加热至1000~1300℃时分解所得到的 液态产物——煤焦油,其中含有大量芳烃化合物。 再经分馏得到各类芳烃。
馏分名称 轻油 酚油 萘油 洗油 蒽油
高教第二版(徐寿昌)有机化学课后习题答案第7章

第七章 多环芳烃和非苯芳烃一、 写出下列化合物的构造式。
1、α-萘磺酸2、 β-萘胺3、β-蒽醌磺酸SO 3HNH 2C C OO SO 3H4、9-溴菲5、三苯甲烷6、联苯胺BrCHNH 2二、 命名下列化合物。
1.2.C COO 3.SO 3HNO 24.CH 25.6.CH 3CH 3OHNO 2二苯甲烷 对联三苯 1,7-二甲基萘三、 推测下列各化合物发生一元硝化的主要产物。
SO 3HSO 3H1.HNO 3H 2SO 4O 2NSO 3HNO 2+2.CH 3H 2SO 4HNO CH 3NO 23.OCH HNO 3H 2SO 4NO 2OCH4.CNCNNO 2HNO 3H 2SO 4NO 2CN四、 回答下列问题:1,环丁烯只在较低温度下才能生成,高于350K 即(如分子间发生双烯合成)转变为二聚体什么?写出二苯环丁烯三种异构体的构造式。
解:环丁二烯π-电子为四个,具有反芳香性,很不稳定,电子云不离域。
三种二苯基环丁二烯结构如下:2,1,3,5,7-环辛四烯能使高锰酸钾水溶液迅速褪色,和溴的四氯,已知它的衍生物二苯基环丁二烯,有三种异构体。
上述现象3 3化碳溶液作用得到C 8H8Br8。
(a),它具有什么样结构?这两个共振结构式表示?解:不可以,因为1,3,5,7-辛环四烯不具有离域键,不能用共振结构式表示。
(c),用金属钾和环辛四烯作用即得到一个稳定的化合物2K+C8H8(环辛四烯二负离子),这种盐的形成说明了什么?预期环辛四烯二负离子将具有怎样的结构?解:环辛四烯二负离子具有芳香性,热力学稳定,其结构为:五、写出萘与下列化合物反应所生成的主要产物的构造式和名称。
1,CrO3, CH3COOH 2,O2,V2O5 3, Na,C2H5OHOO C O CO O解:具有右式结构,不是平面的(b),π-电子云是离域的。
1,4-萘醌邻苯二甲酸酐 1,2-二氢萘4,浓硫酸,800C 5,HNO3,H2SO4 6,Br2α-萘磺酸α-硝基萘 1-溴萘7,H2,Pd-C加热,加压 8,浓硫酸,1650C四氢萘β-萘磺酸六、用苯、甲苯、萘以及其它必要试剂合成下列化合物:1.CH 2CH 3Cl ,hvCH 2ClAlCl 3CH 2ClCl 2FeCH 2Cl2.(C 6H 5)3CHCH 3Cl ,hvCHCl2AlCl 3(C 6H 5)3CH3.NO 2Br23H 2SO 424.NO 2SO 3HSO 3H NO 2SO 3HH 2SO 4165C3H 2SO 45.C C OOCO O COAlCl 3O 2,V 2O 5450CC COOHO 97%H 2SO 4C C OO七、 写出下列化合物中那些具有芳香性? 解:1.2.3..4.+5.6.7.8.9.10.H HH HHH11.CH 2=CHCH=CHCH=CH 2代表有芳香性代表无芳香性。
《有机化学》第7章 芳香烃

所以如果希望获得所需的产物,使用正确的反应步骤是重要的。
2023/6/13
18
第三节 稠环芳烃
一、 萘
萘,分子式C10H8,光亮的片状结构,熔点80.2 ℃,沸点218 ℃,有特殊气味,易 升华,不溶于水,易溶于乙醇、乙醚、苯等有机溶剂。其化学性质与苯相似。
2023/6/13
11
⑷ 傅-克(Friedel-Crafts)反应 ① 烷基化反应 凡在有机化合物分子中引入烷基的反应,称为烷基化反应。反
应中提供烷基的试剂叫烷基化剂,它可以是卤代烷、烯烃和醇。
当烷基化剂含有三个或三个以上直链碳原子时,产物发生碳链异构。
② 酰基化反应 凡在有机化合物分子中引入酰基(
①若原有两个取代基不是同一类的,则第三个取代基进入的位置一般受邻、对 位定位基的支配,因为邻、对位基反应的速率大于间位基。
②若原有两个取代基是同一类的,则第三个取代基进入的位置主要受强的定位基 的支配。
2023/6/13
17
⑵ 选择适当的合成路线
例如:由甲苯制备对硝基苯甲酸。
比较这两个结构,反应步骤必须是先硝化,后侧链氧化。
1.取代反应
在萘环上,p电子的离域并不像苯环那样完全平均化,而是在α-碳原子上的电子 云密度较高,β-碳原子上次之,中间共用的两个碳原子上更小,因此亲电取代反应 一般发生在α位。
⑴ 卤化反应
在Fe或FeCl3存在下,将Cl2 通入萘的苯溶液中,主要得到α-氯萘。α-氯萘为无 色液体,沸点259 ℃,可做高沸点溶剂和增塑剂。
2023/6/13
6
苯分子去掉一个氢原子后的基团(C6H5―)叫做苯基,也可以用Ph―代 表。芳烃分子的芳环上去掉一个氢原子后的基团叫做芳基,可用Ar―代表。甲 苯分子中苯环上去掉一个氢原子后所得的基团CH3C6H5―称甲苯基;如果甲苯 的甲基上去掉一个氢原子,C6H5CH2―称苯甲基,又称苄基。
有机化学第七章 芳烃

1
一、教学目的和要求 通过对本章的学习,掌握芳烃的定义、分类、苯的结构、 闭合共轭体系、芳香性及苯的同系物的命名,掌握苯环上 的亲电取代反应及定位规则,侧链卤代和氧化反应,掌握 萘的结构及命名,萘的亲电取代反应、氧化反应;熟悉休 克尔规则及非苯芳烃的芳香性判断;了解联苯、蒽、菲的 结构及命名以及苯及其同系物的主要物理性质(易燃性)。 二、教学重点内容 芳烃的结构、闭合共轭体系、命名、亲电取代反应及其定 位规律、侧链氧化、萘的结构、命名及亲电取代反应、非 苯芳烃芳香性的判断是本章的重点。
CH3 CH3 CH3
(1)单环芳烃
苯 甲苯 间二甲苯
(2)多环芳烃
连 苯 三
C H 苯 甲
烷
(3)稠环芳烃
萘 蒽 菲
4
5.1
芳烃的构造异构和命名
5.1.1 构造异构
苯及其同系物的通式为:CnH2n-6。 例如苯有六个碳和六个氢,其六个碳和六个氢是等同的; 结构异构: 一元取代:只有一种
CH3 CH CH2 H3C CH CH3
(a)
(b) (c) (d) (e)
卤化
硝化 磺化 Friedel-Crafts反应 氯甲基化
17
(1)亲电取代反应
(a) 卤化
苯环上和卤代反应较困难,常用FeX3(Lewis酸)作催化剂。
+ Cl2
FeCl3,25oC 90%
Cl + HCl
控制苯过量,不要太激烈,避免二卤代。 因是亲电反应,所以苯的同系物(甲苯)比苯更易反应。 Cl 卤代活性: F2>Cl2>Br2>ICH CH3 CH3 CH3 2。 3
14
5.3
单环芳烃的物理性质
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碳原子的P轨道重叠程度
不完全相同, 由此导致其
中某些原子(α-位)的性质
活泼, 易发生化学反应.
h
5
7-2 萘的结构、命名和性质
萘的性质 离域能(共轭能) 152 kJ/mol
预测值:152×2=304 实测值: 255
萘的稳定性 比苯差,比 苯容易发生 亲电取代、 氧化、加成 等反应。
由于P轨道重叠程度的差异,造成萘环上 α碳的性质最活泼,h 最容易发生反应。 6
0.1436 nm
0.1423 nm
轨道重叠程度不完 全相同, 分子中的碳 -碳键长也不完全
相等, 反应活泼位为
h γ-位。
15
蒽的化学性质
总离域能 每个环的离域能 化
学
152 kJ/mol 152 kJ/mol
反 应
255 kJ/mol 128 kJ/mol
活 泼
性
增
351 kJ/mol 117 kJ/mol 大
➢取代反应
卤代、硝化、磺化
① 萘环上无取代基时
产物以-位取代为主
Cl2 FeCl3
Br2 / CCl4
90%
Cl
Br
混酸
h
NO2
79%
7
磺化 原因:
浓 H2SO4, <80℃ 浓 H2SO4, >165℃
S O3H
96%
浓 H2SO4 165℃
SO3H
85%
① -萘磺酸受动力学控制, 生成速度快; β-萘
C H3
Cl2 FeCl3
O CH3 混 酸
C H3
Cl NO2 O CH3
h
10
② 萘环上的一元定位规律
B: 第二类定位基
钝化此基团所在环,进行异环-取代。
NO2
Cl2 FeCl3
Cl N O 2
NO2
+
Cl
h
11
➢氧化反应
① 空气氧化
O
C
O2 / V2O5
O
400~500℃ C
O
② CrO3氧化
CrO3 / CH3COOH
10~15℃
h
邻苯二甲酸酐
O
1,4-萘醌 α-萘醌
O
12
➢加氢
N a+ C2 H5 O H
Na+C2H5OH
1,4-二氢化萘 1,2-二氢化萘
H2/Rh或Pt-C 加压、加热
十氢化萘
h
H2/Ni 或Pd-C 加压、加热
四氢化萘
13
7-3 蒽
命名
分子式C14H10,命名与萘相似, 蒽环也有固定的编号次序.
h
16
➢加成反应 蒽比苯易发生加成反应,多在9、10位。
Z n + H C l Na + C2H5OH
9,10-二氢化蒽
Br2 / CCl4 0℃
Br H
Br H
9,10-二溴-9,10-二氢化蒽
h
17
➢氧化
蒽比苯易氧化,发生在位。
O
O2 / V2O5 300~500℃
9,10O -蒽醌
O
K2Cr2O7 H2SO4
作业
1、(1)(2)(5) 2、(3)(6) 5、(2)(4) (6)(8) 6、(4)(5)
h
26
NH2
NO2
1,6-二硝基萘
C H3
Cl
6-氯-2-萘胺
S O3H
4-甲基萘磺酸
h
4
7-2 萘的结构、命名和性质
萘的结构
分子式为C10H8 , 平面结构,
0.1404 nm所有碳原子都是sp2杂化的,
是大π键体系.
0.1365 nm 0.1424 nm
0.1393 nm
萘分子中的碳-碳键长
并不相等, 说明萘环中各
第七章 多环芳烃和非苯芳烃
联苯和联多苯
多环芳烃 多苯代脂烃类
稠环芳烃
蒽
h
1
7-1 联苯
3′ 2′ 2 3
1′ 1
4′
4
5′ 6′
65
O2N O2N
2,4′-二硝基联苯
联苯的化学性质与苯很相似,两个
苯环上均可发生亲电取代反应。
混 酸 O2N
O2N
混酸
NO2
主要
O2N
h
O2N
2
7-2 萘的结构、命名和性质
磺酸受热力学控制, 产物的平衡常数大.
② 空间效应
h
8
磺化时的空间作用
H SO3H
H SO3H
α-萘磺酸
H
β-萘磺酸
应用:合成萘的β位衍生物
SO3H NaOH
+
H
300℃
亚硫酸铵 水溶液 150℃,加压
h
OH
NH2
布赫雷尔反应
9
② 萘环上的一元定位规律
A: 第一类定位基
活化此基团所在环,
进行同环-取代.
O
h
18
➢取代反应
卤代、硝化多是以9位(γ位)取代为主, 得到的是混合物。
Br
Br2 FeBr3
但磺化同萘类似, 多发生在位或位, 且 较低温度下为位取代, 较高温度下多为位
磺化。
H2SO4 高温
h
SO3H
19
7-4 菲
分子式C14H10,与蒽互为同分异构体。
性质与蒽相似, 可 发生加成、氧化、 取代等反应, 且多 发生于9、10位。
h
21
7-5 非苯芳烃及休克尔规则(4n+2规则)
由一个五元环和一个七元环稠合而 成, 其外围有10个π电子。
经测定, 该化合物偶极距 =1.0D( 烃 类, 应无偶极矩或偶极矩很小), 这说 明分子中发生了电子偏移.
原因:七元环中的一个电子转移到 + 五元环中, 则两个环都有6个电子, 符
合4n+2规则, 则两部分都有芳香性, 使体系能量降低, 分子稳定。该化合 物是一个芳香h 化合物, 具有芳香性。22
9 10
8
1
7
2
65 43
h
20
7-5 非苯芳烃及休克尔规则(4n+2规则)
① 单环化合物 ; ② 平面环状闭合的π电子离域体系(共轭体系); ③ π电子数符合4n+2(n=0,1,2,3 …)。
满足上述条件,该化合物即具有芳香性(难 加成、难氧化、易取代)。
如:环丙烯正离子、环戊二烯负离子、苯、环 庚三烯正离子、环辛四烯二负离子
萘的命名
——1,4,5,8位称位 ——2,3,6,7位称为位。
1 9
8
2
7
3
10
6
4
5
命名时, 不论取代基位置如何, 编号都要从
一个位开始, 并经过该环编到另一个环.
萘的衍生物的命名与苯的衍生物的命名相
似,选择母体同样要用到“优先次序”。
只是编号应遵守萘环的编号原则。
h
3
NO2
NO2
2-硝基萘 -硝基萘
轮烯 具有交替的单双键的环多烯烃, 通称为轮烯. 分子式:(CH)n,n≥10 命名:[n]轮烯
[10]轮烯——C10H10
HH
环癸五烯
π电子数10,n=2,但由
于轮内氢原子间斥力大,
使环发生扭转,不能共面,
故无芳香性。
h
23
[14]轮烯——C14H14
H HH H
环十四碳七烯 [18] 轮烯——C18H18
π电子数14,n=3,但 仍无芳香性。
H HH HH
H
环十八碳 九烯
[18]轮烯受热至230℃仍然稳定,可发生溴代,硝 化等反应,足可见其芳性。
[26] 轮烯 目前已知的最大的芳香性轮烯。
h
24
多环芳烃小结
【本章重点】 萘、蒽的命名及化学性质。
【本章难点】 萘、蒽的化学性质。
【教学要求】 ✓了解联苯及其衍生物的命名、性质; ✓ 掌握萘、蒽的命名及化学性质; ✓ 掌握休克尔规则及其应用; ✓ 其它稠环芳烃(了h解其致癌性)。 25
8
9
1
7
2
CH3
9-甲基蒽
6 5 10
3 4
-甲基蒽
1,4,5,8位——位
2,3,6,7位——位
9, 10 位——γ位
h
C2H5 2-乙基蒽
-乙基蒽
14
7-3 蒽
蒽的结构
平面结构, 所有碳原子 0.1408 nm 为sp2杂化, 是大π键体
系.
蒽环中各碳原子的P
0.1396 nm 0.1370 nm
