工程热力学课程纲要-物理化学-上海交通大学
上海交通大学物理化学PPT 化学平衡
将化学势表示式代入 ( r Gm )T , p 的计算式,得:
( r Gm )T , p
fB B B B (T ) B RT ln $ p B B B fB rG (T ) B RT ln $ p B
$ m
$ $ G ( T ) 令: r m B B (T ) B
自发
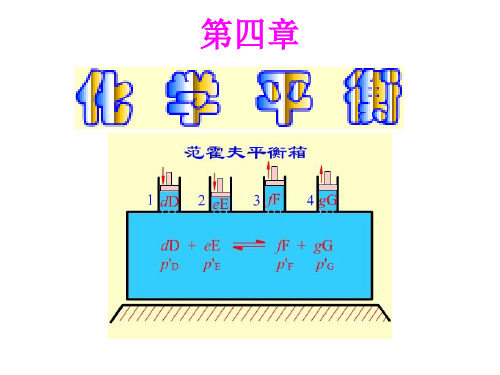
例: NO2气体溶于水可生成硝酸。但NO2气体也很容易发生双聚,生 成 N2O4,N2O4亦可解离,生成NO2,二者之间存在如下平衡:
N 2O4 (g) 2NO2 (g)
已知25 ℃下的热力学数据如下表所示
物质 NO2 N 2 O4
$ fH m / kJ mol -1
$ Sm / kJ mol -1 K
G 用 ( )T , p , B B 或 ( r Gm )T , p 判断都是等效的。 B
(r Gm )T , p 0 反应自发地向右进行
(r Gm )T , p 0
( r Gm )T , p 0
反应自发地向左进行,不可能自发 向右进行 反应达到平衡
用(
G ) T , p 判断,这相当于 G ~ 图上曲线的斜率,
θ
K K p p
θ
θ
p Ky θ p
p Kn θ p n 总
(2)实际气体反应体系
i i
fi RT ln p
i
fi pi i
令K f fi
v
K Kf ( p )
3.为什么化学反应通常不能进行到底?
以反应 D E 2F 为例,在反应过程中吉布斯自 由能随反应过程的变化如图所示。 R点,D和E未混合时吉布 斯自由能之和; P点,D和E混合后吉布斯 自由能之和; T点,反应达平衡时,所有 物质的吉布斯自由能之总 和,包括混合吉布斯自由 能; S点,纯产物F的吉布斯自由能。
《材料热力学》教学大纲.

《材料热力学》教学大纲课程名称:材料热力学/ Material Thermodynamics课程编号:050306学时:32 学分:2先修课程:大学化学、大学物理、物理化学适用专业:材料科学及工程专业大学本科开课院系:材料学院教材:江伯鸿.《材料热力学》.上海交通大学出版社.1999年一、课程的性质和任务本课程是材料科学与工程类专业的一门专业基础课。
学习本课程的主要目的是使学生能以热力学原理和方法研究材料,较全面系统地获得材料相变的热力学原理。
学生学习本课程后,能将宏观热力学与统计热力学结合起来,能用微观机制诠释宏观规律,从而更深刻地理解和掌握热力学的基本原理,为后续课程的学习打下基础。
二、教学内容和基本要求第一章绪论§1-1 材料热力学研究对象§1-2 几个基本概念§1-3 理想气体状态方程第二章热力学第一定律第三章热力学第二定律第四章封闭体系中热力学的基本方程和性质间的关系§4-1 Gibbs公式§4-2 对应系数关系式和Mexwell关系式§4-3 热力学关系式的应用第五章敞开体系与溶液§5-1 敞开体系的热力学函数§5-2 理想溶液§5-3 稀溶液§5-4 非理想溶液§5-5 溶液的准化学模型§5-6 聚合物溶液第六章相平衡与相图§6-1 相平衡与相律§6-2 单元系的复相平衡§6-3二元系中的相平衡与相图§6-4 二元相图的规律第七章表面与界面§7-1 表面能与表面张力§7-2 润湿现象及毛细管现象§7-3 曲界面热力学§7-4 表面吸附与内吸附第八章统计热力学基础§8-1 统计热力学概述§8-2 熵的统计概念§8-3 理想气体的状态方程三、实验与讨论课的内容和基本要求本课程不安排实验。
资料:上海交通大学810传热学考研大纲

上海交通大学动力工程与工程热物理考试大纲与解析一、专业科目与代码:810传热学二、指定参考书《传热学》(第4版)杨世铭陶文铨高等教育出版社 2006.8《传热学重点难点及典型题精解》王秋旺西安交通大学大学出版社 2001.10三、810动力工程与工程热物理考试大纲(传热学)与解析一、序论1.热量传递的基本方式及传热机理[conduction, convection, radiation,总结三种方式传热原理以及区别]2.一维傅立叶定律的基本表达式及其中各物理量的定义.单位。
[q=λdtdx,基本公式]3.牛顿冷却公式的基本表达式及其中各物理量的定义.单位。
[q=ℎΔt,h为过程量,区别状态量λ]4.黑体辐射換热的四次方定律基本表达式及其中各物理量的定义.单位。
[q=εσT4,黑度ε,玻尔兹曼常量σ,热力学温度T]5.传热过程及传热系数的定义及物理意义。
[传热过程概念、区别传热过程系数和表面传热系数]6.热阻的概念,对流热阻.导热热阻的定义及基本表达式。
[1Aℎ,δAλ]7.接触热阻及污垢热阻的概念。
8.使用串联热阻叠加的原则和在換热计算中的应用。
[原理与电路相似]9.对流热换和传热过程的区别。
表面传热系数(对流換热系数)和传热系数的区别。
10.导热系数,表面传热系数和传热系数之间的区别。
[过程量与状态量,物性参数相同(温度压力)导热系数一定,表面传热系数和流动过程量(流动速度、状态等)有关,过程不同大小不同,不是恒定的]二、导热基本定律及稳态导热1.矢量傅立叶定律的基本表达式及其中各物理量的定义.单位。
[负号表示热流方向与温度升高方向相反]2.温度场.等温面.等温线的概念。
[等温线(面)上温度相同、区域内温度分布叫做温度场]3.利用能量守恒定律和傅立叶定律推导导热微分方程的基本方法。
[能够推导传热微分方程,以及无内热源、常物性稳态、一维等特殊条件的简化]4.使用热阻概念,对通过单层和多层面板.圆筒和球壳壁的一维导热问题的计算方法。
《工程热力学》课程教案

《工程热力学》课程教案***本课程教材及主要参考书目教材:沈维道、蒋智敏、童钧耕编,工程热力学(第三版),高等教育出版社,2001。
6手册:严家騄、余晓福著,水和水蒸气热力性质图表,高等教育出版社,1995。
5 实验指导书:华北电力大学动力系编,热力实验指导书,2001参考书:曾丹苓、敖越、张新铭、刘朝编,工程热力学(第三版),高等教育出版社,2002.12王加璇等编著,工程热力学,华北电力大学,1992年。
朱明善、刘颖、林兆庄、彭晓峰合编,工程热力学,清华大学出版,1995年。
曾丹苓等编著,工程热力学(第一版),高教出版社,2002年全美经典学习指导系列,[美]M。
C. 波特尔、C.W. 萨默顿著郭航、孙嗣莹等译,工程热力学,科学出版社,2002年。
何雅玲编,工程热力学精要分析及典型题精解,西安交通大学出版社,2000。
4概论(2学时)1. 教学目标及基本要求从人类用能的历史和能量转换装置的实例中认识理解:热能利用的广泛性和特殊性;工程热力学的研究内容和研究方法;本课程在专业学习中的地位;本课程与后续专业课程乃至专业培养目标的关系.2。
各节教学内容及学时分配0-1 热能及其利用(0.5学时)0-2 热力学及其发展简史(0。
5学时)0—3 能量转换装置的工作过程(0.2学时)0-4 工程热力学研究的对象及主要内容(0.8学时)3。
重点难点工程热力学的主要研究内容;研究内容与本课程四大部分(特别是前三大部分)之联系;工程热力学的研究方法4. 教学内容的深化和拓宽热力学基本定律的建立;热力学各分支;本课程与传热学、流体力学等课程各自的任务及联系;有关工程热力学及其应用的网上资源。
5。
教学方式讲授,讨论,视频片段6。
教学过程中应注意的问题特别注意:本课程作为热能与动力工程专业学生进入专业学习的第一门课程(专业基础课),要引导学生的学习兴趣和热情。
另,用例应尽量采用较新的事实和数据。
7. 思考题和习题思考题:工程热力学的宏观研究方法与微观方法的比较作业:(短文,一、二页即可)网络文献综述——能源利用与工程热力学8。
工程热力学-西安交通大学教师个人主页

“工程热力学”多媒体课件程热力Engineering Thermodynamics《工程热力学》(上海交通大学、南京航空航天大学、哈尔滨工业大学等)多媒体教学课件的基础上,结合本校的教学特点和个人理解能力,而独立整理完成的适合于热能动力专业学生学习的多©2019 Y.W Liu. All Rights Reserved.2019 Y.W Liu. All Rights Reserved.、给出结果。
[作业范本]工程热力学-绪论©2019 Y.W Liu. All Rights Reserved.“工程热力学”多媒体课件《大英百科全书》对能源的解释为“能源是一个包括所有燃料、流水、阳光和风的术语,人类采用适当的转换手段,给如燃料、水力、风力等”。
凡是能直接或者经过转换而获取某种能量的自然资源统称为能源能源及其利用©2019 Y.W Liu. All Rights Reserved.水力能、风能、波浪能、生物质能、海洋温差能、化石燃料(煤炭、石油、天然气)地球与其它天体(月球等)相互作用的能源地球上的能量来源工程热力学-绪论©2019 Y.W Liu. All Rights Reserved.和煤、石油、天然气、核燃料等 能源存在形态使用程度能源本身性质污染程度©2019 Y.W Liu. All Rights Reserved.2019 Y.W Liu. All Rights Reserved.050100150200250300350400$0$5,000$10,000$15,000$20,000$25,000$30,000$35,000$40,人均 GDP ,US$ 1995 pppGlobal Trend EU-15North AmericaKorea 1970-2000Malaysia 1970-2000China 1970-2002工程热力学-绪论“工程热力学”多媒体课件世界各国经济发展和人类生活的实践证明:在经济正常发展的情况下,能源消耗总量和能源消耗增长速度与国民经济生产总值、国民经济生产总值增长率成正比例关系。
(精品)工程热力学(全套467页PPT课件)

我国能源现状
据预测,目前中国主要能源煤炭、石油和天然气的储 采比分别为约80、15和50,大致为全球平均水平的 50%、40%和70%左右,均早于全球化石能源枯竭 速度。
工程热力学
Engineering Thermodynamics
绪论
工程热力学属于应用科学(工程科学) 的范畴,是工程科学的重要领域之一。
工程热力学 是一门研究热能有效利用及 热能和其 它形式能量转换规律的科学
工程热力学所属学科
工
工程热力学
程
传热学 Heat Transfer
热
流体力学 Hydrodynamics
工程热力学是节能的理论基础
能量转化的一般模式
一
次 能
热能
源
电能 机械能
问题:下面哪些是热机,哪些不是?
燃气轮机、蒸气机、汽车发动机、燃料电池、制冷机、 发电机、电动机
能量转化的一般模式
风 能
燃
水 能
化 学 能
料 电 池
风 车
水 轮 机
水 车
燃 烧
核 能
聚裂 变变
热
生物质
地太 热阳 能能
利 光转 用 热换
大气压(at),毫米汞柱(mmHg),毫米水柱(mmH2O)
1 kPa = 103 Pa
1bar = 105 Pa
换 1 MPa = 106 Pa
算 关
1 atm = 760 mmHg = 1.013105 Pa
工程图学课程教学大纲-上海交通大学智能机器人试验室

《测量与控制技术》课程教学大纲课程名称:测量与控制技术课程代码:学分/学时:4学分/68学时开课学期:春季学期适用专业:机械工程及自动化、热能与动力工程、核工程、航空航天工程先修课程:《大学物理》、《高等数学》、《电工与电子技术G类》、《模型、分析与系统控制》、《理论力学》、《工程热力学》、《工程流体力学》、《机械振动》后续课程:《机械与动力综合实验》开课单位:机械与动力工程学院一、课程性质和教学目标(需明确各教学环节对人才培养目标的贡献,专业人才培养目标中的知识、能力和素质见附表)课程性质:《测量与控制技术》是机械工程、热能动力工程、核科学与工程、航空航天工程等专业的一门重要技术基础课,是机械、能源动力类专业必修主干课。
教学目标:《测量与控制技术》是一门与工程实际密切结合的课程,它的主要任务是通过各教学环节,应用各种教学手段,使学生掌握如何测量、处理和分析信号,掌握工程中常用的控制技术和方法,并将两者结合,实现完整的测控系统。
本课程不仅为学生提供必要的基础理论知识,重点培养学生利用专业技能分析解决问题的能力,为学生从事与测试、控制相关专业技术工作、科学研究工作等打下坚实的基础。
具体来说:(1)测量与控制技术的概述,了解传感、信号获取、处理和反馈控制、计算机集成应用等各关键技术环节。
(A5.1)(2)掌握机械自动化系统中常用的测量传感器和测量装置的特性(A5.1)(3)掌握常用的信号测量和处理方法,能根据工程实际的要求,对静动态实验数据的描述,设计基本的测量系统(A5.2)(4)掌握常用的控制方法(数字和模拟控制),初步具有从实际问题抽象为理论,并运用理论分析解决实际问题能力。
(A5.1, B2,B3)(5)了解常用的控制电路的与控制器件,掌握从测量、传感与控制系统的设计和实现方法(A5.2)(6)测量与控制系统工程设计实例讲解(A5.3, A5.4)(7)强化实践教学,通过信号测量、单片机和可编程控制器的实践环节,培养学生对系统分析能力和动手能力。
物理化学-第二章-热力学第一定律及其应用精选全文

上一内容 下一内容 回主目录
返回
2024/8/13
状态与状态函数
状态函数的特性: 异途同归,值变相等;周而复始,数值还原。
状态函数的性质:
(1) 状态函数的值取决于状态,状态改变则状态函数必定改 变(但不一定每个状态函数都改变);任何一个状态函数 改变,系统的状态就会改变。
上一内容 下一内容 回主目录
即
ΔU=Q+W (封闭系统)
对于无限小过程,则有
dU=δQ+δW (封闭系统)
上一内容 下一内容 回主目录
返回
2024/8/13
3. 焦耳实验 盖.吕萨克—焦尔实验
实验结果:水温未变 dT=0 dV≠0
表明:Q =0
自由膨胀 W=0
上一内容 下一内容 回主目录
返回
2024/8/13
dU= Q+ W =0
1. 热(heat)
a) 定义:体系与环境之间因温差而传递的能量称为热,用 符号Q 表示。单位:KJ 或 J。 b) Q的取号:体系吸热,Q>0;体系放热,Q<0 。
c) 性质:热不是状态函数,是一个过程量;热的大小和具 体的途径有关。
上一内容 下一内容 回主目录
返回
2024/8/13
功和热
不能说在某个状态时系统有多少热量,只能说 在某个具体过程中体系和环境交换的热是多少。
热力学能是状态函数,用符号U表示,单位为J。它 的绝对值无法测定,只能求出它的变化值。
U= U2 –U1
上一内容 下一内容 回主目录
返回
2024/8/13
热力学能
纯物质单相系统
若n确定
U=U ( n,T,V ) U=U (T,V )
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物理化学教学大纲课程名称:物理化学A(2)(3)Physical Chemistry 课程性质:专业基础课学时:102学时授课对象:化学专业本科生授课学期:第三、第四学期考试方式:闭卷式笔试+平时作业2009年4月★前言化学与物理学之间的紧密联系是不言而喻的:化学过程包含或是伴有物理过程,而分子中电子的运动,原子的转动、振动,分子中原子相互间的作用力等微观物理运动形态,则直接决定了物质的性质及化学反应能力。
人们在长期的实践过程中注意到这种相互联系,并且加以总结,逐步形成一门独立的学科分支叫做物理化学。
物理化学是从物质的物理现象和化学现象的联系入手来探究化学变化基本规律的一门科学,在实验方法上也主要是采用物理学中的方法。
化学是一门中心学科,它与社会多方面的需要有关。
进入20世纪的前期,在工业生产和化学的科学研究中,物理化学的基本原理得到了广泛应用,发挥了它的指导作用,特别是新兴的石油炼制和石油化工工业,更是充分地利用了化学热力学、化学动力学、催化和表面化学等的成果。
而工业技术的发展和其他学科的发展,特别是物理学的进展和各种测试手段的大量涌现,极大的影响着物理化学的发展。
在物理化学所属的分支领域中如结构化学、热化学、化学热力学、电化学、溶液理论、流体界面化学、化学动力学、量子化学、催化化学及其理论等都得到了迅速的发展。
现代物理化学是研究所有物质体系的化学行为的原理、规律和方法的学科,涵盖从宏观到微观与性质的关系规律、化学过程机理及其控制的研究,是化学以及在分子层次上研究物质变化的其他学科领域的理论基础。
作为化学学科的一个重要分支,物理化学所担负的主要任务是探讨和解决化学变化的方向和限度问题、化学反应的速率和机理问题及物质结构和性能之间的关系问题,这三方面问题往往是相互联系、相互制约而不是孤立无关的。
在探讨和解决这些问题的过程中逐渐了解化学变化在客观上存在的规律性,有助于我们了解世界、能动地改造客观世界,使之为我们所用。
★先修课程:无机化学、分析化学、有机化学、基础化学实验、大学数学、大学物理等。
★适用专业:化学专业。
★教材:《物理化学》(第五版),傅献彩等编,高等教育出版社,2005★教学参考书:《物理化学》,高丕英李江波编,科学出版社;《物理化学》,胡英等编,第四版,高等教育出版社。
Physical Chemistry.6th ed., Atkins P.W.,Oxford University Press.(有中译本)《物理化学习题精解与考研指导》,高丕英李江波编,上海交通大学出版社;Physical Chemistry.7th ed., Atkins P.W.,Oxford University Press.(有中译本)附:关于教材本课程采用的教材是由南京大学教师编写高等教育出版社出版(2005年)的《物理化学》(第五版),它是普通高等教育“十一五”国家级规划教材。
第五版是在第四版的基础上,遵照教育部高等学校化学与化工学科教学指导委员会2004年通过的“化学专业和应用化学专业化学教学基本内容”进行了适当的调整和增删,并总结近年来教学研究和教学改革成果修订而成的。
全书重点阐述了物理化学的基本概念和基本理论,同时考虑到不同读者的需要也适当介绍了一些与学科发展趋势有关的前沿内容。
★本课程的性质、地位、作用和任务本课程是高等院校化学专业的一门重要基础课,为化学专业二级学科。
课程以化学热力学、化学动力学、电化学、表面化学和胶体化学为基本结构,主要内容有化学热力学第一、二、三定律、相平衡和化学平衡;电解质溶液、可逆电池的电动势、电解与极化作用;化学动力学基础一、二;表面化学和胶体化学。
通过对本课程的学习,一方面使学生掌握物理化学的基本知识,掌握处理问题的基本方法;了解该研究领域的一些新进展,从而进一步扩大知识面,打好专业基础,加深对先行课程如无机化学、有机化学、分析化学的理解,做到知识面宽、基础深。
另一面进一步培养学生的独立工作能力,提高学生的自学能力,学习前人提出问题、考虑问题和解决问题的方法,逐步培养独立思考和独立解决问题的能力,以便在生产实践和科学研究中碰到问题时,能得到一些启发和帮助。
★实施本课程教学任务的方法、手段本课程以课堂讲授为主、自学和讨论为辅的方式组织教学,采用多媒体投影辅助教学手段,并通过阅读主要参考书目、网上查询、资料整理和专题讨论,加深对物理化学基本原理的了解,并掌握该学科的前沿发展动态。
对每章进行一次习题课,以巩固难掌握的知识点,并掌握运用物理化学方法初步解决问题的能力。
物理化学课堂教学纲要绪论(1 学时)一、知识点着重阐明物理化学的意义、介绍物理化学的研究内容以及学习物理化学的方法。
二、教学内容与教学方法教学内容1. 物理化学的建立与发展2. 物理化学的目的和内容3. 物理化学的研究方法4. 物理化学课程的学习方法教学方法以教师讲授为主,穿插大量实例,启发学生思考,重点为介绍物理化学的学习方法。
第二章热力学第一定律(9 学时)一、知识点群● 系统、环境● 热力学平衡态、状态函数、热和功●准静态过程、可逆过程● 热力学第一定律●Joule-Thomson 效应●热效应、Hess定律●Kirchhoff定律二、教学内容与教学方法教学内容2.1 热力学概论2.2 热平衡和热力学第零定律----温度的概念2.3 热力学的一些基本概念系统与环境系统的状态和性质热力学平衡态与状态函数状态系数热和功2.4 热力学第一定律热力学第一定律的表述法与数学表达式;热力学能;准静态过程与可逆过程;功与过程2.5 准静态过程与可逆过程功与过程准静态过程可逆过程2.6焓2.7 热容热容及热量的计算C p与C V之间的关系2.8 热力学第一定律对理想气体的应用盖·吕萨克—焦耳实验相变过程和化学过程绝热过程的功和过程方程式2.9 Carnot循环Carnot循环热机效率冷冻系数2.10 Joule-Thomson效应----实际气体的ΔU和ΔHJ-T 效应J-T 系数与J-T 转化温度实际气体的ΔU和ΔH2.11 热化学化学反应的热效应反应进度热化学方程式2.12 盖斯定律2.13几种热效应标准摩尔生成焓燃烧焓溶解热和稀释热由键焓估算反应热2.14 反应焓变与温度的关系----基尔霍夫定律2.15 绝热反应----非等温反应2.16*热力学第一定律的微观说明教学方法以教师讲授为主,学生自学和课堂讨论为辅,学习重点为热力学的基本概念和热力学第一定律,可通过实例辅以课后习题加深学生对其理解,以及对准静态过程和可逆过程的理解。
三、教学目标通过对热力学第一定律的学习使学生了解热力学的一些基本概念,如体系、环境、状态、功等;明确热力学第一定律和内能的概念;了解热力学方法的特点,特别是要了解状态函数、准静态过程和可逆过程的概念;了解热力学第一定律的一些应用,如热化学和理想气体在几种过程中功和热量的计算等,能够较熟练地应用热力学第一定律,从微观角度了解热力学第一定律的本质。
第三章热力学第二定律(12 学时)一、知识点群● 热力学第二定律●Carnot定理● 熵、Clausius不等式●Helmbolz 自由能、Gibbs自由能● 热力学第三定律二、教学内容与教学方法教学内容3.1 自发变化过程的共同特征----不可逆性3.2 热力学第二定律3.3 卡诺定律3.4 熵的概念3.5 Clausius不等式与熵增加原理Clausius不等式熵增加原理3.6 热力学基本方程与T-S图T—S图及其应用3.7 熵变的计算等温过程ΔS的计算非等温过程ΔS的计算3.8 熵和能量退降3.9 热力学第二定律的本质和熵的统计意义热力学第二定律的本质Boltyman公式3.10 亥姆霍兹自由能和吉布斯自由能Helmbolz 自由能Gibbs自由能3.11 变化的方向和平衡条件3.12 ΔG 的计算示例等温物理变化过程ΔG化学变化过程ΔG —化学反应等温式3.13 几个热力学函数的关系基本公式特性函数Maxwell 关系式及其应用Gibbs自由能与温度、压力的关系3.14 热力学第三定律与规定熵热力学第三定律规定熵值化学反应过程中的ΔS计算3.15 绝对零度不能达到原理----热力学第三定律的另一种表述法3.16 不可逆过程热力学简介教学方法以教师讲授为主,学生自学和课堂讨论为辅,学习重点为热力学第二定律、熵的意义及ΔG、ΔS的计算。
三、教学目标通过本章的学习使学生明确热力学第二定律的意义,了解自发变化的共同性质;了解热力学第二定律与卡诺定理的联系,理解克劳修斯不等式的重要性;熟记热力学函数U、H、S、F、G 的定义,了解其物理意义;能熟练运用吉布斯-亥姆霍兹公式、克拉贝龙和克劳修斯-克拉贝龙方程式,能够利用范霍夫等温式来判别化学变化的方向;了解熵的统计意义,明确偏摩尔量和化学势的意义及它们之间的区别;初步了解热力学第三定律的内容。
第四章多组分系统热力学及其在溶液中的应用(7学时)一、知识点群● 偏摩尔量● 化学势●Raoult 定律、Henry 定律●稀溶液的依数性●活度、活度因子● 分配定律二、教学内容与教学方法教学内容4.1 引言4.2 多组分系统的组成表示法4.3 偏摩尔量与化学势偏摩尔量的定义及其集合公式Gibbs-Duhem 公式4.4 化学势化学式的定义及其在相平衡中的应用化学势与T、P的关系4.5 气体混合物中各组分的化学势理想气体及其混合物的化学势非理想气体混合物的化学势----逸度的概念逸度因子的求法4.6 稀溶液中的两个经验定律Raoult 定律Henry 定律4.7 理想液态混合物理想液态混合物的定义理想液态混合物中任一组分的化学势理想液态混合物的通性4.8 理想稀溶液中任一组分的化学势4.9 稀溶液的依数性4.10 Duhem -Margules 公式4.11 活度与活度因子非理想溶液中各组分的化学势—活度的概念非理想稀溶液双液系中活度因子之间的关系4.12 渗透因子和超额函数溶剂A的渗透因子超额函数4.13 分配定律—溶质在两互不相溶液相中的分配4.15 绝对活度教学方法教师讲授和引导学生共同思考方式。
三、教学目标本章主要介绍溶液的热力学(即热力学第一、第二定律在多组分体系中的一些应用),引入了理想溶液、活度、逸度、标准态、超额函数等概念,介绍了理想溶液以及非理想溶液中任一组分的化学势的表示法。
这些表示法在处理溶液中的问题(相平衡和化学平衡)是很有用。
此外还介绍了稀溶液中两大经验定律:拉乌尔定律和亨利定律。
学习本章的具体要求是:熟悉溶液浓度的各种表示法及其相互关系;了解什么是理想溶液、理想溶液的通性;了解拉乌尔定律和亨利定律的区别;了解活度和逸度的概念;能够熟练表示溶液中各组分的化学势,了解从微观角度讨论溶液形成是一些热力学函数的变化;了解稀溶液依数性公式的推导,以及分配定律的推导,了解热力学处理溶液问题的一般方法。
