急性髓系细胞白血病
急性髓细胞白血病
急性髓细胞白血病要点1:分类M1(急性粒细胞白血病微分化型)、M2(急性粒细胞白血病部分分化型)、M3(急性早幼粒细胞白血病)、M4(急性粒-单核细胞白血病)、M5(急性单核细胞白血病)、M6(急性红白血病)和M7(急性巨核细胞白血病)。
要点2:急性粒细胞白血病外周血基本特点:贫血、部分白血病可见幼红细胞,例如M1、M6和M7;白细胞数多数增高,但有的病例可以正常,甚至减少,减少多见于M6和M7;出现大量幼稚细胞,特别是原始细胞是主要的特征,原始和幼稚细胞应超过30%;M3以异常早幼粒细胞为主,可高达90%;M4原单和幼单细胞可占30%~40%,M5原单和幼单可占30%~45%。
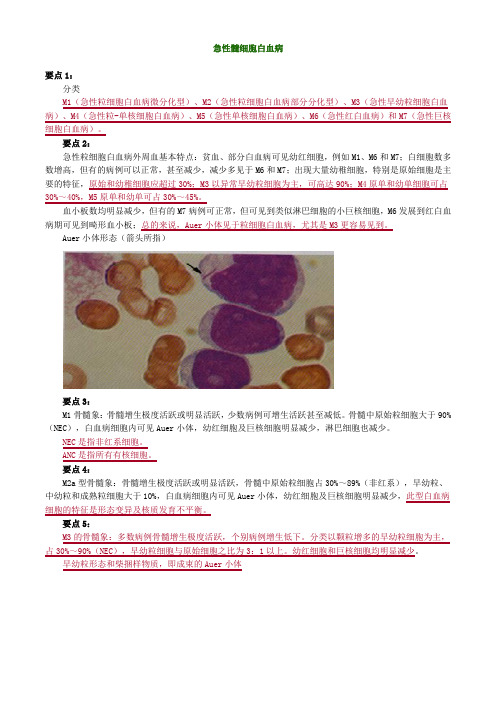
血小板数均明显减少,但有的M7病例可正常,但可见到类似淋巴细胞的小巨核细胞,M6发展到红白血病期可见到畸形血小板;总的来说,Auer小体见于粒细胞白血病,尤其是M3更容易见到。
Auer小体形态(箭头所指)要点3:M1骨髓象:骨髓增生极度活跃或明显活跃,少数病例可增生活跃甚至减低。
骨髓中原始粒细胞大于90%(NEC),白血病细胞内可见Auer小体,幼红细胞及巨核细胞明显减少,淋巴细胞也减少。
NEC是指非红系细胞。
ANC是指所有有核细胞。
要点4:M2a型骨髓象:骨髓增生极度活跃或明显活跃,骨髓中原始粒细胞占30%~89%(非红系),早幼粒、中幼粒和成熟粒细胞大于10%,白血病细胞内可见Auer小体,幼红细胞及巨核细胞明显减少,此型白血病细胞的特征是形态变异及核质发育不平衡。
要点5:M3的骨髓象:多数病例骨髓增生极度活跃,个别病例增生低下。
分类以颗粒增多的早幼粒细胞为主,占30%~90%(NEC),早幼粒细胞与原始细胞之比为3:1以上。
幼红细胞和巨核细胞均明显减少。
早幼粒形态和柴捆样物质,即成束的Auer小体早幼粒形态和柴捆样物质,即成束的Auer小体要点6:M4型骨髓象:骨髓增生极度活跃或明显活跃。
粒、单核两系同时增生,红系、巨核系受抑制。
急性髓系白血病微小残留病检测与临床解读

和NGS等方法在患者体内检测不到白血病细胞;部分MRD阴性患者可再 次转为MRD阳性导致晚期复发;部分患者获得临床治愈(图1)。
二、MRD的概念和检测方法
(二)分子学方法检测MRD
2.分子标志检测MRD的技术要求: 应用1 μg RNA逆转录为cDNA,每次反应的cDNA相当于100 ng RNA(约
为200 000个细胞,如果基因表达水平高则需要的细胞数量少)。 对于基于DNA的方法,每次反应需要至少100 ng DNA(约为15 000个细
此外,包括RUNX1、GATA2、CEBPA、DDX41和ANKRD26在内的某些 胚系基因突变与AML发生风险相关,如果把这些基因突变作为MRD评估 的标志,就需要应用DNA测序的方法除外它们是胚系组织(皮肤组织、 毛囊或颊黏膜)来源的突变。
多个MRD分子标志物组合应用可克服单个分子标志物评估MRD的缺陷, 该缺陷包括AML亚克隆的异质性和CHIP的存在对MRD的影响等。
二、MRD的概念和检测方法
二、MRD的概念和检测方法
二、MRD的概念和检测方法
(一)MFC检测MRD
用于MFC评估表型异常白血病细胞的单克隆免疫荧光抗体包括CD34、 CD117、CD13和CD33,跨系表达抗原CD2、CD7、CD19和CD56等。
利用MFC检测MRD的方法包括白血病相关异常表型(LAIP)以及与正常 骨髓细胞表型相鉴别(D-F-N,different from normal),前者是指初诊时 确定患者的LAIP,在随后的治疗过程中利用LAIP进行MRD检测;后者可 用于缺乏初诊LAIP的患者,也可检测治疗过程中出现的抗原漂移 (Antigen shift)。
急性白血病分型及其特点
预后因素
一些预后因素包括年龄、白血病细胞的遗传异常和 治疗反应等,它们会对患者的预后产生影响。
急性白血病分型及其特点
急性白血病(Acute Leukemia)是一种白血病的类型,其特点是白血病细胞 的发展速度非常快,并且在短时间内大量增加。了解分型和特点有助于诊断 和治疗。
急性白血病的定义和背景
急性白血病是一种骨髓中恶性白血病细胞异常增生的疾病。它会影响造血系统,导致正常细胞的数量减少,而 白血病细胞的数量迅速增加。
克隆异常
淋巴细胞发生了遗传异常,导致其无法正常发育,从而形成了白血病细胞。
增殖速度快
淋巴母细胞迅速增殖,使其在骨髓中的比例迅速增加,抑制了正常造血细胞的产生。
急性髓系细胞白血病的特点
骨髓受侵
急性髓系细胞白血病以骨髓为中 心,造血系统中的干细胞出现恶 性增殖。
早幼粒细胞
髓系细胞白细胞特别是早幼粒细 胞的增生,使正常的造血细胞无 法充分发育和成熟。
染色体异常
急性髓系细胞白血病患者的染色 体有一些异常,这可能有助于诊 断和指导治疗。
其他非常见类型的急性白血病
1 急性单核细胞白血病
源于骨髓或外周血单核细胞的增殖异常,发病率较低。
2 急性浆细胞白血病
浆细胞白血病细胞异常形成,此类型白血病非常罕见。
3 急性轴突性髓细胞白血病
髓细胞白血病的一种亚型,以特定细胞的异常增生为特征。
不同类型急性白血病的诊断和治疗方法
1
诊断
通过骨髓穿刺、病理分析和染色体检查等
治疗
2
方法确定急性白血病的类型。
常见方法包括化疗、骨髓移植和靶向治疗
等,根据个体情况制定最佳治疗方案。
急性髓系白血病

急性髓系白血病育过程中不同阶段的造血祖细胞恶性变转化。
基本信息2主要病因白血病的病因和发病机制非常复杂,尽管这一领域的研究已经取得了很大的进展,但白血病的病因仍未被完全了解。
目前普遍认为,绝大多数白血病是环境因素与细胞的遗传物质相互作用引起的。
2、化学物质如油漆、苯、染发剂等通过对骨髓损害,也可诱发白血病。
最近北京的一份调查报告发现许多儿童白血病患者在半年来均做过室内装饰。
3、细胞毒药物致病:急性白血病与口服氯霉素可能有关,其它尚有氨基比林、安乃近、磺胺类、保泰松等。
4、病毒感染:近十年来的研究提示白血病很可能是病毒引起的。
病毒引起禽类、小鼠、大鼠、豚鼠、猫、狗、牛、猪、猴的白血病,此外,目前认为C类RNA肿瘤病毒与人类白血病的病因有关。
3诊断标准3.1英法美协诊断标准英法美协作组(FAB协作组)于1976和1985年先后提出了AML的形态学诊断标准及修改建议,1991年又增补一特殊亚型,即AML微分化型,先介绍如下。
(1)M0(急性髓系白血病微分化型):骨髓中原始细胞≥90%(NEC),胞浆大多透亮或中度嗜碱,五嗜天青及(或)CD13可阳性。
淋系抗原阴性,但可有CD7+,Td T+;电镜髓过氧化酶(MPO)阳性。
(2)M1(急性白粒细胞白血病未化型);原理细胞(I+II型)≥90%(NEC),其中至少有3%的原粒细胞过氧化至中性分叶核粒细胞>10%,单核细胞10%时,亦属此型。
核细胞(常为幼稚及成熟单核细胞)>20%。
2) 骨髓象如上所述,外周血中单核细胞系(包括原始、幼稚及成熟单核细胞)≥5X109/L。
3) 骨髓象如上所述,外周血单核细胞系<5×109/L,而血清溶菌酶以及细胞化学支持单核细胞数量显著者。
4) 骨髓象类似M2,而单核细胞系>20%,或血清溶菌酶超过正常(11.5±4)mg/L,的3倍,或尿溶菌酶超过正常(2.5mg/L)的3倍。
5) 骨髓象类似M2,而外周血单核细胞系≥5×109/L时亦可划分为M4。
急性髓性白血病的分类及其进展

02
03
04
05
三、FAB分类
FAB分类 --AL诊断标准
除临床症状、体征与血象外,骨髓形态学分类是诊断急性白血病的主要依据,尤其是原始细胞(包括原粒、原单核及原淋巴细胞)的百分比。
1845年,英国的Bennett 和德国的Virchow又分别报道一例血液中有大量脓样球体的类似病例
1856年,Virchow进一步对白血病做了综合描述,对血液中的这些无色或白色的球体的来源,提出了三种可能性:即血液、淋巴,也可能来自血管壁,并认为来自淋巴的可能性最大。
2
3
4
1
一、白血病的发现
二、白血病的分类
1917年,Di Guglielmo分出红白血病这一类型
1938年,单核细胞白血病分为粒-单核细胞白血病和单核细胞白血病
1938年,Forkner在《白血病及其有关疾病》一书中,将白血病分为急性和慢性两大类,急性白血病又分为髓细胞型、淋巴细胞型、单核细胞型
1957年,Hillested首先报道了急性早幼粒细胞白血病
WHO分类 -先决条件 1.白血病“原始细胞”的确定
“计数原始细胞要求分别分类May-Grunwald Giemsa染色的血和骨髓片200和500个细胞,必要时作骨髓活检核实。
1
在急性早幼粒细胞白血病(APL)中,原始细胞则指异常早幼粒细胞。
2
除在罕见的“纯”红白血病外,计数原始细胞时不包括红系前体细胞(有核红细胞),发育异常的小巨核细。
大量实践证实,MDS相关AML在临床和细胞生物学特征方面具有重要的独特意义,因此将具有多系病态造血的AML作为一种亚型。
成人急性髓系白血病治疗指南

成人急性髓系白血病治疗指南成人急性髓系白血病治疗指南引言:髓系白血病是一种恶性血液疾病,其中成人急性髓系白血病(Adult Acute Myeloid Leukemia, AML)是最常见的类型之一。
由于它的快速进展和高度侵袭性,寻找最佳的治疗方法至关重要。
本文将使用现有的临床经验和专家建议,为成人急性髓系白血病的治疗提供指南。
一、诊断与分期1. 临床表现:成人急性髓系白血病的主要表现包括出血、感染、贫血和骨痛等症状。
临床医生应仔细评估患者的症状和体征,以初步确定诊断。
2. 血常规与骨髓穿刺:对于疑似患者,应及时进行血常规和骨髓穿刺检查。
血常规可以观察到异常的血细胞计数及形态,而骨髓穿刺则可以确定细胞遗传学异常,并进一步明确诊断。
3. 分期:根据法国美国英国协作小组(French-American-British Cooperative Group, FAB)制定的分期系统,可以将成人急性髓系白血病分为M0至M7七个亚型。
这有助于更准确地指导治疗方案的选择。
二、治疗原则1. 合作治疗:成人急性髓系白血病的治疗需要多个学科的合作,包括内科、血液学、放射学、病理学等。
医生们应进行全面评估,并根据患者的病情选择最佳的治疗方案。
2. 化疗:化疗是成人急性髓系白血病治疗的基础。
根据患者的年龄、性别、细胞遗传学异常和分期等因素,选择适当的化疗药物和方案。
常用的化疗药物包括阿糖胞苷、阿霉素、环磷酰胺等。
3. 骨髓移植:对于高危、复发或难治的患者,骨髓移植是一种有效的治疗手段。
可以选择同种异基因骨髓移植或自体骨髓移植,但需要严格的配型和免疫抑制治疗。
4. 其他治疗方法:除了化疗和骨髓移植,还可以考虑使用靶向治疗药物、干细胞因子和放射治疗等辅助治疗手段。
这些方法在疗效和副作用方面与传统治疗不同,应根据患者实际情况进行选择。
5. 支持治疗:成人急性髓系白血病治疗过程中,常常伴随着一系列副作用和并发症,例如骨髓抑制、感染和出血。
急性髓性白血病-病例分析

由于两性霉素B需与麦角固醇结合 而发挥作用. 而三唑类抗真菌药物则抑制其合成。 二者联用目前尚有争议。
目前卡泊芬净联合其他抗真菌药物治 疗IFI受到关注。 •因卡泊芬净可增加细胞的通透性, 因此有利于两性霉素B和唑类穿过细 胞壁,这就意味着卡泊芬净与其他两 种药物联用可能表现出很好的协同作 用。
白血细小胞板计数变化趋势图
粒缺期预防感染
<<2010 IDSA--中性粒细胞减少肿瘤患者抗菌药物应用 临床实践指南>> : 高危患者在中性粒细胞减少时发热的初始经验性抗菌 治疗:推荐单用β内酰胺类药物,例如: 头孢吡肟 碳青霉烯类(美罗培南或亚胺培南-西司他丁) 哌拉西林-三唑巴坦治疗(A-Ⅰ)
半数为早期表现
主乏发要 所与致热粒的细感胞染缺或
白血病本身有关
半数患者就诊时已
有贫重度血贫血,尤其
是继发于骨髓增生 异常综合征者
主要与PLT减少
和出凝血血功能异常
有关
临
床
现
表 淋巴结和肝脾肿大, 骨组骼和织关器节官疼浸痛润、中 枢神经系统白血病、 粒细胞肉瘤、皮疹等
病例简介
3月12日
维甲酸综合症
本次入院后化疗方案 第2周期化疗, 方案采用高三尖杉酯碱 4mg×7d、
阿糖胞苷 150mg×7d, 临床需注意肝功能损害、心肌损害、骨髓抑制等副作用。
予粒1/细8头细多血h菌孢静胞次液热培哌滴严血科养,酮,重培沟可暂舒预缺养通继未巴防乏及,续发坦,感中 患目现3建染心 者氟g真前致刘 欠议。、静 近康菌用病主 佳脉 两唑治菌药任 ,导 日胶疗,表 须每管 高囊,与示 联日伏首单 合5立剂0用卡m康量伏泊g唑7静立芬0粉滴m康净针g唑强,效化以果抗后
【培训课件-;临床血液学】_急性髓系白血病

一、M1 急性髓系白血病,未分化型
【概述】 临床特点:
①起病急骤,进展迅速,病情凶险 ② 常伴有严重感染、发热和出血、贫血
口腔粘膜和咽喉常有炎症、溃疡和坏死 ③肝脾淋巴结肿大,但较急淋少见,且程 度轻 ④绿色瘤(chloroma)常见
绿色瘤常见
A B C
【检验】
1、血象 贫血显著, Hb<60g/L WBC总数升高,(10-50)×109/L 血片中以原始粒细胞为主,可见畸形原粒 血小板中-重度减少,半数在50×109/L以下
四、免疫学检验:粒系抗体均可阳性 五、遗传学和分子生物学检验:此型不特异
诊断
• 符合急性白血病诊断标准 • 骨髓中原始粒细胞30%-89%(NEC)并伴形态学异
常 • 单核细胞<20%,早幼粒以下细胞>10% • 免疫表型
三、 M2b 急性髓细胞白血病部分成熟性
ª又称为亚急粒 ª亚急性过程,起病缓慢,以贫血为首发症状 ª出血发生率较低,以皮肤淤点和鼻出血为主 ª骨髓中以中性中幼粒为主 ª髓外浸润发生率高 ª治疗反应好,完全缓解率高 ª特异性遗传标志:t(8:21)染色体易位
骨髓象
三、细胞化学染色 POX、SBB,ACP染色:均阳性 AS-D-NCE阳性,NaF不抑制 α-NBE阴性(主要 存在于单核细胞),与急单鉴别
四、超微结构检验: 电镜对细颗粒型的诊断有价值 五、免疫学检验: CD13、CD33阳性 CD34及HLA-DR阴性 六、遗传学和分子生物学:
染色体t(15;17)形成PML/RARa融合基因,此 白血病可被全反式维甲酸诱导分化
M4Eos: 异常嗜酸细胞>5% 常伴重现性16号染 色体异常
主要异常为幼稚嗜酸粒 细胞中的异常颗粒,细 胞除典型的嗜酸性颗粒 外,还有大的嗜碱性颗 粒
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实用标准文案 精彩文档 急性髓系细胞白血病(AML-M3) 【概述】
1986~1988年全国白血病发病情况调查显示,我国白血病的发病率为2.76/105,其中急性髓细胞白血病(Acute myeloblasticleukemia , AML)年发病率最高,达1.62/105(美国为2.25/105),约占所有白血病的58.7%,与急性淋巴细胞白血病(Acute Lymphocytic Leukemia,ALL)不同的是AML以成人多见(成人急性白血病中ALL占20%,AML占80%),其发病率随年龄增长渐次上升,20岁以下的年轻患者仅占全部AML的5%,一般过40岁后发病呈指数增加,而50%以上的AML年龄≥60岁,中位发病年龄为60~65岁。两性发病率相比,则男性比女性略高。我国调查资料也证实AML的发病率高峰在60~69岁,50岁以前两性发病率基本相似,至老年期男性发病率明显高于女性。
【临床表现】 一、 贫血 如苍白、无力、心悸、气短等,老年病人贫血更为多见。少数病例可在确诊前数月至数年先出现难治性贫血(refractory anemia,RA),以后再逐渐发展成AML(但绝少发展为ALL)。发生贫血的原因有:由于正常造血干细胞因白血病克隆增殖而受抑,红系祖细胞对红细胞生成素(erythropoietin,EPO)的反应性降低,骨髓微环境破坏,使红细胞生成减少;出现无效红细胞生成;合并明显或隐性溶血,红细胞寿命缩短;合并急、慢性失血,或脾功能亢进等。 二、 发热和感染 发热是初诊尤其是化疗骨髓抑制期患者的常见症状,其原因主要是感染,感染可发生在体表、体内任何部位。中性粒细胞减少伴功能缺陷,化疗和皮质激素的应用使机体免疫功能下降,皮肤、黏膜(口腔、胃肠道等)出血、溃疡导致屏障破坏是引起感染的主要因素。 三、 出血 约60%的初诊AML有不同程度的出血,皮肤黏膜(鼻、口腔及牙龈)出血最常见,眼底、球结膜出血较易见,女性可有月经增多,血尿较少见,但镜下血尿不易被发现,严重的胃肠、呼吸道和颅内出血虽不多见却常是致死的原因。急性白血病出血的机制比较复杂:骨髓衰竭导致血小板减少最重要的原因。通常血小板< 20×109 /L时多伴高危出血倾向,若合并全身感染或严重贫血时更可加重出血;化疗、细菌内毒素和白血病细胞浸润损伤血管内皮以及凝血障碍都是引起出血的原因。 AML-M3亚型(急性早幼粒细胞白血病)的出血比ALL和AML其他亚型更严重而多见,其明显出血往往与血小板减少的程度不相适应,这是因为白血病细胞破坏(尤其在化疗开始后),大量促凝物质和组织因子释放,可使50%~75%的M3病例发生弥漫性血管内凝血(disseminated intravascular coagulation,DIC)伴原发纤维蛋白溶解(fitrinolysis),偶尔DIC也出现于其它亚型如M5(急性单核细胞白血病)。 四、 白血病浸润表现 AML髓外浸润可发生在本病各亚型,但以M5和M4(急性粒单核细胞白血病)为较频见。 1、 皮肤浸润 以M5和M4型多见。外观呈斑丘疹、结节状或肿块,色泽紫红,可多发而布及全身或少数几个散布于体表,且对放疗敏感。偶尔也有在血象、骨髓象出现白血病改变前皮肤浸润先被发现。与AML相关的良性皮肤损害还有多形性红斑、S综合征、脓疮病、坏疽病等,籍皮肤活检可资鉴别。 2、 眼部改变 AML视网膜、脉络膜浸润比ALL少见,可合并出血或引致失明,眼底浸润往往提示合并CNS受累。 3、 口腔牙龈改变 25%~50%的M5和M4患者可因白血病浸润出现牙龈增生,严重者牙龈肿胀如海绵状,表面破溃出血,但AML其他亚型牙龈增生少见。口鼻黏膜、扁桃体或舌体浸润则较不多见。 4、 肝、脾、淋巴结肿大 见于约40%的病例(M5型较多见),与ALL相比其发生率较低,肿大的程度也较轻(肝脾通常肋下刚触及至肋下<4CM),明显的肝、脾、淋巴结肿大发生率一般≤10%。对有明显肝、脾肿大的患者应注意与慢性粒细胞白血病(chronic myclocytic leukemia,CML)急性相鉴别。 5、 骨关节痛 发生率约20%,比ALL少见。骨关节痛易发生在肋骨、脊椎骨,或肢体长骨及肘、踝等大关节,偶尔可出现骨坏死,但关节渗液稀见。胸骨压痛是常见体征,有助于白血病诊断。 6、 中枢神经系统受累(CNSL) 初诊AML的发生率不详,但包括复发时的全病程CNSL总发生率儿童为5%~20%,成人约15%,明显低于ALL。 7、 粒细胞肉瘤 是有原粒或原单核细胞组成的一种髓外肿瘤,又名绿色瘤,常累及骨、骨膜、软组织、淋巴结和皮肤,好发在眼眶、副鼻窦、胸璧、乳房、唾液腺、纵隔、神经、胃肠道和泌尿生殖系等处。 AML还可以发生心脏、心包、肺、胸膜、肾及胃肠等各种器官、组织的浸润,但一般很少导致出现临床症状。睾丸、前列腺、卵巢、子宫浸润较少见。
【实验室检查】 实用标准文案 精彩文档 1、 血象 半数AML患者白细胞数增高,多在10×109 /L~100×109 /L之间,20%的病例甚至>100×109 /L。部分患者白细胞数可正常,少数病人(常为M3型或老年病例)白细胞数< 4.0×109 /L。80%患者血红蛋白低于正常值,甚至出现严重贫血,网织红细胞常减少。血小板数多数患者减少,少数正常或轻度增高。 2、 骨髓象 多数患者高度增生,正常造血细胞被白血病细胞取代;少数患者骨髓增生低下,但原始细胞仍在30%以上。如胞浆内发现Auer小体,更有助于排除ALL而确诊为AML。 3、 凝血异常 出现DIC时可出现血小板减少,凝血酶原和部分凝血活酶时间延长,血浆纤维蛋白原减少,纤维蛋白降解产物增和凝血因子V、VII、VIII、X等的缺乏。 4、 代谢异常 高尿酸血症常见于白细胞数增高和诱导化疗期患者,且与肿瘤溶解有关,但AML的高尿酸血症发生率比ALL低;血清乳酸脱氢酶(LDH)可升高,尤其是M4和M 5亚型,其增高程度一般也轻于ALL;血清溶菌酶增高也以M4和M 5型多见。
【分型标准】 FAB分型有利于诊断标准的统一 [FAB:M1] [ FAB:M7]急性粒细胞白血病未分化型(axute myeloblsdtic leukemia without maturation)。骨髓中原粒细胞(I型和II型)>90%(非红系细胞——nonerythroid cells,NEC)。原始细胞3%以上为过氧化物酶阳性。可有奥尔小体。早幼粒细胞很少,中幼粒细胞以下阶段不见或罕见,单核系细胞<10%(NEC)。
[FAB:M2]急性粒细胞白血病部分分化型(acute myelocytic leukemia with maturation)。骨髓中原粒细胞(I型+II型)>30%-<90%(非红系细胞),单核细胞<20%,早幼以下个阶段的粒细胞>NEC的10%。易见含奥尔小体或8;21染色体易位的病例,其胞浆丰富并有颗粒,这种细胞应与早幼粒细胞相鉴别。
[FAB:M3]颗粒增多的早幼粒细胞白血病(hypergranular promyelocytic leukeia)。骨髓中以颗粒增多的异常早幼粒细胞增生为主(>NEC的30%),其胞核大小不一,胞浆中有大小不等的异常颗粒,多数奥尔小体呈束状,称为束状细胞(faggot cell),易发生播散性血管内凝血(DIC),与第15号17号染色体易位[t(15;17)]。可分为二型: [M3a]粗颗粒型:嗜苯胺蓝颗粒粗大,密集甚或融合。易见柴束状奥尔小体。 [M3b]细颗粒型:嗜苯胺蓝颗粒密集而细小,为M3的变种(variantM3)
[FAB:M4]急性粒-单核细胞白血病(acute myelomonocytic leukemia)。急性单是粒细胞和单核细胞系两系分化所致。骨髓中原粒和早幼粒细胞增生为主,其中原粒细胞>NEC的30%而>80%。原始、幼稚和成熟单核细胞>NEC的20%。
按粒细胞和单核细胞系形态不同,可包括下列4中类型: [M4a]骨髓中原+早为主(原始细胞>NEC的30%)。单核系细胞>NEC的20%。 [M4b]骨髓中的原、幼单核细胞增生为主,原始和早幼粒细胞>20%(非红系细胞)。 [M4c]骨髓中的原始细胞:既具有粒细胞系又具有单核细胞系特征的细胞>30%。 [M4Eo]骨髓细胞除上述特点外,特异性嗜酸颗粒粗大而圆,着色较深的嗜酸粒细胞>5-<30%。常见在一个细胞中既有特异性嗜酸颗粒又有粗大深蓝色的嗜碱颗粒(嗜碱联合粒细胞),核不分叶。氯乙酸酯酶和PAS反应呈强阳性。16号染色体异常,16:del(16)(q22),inv(16)(p13q22),这也是本病的特征之一。 [FAB:M5]急性单核细胞白血病(acute monocytic leukemia)。骨髓中原单核细胞、幼单核细胞和单核细胞>NEC的80%。 分以下二型: [M5a]未分化型:骨髓全部单核系细胞中原单核细胞>NEC的30%。 [M5b]部分分化型:骨髓全部单核系细胞中原单核细胞NEC的30%。 [FAB:M6]红白血病(axute erythroleukemia)。骨髓中红系>50%,且常有形态学异常,骨髓非红系细胞中原粒细胞(或原始+幼单核细胞)>30%;若血片中原粒(或原单)细胞>5%,骨髓非红系细胞中 实用标准文案 精彩文档 原粒细胞(或原始+幼单核细胞)>20%也可诊断。
[FAB:M7]急性巨核细胞白血病(acute megakaryocytic leukemia)。 1、 外周血有小原巨核细胞,过氧化物酶与苏丹黑B均呈阴性反应,电镜细胞化学血小板过氧化物酶呈阳性反应。 2、 骨髓中原巨核细胞>30%,呈多形性,似小淋巴细胞,有1-3个核仁。胞浆颗粒为(+)——(-),有嗜碱性细胞突起(bleb),有血小板生成像,显示巨核细胞的分化。外周血可见血小板片段(fragment)。 3、 原巨核有电镜或单克隆抗体证实。(PPO或/和GPIIb/IIIa阳性细胞)>10%,MPO阳性细胞<5%。 4、 骨髓网状纤维(reticular)增加,细胞少,往往干抽,活检有原始和巨核细胞增多 。 [Mo]急性未分化型白血病(acute undifferentiated leukemia ,AUL)或称急性干细胞型白血病(acute stem cell leukemia, ASL),约占急性白血病的5~10%。有些中外学者建议称为Mo。其特点是原始细胞缺乏任何特异性标志(标志阳性细胞<20%)。
【预后因素】 与ALL相比,AML的预后因素更多变而不统一。一些因素的预后意义往往随患者年龄、个体特异性、白血病细胞形态学表型和治疗方案的不同而有所不同,而同一患者的预后也总是受多个因素的共同影响。目前比较肯定的预后因素有患者的发病年龄,初诊时白细胞数,有无MDS病史,是否继发性白血病,达缓解时间和细胞遗传学特征等。 临床特征 1、 年龄 几乎一致公认发病时患者的年龄是决定AML完全缓解(CR)率和缓解生存时间最重要的预后因素之一。通常小于45岁者CR率较高,缓解生存时间较长,小于15岁预后更好,但小于2岁和大于60岁的患者由于常合并其他高危因素,预后多差。老年病例的CR率仅及年轻人的一半,获得长期无复发生存(RFS)的机率更低。 2、 前因 白血病发病前经历过MDS或骨髓增殖性疾病(myeloproliferative disorder,MPD)阶段,或曾有化、放疗史的继发性白血病,初诊时外周血白细胞数增高(>100×109/L),原始细胞百分率高,合并明显的髓外和CNS浸润,这些因素既不利于获取CR,即便获得缓解也容易复发,有碍于延长生存。 3、 缓解 为获得良好的远期疗效,诱导化疗开始后应争取使患者在1~2疗程内迅速达到CR,治疗>2疗程才逐渐达到CR的患者,长期无病生存率(DFS)可能明显降低。 4、细胞遗传学改变 与其他因素相比,染色体核型异常可能是最重要和独立的预后因素。正常核型预后较好,但利用分子学技术可在部分正常核型患者中发现分子学改变(白血病融合基因),并具预后意义。 5、其他不良预后因素 患者的一般情况差,伴严重贫血和血小板减少,合并慢性肾病、肝病或糖尿病,低白蛋白或低纤维蛋白血症,白血病细胞标记指数降低,血清碱性磷酸酶和乳酸脱氢酶(LDH)升高等 。
