高中化学第3章物质的聚集状态与物质性质第4节几类其他聚集状态的物质教学案鲁科版选修3word格式
第4节 几类其他聚集状态的物质——A学习区 夯实基础一遍过(鲁科版选修3)(word无答案)

第4节几类其他聚集状态的物质——A学习区夯实基础一遍过(鲁科版选修3)一、单选题(★) 1 . 下列关于聚集状态的叙述中,错误的是()A.物质只有气.液.固三种聚集状态B.气态是高度无序的体系存在状态C.固态中的原子或者分子结合的较紧凑,相对运动较弱D.液态物质的微粒间距离和作用力的强弱介于固.气两态之间,表现出明显的流动性(★) 2 . 下列物质中,不属于非晶体的是()A.石蜡B.沥青C.橡胶D.干冰(★) 3 . 关于非晶体的叙述错误的是()A.玻璃属于非晶体B.内部微粒的排列是长程无序和短程有序的C.非晶体材料的所有性能都优于晶体材料D.金属形成的合金也有非晶体(★★) 4 . 有关液晶的叙述不正确的是 ( )A.液晶既具有液体的可流动性,又具有晶体的各向异性B.液晶最重要的用途是制造液晶显示器C.液晶不是物质的一种聚集状态D.液晶分子聚集在一起时,其分子间相互作用很容易受温度、压力和电场的影响(★) 5 . 下列关于液晶的说法正确的是()A.液晶是液体和晶体的混合物B.液晶是一种晶体C.液晶分子在特定条件下排列比较整齐,但不稳定D.所有物质在一定条件下都能成为液晶(★) 6 . 纳米材料具有一些与传统材料不同的特征,下列关于纳米材料的叙述中,错误的是A.三维空间尺寸必须都处于纳米尺度B.具有既不同于微观粒子也不同于宏观物体的独特性质C.是原子排列成的纳米数量级原子团D.具有与晶态、非晶态均不同的一种新的结构状态(★) 7 . 有关等离子体的说法不正确的是()A.等离子体内部全部是带电荷的微粒B.等离子体中正、负电荷大致相等C.等离子体具有很好的导电性D.等离子体用途十分广泛(★★) 8 . 下列关于等离子体的叙述正确的是()A.物质一般有固态、液态和气态三态,等离子体却被认为是物质存在的第四态B.为了使气体变成等离子体,必须使其通电C.等离子体通过电场时,所有粒子的运动方向都发生改变D.等离子体性质稳定,不易发生化学反应(★) 9 . 下列与等离子体无关的是()A.等离子体显示器B.日光灯和霓虹灯C.把温度升高到几千摄氏度时水蒸气发生的变D.液晶显示器(★) 10 . 用烧热的钢针去接触涂有薄薄一层石蜡的云母片的反面,熔化了的石蜡呈椭圆形,这是因为()。
最新精选高中化学选修3 物质结构与性质第3章 物质的聚集状态与物质性质第4节 几类其它聚集状态的物质鲁科版

最新精选高中化学选修3 物质结构与性质第3章物质的聚集状态与物质性质第4节几类其它聚集状态的物质鲁科版课后练习第五十一篇第1题【单选题】针对能源、环境、水资源等方面的危机,以下四条设想合理可行的是( )A、大量开采地下水,以满足社会对水的需求B、生活中严禁使用塑料制品,以解决“白色污染”问题C、面对金属矿物储量有限不能再生的危机,寻找金属的代用品D、工业上禁止开发和使用化石燃料,以应对全球能源危机【答案】:【解析】:第2题【单选题】水是生命之源,下列有关水的说法正确的是( )A、将河水经过沉淀、过滤、活性炭吸附等净化处理后,所得的水就是纯水B、水是一种常见的溶液C、煮沸可以降低自来水的硬度D、电解水实验说明水是由氢气和氧气组成的【答案】:【解析】:第3题【单选题】下列晶体性质的比较中正确的是( )A、沸点:NH3>H2O>HFB、熔点:金刚石>碳化硅>晶体硅C、硬度:白磷>冰>二氧化硅D、熔点:SiI4<SiBr4<SiCl4【答案】:【解析】:第4题【单选题】下列有关性质的比较中,不正确的是( )A、金属原子化热:Na<Mg<AlB、晶格能:NaBr<NaCl<MgOC、键的极性:N﹣H<O﹣H<F﹣HD、熔点:【答案】:【解析】:第5题【单选题】下列说法正确的是( )A、用乙醇或CCl4提取碘水中的碘单质B、NaCl和SiC晶体熔化时,克服粒子间作用力类型相同C、^24Mg^32S晶体中电子总数与中子总数之比为1:1D、H2S与SiF4分子中各原子最外层都满足8电子结构【答案】:【解析】:第6题【单选题】下列物质的熔沸点高低比较正确的是( )A、邻二甲苯()、邻羟基苯甲醛()熔沸点均于其对应对位取代物B、卤素元素的单质及其氢化物的熔沸点随原子半径的增大而升高C、石墨、金刚石、碳化硅、晶体硅、白磷、水、干冰熔沸点依次降低D、NaCl、MgCl2、MgO,Al2O3熔沸点依次减小【答案】:【解析】:第7题【单选题】下列说法正确的是( )A、原子晶体中只存在非极性共价键B、稀有气体形成的晶体属于分子晶体C、干冰升华时,分子内共价键会发生断裂D、金属元素和非金属元素形成的化合物一定是离子化合物【答案】:【解析】:第8题【单选题】下列物质属于分子晶体的是( )A、熔点是1070℃,易溶于水,水溶液能导电B、熔点是10.31℃,液态不导电,水溶液能导电C、能溶于水,熔点812.8℃,沸点是1446℃D、熔点是97.80℃,质软、导电,密度是0.97g/cm^3【答案】:【解析】:第9题【单选题】氯化硼的熔点为﹣107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )A、氯化硼分子间含有氢键B、氯化硼中心原子采用sp杂化C、氯化硼分子呈正三角形,属非极性分子D、其分子空间结构类似CH4O【答案】:【解析】:第10题【单选题】沸腾时只需克服范德华力的液体物质是( )A、水B、酒精C、溴D、水银【答案】:【解析】:第11题【单选题】能与氢氧化钠溶液反应的分子晶体是( )A、氧化铝B、金刚石C、二氧化碳D、二氧化硅【答案】:【解析】:第12题【单选题】下列物质的熔、沸点高低顺序中,正确的是( )A、金刚石>晶体硅>二氧化硅>碳化硅B、I2>Br2>Cl2>F2C、H2Te>H2Se>H2S>H2OD、金刚石>CsCl>NaCl>钠【答案】:【解析】:第13题【单选题】下列有关化学键、氢键和范德华力的叙述中,不正确的是( )A、金属键是金属离子与“电子气”之间的较强作用,金属键无方向性和饱和性B、共价键是原子之间通过共用电子对形成的化学键,共价键有方向性和饱和性C、范德华力是分子间存在的一种作用力,分子的极性越大,范德华力越大D、氢键不是化学键而是分子间的一种作用力,所以氢键只存在于分子与分子之间【答案】:【解析】:第14题【单选题】图为冰晶体的结构模型,大球代表O原子,小球代表H原子,下列有关说法正确的是( )A、冰晶体中每个水分子与另外2个水分子形成四面体B、冰晶体具有空间网状结构,是原子晶体C、水分子间通过H﹣O…H键形成冰晶体D、冰晶体熔化时,水分子之间的空隙增大【答案】:【解析】:第15题【综合题】自从英国化学家巴特列(N.Bartlett)首次合成了第一种稀有气体的化合物XePtF6以来,人们又相继发现了氙的一系列化合物,如XeF2、XeF4等.巴特列为开拓稀有气体化学作出了历史性贡献.请根据XeF4的结构示意图(图1)判断这个分子是极性分子还是非极性分子?______.XeF2晶体是一种无色晶体,图2为它的晶胞结构图.XeF2晶体属于哪种类型的晶体?______.【答案】:【解析】:。
最新高中化学 第3章 物质的聚集状态与物质性质章末重难点专题突破学案 鲁科版选修3(考试必备)

第3章物质的聚集状态与物质性质章末重难点专题突破[学习目标定位] 1.能根据晶体的组成、结构和物理性质判断晶体类型。
2.了解晶体熔、沸点的变化规律,理解晶体性质与结构之间的关系。
3.能利用均摊法进行晶胞的分析和计算。
一、晶体类型的判断例1(2017·北京四中高二期中)(1)判断下列晶体类型。
①SiI4:熔点为120.5 ℃,沸点为271.5 ℃,易水解,为__________。
②硼:熔点为2 300 ℃,沸点为2 550 ℃,硬度大,为______________。
③硒:熔点为217 ℃,沸点为685 ℃,溶于氯仿,为______________。
④锑:熔点为630.74 ℃,沸点为1 750 ℃,可导电,为__________________。
(2)三氯化铁常温下为固体,熔点为282 ℃,沸点为315 ℃,在300 ℃以上易升华。
易溶于水,也易溶于乙醚、丙酮等有机溶剂。
据此判断三氯化铁晶体为______________(填晶体类型)。
答案(1)①分子晶体②原子晶体③分子晶体④金属晶体(2)分子晶体解析(1)①SiI4为低熔点化合物,为分子晶体;②晶体硼熔点高,硬度大,是典型的原子晶体;③硒熔、沸点低,易溶于CHCl3,为分子晶体;④锑可导电,为金属晶体。
(2)FeCl3熔、沸点低,易溶于水及有机溶剂,应为分子晶体。
二、晶体熔、沸点的比较例2下列各组物质的沸点按由低到高的顺序排列的是( )A.NH3、CH4、NaCl、NaB.H2O、H2S、MgSO4、SO2C.CH4、H2O、NaCl、SiO2D.Li、Na、K、Rb、Cs答案 C解析C项中SiO2是原子晶体,NaCl是离子晶体,CH4、H2O都是分子晶体,且常温下水为液态,CH4是气态。
方法规律——比较不同晶体熔、沸点的基本思路首先看物质的状态,一般情况下是固体>液体>气体;二是看物质所属类型,一般是原子晶体>离子晶体>分子晶体(注意:不是绝对的,如氧化铝的熔点大于晶体硅),结构类型相同时再根据相应规律进行判断。
高中化学 第3章 物质的聚集状态与物质性质 第4节 几类其他聚集状态的物质学业分层测评 鲁科版选修3

几类其他聚集状态的物质(建议用时:45分钟)[学业达标]1.下列物质中,不属于非晶体的是( )A.玻璃B.石蜡和沥青C.塑料D.干冰【解析】干冰属于分子晶体,玻璃、石蜡、沥青、塑料均属于非晶体。
【答案】 D2.物质的非晶体能自动转变为晶体,而晶体却不能自动地转变为非晶体,这说明( ) A.非晶体是不稳定的,处于非晶体时能量大B.晶体是稳定的,处于晶体时能量大C.非晶体是不稳定的,处于非晶体时能量小D.晶体是不稳定的,处于非晶体时能量小【解析】根据“非晶体能自动转变为晶体”可知,非晶体不稳定;能量越低越稳定,说明非晶体是处于高能量状态,转变为晶体后趋向于低能量的稳定状态。
【答案】 A3.下列关于各向异性的描述中正确的是 ( )A.各向异性是指非晶体没有规则的几何形状B.各向异性是指非晶体的物理性质与方向的关系C.各向异性是指非晶体的内部结构与方向有关D.各向异性是指晶体的物理性质与方向的关系【解析】各向异性指晶体在不同的方向上表现出不同的物理性质。
【答案】 D4.下列有关等离子体的叙述,不正确的是( )A.等离子体是物质的另一种聚集状态B.等离子体是很好的导体C.水可能形成等离子体状态D.等离子体中的微粒不带电荷【解析】等离子体中的微粒带有电荷,而且能自由移动,所以等离子体具有良好的导电性。
【答案】 D5.(2016·莱芜高二检测)电子表、电子计算器、电脑显示器都运用了液晶材料显示图像和文字。
有关其显示原理的叙述中,正确的是( )A.施加电压时,液晶分子沿垂直于电场方向排列B.移去电压后,液晶分子恢复到原来状态C.施加电场时,液晶分子恢复到原来状态D.移去电场后,液晶分子沿电场方向排列【解析】液晶的显示原理为施加电压时,液晶分子沿电场方向排列;移去电场后,液晶分子恢复到原来状态。
【答案】 B6.关于纳米材料,下列说法正确的是 ( )①纳米材料可大大提高材料的强度和硬度②纳米材料可提高材料的磁性③纳米材料能制作高贮存密度的量子磁盘④纳米机器人“医生”能进入人体杀死癌细胞⑤纳米是长度单位A.①②③④⑤B.②③④C.②③④⑤D.①②③④【解析】纳米材料的性能包括提高材料的强度、硬度、改变颜色、增强磁性等。
2020高中化学 第3章 物质的聚集状态与物质性质章末知识网络构建学案 鲁科版选修3
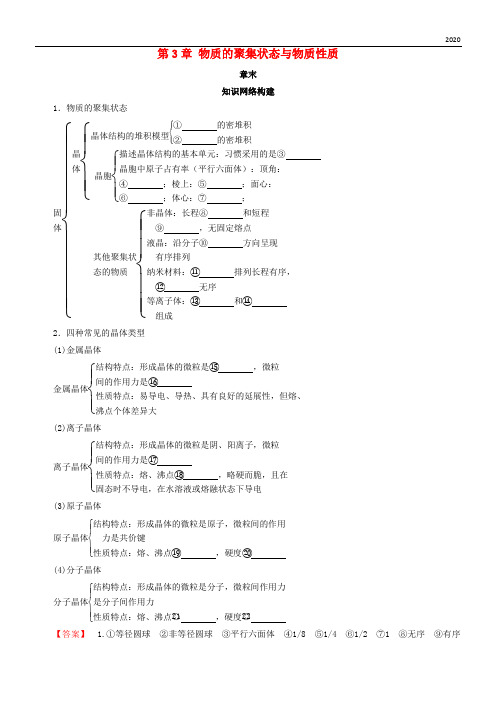
第3章 物质的聚集状态与物质性质
章末
知识网络构建
1.物质的聚集状态
固体⎩⎪⎪⎪⎪⎨⎪⎪⎪⎪⎧晶体⎩⎪⎨⎪⎧晶体结构的堆积模型⎩⎪⎨⎪⎧① 的密堆积② 的密堆积晶胞⎩⎪⎨⎪
⎧
描述晶体结构的基本单元:习惯采用的是③ 晶胞中原子占有率(平行六面体):顶角:
④ ;棱上:⑤ ;面心:⑥ ;体心:⑦ ;
其他聚集状态的物质⎩⎪⎪⎨
⎪⎪⎧非晶体:长程⑧
和短程
⑨ ,无固定熔点
液晶:沿分子⑩ 方向呈现
有序排列
纳米材料:⑪ 排列长程有序,
⑫ 无序
等离子体:⑬ 和⑭
组成
2.四种常见的晶体类型
(1)金属晶体
金属晶体⎩⎪⎨⎪⎧
结构特点:形成晶体的微粒是⑮ ,微粒间的作用力是⑯
性质特点:易导电、导热、具有良好的延展性,但熔、沸点个体差异大
(2)离子晶体
离子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是阴、阳离子,微粒
间的作用力是⑰
性质特点:熔、沸点⑱ ,略硬而脆,且在固态时不导电,在水溶液或熔融状态下导电
(3)原子晶体
原子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是原子,微粒间的作用
力是共价键
性质特点:熔、沸点⑲ ,硬度⑳
(4)分子晶体
分子晶体⎩⎪⎨⎪⎧
结构特点:形成晶体的微粒是分子,微粒间作用力是分子间作用力
性质特点:熔、沸点○21 ,硬度○22
【答案】 1.①等径圆球 ②非等径圆球 ③平行六面体 ④1/8 ⑤1/4 ⑥1/2 ⑦1 ⑧无序 ⑨有序
⑩长轴⑪颗粒⑫界面⑬带电微粒⑭中性微粒2.⑮金属阳离子、自由电子⑯金属键⑰离子键⑱较高⑲高⑳大○21低○22小。
2020高中化学 第3章 物质的聚集状态与物质性质章末知识网络构建学案 鲁科版选修3
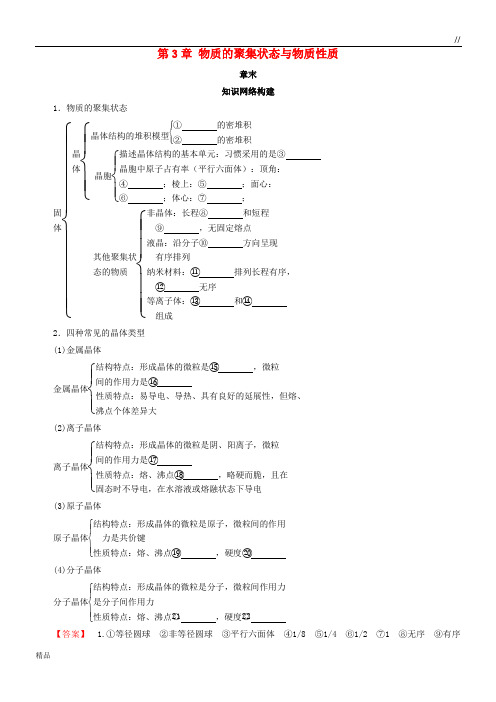
第3章 物质的聚集状态与物质性质
章末
知识网络构建
1.物质的聚集状态
固体⎩⎪⎪⎪⎪⎨⎪⎪⎪⎪⎧晶体⎩⎪⎨⎪⎧晶体结构的堆积模型⎩⎪⎨⎪⎧① 的密堆积② 的密堆积晶胞⎩⎪⎨⎪
⎧
描述晶体结构的基本单元:习惯采用的是③ 晶胞中原子占有率(平行六面体):顶角:
④ ;棱上:⑤ ;面心:⑥ ;体心:⑦ ;其他聚集状态的物质⎩⎪⎪⎨
⎪⎪⎧非晶体:长程⑧ 和短程 ⑨ ,无固定熔点
液晶:沿分子⑩ 方向呈现
有序排列
纳米材料:⑪ 排列长程有序,
⑫ 无序
等离子体:⑬ 和⑭
组成
2.四种常见的晶体类型
(1)金属晶体
金属晶体⎩⎪⎨⎪⎧
结构特点:形成晶体的微粒是⑮ ,微粒间的作用力是⑯
性质特点:易导电、导热、具有良好的延展性,但熔、沸点个体差异大
(2)离子晶体
离子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是阴、阳离子,微粒
间的作用力是⑰
性质特点:熔、沸点⑱ ,略硬而脆,且在固态时不导电,在水溶液或熔融状态下导电
(3)原子晶体
原子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是原子,微粒间的作用
力是共价键
性质特点:熔、沸点⑲ ,硬度⑳
(4)分子晶体
分子晶体⎩⎪⎨⎪⎧
结构特点:形成晶体的微粒是分子,微粒间作用力是分子间作用力
性质特点:熔、沸点○21 ,硬度○22
【答案】 1.①等径圆球 ②非等径圆球 ③平行六面体 ④1/8 ⑤1/4 ⑥1/2 ⑦1 ⑧无序
⑨有序
⑩长轴⑪颗粒⑫界面⑬带电微粒⑭中性微粒2.⑮金属阳离子、自由电子⑯金属键⑰离子键⑱较高⑲高⑳大○21低○22小。
新教材高中化学第3章不同聚集状态的物质与性质第2节能力课时4四类典型晶体的熔沸点比较及应用课件鲁科版
通过本情境素材中对晶格能的影响因素及晶体性质的影响因素 的探究,提升了“宏观辨识与微观探析”的学科素养。
探究二
石墨不同于金刚石,它的碳原子不像金刚石的碳原子那样呈 sp3 杂化,而是呈 sp2 杂化,形成平面六元并环结构(如下图①),因此, 石墨晶体是层状结构的,层内的碳原子的核间距为 142 pm,层间距 离为 335 pm(比键长大得多)说明层间没有化学键相连,是靠范德华 力维系的(如图②)
[答案] (1)TiF4 为离子化合物,熔点高,其他三种均为共价化合 物,其组成和结构相似,随相对分子质量的增大,分子间作用力增 大,熔点逐渐升高 (2)Li2O、MgO 为离子晶体,P4O6、SO2 为分子 晶体,晶格能 MgO>Li2O,分子间作用力(相对分子质量)P4O6>SO2 (3)GaF3 是离子晶体,GaCl3 为分子晶体 (4)GeCl4、GeBr4、GeI4 的熔、沸点依次增高。原因是分子的组成和结构相似,相对分子质 量依次增大,分子间作用力逐渐增强
(2)氧化锂、氧化镁是离子晶体,六氧化四磷和二氧化硫是分子 晶体,离子键比分子间作用力强。
(3)晶体类型是决定物质熔、沸点的主要因素,从 GaF3 的熔点较 高知其为离子晶体,从 GaCl3 的熔点较低知其为分子晶体。一般来 说,离子晶体的熔点高于分子晶体的熔点。
(4)根据表中数据得出,三种锗卤化物都是分子晶体,其熔、沸 点依次增高,而熔、沸点的高低与分子间作用力强弱有关,分子间 作用力强弱与相对分子质量的大小有关。
C [HF 分子间存在氢键,故沸点相对较高,A 项正确;能形成 分子间氢键的物质熔、沸点较高,邻羟基苯甲醛易形成分子内氢键, 对羟基苯甲醛易形成分子间氢键,所以邻羟基苯甲醛的熔、沸点比 对羟基苯甲醛的熔、沸点低,B 项正确;H2O 分子中的 O 可与周围 H2O 分子中的两个 H 原子形成两个氢键,而 HF 分子中的 F 原子只 能形成一个氢键,氢键越多,沸点越高,所以 H2O 的沸点高,C 项 错误;氨气分子和水分子间形成氢键,导致氨气极易溶于水,D 项 正确。]
高中化学第3章物质的聚集状态与物质性质章末知识网络构建学案鲁科版选修3
第3章 物质的聚集状态与物质性质
章末
知识网络构建
1.物质的聚集状态
固体⎩⎪⎪⎪⎪⎨⎪⎪⎪⎪⎧晶体⎩⎪⎨⎪⎧晶体结构的堆积模型⎩⎪⎨⎪
⎧① 的密堆积② 的密堆积
晶胞
⎩⎪⎨⎪⎧
描述晶体结构的基本单元:习惯采用的是③
晶胞中原子占有率(平行六面体):顶角:
④ ;棱上:⑤ ;面心:⑥ ;体心:⑦ ;
其他聚集状态的物质⎩⎪⎪⎨⎪⎪⎧非晶体:长程⑧
和短程
⑨ ,无固定熔点
液晶:沿分子⑩ 方向呈现
有序排列
纳米材料:⑪
排列长程有序,
⑫ 无序
等离子体:⑬ 和⑭
组成
2.四种常见的晶体类型
(1)金属晶体
金属晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是⑮ ,微粒
间的作用力是⑯
性质特点:易导电、导热、具有良好的延展性,但熔、沸点个体差异大
(2)离子晶体
离子晶体⎩⎪⎨⎪⎧
结构特点:形成晶体的微粒是阴、阳离子,微粒间的作用力是⑰
性质特点:熔、沸点⑱ ,略硬而脆,且在固态时不导电,在水溶液或熔融状态下导电
(3)原子晶体
原子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是原子,微粒间的作用
力是共价键
性质特点:熔、沸点⑲ ,硬度⑳
(4)分子晶体
分子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是分子,微粒间作用力
是分子间作用力
性质特点:熔、沸点○21 ,硬度○22
【答案】 1.①等径圆球②非等径圆球③平行六面体④1/8⑤1/4 ⑥1/2⑦1⑧无序⑨有序⑩长轴⑪颗粒⑫界面⑬带电微粒⑭中性微粒
2.⑮金属阳离子、自由电子⑯金属键⑰离子键
⑱较高⑲高⑳大○21低○22小。
高中化学第3章物质的聚集状态与物质性质章末知识网络构建鲁科版选修320170804367.doc
第3章 物质的聚集状态与物质性质章末知识网络构建1.物质的聚集状态固体⎩⎪⎪⎪⎪⎨⎪⎪⎪⎪⎧晶体⎩⎪⎨⎪⎧晶体结构的堆积模型⎩⎪⎨⎪⎧① 的密堆积② 的密堆积晶胞⎩⎪⎨⎪⎧描述晶体结构的基本单元:习惯采用的是③晶胞中原子占有率(平行六面体):顶角:④ ;棱上:⑤ ;面心:⑥ ;体心:⑦ ;其他聚集状态的物质⎩⎪⎪⎨⎪⎪⎧非晶体:长程⑧ 和短程⑨ ,无固定熔点液晶:沿分子⑩ 方向呈现有序排列纳米材料:⑪ 排列长程有序,⑫ 无序等离子体:⑬ 和⑭组成2.四种常见的晶体类型(1)金属晶体金属晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是⑮ ,微粒间的作用力是⑯性质特点:易导电、导热、具有良好的延展性,但熔、沸点个体差异大(2)离子晶体离子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是阴、阳离子,微粒间的作用力是⑰性质特点:熔、沸点⑱ ,略硬而脆,且在固态时不导电,在水溶液或熔融状态下导电(3)原子晶体原子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是原子,微粒间的作用 力是共价键性质特点:熔、沸点⑲ ,硬度⑳(4)分子晶体分子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是分子,微粒间作用力是分子间作用力性质特点:熔、沸点○21 ,硬度○22【答案】 1.①等径圆球 ②非等径圆球 ③平行六面体 ④1/8 ⑤1/4⑥1/2 ⑦1 ⑧无序 ⑨有序 ⑩长轴 ⑪颗粒 ⑫界面 ⑬带电微粒 ⑭中性微粒2.⑮金属阳离子、自由电子⑯金属键⑰离子键⑱较高⑲高⑳大○21低○22小精美句子1、善思则能“从无字句处读书”。
读沙漠,读出了它坦荡豪放的胸怀;读太阳,读出了它普照万物的无私;读春雨,读出了它润物无声的柔情。
读大海,读出了它气势磅礴的豪情。
读石灰,读出了它粉身碎骨不变色的清白。
2、幸福幸福是“临行密密缝,意恐迟迟归”的牵挂;幸福是“春种一粒粟,秋收千颗子”的收获. 幸福是“采菊东篱下,悠然见南山”的闲适;幸福是“奇闻共欣赏,疑义相与析”的愉悦。
部编版2020高中化学 第3章 物质的聚集状态与物质性质章末知识网络构建学案 鲁科版选修3
第3章 物质的聚集状态与物质性质
章末
知识网络构建
1.物质的聚集状态
固体⎩⎪⎪⎪⎪⎨⎪⎪⎪⎪⎧晶体⎩⎪⎨⎪⎧晶体结构的堆积模型⎩⎪⎨⎪⎧① 的密堆积
② 的密堆积
晶胞⎩⎪⎨⎪⎧描述晶体结构的基本单元:习惯采用的是③
晶胞中原子占有率(平行六面体):顶角:
④ ;棱上:⑤ ;面心:⑥ ;体心:⑦
;其他聚集状态的物质⎩⎪⎪⎨⎪⎪⎧非晶体:长程⑧ 和短程
⑨ ,无固定熔点
液晶:沿分子⑩ 方向呈现
有序排列
纳米材料:
⑪ 排列长程有序,
⑫ 无序
等离子体:⑬ 和⑭
组成
2.四种常见的晶体类型
(1)金属晶体
金属晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是⑮ ,微粒
间的作用力是⑯
性质特点:易导电、导热、具有良好的延展性,但熔、沸点个体差异大
(2)离子晶体
离子晶体⎩⎪⎨⎪⎧
结构特点:形成晶体的微粒是阴、阳离子,微粒间的作用力是⑰
性质特点:熔、沸点⑱ ,略硬而脆,且在固态时不导电,在水溶液或熔融状态下导电
(3)原子晶体
原子晶体⎩⎪⎨⎪⎧结构特点:形成晶体的微粒是原子,微粒间的作用
力是共价键
性质特点:熔、沸点⑲ ,硬度⑳
(4)分子晶体
分子晶体⎩⎪⎨⎪⎧
结构特点:形成晶体的微粒是分子,微粒间作用力是分子间作用力
性质特点:熔、沸点○21 ,硬度○22
【答案】 1.①等径圆球②非等径圆球③平行六面体④1/8⑤1/4⑥1/2⑦1⑧无序⑨有序⑩长轴⑪颗粒⑫界面⑬带电微粒⑭中性微粒
2.⑮金属阳离子、自由电子⑯金属键⑰离子键
⑱较高⑲高⑳大○21低○22小。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第4节 几类其他聚集状态的物质 [课标要求] 1.了解非晶体和液晶。 2.了解纳米材料和等离子体。
1.其他聚集状态的物质有非晶体、液晶、纳米材料、等离子体。 2.非晶体是指内部原子或分子的排列呈杂乱无章的分布状态的固体。 3.液晶是指在一定的温度范围内既具有液体的可流动性,又具有晶体的各向异性的物质。 4.纳米材料是指三维空间尺寸至少有一维处于纳米尺度的、具有特定功能的材料。 5.等离子体是指由大量带电微粒(离子、电子)和中性微粒(原子或分子)所组成的物质聚集体。
非晶体和液晶 1.非晶体 (1)概念:内部原子或分子的排列呈杂乱无章的分布状态的固体。 (2)非晶体和晶体的区别 物质类别 晶体 非晶体 内部微粒排列 长程有序 长程无序和短程有序 性质 有对称性、各向异性、自范性 无对称性、各向异性、自范性
2.液晶 (1)概念:在一定的温度范围内既具有液体的可流动性,又具有晶体的各向异性的物质。
(2)结构特点 液晶内部分子的排列沿分子长轴方向呈现出有序排列,使液晶在折射率、磁化率、电导率等宏观性质方面表现出类似晶体的各向异性。
1.有关非晶体的描述,不正确的是( ) A.非晶体和晶体均呈固态 B.非晶体内部的粒子是长程无序和短程有序 C.非晶体结构无对称性、各向异性和自范性 D.水晶属于非晶体 解析:选D 水晶(SiO2)属于原子晶体。 2.关于液晶的叙述中,错误的是( ) A.液晶是物质的一种聚集状态 B.液晶具有流动性 C.液晶和液态是物质的同一种聚集状态 D.液晶具有各向异性 解析:选C 液晶是固态、液态、气态之外的一种聚集状态,与液态不是同一种聚集状态。 纳米材料和等离子体
1.纳米材料 (1)概念:三维空间尺寸至少有一维处于纳米尺度的、具有特定功能的材料。 (2)结构特点: ①纳米材料由纳米颗粒和颗粒间的界面两部分组成。纳米颗粒内部具有晶状结构,界面则为无序结构。 ②组成粒子为原子排列成纳米量级的原子团。 2.等离子体 (1)概念:由大量带电微粒(离子、电子)和中性微粒(原子或分子)所组成的物质聚集体。 (2)组成特点: ①等离子体中正、负电荷数大致相等,总体上等离子体呈准电中性。 ②等离子体中的微粒带有电荷且能自由运动,使等离子体具有很好的导电性。 [特别提醒] (1)纳米材料既不属于晶体也不属于胶体,有其他聚集状态,如非晶体、等离子体、液晶等。 (2)等离子体是由大量带电微粒(离子、电子)和中性微粒(原子或分子)所组成的物质聚集体,由于正、负电荷大致相等,所以总体上说等离子体呈准电中性,不是离子。
1.判断正误(正确的打“√”,错误的打“×”)。 (1)纳米是一种非晶体( ) (2)纳米材料具有丁达尔效应( ) (3)SO2-4和PO3-4属于等离子体( ) (4)等离子体具有导电性( ) (5)等离子体属于晶体,故属于纯净物( ) 答案:(1)× (2)× (3)× (4)√ (5)× 2.关于纳米材料,下列说法正确的是( ) ①纳米材料可大大提高材料的强度和硬度 ②纳米材料可提高材料的磁性 ③纳米材料能制作高贮存密度的量子磁盘 ④纳米机器人“医生”能进入人体杀死癌细胞 ⑤纳米是长度单位 A.①②③④⑤ B.②③④ C.②③④⑤ D.①②③④ 解析:选A 纳米材料的性能包括提高材料的强度、硬度、改变颜色、增强磁性等。纳米技术能制造出纳米“机器人”,进入人体杀死癌细胞,制作的量子磁盘,能作高密度的磁记录。纳米是长度单位。 [三级训练·节节过关]
1.下列物质中,不属于非晶体的是( ) A.玻璃 B.石蜡和沥青 C.塑料 D.干冰 解析:选D 干冰属于分子晶体,玻璃、石蜡、沥青、塑料均属于非晶体。 2.从我们熟悉的食盐、金属、冰到贵重的钻石等都是晶体,而同样透明的玻璃却是非晶体。下列关于晶体和非晶体本质区别的叙述中,正确的是( ) A.是否具有规则的几何外形的固体 B.是否具有固定组成的物质 C.是否具有美观对称的外形 D.内部基本构成微粒是否按一定规律做周期性重复排列 解析:选D 有规则几何外形或美观对称外形的固体不一定都是晶体,如玻璃制品可以塑造出规则的几何外形,也可以具有美观对称的外观;具有固定组成的物质也不一定是晶体,如某些无定形体也有固定的组成。晶体和非晶体的本质区别在于其微观结构不同。 3.有关液晶的叙述,不正确的是( ) A.液晶既具有液体的流动性,又具有晶体的各向异性 B.液晶最重要的用途是制造液晶显示器 C.液晶不是物质的一种聚集状态 D.液晶分子聚集在一起时,其分子间相互作用很容易受温度、压力和电场的影响 解析:选C 从液晶的结构特征看,液晶具有晶体的某些性质,如各向异性。在电场作用下,液晶分子能够沿电场方向排列,这也是制造液晶显示器的依据。液晶是介于液态和固态之间的一种聚集状态,故只有C选项错误。 4.等离子体的用途十分广泛,运用等离子体来切割金属或者进行外科手术,其利用了等离子体的特点是( ) A.微粒带有电荷 B.高能量 C.基本构成微粒多样化 D.准电中性 解析:选B 运用等离子体来切割金属或者进行外科手术,是利用了等离子体具有高能量的特点。
( 1.普通玻璃和水晶的根本区别在于( ) A.外形不一样 B.普通玻璃的基本构成粒子无规则地排列,水晶的基本构成粒子按一定规律周期性重复排列 C.水晶有固定的熔点,普通玻璃无固定的熔点 D.水晶可用于能量转换,普通玻璃不能用于能量转换 解析:选B 普通玻璃属于非晶体,水晶属于晶体,二者的根本区别在于内部结构不同。 2.下列关于各向异性的描述中正确的是( ) A.各向异性是指非晶体没有规则的几何形状 B.各向异性是指非晶体的物理性质与方向的关系 C.各向异性是指非晶体的内部结构与方向有关 D.各向异性是指晶体的物理性质与方向的关系 解析:选D 各向异性指晶体在不同的方向上表现出不同的物理性质。 3.下列关于等离子体的叙述中,错误的是( ) A.是物质的一种聚集状态 B.是一种混合物存在状态 C.具有导电性 D.基本构成微粒只有阴、阳离子 解析:选D 根据等离子体的构成,可知既有带电的阴、阳离子,也有中性的分子或原子,是个复杂的混合体系。 4.下列叙述正确的是( ) A.食盐粉末为非晶体 B.液体与晶体混合物叫液晶 C.最大维度处于纳米尺度的材料叫纳米材料 D.等离子体的外观为气态 解析:选D 食盐粉末仍由无数晶体颗粒组成;液晶是指外观为液态但具有晶体特性的物质;纳米材料指三维空间尺寸至少有一维处于纳米尺度的、具有特定功能的材料;等离子体是物质在气态的基础上进一步形成的气态微粒聚集体。 5.下列关于物质聚集状态的叙述中,错误的是( ) A.物质只有气、液、固三种聚集状态 B.气态是高度无序的体系存在状态 C.固态中的原子或者分子结合的较紧凑,相对运动较弱 D.液态物质的微粒间距离和作用力的强弱介于固、气两态之间,表现出明显的流动性 解析:选A 物质除气、液、固三种聚集状态以外,还有其他的聚集状态,如液晶、纳米材料、非晶体、等离子体。 6.下列说法不正确的是( ) A.晶体具有固定的熔、沸点,而非晶体没有固定熔、沸点 B.晶体与非晶体具有相同的性质 C.部分电子表、电脑的显示器是由液晶材料制成的 D.等离子体是一种很好的导电体,在信息产业等领域有非常好的应用前景 解析:选B 晶体与非晶体内部结构不同,故表现的性质不同。 7.下列关于特殊聚集状态应用的描述中,错误的是( ) A.运用等离子束切割金属 B.晶体合金的硬度和强度均比非晶体合金的硬度和强度高 C.液晶用于各种显示仪器上 D.化妆品中加入纳米颗粒可使其具备防紫外线的功能 解析:选B 某些非晶体合金的硬度和强度比晶体合金的硬度和强度高。 8.下列关于纳米技术的叙述不正确的是( ) A.将“纳米材料”均匀分散到液体分散剂中可制得液溶胶 B.用纳米级金属颗粒粉剂作催化剂可加快反应速率,提高反应物的平衡转化率 C.用纳米颗粒粉剂做成火箭的固体燃料将有更大的推动力 D.银器能抑菌、杀菌,纳米银微粒植入内衣织物中,有奇异的抑菌、杀菌效果 解析:选B 纳米材料的直径在1 nm~100 nm范围内,与胶粒直径范围相同,A正确;催化剂可加快化学反应的速率,但不能使化学平衡发生移动,B不正确;与块状固体相比,纳米颗粒直径小,表面积大,因而化学反应的速率快,所以短时间内可产生更大推动力,C正确;银为重金属,重金属微粒可使蛋白质变性,故有杀菌作用,D正确。 9.将下列物质和用途对应连接。 A金刚石 (1)用作导线 B金属铜 (2)显示器 C液晶 (3)吸光材料 D非晶体硅 (4)钻磨材料 答案:A—(4) B—(1) C—(2) D—(3)
1.液晶广泛用于电子仪表产品等,MBBA是一种研究较多的液晶材料,其化学式为C18H21NO,下列有关说法正确的是( ) A.MBBA属于有机高分子化合物 B.MBBA由碳、氢、氧、氮四种元素组成 C.MBBA中碳、氢、氧、氮的原子个数比为18∶21∶2∶1 D.MBBA中含有一氧化氮分子
