甲苯液相空气氧化制苯甲酸扩大实验报告
甲苯氧化
MnO2,用5~15ml热水少量多次冲
洗MnO2沉淀,滤液和洗液合并于
烧杯内,用冰水冷却。
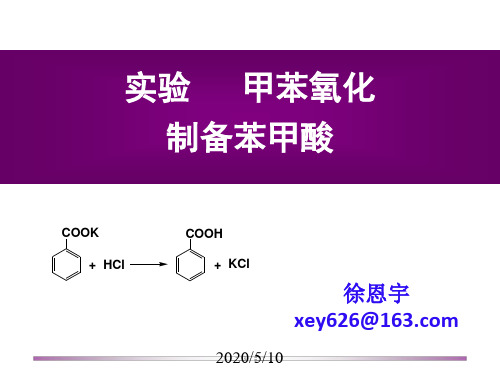
CH3 + 2KMnO4 COOK + KOH + MnO2 + H2O
有机化学实验
步骤: 3、酸化: 6mol/L HCl酸化→刚果红试纸深蓝色(pH值≤3,
白色苯甲酸析出) {若溶液仍呈淡棕色/紫色加少许固
Erlenmeyer flask
COOK + HCl COOH + KCl
Organic chemistry experiment
3. Vacuum filter 2nd:
need your Suction filtration and proper filter papers
After cooling thoroughly, filter benzoic acid under reduced pressure, wash it with a little cold water, keep filtering for 3 mins to dry thoroughly. Try to calculate the yield of your crude product?
实验 甲苯氧化 制备苯甲酸
COOK + HCl COOH + KCl
徐恩宇 xey626@
2015-4-25
有机化学实验
目的: 1、通过实验加深芳烃侧链氧化变成羧基的感性认识 2、掌握有机实验中的回流加热的方法
3、掌握减压过滤操作
原理:当苯环有侧链时,不管侧链长短,只要靠酸
有机化学实验
注意: 1、保证回流时间,回流温度不要过高(否则甲苯处 于气态),否则影响产率。
苯甲酸的制备实验报告

苯甲酸的制备实验报告
实验目的:
通过本实验,我们旨在掌握苯甲酸的制备方法,了解有机合成的基本原理和实验操作技巧。
实验原理:
苯甲酸的制备方法有多种,其中一种常用的方法是通过苯甲醛的氧化反应得到苯甲酸。
具体反应方程式如下:
C6H5CHO + [O] → C6H5COOH。
实验仪器与试剂:
1. 实验仪器,反应釜、冷凝器、蒸馏装置等。
2. 实验试剂,苯甲醛、氧化剂、溶剂等。
实验步骤:
1. 将苯甲醛溶解于适量溶剂中,得到苯甲醛溶液。
2. 在反应釜中加入苯甲醛溶液,然后加入氧化剂。
3. 开始加热反应釜,观察反应过程。
4. 反应结束后,进行蒸馏提取得到苯甲酸。
实验结果与分析:
通过实验操作,我们成功地制备得到了苯甲酸。
实验过程中需要注意控制反应温度和反应时间,避免产生副反应。
同时,也需要注意操作安全,避免接触有毒气体和化学品。
实验结论:
本实验通过氧化反应制备了苯甲酸,掌握了有机合成的基本原理和实验操作技巧。
同时也加深了对苯甲酸制备方法的理解,为今后的有机合成实验打下了基础。
总结:
苯甲酸的制备实验是有机合成实验中的重要内容,通过本实验的操作,我们不仅学会了具体的制备方法,还培养了实验操作技巧和安全意识。
希望大家能够在今后的实验中继续努力,掌握更多有机合成的知识和技能。
苯甲酸的实验报告

苯甲酸的实验报告1. 实验目的本实验旨在通过合成苯甲酸的实验,掌握苯甲酸的制备方法及其反应原理,并了解化学实验操作的基本技能。
2. 实验原理苯甲酸(C7H6O2)是一种有机化合物,也是一种常见的羧酸。
本实验中使用苯乙烯为原料,通过氧化反应制备苯甲酸。
反应方程式如下所示:苯乙烯 + 氧气→ 苯甲酸 + 水其中,氧气是氧化剂,苯乙烯是反应的底物。
3. 实验器材和试剂•实验器材:圆底烧瓶、反应容器、水浴锅、减压漏斗、漏斗支架、玻璃棒、窥视镜、试管架等•试剂:苯乙烯、浓硫酸、高锰酸钾、稀硫酸4. 实验步骤4.1 实验前的准备• 4.1.1 准备实验器材和试剂• 4.1.2 在实验室内做好充分通风的准备4.2 实验操作步骤• 4.2.1 在一个圆底烧瓶中加入30ml苯乙烯• 4.2.2 加入适量的浓硫酸,与苯乙烯进行反应• 4.2.3 将反应物移至反应容器中,并加入少量的高锰酸钾作为氧化剂• 4.2.4 放入水浴锅中进行加热• 4.2.5 观察反应过程,注意反应是否正常进行• 4.2.6 反应结束后,用稀硫酸对反应产物进行中和处理• 4.2.7 过滤产物并洗净,得到苯甲酸固体产物5. 实验结果与讨论通过以上实验操作步骤,成功合成了苯甲酸。
在实验过程中,我们观察到反应正常进行,没有发生意外情况。
反应结束后得到固体产物,经过过滤和洗净后得到纯净的苯甲酸。
苯甲酸是白色固体,有较强的刺激性气味。
在实验过程中,注意了防止苯甲酸的蒸气进入呼吸道,避免对人体造成伤害。
同时,在处理反应产物时,要注意避免与皮肤和眼睛接触。
6. 实验总结本次实验成功合成了苯甲酸,并且实验过程顺利完成。
通过这个实验,我们进一步学习了有机化学合成的基本方法,掌握了苯甲酸的制备技巧和操作要点。
同时,在实验过程中也加深了对实验安全的重视和操作技能的培养。
在今后的学习中,我们将进一步学习和探索有机化学合成的方法,提高实验技能,并注重实验安全,保证实验操作的准确性和可靠性。
苯甲酸制备实验装置操作说明1

甲苯空气氧化制苯甲酸实验装置说明一、前言本装置为塔式鼓泡反应器和玻璃精馏塔组成一套完整的苯甲酸制备实训装置,塔式设备广泛用于气液相反应或气液固相反应。
它是一个非均相反应过程,气体可为一种或多种类型,而液体可以为反应物或催化剂,其反应速度决定化学反应速度和两界面上组分分子扩散速度,充分接触是加快反应的必要条件,实验室常用该反应器做有机化合物氧化,如烷烃氧化制有机酸、对二甲苯氧化生成对苯二甲酸、环已烷氧化生成环己醇和环已酮、乙醛氧化制乙酸、乙烯氧化制乙醛、苯氯化制氯苯、甲苯氯化制氯甲苯、乙烯氯化制氯乙烯、烯烃加氢、脂肪酯加氢等。
此外,还可进行SO3、NO2、CO2、H2S的吸收反应、生化反应、污水处理等。
采用鼓泡氧化反应器的原因是:(1)进气体能以小气泡形式分布,可连续不断进入保证气液接触反应效果良好;(2)反应器结构简单,容易稳定操作;(3)有较高的传质、传热效率,适于慢反应和强放热反应;(4)换热件安装方便。
可处理悬浮液体,塔内可填加构件;采用精馏塔分离的原因是:(1)从苯甲酸与甲苯混合液中分离回收甲苯;(2)从粗苯甲酸溶液中提纯苯甲酸。
采用分相器的原因是:氧化反应会产生一些水,水会影响甲苯转化,故必须排水,排水过程甲苯也会排出,用分相器可使甲苯与水分离。
二、技术指标1、最高操作压力0.6MPa,使用温度170℃。
2、甲苯氧化反应器,下段φ57×4mm,高度440mm,外加套76mm,内插加热管φ10×1.5mm;上段φ89×4mm,外加套108mm,高度150mm。
气体分布器开孔率10%。
3、转子流量计N2 0.1—10L/min、O20.2—20L/min。
4、热液体循环齿轮泵30L/hr。
5、无油空压机1000L/hr。
6、导热油加热器25—150℃。
7、甲苯加料电磁泵0.79L/hr。
8、精馏塔釜1L,电热包加热功率400w、精馏塔直径20mm,塔高1400mm,塔外壁有两段透明膜导电加热保温,加热功率各200w。
苯甲酸的合成_实验报告
有机化学实验报告 2010 年 10 月 11 日第一部分:实验预习部分一、实验目的(要求)1.学习由芳香烃通过氧化反应制备羧酸的原理和方法。
2.掌握电动搅拌器的安装及使用方法。
3.进一步熟练回流加热和减压过滤等基本操作。
二、实验原理(概要)1、反应方程式C6H5CH3+2KMnO4→C6H5COOK+KOH+2MnO2+H2O4KMnO4+6NaHSO3+2KOH=4MnO2+3K2SO4+3Na2SO4+4H2OC6H5COOK+HCl→C6H5COOH+KCl2、粗产品纯化过程及原理滤液滤渣C6H5COOK,KOH,K2SO4,Na2SO4,NaHSO3,H2O MnO2冷却浓盐酸C6H524242滤液滤渣KCl,K2SO4,Na2SO4,NaCl,H2O,HCl C6H5COOH,H2O干燥C6H5COOH三、装置图:搅拌回流反应装置减压过滤装置五、实验过程概述②100ml H210ml H2O冲洗量筒通冷却水③5.4ml加热回流液中几乎无油珠时撤去电热套冰水冷却停止加热反应液用水降温加入适量NaHSO3玻璃棒不断搅拌滤渣干燥、称质量、计算产率加入浓盐酸第二部分:实验过程及结果记录部分一、实验仪器、试剂和材料1.仪器:三口烧瓶(250ml)、球形冷凝管、电热套、升降台、水浴锅、电动搅拌装置(电动搅拌器、搅拌棒、搅拌器套管)、抽滤装置(抽滤瓶、布氏漏斗、水泵)、量筒、胶头滴管、玻璃棒、表面皿、洗瓶、天平等。
2.试剂:甲苯(AR,5.4ml)、高锰酸钾(AR,16.0g)、亚硫酸氢钠固体(AR)、浓盐酸(AR,36%-38%)、蒸馏水,甘油。
3.材料:中速定性滤纸、广泛pH试纸、冰块。
二、实验步骤及现象记录第三部分:实验结果分析及思考题一、数据处理1.产率计算产品理论产量:m理论= 0.05×122.12 g = 6.1g产品实际质量:m实际= 5.1g83.6%100%6.15.1100%mm率理=⨯=⨯=论实际产2.结果分析(1)可引起产量减小的原因:①在搅拌下反应不够完全,仍有少量甲苯剩余,可适当增加高锰酸钾的用量。
食品添加剂苯甲酸的合成(氧化)

食品添加剂苯甲酸的合成1.1合成苯甲酸的工作任务1.苯甲酸概述苯甲酸又名安息香酸,是一种重要的精细有机化工产品,世界年产量达数十万吨。
苯甲酸主要用于生产苯甲酸钠食品防腐剂、染料、农药、增塑剂、媒染剂、医药、香料的中间体,还可用作醇酸树脂和聚酰胺树脂的改性剂,用于生产涤纶的原料对苯二甲酸以及用作钢铁设备的防锈剂等。
1.2苯甲酸合成任务分析1.2.1 苯甲酸分子结构的分析首先要搞清需要合成的物质是什么?对于有机化合物而言,必须搞清楚其分子结构式、分子的基本骨架结构、相关基团组成以及连接的方式等。
①苯甲酸分子式:C6H5C00H。
②苯甲酸分子结构式:不难看出,目标化合物基本结构为苯的结构,在苯环上接有一个羧基。
1.2.2 苯甲酸的合成路线分析一种化合物的制备路线可能有多种,但并非所有的路线都能适用于实验室合成或工业化生产,选择正确的制备路线是极为重要的。
比较理想的制备路线几乎应同时具备下列条件:①原料资源丰富,价廉易得,生产成本低;②副反应少,产物容易分离、提纯,总收率高;③反应步骤少,时间短,能耗低,条件温和,设备简单,操作安全方便;④产生的废水、废气、废渣少,“三废”能得到有效控制,不污染环境;⑤副产品可综合利用。
物质的制备过程中还经常需要应用一些酸、碱及各种溶剂作为反应的介质或精制的辅助材料,如能减少这些材料的用量或用后能够回收,便可节省费用,降低成本,避免对环境的污染。
另一方面,制备中如能采取必要措施避免或减少副反应的发生及产品分离、提纯过程中的物料损失,就可有效地提高产品的收率。
因此,要选择一条合理的产品制备路线,根据不同的原料有不同的方法。
何种方法比较优越,需要综合考虑各方面的因素,最后确定一条技术可行、经济效益较好、符合国家环保要求的制备路线。
在有机化学课程里,我们学习了有关苯环侧链氧化的知识,即中性或碱性条件时苯环的侧链在强氧化剂(如高锰酸钾)的作用下,侧链可被氧化为羧基。
故要合成苯甲酸,可以用含侧链的苯(如甲苯、乙苯等)为原料,在中性或碱性条件下经高锰酸钾(或其它氧化剂,可在酸性条件下)氧化即可。
苯甲酸制备实验装置操作说明
甲苯空气氧化制苯甲酸实验装置说明一、前言本装置为塔式鼓泡反应器和玻璃精馏塔组成一套完整的苯甲酸制备实训装置,塔式设备广泛用于气液相反应或气液固相反应。
它是一个非均相反应过程,气体可为一种或多种类型,而液体可以为反应物或催化剂,其反应速度决定化学反应速度和两界面上组分分子扩散速度,充分接触是加快反应的必要条件,实验室常用该反应器做有机化合物氧化,如烷烃氧化制有机酸、对二甲苯氧化生成对苯二甲酸、环已烷氧化生成环己醇和环已酮、乙醛氧化制乙酸、乙烯氧化制乙醛、苯氯化制氯苯、甲苯氯化制氯甲苯、乙烯氯化制氯乙烯、烯烃加氢、脂肪酯加氢等。
此外,还可进行SO3、NO2、CO2、H2S的吸收反应、生化反应、污水处理等。
采用鼓泡氧化反应器的原因是:(1)进气体能以小气泡形式分布,可连续不断进入保证气液接触反应效果良好;(2)反应器结构简单,容易稳定操作;(3)有较高的传质、传热效率,适于慢反应和强放热反应;(4)换热件安装方便。
可处理悬浮液体,塔内可填加构件;采用精馏塔分离的原因是:(1)从苯甲酸与甲苯混合液中分离回收甲苯;(2)从粗苯甲酸溶液中提纯苯甲酸。
采用分相器的原因是:氧化反应会产生一些水,水会影响甲苯转化,故必须排水,排水过程甲苯也会排出,用分相器可使甲苯与水分离。
二、技术指标1、最高操作压力0.6MPa,使用温度170℃。
2、甲苯氧化反应器,下段φ57×4mm,高度440mm,外加套76mm,内插加热管φ10×1.5mm;上段φ89×4mm,外加套108mm,高度150mm。
气体分布器开孔率10%。
3、转子流量计N2 0.1—10L/min、O20.2—20L/min。
4、热液体循环齿轮泵30L/hr。
5、无油空压机1000L/hr。
6、导热油加热器25—150℃。
7、甲苯加料电磁泵0.79L/hr。
8、精馏塔釜1L,电热包加热功率400w、精馏塔直径20mm,塔高1400mm,塔外壁有两段透明膜导电加热保温,加热功率各200w。
苯甲酸实验报告数据
一、实验目的1. 掌握苯甲酸的制备原理及实验操作步骤。
2. 学习苯甲酸的提纯方法,提高苯甲酸的纯度。
3. 了解苯甲酸的物理性质及化学反应。
二、实验原理苯甲酸(C6H5COOH)是一种重要的有机酸,广泛用于食品、医药、化工等领域。
本实验采用甲苯氧化法制备苯甲酸,通过苯甲酸的溶解度随温度变化较大的特性,采用重结晶法进行提纯。
三、实验仪器与试剂1. 仪器:烧杯、铁架台、酒精灯、普通漏斗、玻璃棒、坩埚钳、滤纸、石棉网、药匙、三脚架、试管、胶头滴管、火柴等。
2. 试剂:甲苯、硝酸、硫酸、蒸馏水、NaOH、活性炭等。
四、实验步骤1. 苯甲酸的制备(1)将一定量的甲苯加入烧杯中。
(2)向烧杯中加入适量的硝酸和硫酸,混合均匀。
(3)加热烧杯,使反应液温度保持在60-70℃。
(4)反应一段时间后,停止加热,用玻璃棒搅拌反应液。
(5)将反应液倒入过滤器中,过滤掉杂质。
2. 苯甲酸的提纯(1)将过滤后的反应液加热至沸腾,加入适量的NaOH溶液,调节pH值至8-9。
(2)加入活性炭,搅拌反应液,使苯甲酸充分吸附。
(3)将反应液过滤,去除活性炭。
(4)将滤液加热至沸腾,逐渐加入NaOH溶液,使苯甲酸沉淀。
(5)将沉淀物过滤,用蒸馏水洗涤沉淀物。
(6)将洗涤后的沉淀物干燥,得到苯甲酸纯品。
五、实验数据1. 苯甲酸的制备(1)甲苯用量:10g(2)硝酸用量:5mL(3)硫酸用量:5mL(4)反应时间:1.5h(5)苯甲酸产量:约3g2. 苯甲酸的提纯(1)NaOH用量:10g(2)活性炭用量:1g(3)洗涤次数:3次(4)苯甲酸纯度:>98%六、实验结果分析1. 本实验成功制备了苯甲酸,产率为30%。
2. 通过重结晶法,苯甲酸的纯度达到了98%以上,达到了实验要求。
3. 实验过程中,苯甲酸的制备和提纯过程较为简单,操作方便。
七、实验讨论1. 在苯甲酸的制备过程中,控制反应温度和反应时间是关键因素。
2. 在苯甲酸的提纯过程中,活性炭吸附效果较好,能有效去除杂质。
苯甲酸制备__第三组
急救措施 防护措施
苯甲 酸
可燃、 刺激性
对皮肤有轻度刺激性 。蒸气对上呼吸道、 眼和皮肤产生刺激。 本品在一般情况下接 触无明显的危害性。
LD50:2530 mg/kg(大鼠经口) ;2370 mg/kg(小
鼠经口)
食入:饮 足量温水 ,催吐。 就医。
戴化学安 全防护眼 镜、穿防 毒物渗透 工作服、 戴橡胶耐 油手套。
手套。
佩戴自吸过
盐酸
眼结膜炎、 眼结膜炎、
灼伤
灼伤
无
食入:用水 漱口,给饮 牛奶或蛋清 。就医。
滤式防毒面 具(全面罩 )、穿橡胶 耐酸碱服、 戴橡胶耐酸
碱手套。
LOGO
苯甲醛
可燃、有毒 、刺激性
有刺激性,
但不足以造 成危害
LD50:1300 mg/kg(大鼠
经口)
食入:饮足
量温水,催 吐。就医。
74.551
易溶于 水、醚 、甘油 及碱类 ,微溶 于乙醇 ,但不 溶于无 水乙醇 。
770℃
——
——
——
LD50: 小鼠腹 腔注射 552
LOGO
三、原料、产品的分析测试草案 1、苯甲酸 气相色谱法 仪器:气相色谱仪 2、甲苯 甲苯测试仪检测 3、氯化钾 沉淀滴定法 滴定管
LOGO
Page 2
LOGO
3、以苯甲醛合成 苯甲醛经坎尼扎罗反应得到苯甲酸与苯甲醇,苯甲醇可通
过蒸馏除去。
4、以溴苯合成 溴苯加入格氏试剂反应形成苯甲酸 5、以氯苯合成 氯苯经由碱性的过氧化锰反应氧化形成苯甲酸 6、甲苯、高锰酸钾合成 甲苯+高锰酸钾+水——苯甲酸钾+氢氧化钾+二氧化锰+水 7、苄卤氧化法 苄氯用高锰酸钾做催化剂,氧化得到
苯甲酸的制备实验
苯甲酸的制备实验实验原理:制备苯甲酸的常用方法是氧化反应。
芳香族羧酸通常用氧化含有α-H的芳香烃的方法来制备。
制备羧酸采用的都是比较强烈的氧化条件,因此控制反应在一定的温度下进行非常重要。
本实验中,主要反应为苯甲酸的制备反应。
反应试剂、产物、副产物的物理常数:反应试剂:高锰酸钾、甲苯、水;产物:苯甲酸;副产物:二氧化锰。
药品:高锰酸钾、甲苯、浓盐酸。
实验装置图:电动搅拌器、回流搅拌装置、抽滤装置。
实验流程:1.在250ml三口圆底烧瓶中放入1.4ml甲苯和70ml水,加热至沸。
2.从冷凝管上口分批加入4.3g高锰酸钾,粘附在冷凝管内壁的高锰酸钾最后用25ml水冲洗入瓶内。
3.继续煮沸并间歇摇动烧瓶,直到甲苯层几乎近于消失、回流液不再出现油珠(约需4-5h)。
4.将反应混合物趁热减压过滤,用少量热水洗涤滤渣(MnO2)。
合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化(刚果红试纸检验),至苯甲酸析出完全。
5.将析出的苯甲酸减压过滤,用少量冷水洗涤,挤压去水分。
把制得的苯甲酸放在沸水浴上干燥。
产量:约1.0g。
6.若要得到纯净产品,可在水中进行重结晶。
纯净的苯甲酸为白色片状或针状晶体,熔点mp=122.4℃。
制备过程:首先安装制备装置,包括电动搅拌器、回流冷凝管和250ml三口圆底烧瓶。
将甲苯和水加入烧瓶中并加热至沸,然后分批加入高锰酸钾。
继续煮沸并间歇摇动烧瓶,直到甲苯层几乎近于消失、回流液不再出现油珠。
将反应混合物趁热减压过滤,用少量热水洗涤滤渣(MnO2)。
合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化(刚果红试纸检验),至苯甲酸析出完全。
将析出的苯甲酸减压过滤,用少量冷水洗涤,挤压去水分。
把制得的苯甲酸放在沸水浴上干燥。
产量约为1.0g。
若要得到纯净产品,可在水中进行重结晶。
最终得到的苯甲酸为白色片状或针状晶体,熔点为122.4℃。
注:文章中没有明显的格式错误或有问题的段落,因此无需删除和改写。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
甲苯液相空气氧化制苯甲酸扩大实验报告
一、实验目的
本次实验的目的是探索用空气氧化法制取苯甲酸的工艺条件。
二、实验原理
苯甲酸的制备常用空气氧化法:空气与甲苯混合通过超声氧化反应,生成氧化产物,然后将氧化产物与强碱反应,最终得到苯甲酸。
三、实验方法
(1)首先将甲苯和氧气按照1:1的比例混合在一容器内,再施加超声波,使甲苯完成高效氧化反应。
(2)将甲苯氧化产物灌入钠基固定床中,然后加入27wt%的碳酸氢钠溶液作为反应剂。
(3)调节反应的温度为70~80℃,碳酸氢钠浓度约为30%,反应时间约为2小时,用大火加热推进反应,气流方向从上往下,以保证产物完全回流。
(4)冷却后,将反应物过滤,用水过滤等方法将反应产物稀释,再经过中和处理,最后经过沉淀分离得到苯甲酸。
四、实验结果
通过本次实验,苯甲酸的收率可达到83%,且其中残留物极低,保证制备的苯甲酸产品质量较高。
五、实验结论
本次实验获得了较高的收率,说明采用空气氧化法制取苯甲酸,其收率高、浩昂极低,属于一种较优的工艺方法。
