电沉积理论
乏燃料中稀土在熔盐中电沉积过程机理研究

乏燃料中稀土在熔盐中电沉积过程机理研究乏燃料中稀土是指含有镧系稀土元素的燃料,在熔盐中电沉积是指将乏燃料中的稀土元素通过电沉积的方式提取出来。
这一过程的机理研究包括以下几个方面:
1.电沉积原理:电沉积是利用电场的力使某些物质在电极上沉积的
过程。
在熔盐中电沉积时,熔盐会扮演电解质的角色,将稀土元素的离子提取出来。
2.稀土元素的电沉积行为:稀土元素在熔盐中的电沉积行为受到电
极材料、电解质种类、温度、电流密度等因素的影响。
3.电沉积过程中的化学反应:在熔盐中电沉积过程中,会发生许多
化学反应,影响着稀土元素的提取效率和产物的质量。
4.电沉积的工艺条件:电沉积的工艺条件包括电极材料、电解质种
类、电流密度、温度等,应根据研究目标和实际情况确定。
5.电沉积产物的特性:稀土元素在熔盐中电沉积后得到的产物具有
独特的特性,如结构、形貌、晶体等。
这些特性可以影响稀土元素的分离和回收率,也可以对稀土元素的用途产生影响。
总之,稀土元素在熔盐中电沉积过程是一个复杂的过程,涉及许多方面的机理。
研究这一过程的机理,有助于提高稀土元素的提取效率,并且为稀土元素的应用提供理论依据。
电镀理论

(一) 法拉第定律第一定律──在镀液进行电镀时(电解)阴极上所“附积”的金属重量(或阳极所溶蚀者)与所通过的电量成正比. 第二定律──在不同镀液中以相同的电量进行电镀时,其各自附积出来的重量与其化学当量成正比.上述第一定律中的“电量”,即为电流强度与时间的乘积,理论单位是库伦,实肜电位为安培.分或安培.小时. 以硫酸铜中的二价铜离子为例,其第一个库伦的电量在100%的阴极效率下可以镀出0.3294mg的纯铜,每1安培小时可镀出1.186g的纯铜.电量越多镀出越多.第二定律是对不同镀液的比较而言,上述的镀铜量是指硫酸铜的二价铜离子而言,若镀液换成氰化铜液的一价铜离子之时,则同样1个安培小时的电量可以镀出纯铜2.372g,只因1价铜的化当量为63.57/1,2价铜的化学当量是63.57/2,故前者的附积量在同电量时是后者的两倍.(二) 阴极膜电镀进行时愈接近阴极被镀物表面时其金属离子浓度愈低,现以其浓度下降1%处起直到被镀物表面为止的一薄层液膜称之为“阴极膜”.薄层中由于金属离子渐少且发生氢气以致电阻增加导电不良阻碍金属之顺利登陆.且此膜也因镀体之外形起伏而有原薄不同,外形凸起峰处膜层较薄故远方之高浓度离子容易补充使该处优先被镀上,即所谓之高电流密度区,反之低凹谷处自然不容易镀上.现将各局部区域之电流强度以公式讨论之: Ilim=nFADCb/∮Ilim──局部区域电流之大小n───电子数F───法拉第常数(镀出1g金属所需之电量) A───该处面积大小D───金属离子之扩散系数Cb──大量镀液之平均浓度∮──阴极膜厚度由上式可知降低阴极膜的厚度有助于镀层之均匀.故电镀需作各种搅拌如吹气、镀流动、阴极的摆动等其目的都在降低阴极膜的厚度,在接近被镀物表面处得以增多金属离子的供应量.(三) 镀液的电阴总电阴=外路及接点+生液体+阴极膜.电路板在进行量产时待镀的面积都很大,故需要的直流电流也极高而常达数千安培,为求良好的镀层其电压多控制在5伏之下.但按A=V/R之公式看来,其总电阻必须极小才能满足此奥姆定律,故应保持外路及接点低外路及接点,加热镀液以降低生液体,搅拌镀液以降低阴极膜.否则电压太高了会造成水彼电,解会产生多量的气压,大大影响镀层的品质.(四) 当金属浸于其盐类之溶液中时,其表面即发生金溶成离子或离子登陆成为金属之置换可逆反应,直到某一电位下达到平衡.若在常温常压下以电解稀西安液时白金阴极表面之氢气光做为任意零值,将各种金属与此“零值极”连通做对比时,可找各种金属对氢标准电极之电位来.再将金属及其离子间之氧化或还原电位对NHE比较排列而成“电化学次序”或电动次序.以还原观点而言,比氢活泼的金属冠以负值使其排列在氢的上位,如锌为-0.762,表示锌很容易氧化成离子,不容易登陆成金属,理论上至少要外加0.762V以上才能将之镀出. 比氢高贵者冠以正值,排在氢的下位。
电沉积法制备多孔金属材料的研究

电沉积法制备多孔金属材料的研究随着科学技术的不断发展和创新,许多新的制备材料的方法也随之涌现。
其中,电沉积法是一种非常重要的制备技术,它可以利用电化学原理在电极表面上制备各种材料。
多孔金属材料是一类具有很好性能的新兴材料,在很多领域都有广泛的应用前景。
本文将阐述电沉积法制备多孔金属材料的研究进展和方法。
一、多孔金属材料的研究现状多孔金属材料是指表面或内部具有微孔和介孔的金属材料。
这种材料相较于传统的普通金属材料,具有更大的比表面积和更好的吸附性能等优点,因而在光催化、电催化、电极等领域有广泛的应用。
以光催化为例,多孔金属材料由于其多孔的结构,在提高催化剂利用率的同时,也能够提高反应速率和稳定性。
因此,多孔金属材料在新能源、环境保护、生命医学等领域中都有着很大的应用前景。
二、电沉积法制备多孔金属材料的基本原理电沉积法是一种通过电极表面的化学反应,在电极表面沉积金属或合金的方法。
其基本原理是利用电化学原理,在外场的作用下,将无机离子从电解质中沉积在电极上,从而形成所需的材料。
在制备多孔金属材料时,电沉积法可通过控制电极电位、电流密度和电解液的成分和条件等参数,调整所沉积的金属材料的孔径大小、形貌和分布等特征,从而达到制备所需的多孔金属材料的目的。
三、电沉积法制备多孔金属材料的制备步骤(1)电解液溶液制备电解液是电沉积法制备多孔金属材料时不可忽略的一个重要参数。
具体来说,它需要提供必要的金属离子,同时还要满足调节电极电位、控制沉积速率和影响孔径大小等多重作用。
因此,电解液的选择对于制备多孔金属材料来说至关重要。
(2)电极材料选择电极材料的选择直接影响多孔金属材料的品质和形态。
以普通的铜箔为例,酸性电解液可以使其表面产生空洞;而碱性电解液中,即使使用铜颗粒作为电极,也无法实现孔径的控制。
因此,在选择电极材料的过程中,需要考虑其特性和适用性,并对不同电解液的特殊适应性进行测试。
(3)电化学条件的控制在电沉积制备多孔金属材料时,电化学条件的控制也是十分关键的一点。
电沉积Pt的成核与生长机理
电沉积Pt的成核与生长机理
2016-09-23 12:33来源:内江洛伯尔材料科技有限公司作者:研发部
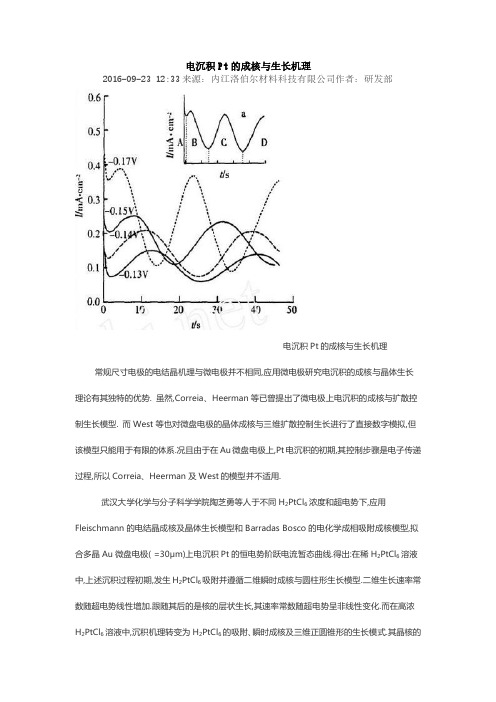
电沉积Pt的成核与生长机理常规尺寸电极的电结晶机理与微电极并不相同,应用微电极研究电沉积的成核与晶体生长理论有其独特的优势. 虽然,Correia、Heerman等已曾提出了微电极上电沉积的成核与扩散控制生长模型. 而West等也对微盘电极的晶体成核与三维扩散控制生长进行了直接数字模拟,但该模型只能用于有限的体系.况且由于在Au微盘电极上,Pt电沉积的初期,其控制步骤是电子传递过程,所以Correia、Heerman及West的模型并不适用.
武汉大学化学与分子科学学院陶芝勇等人于不同H2PtCl6浓度和超电势下,应用Fleischmann的电结晶成核及晶体生长模型和Barradas Bosco的电化学成相吸附成核模型,拟合多晶Au微盘电极( =30μm)上电沉积Pt的恒电势阶跃电流暂态曲线.得出:在稀H2PtCl6溶液中,上述沉积过程初期,发生H2PtCl6吸附并遵循二维瞬时成核与圆柱形生长模型.二维生长速率常数随超电势线性增加.跟随其后的是核的层状生长,其速率常数随超电势呈非线性变化.而在高浓H2PtCl6溶液中,沉积机理转变为H2PtCl6的吸附、瞬时成核及三维正圆锥形的生长模式.其晶核的
垂直生长速率常数k PERP比水平生长速率常数k PARA大两个数量级以上.况且,logk PERP随超电势线性增加,而logk PARA则随超电势呈反S形变化的关系.相同超电势下,无论k PERP还是k PARA,均比稀H2PtCl6溶液中的二维层状生长速率常数大几个数量级.。
电镀基本原理及应用

电镀液覆盖能力的测定 • 电镀液的覆盖能力 表征镀层在镀件的深凹部位或内孔部位能否镀 上镀层的能力 • 影响因素 1.基体金属本性的影响 2.基体金属组织均匀程度的影响 3.基体金属表面关态的影响 测定方法 1.直角阴极法 2.内孔法 3.凹穴法 4.平行阴极法
18
电镀Hull Cell试验 • 电镀过程中,电流的初次分布取决于溶液的电阻,溶液的电阻与阴 极之间的距离成正比。Hull Cell槽就是利用电流密在远,近阴极上 分布不同的原理,设计一种 平面阴极和平面阳极构成一定斜度的小 型电镀试验槽。 • • • • • • Hull Cell槽用途 1. 1.确定电镀工艺的电流密度范围 。 2.维护和调整镀液 3.电镀工艺的研究 4.测量镀液的分散能力 5.测量镀液的整平能力
电镀液性能的测试技术
• • • • • •
1.电镀液的pH值的测定 2.电镀液阴极电流效率的测定 3.电镀液分散能力的测定 4.电镀液覆盖能力的测定 5.电镀Hull Cell试验 6.电镀液整平能力的测定
13
电镀液的pH值的测定 一.用pH试纸测pH值 pH试纸是用滤纸浸泡在几种酸碱指示剂的混合液中,取出后经 晾干而制成。在不同的酸性或碱性溶液中会显示不同的颜色。 二.pH计法测pH值 pH也称酸度计,仪器的基本原理相当一台电位测量仪,采用玻 璃电极为测量电极,甘汞电极为参比电极,测量两电极在溶液中的 电位差,溶液中氢离子的浓度不同,则玻璃电极有不同的电位,经 过信号的转换处理,把测的电位值显示为pH值。
15
电镀液分散能力的测定 一.电镀液分散能力 表征镀层厚度分布的均匀性,用“分散能力”这一术语,其含义是 “电 镀液所具有的使镀件表面镀层厚度均匀分布的能力”。 二.电极在阴极表面的分布情况 (一)电流通过电镀槽时遇到的阻力 1.金属电极和导线的欧姆电阻(Rd)。 2.电解液本身的溶液欧姆电阻(Rr). 3.当电流通过电极和溶液的两相界面时也有一定的阻力,这个阻力是由于电化学反应 过程或离子放电过程的迟缓引起的电化学极化和浓差极化所造成的,称之为极化电 阻(Rj)。 (二)电流在电极表面的分布 1.电流的初次分布 假设极化电阴不存在,Rj=0,只讨论溶液欧姆电阻(Rr)对阴极电 流分布的影响,我们把该情况下的电流分布称之为电流的初次分布。 2.电流的二次分布 在电镀过程中,阴极极化是一定存在的,也就是说极化电阻Rj必 然要影响电流在阴极上的分布,此时的电流分布称之为电流的二次分布或称为电流 的实际分布。 电解液的分散能力就用电流的二次分布与初次分布的相结偏差来表示。 分散能力表达式:T= K-(I1/I2) ×100% K
电泳沉积和电化学沉积

电泳沉积和电化学沉积全文共四篇示例,供读者参考第一篇示例:电泳沉积和电化学沉积都是一种利用电化学原理进行材料沉积的技术,广泛应用于表面涂层、薄膜制备和纳米材料合成等领域。
它们在材料科学和工程领域具有重要的应用价值,能够实现对材料表面和结构的精确控制,提高材料的性能和功能。
电泳沉积是一种利用电场作用下的粒子在电解质溶液中沉积到电极表面的方法。
它的原理是在电场的作用下,带有电荷的颗粒会在电极表面沉积形成涂层。
通过控制电场强度、溶液浓度和沉积时间等参数,可以实现对沉积膜厚度、成分和结构的调控。
电泳沉积具有沉积速度快、成本低、操作简单等优点,适用于制备复杂形状和微纳米尺度结构的材料。
电化学沉积是利用电化学反应在电极表面沉积材料的方法。
通过在电解质溶液中加入含有金属离子的溶液,并在电极表面施加电压或电流,金属离子可以在电极表面还原成金属形成沉积层。
电化学沉积的优点在于对沉积层的成分和结构具有很好的控制能力,可以实现对材料性能的精确调控。
电化学沉积也具有较高的沉积速度和成本效益,适用于大面积、均匀沉积的需求。
电泳沉积和电化学沉积在材料表面涂层、薄膜制备和纳米材料合成等领域都具有重要的应用价值。
在表面涂层方面,通过调控沉积参数,可以实现对涂层的厚度、成分和结构的精确控制,提高涂层的耐磨性、耐腐蚀性和导电性等性能。
在薄膜制备方面,电泳沉积和电化学沉积可以实现对薄膜的组分和结构的精确控制,制备出具有特定功能的薄膜,如光电材料、催化剂和传感器等。
在纳米材料合成方面,电泳沉积和电化学沉积可以实现对纳米粒子的精确控制,制备出具有特定形貌和性能的纳米材料,如纳米线、纳米颗粒和纳米管等。
电泳沉积和电化学沉积是一种灵活、高效的材料制备技术,具有多样化的应用前景。
随着材料科学和工程领域的不断发展,电泳沉积和电化学沉积技术也将不断完善和创新,为材料研究和应用提供更多的可能性。
希望通过本文的介绍,读者对电泳沉积和电化学沉积有更深入的了解,并进一步探索它们在材料领域的应用和发展。
金属的电沉积
(P83)
由此我们可以得出络合离子的直接还原理论的结 论是:络合物的电解液中,在阴极上直接放电的 络合离子既不是简单的金属离子,也不是浓度最 大的具有特征配位数的络合离子,而是配位数较 低、且浓度适中的络合离子。 关于络合离子的直接还原理论,我们可以通过以 下几方面作进一步的阐述: 为什么不是配位数较高的络合离子放电? (1) 配位体和金属离子形成络合离子以后,使得
考虑了未通电时络合离子的离解平衡反应,而没 有考虑到通电以后电极反应的特征。那么,在溶 液中的不同配位数的各种络合离子又是哪一种络 合离子在电极上直接放电呢?例如在碱性镀锌溶 液中,电解液的组成主要是ZnO和NaOH,OH-离 子和Zn2+离子形成络合物的形式有以下几种:
Zn2+ + OH- Zn(OH)+ + OH- Zn(OH)2 Zn(OH)2 + OH- Zn(OH)3- + OH- Zn(OH)4当OH-离子的浓度比Zn2+离子的浓度大的多时, 锌的氢氧络离子的特征配位数为4,即在碱性镀
[M(H2O)x]n+ + ne = M + xH2O 实际上,它的还原过程是分好几步进行的,具体如
下:
(1) 水合金属离子失去部分水化膜 [M(H2O)x]sn+ [M(H2O)x-y]吸附n+ + yH2O
(2) 电子在电极和离子之间跃迁,生成带有部分 水化层的金属原子
[M(H2O)x-y]吸附n+ +ne = [M(H2O)x-y]吸附 (3) 金属原子失去剩余的水化膜变成金属原子
[M(H2O)x-y]吸附= M原子 + (x-y) H2O M原子 → M晶核 M晶核 → M晶格 上述还原反应的历程实际上只适合一价金属离
化学中的电沉积技术
化学中的电沉积技术电沉积技术是通过电化学反应的原理,将金属离子还原成为固体金属,沉积在电极表面的一种技术。
电沉积技术广泛应用于电子工业、材料工业以及制造业领域。
在化学工业中,电沉积技术是实现表面处理和增强金属材料耐腐蚀性的关键技术之一。
电沉积技术的原理是基于电解质溶液和金属电极之间发生的反应。
当电解质中含有金属离子时,将电极浸入其中,并在电极表面通以电流,电化学反应开始发生。
电流流过电解质时,金属离子被加电,成为金属原子,并沉积在电极表面。
这个过程可以被独立的改变,以产生不同的沉积表面形态和金属结构。
电沉积技术有多种应用。
最常见的应用是通过该技术实现金属表面的处理,以改善金属的表面性能。
例如,电镀铬可以增强不锈钢的耐腐蚀性和保护钢材表面损伤;电镀镍可以改善金属表面的摩擦和磨损性,电镀铜则可以对不锈钢进行表面涂覆,以增加其导电性能。
此外,电沉积技术在制造和维修汽车、航空、医疗器械和精密仪器等方面也有广泛的应用。
电沉积技术已经发展成为一门独立的学科领域,被广泛研究和应用。
在众多的电沉积技术中,电沉积合金是最为常见的技术之一。
通过将两种或更多金属组成合金,可以生成出有特殊性质的金属合金,为制造高质量材料奠定了基础。
电沉积合金的主要优点是可以生产出不同比例的合金,包括具有纯金属性质、合金性质、金属和非金属复合材料以及多达几百种复合材料,以满足不同的工业领域的需求。
除了电沉积合金外,还有纳米电沉积技术。
纳米电沉积技术是通过控制沉积液中溶解度,使金属离子浓度保持在一个亚纳米尺度范围内,使其得到自组装,从而在纳米尺度下生成金属薄膜。
该技术已经成为了纳米材料制备中最常用的方法之一,并在光电领域、生物医学、能源储存和电化学催化等方面有着广泛应用。
总之,电沉积技术已经成为化学中一个非常重要的技术,具有广泛应用的前景。
通过对电沉积技术进行更深入的研究,不仅能够提高其应用效率和产品质量,还能够不断创新和发展,为各行各业的制造和研究领域提供更加丰富和多样的技术支持。
电沉积技术制备金属纳米结构的研究
电沉积技术制备金属纳米结构的研究金属纳米结构在纳米科技领域中占有重要地位,因其在光学、电子、催化、医学以及传感器等领域中的应用前景广阔。
电沉积技术作为一种重要的制备金属纳米结构的方法,被广泛应用于金属纳米结构的制备领域。
本文将从电沉积技术的基本原理、常见的电解液及其影响因素、金属纳米结构的制备方法以及电沉积制备金属纳米结构的研究现状等方面进行介绍。
一、电沉积技术的基本原理电沉积又称电化学沉积,是指通过在电极表面施加稳定的电场以控制导体表面的离子沉积。
这种方法可以制备出具有高度相同形状、结构和组成的纳米颗粒或纳米线。
电沉积技术可以实现精密的控制、恒定的环境条件下的结构调节和形貌控制,并且可以在不同的电解液体系中进行。
二、常见的电解液及其影响因素常见的电解液有硫酸铜、硫酸镍、硫酸铁等。
电解液的选择决定了电化学行为的特性。
例如,电解液中的金属离子浓度、氧化还原电位和酸度等参数会影响电沉积过程的物理化学性质,从而影响沉积物的成分、形貌、结构和性能。
此外,电解液的附加物如表面活性剂、添加剂、缓冲剂等也会对电沉积过程起到一定的影响。
三、金属纳米结构的制备方法金属纳米结构的制备方法主要包括物理法和化学法两种。
金属纳米结构的制备方法可以分为自发成核、生长机制和后处理三个阶段。
自发成核阶段是指在电极表面形成原子尺度的固体核,成为后续沉积的起始点。
生长机制阶段是指沉积物开始形成,并随时间演化成为所有期望的结构,包括表面形貌和化学成分。
后处理阶段是指通过加工和处理等方法进一步改变电极表面形貌和结构。
四、电沉积制备金属纳米结构的研究现状在电沉积技术制备金属纳米结构的研究中,许多科学家已经开发出多种定量实验和模拟方法,可以微观地描述电极表面物理化学变化和沉积物的演化。
其中,应用模型可以预测金属纳米颗粒的性质和结构,包括大小、形状和类型等。
在这方面,模型建立的挑战在于描述电化学行为和相变机制之间的复杂关系。
此外,尚需深入研究电沉积的反应动力学和金属纳米结构的表面组成和形貌对电沉积反应的影响等问题。
电沉积和电泳
电沉积和电泳
电沉积(Electroplating)和电泳(Electrophoresis)是两种与电化学过程相关的技术,它们用于在材料表面或液体中分离、涂覆或分析物质。
以下是它们的简要介绍:
1. 电沉积(Electroplating):
-电沉积是一种将金属沉积到另一金属表面的电化学过程,以改善外观、耐腐蚀性、导电性和其他性能。
-这个过程涉及两个电极:阳极和阴极,它们分别连接到电源,然后浸入电解液中。
-金属离子从阳极释放,然后在阴极上还原并沉积在其表面,形成均匀、致密的金属涂层。
-电沉积常用于制造金属物品,如镀金、镀银、镀镍、镀铬、镀锌等,以改善它们的外观和性能。
2. 电泳(Electrophoresis):
-电泳是一种在电场中移动带电粒子(如蛋白质、DNA片段、RNA等)的技术,通常用于分离、分析和检测生物分子。
-过程涉及将带电粒子在电场中放置在凝胶或液体介质中,然后应用电压,使粒子根据其电荷和大小在电场中移动。
-在凝胶电泳中,质子或蛋白质根据其大小和电荷在凝胶中分离开来,从而实现分析和定量。
-电泳还有各种变体,如聚丙烯酰胺凝胶电泳、琼脂糖凝胶电泳、DNA电泳等,用于不同类型的生物分子分离和分析。
总之,电沉积和电泳是两种不同的电化学过程,分别用于在材料表面涂覆金属或在生物分析中分离带电粒子。
它们在不同应用领域中具有重要作用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
金属电沉积理论一.研究概况在电化学中,金属的电化学沉积学是一种最古老的学科。
在电场的作用下,金属的电沉积发生在电极和电解质溶液的界面上,沉积过程含有相的形成现象。
首先,在金属的电化学沉积实验的研究时间要追溯到19世纪,并且在引进能产生直流电的电源以后,电镀很快成为一种重要的技术。
电镀被用来制造各种不同的装饰性和功能性的产品,尽管在开始的早期,电镀技术的发展和应用建立是在经验的基础上。
金属电沉积的基本原理就是关于成核和结晶生长的问题。
1878年,Gibbs在他的著名的不同体系的相平衡研究中,建立了成核和结晶生长的基本原理和概念。
20世纪初,Volmer、Kossel、Stransko、Kaischew、Becker和Doring用统计学和分子运动模拟改进了基本原理和概念。
按照这些早期的理论,成核步骤不仅要求一个新的三维晶体成核,而且完美单晶表面的层状二维生长。
对于结晶理论的一个重要改进是由Avrrami提出的结晶动力学,他认为在成核和生长过程中有成核中心的重复碰撞和相互交迭。
在1949年,Frank提出在低的过饱和状态下的一个单一晶面成长会呈螺旋状生长。
Cabrera和Frank等考虑到在成长过程中吸附原子的表面表面扩散作用,完善了螺旋成核机理。
20世纪二三十年代,Max、Volmer等人对电化学结晶进行了更为广泛的基础研究。
Erday-gruz和Volmer是第一次认识到过饱和度与过电位,稳态电流密度和由电荷转移引起的电结晶过电位之间的关系。
20世纪三四十年代,Finch和他的同事做了大量的关于多晶电化学沉积的实验,研究了决定结晶趋向与金属薄膜的组织结构的主要因素。
在这一时期,Gorbunova还研究了底层金属与电解质溶液组成对电结晶过程的影响,并发现了由于有有机添加剂的吸附作用可能导致金属晶须的生长。
1945年,Kaischew对电结晶理论做了重大改进。
考虑到单一晶体表面上金属原子的结合和分开的频率,可利用分子运动学模拟电化学结晶过程。
这项工作对电结晶理论的发展有着重大的影响。
20世纪50年代是在电化学结晶理论与实验技术取得重大进步的阶段。
Fincher等人完成在实际的电镀体系中抑制剂对电结晶成核与生长的影响的系统研究,并按照其微观结构和形态对金属电沉积进行了分类。
Piontell等人对基体的取向作用和在金属沉积系统中同向和异向的金属沉积的阴离子的特性进行了进一步的研究。
Kardos、Kaischew等人利用新的实验技术证实Volmer`s 的三维形核的正确性。
Wranglen,Vermilyea等人对结晶树枝状生长进行了深入的研究,提出了新的电化学结晶的理论模型。
20世纪60年代初,Flischman和Thirsh发展了在电结晶状态下多重成核与生长的一般理论,后来Armstrong和Harrason建立和完善了电化学多重成核及多层生长理论。
此后,Bockris、Damjanovic和Despic又研究了表面扩散、增殖和枝状结晶生长等问题。
Epelboin、Froment等研究了基体上成核及生长过程在温度增加、强电解质沉积影响。
在1964年,Budevski和Bostanov在电结晶实验方面取得重大改进,即利用毛细管技术制备很少甚至不含螺旋位错的“近乎完美”的单晶金属表面。
运用这一技术,Bvdevskiv等人定量证实经典的二维成核模型。
20世纪70年代,Lorenz第一次在单一晶体基体上推行UPD实验并由对不同的二维超晶格结构给出了解释。
后来,Yeajer 等人做了大量的金属在各种不同系统UPD热力学和动力学实验,完善了核逐层生长、多核多层生长和等速螺旋生长等理论。
在最近的20年中,材料表面分析方法的进步以及理论化学的发展,金属的电沉积的认识被提到了原子级水平,电结晶理论也在不断的得到完善。
二.经典的电结晶理论电结晶过程可分为两个阶段:第一阶段为离子从电解液中输送到电极表面并放电;第二阶段是原子进入晶格和晶体的生长。
电结晶过程的复杂性既与晶体表面的不均匀性有关,又与形成新相有关。
在形成固相时产生结晶过电位,后者产生的原因时原子进入固体金属晶格的有序结构中的迟缓性,纯粹形式的结晶过电位只有当其它各步骤,即电荷传递,扩散以及在溶液中的化学反应等价电流都非常接近热力学平衡时,才能显现出来。
当电沉积发生在理想的平滑表面时,结晶过电位与形成晶胚有关,金属的晶核由为数不多的配置在同一平面上(二维晶核)的原子或相互重叠的原子(三维晶核)所组成。
有如下关系:晶核的形成几率W与过电位ηk2)W=Bexp(-b/ηk式中B,b为常数。
由上式可知:结晶过电位越高,晶核的形成几率越大,以至晶核形成数目就越多,晶核尺寸随之变小,所得镀层组织结构就越细密。
在近代电结晶理论中,离子放电可在晶面上任何地点发生,先是形成吸附离子(adion),然后在表面扩散,直至生长点后长入晶格。
生长点一般为表面缺陷,如下图所示的坎坷(Kink)或边壁(Ledged),通常为螺旋位错露头。
这一晶体生长模型提出离子放电步骤与新相生成步骤间存在表面扩散步骤。
如果离子放电速度大于表面扩散速度,则将导致吸附原子的表面浓度升高,结果电位负移而产生电结晶极化和电结晶过电位。
三.电结晶的影响因素电结晶过程中,晶核形成与晶体长大是平行进行。
只有晶核形成速度大于晶体长大速度,结晶才有可能细化。
决定晶核形成速度的主要因素是过电位,凡是影响过电位的因素对电结晶质量都有影响。
㈠电解液因素1.金属特性:各种金属自其本身电极还原时具有不同得电化学动力学特征,表现在电极反应速度与交换电流彼此不同。
常见金属按其交换电流得大小可粗略地分为四类,如表一所示。
交换电流越小,电极反应速度越慢,这还原时表现出的电化学极化和过电位越大,具有这种特征的金属从其简单盐溶液中也能沉积出细晶层;反之, 则电化学极化和过电位越小,从其简单盐溶液中只能沉积出粗晶层。
2.离子存在形式与浓度金属离子按其在溶液中的存在形式可分为简单金属离子和金属络离子两类,相应的电解液可分为单盐和络盐两类。
简单金属离子,出交换电流小的体系(如)外,大多因其极化作用小,故从其单盐溶液中往往只能得到结晶较粗的镀层。
当金属离子以络离子存在时,由于络离子在阴极表面还原需要较大的活化能,造成了放电迟缓效应而促使电化学极化和过电位的提高,故从络盐溶液中沉积容易得到结晶细致的镀层。
形成金属络离子通常是靠溶液中添加络合剂,其主要作用是⑴.降低游离金属离子浓度,是平衡电位负移。
电位负移程度与金属络离子稳定性有关, 络离子越稳定, 则平衡电位负移越显著。
金属络离子稳定性由络合物不稳定常数K不表征,当电离平衡为:ML(n-km)=M n++L m-K=[M n+][L m-]/[ML(n-km)]不⑵.提高阴极还原的电化学极化。
金属络离子的界面反应历程,通常是先经过表面转化形成低配位数的表面络合物,如多核络离子或缔合离子,然后放电。
放电前配体的变换和配位数的降低涉及能量变化,导致还原所需活化能的升高,因而表现出比简单金属离子更大的电化学极化。
络合物对电化学极化的贡献取决于配体界面性质和不稳定常数两个因素。
当配体具有对电极过程起阻化作用的性质时,K不越小的配体转化所须的活化能越大,则阴极极化增大效应越显著。
如配体对电极过程起活化作用则很难通过K不来预测阴极极化效果。
络合剂具有选择性。
根据软硬酸碱的原理,形成络合物的稳定性服从“软亲软,硬亲硬”的规律。
金属离子和配体分别当作广义碱时的软硬划分可以软硬势标镀为据。
金属的电子构型对络合物的影响较大。
满d 壳层的d10类金属(如Cd,Sn,Pb,Cu,Zn,Ag等),一般只能形成活性络合物,可选用络合能力很强的络合剂。
d6,d8,d13等类金属(如Fe,Co,Ni,Cr等),与K小的配体移形成惰性络合物而不难以还原析出。
金属离子浓度提高时,界面浓度与交换电流均相应增加,一般会降低电化学极化,故无论在单盐还是络盐溶液中提高金属离子浓度,都具有减小形核率并伴随着镀层粗糙的趋势。
但浓度降低导致浓差极化增强,极限电流也随之下降。
3.游离络合剂游离酸存在于单盐溶液中,并依其含量高低可分为高酸度和低酸度两类镀液。
在高酸度镀液中,游离酸能在一定程度上提高阴极极化,并防止主盐水解或氧化,提高镀液电导率。
但游离酸浓度过高时,主盐溶解度下降,浓差极化趋势增强。
低酸度镀液中,游离酸浓度过低易引起主盐水解或发生沉淀;过高则导致大量析氢,电流效率下降。
游离络合剂具有增大阴极极化,促进结晶细化和保持镀液稳定的作用,并能降低阳极极化使其正常溶解。
但过量的游离络合剂将减低电流效率和许用电流,使沉积速度下降。
4.添加剂有机表面活性剂对电沉积过程的动力学特征有较大影响。
它可以在电极表面产生特性吸附,增大电化学反应阻力,使金属离子的还原反应受到阻滞而增大电化学过电位;或通过它在某些活性较高,生长速度较快的晶面上优先吸附,促使金属吸附原子沿表面作较长距离的扩散,从而增大结晶过电位。
有时有机表面活性剂可在界面与络合物缔合,增大活化能而对电极过程其阻化作用。
这些行为对新晶核的形成是有利的。
此外,有机表面活性剂对镀液的整平性,光亮度,润湿性及镀层的内应力及脆性等都有较大影响。
在单盐镀液中加入一些无机添加剂,其作用一般是增大溶液导电率以改善分散能力,或是其缓冲作用,稳定pH值以避免电极表面碱化而形成氢氧化物或碱性盐析出。
有时无机添加剂是为防止主盐水解,降低内应力或增加光亮度等目的而加入镀液的。
一般无机添加剂对阳极极化的影响不很显著。
㈡工艺因素1.电流密度:电流密度对电结晶质量的影响存在上下限。
在电流密度下限值以下,提高电流密度有利于晶体生长,导致结晶粗化。
在下限值以上,随着电流密度的提高,阴极极化和过电位增大,有利于晶核形成,结晶细化。
但当电流密度达到极限电流D时,出现疏松的海绵状镀层。
k2.温度:镀液升温使放电离子活化,电化学极化降低,粗晶趋势增强。
某些情况下镀液温度升高,稳定性下降,水解或氧化反应容易进行。
但当其他条件有利时,升高镀液温度不仅能提高盐类的溶解度和溶液的导电性,还能增大离子扩散速度,降低浓差极化,从而提高许用电流与阴极电流效率。
此外,温度升高对减少镀层含氢量和降低脆性也有利。
3.搅拌:搅拌促使溶液对流,减薄界面扩散层厚度而使传质步骤得到加快,对降低浓差极化和提高极限电流有显著效果。
4.电流波形:⑴.换向电流换向电流通过直流电流周期性换向,使镀件处于阴极与阳极的交替状态而呈间歇沉积,电流正反向时间比为重要可控参数。
当镀件由阴极转变为阳极时,界面上已被消耗的金属离子得到适当的补充,浓差极化得到抑制,有利于极限电流的提高。
另一方面,原先沉积上的劣质镀层与异常长大的晶粒受到阳极的刻蚀作用而去处,不仅有利于镀层的平整细化,而且去除物溶解在界面上,一定程度上提高了表面有效浓度,对提高电化学极化有利。
