配位聚合反应的特征
高分子化学 第6章 配位聚合
(4)配位聚合引发剂与单体
①引发剂和单体类型
Ziegler-Natta引发剂
-烯烃 有规立构聚合
二烯烃 有规立构聚合
环烯烃 -烯丙基镍型引发剂:专供丁二烯的顺、反1,4聚合 极性单体 烷基锂引发剂(均相) 有规立构聚合 二烯烃 茂金属引发剂(所有乙烯基单体)
②引发剂的相态和单体的极性
非均相引发剂,立构规整化能力强
δ +CH
Mt CH2 δ -
R
过渡金属阳离 子Mt +对烯烃 双键 碳原子的 亲电进攻
插入反应包括两个同时进行的化学过程。
单体的插入反应有两种可能的途径:
一级插入
δδ+
CH CH2 R
Mt
+
CH CH2 R
δδ+
CH CH2 CH CH2 R R
Mt
不带取代基的一端带负电荷,与过渡金属相连 接,称为一级插入。
全同1,2 、间同1,2、顺式1,4-聚丁二烯和反式 1,4-聚丁二烯。
n CH CH CH 2 CH 2 4 3 2 1
1,2加成 3,4加成
[ CH2 CH ]n CH CH2 (R)
丁二烯的1,2或3,4加成有全同和间同二种立构规整聚合物。
[ CH2 CH2 ]n C C H H
顺式1,4-聚丁二烯-1,3
最初的Ziegler-Natta引发剂由两组分构成。 主引发剂 是周期表中Ⅳ~Ⅷ过渡金属化合物。
1955年意大利的Natta改进了Ziegler引发剂。用TiCl3和烷 基金属化合物组成的配位引发剂使丙烯聚合,结果得到高相 对分子质量、高结晶度、耐热150℃的聚丙烯,并于1957年 实现了工业化。 Natta还用这些引发剂使乙烯聚合,所得到的PE无支链、 结晶度也很高, 这种PE、PP具有高的立构规整度。 Ziegler-Natta引发剂的出现使高分子科学和高分子工 业的发展有了重大突破,从而在高分子科学中开创了一 个新的研究领域----配位聚合。 Ziegler和Natta两位学者也于1963年同时获得诺贝尔 化学奖。
配位聚合

7.6 茂金属引发剂
高活性:几乎 100%金属原子可形成活性中心,而Z-N 引发剂只有1~3%形成活性中心。 单一活性中心:茂金属催化剂具有明确的分子结构, 聚合反应在该分子上的一个位臵 ——过渡金属原子发 生,有时称为单活性位臵催化剂。产物的分子量分布 很窄,1.05~1.8。共聚物组成均一。
TiCl4-AlR3或TiCl4-AlR2Cl
在-78oC反应可形成溶于 烃类溶剂的均相引发剂 温度升高,发生不可逆变 化,转化为非均相 TiCl3-AlR3或VCl3-AlR2Cl 反应后仍为非均相, -烯烃的高活性定向引发剂。 低温下只能引发乙 烯聚合 活性提高,可引发 丙烯聚合
7.3 Ziegler-Natta 引发剂
配位聚合
7.1 引言
1938 年,英国 ICI 公司在高温( 180~200 oC )、高压
(150~300 MPa)条件下,以氧为引发剂,合成出了
低密度聚乙烯(LDPE) 1953年,德国化学家 Ziegler发现了乙烯低压(0.2~1.5
MPa)聚合的引发剂,合成出了支链少、密度大、结
根据聚合物的物 理性质进行测定
A975 全同螺旋链段特征吸收,峰面积 聚丙烯全同指数 K A1460 甲基的特征吸收,峰面积
7.3 Ziegler-Natta 引发剂
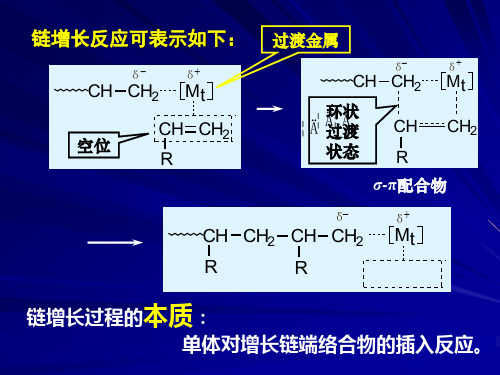
链增长反应 链增长过程的本质是 (以TiCl3-AlR3引发丙烯聚合为例): 单体对增长链端络合 物的插入反应 过渡金属
δδ+
δδ+
-烯烃聚合物的Tm大致随取代基增大而升高
HDPE
Tm (oC) 120
全同PP
175
聚3-甲基-1-丁烯
300
聚4-甲基-1-戊烯
第六章配位聚合

第六章 配位聚合6.1引言乙烯 丙烯和其他a-烯烃为石油裂解懂得主要产物30年代 仅作为燃料后 引发剂高温高压 PE (高压) 1953 Zieglev (德) 70~5034常压、AlEt Ti -θ HDPE 1954 Natta (意) Ti 3θ35)(GH Al - PP接着 Goodrich-Fire 公司 Ti 3524)(H C Al -θ 高顺式1、4-聚异戊二烯(天然橡胶) 同时 Fire-stene 轮胎和橡胶公司 锂或烷基锂(Z-N 引发剂)以后 以金属有机化合物-过渡金属化合物的洛合体系作引发剂单体配位而后聚合,聚合产物呈定向聚合—洛合聚合,配位聚合,定向聚合 (区别)常用术语的区别① 配位聚合和洛合为同义词—采用具有配位(或洛合)能力的引发剂,链增长(有时包括引发)都是单体先在活性种的空位上配位(洛合)并活化,然后插入烷基—金属键(R —M )中。
(配位比洛合表达的意义更明确)② 定向聚合和有规立构聚合是词义词—按IUPAC 规定,均指以形成有规立构聚合物为主的聚合过程。
③ Ziegler —Natto 聚合—指采用Ziegler —Natto 引发剂的任何单体的聚合或共聚合。
所得聚合物可以是立构规整的,也可以是无规聚合物。
6.2 结合物的立构规整性配位聚合,除R P 、n X 外,首先要考虑立构规整性问题。
异构现象—在有机化学中将分子式相同而结构不同因而性质不同的化合物叫异构体,这种现象称~分两类① 结构异构—由于分子中原子或基团相互连接次序不同引起的:如:头—尾和头—头或尾—尾相连的聚合物结构异构体② 立体异构 —由于分子中原子或基团相互连接次序不同引起的,称构型聚合物中同样存在复杂的立体异构现象⎭⎬⎫⎩⎨⎧几何异构光学异构 即:聚合物分子组成和结构相同,只是构型不同。
一、 立体异构⒈光学异构。
(存在手性中心)⎩⎨⎧*(左)右S R C )( —取代基(原子)在手性中心的排布顺序不而产生的立体异构α—烯烃聚合 NCH 2 =CH-R → —CH 2-CH-CH 2-CH-全同立构(等规)各个手性中心*C 构型相同,如~RRRR ~或~SSSS ~(St-pp)无规(at-pp ):手性中心的构型呈无规排列。
配位聚合反应的特征

配位聚合反应的特征1. 引言配位聚合反应是一种重要的有机反应,常用于合成可通过配位聚合反应形成的高分子材料。
这种反应具有许多独特的特征,包括反应机理、催化剂、配体选择和反应条件等方面。
本文将对配位聚合反应的特征进行全面详细、完整且深入的介绍。
2. 反应机理配位聚合反应的反应机理主要涉及金属离子催化剂和配体的配位结合。
一般来说,金属离子作为催化剂参与反应,配体与金属离子形成配位键,并进一步聚合生成高聚物。
配位聚合反应的反应机理可以分为两类:链增长机理和机械增长机理。
链增长机理中,聚合物的长度逐渐增长,每一步都通过与催化剂反应引发。
机械增长机制中,催化剂和配体作用于预聚体和单体,通过金属离子催化发生配位反应,进而引发新的单体参与反应,形成高聚物。
3. 催化剂在配位聚合反应中,选择合适的催化剂对反应的效果至关重要。
常见的催化剂包括过渡金属离子、有机金属化合物和有机催化剂等。
这些催化剂能够提供活性位点,促进配位聚合反应的进行。
过渡金属离子是配位聚合反应中最常用的催化剂之一。
它们具有良好的催化活性和选择性,能够与配体通过配位键结合,并参与反应中间体的生成。
常见的过渡金属离子催化剂包括铜离子、铝离子和镍离子等。
有机金属化合物也是常见的催化剂之一,它们由有机分子与过渡金属离子形成的配合物组成。
这些配合物具有较高的催化活性,能够催化配位聚合反应的进行。
常见的有机金属化合物催化剂包括钯催化剂、铁催化剂和铬催化剂等。
有机催化剂是一种不含金属离子的催化剂,它能够与配位基团发生相互作用,并催化配位聚合反应。
常见的有机催化剂包括蒯欧催化剂、茚咯催化剂和吲哚催化剂等。
4. 配体选择在配位聚合反应中,选择合适的配体对反应的效果同样至关重要。
配体可以调节催化剂的活性和选择性,影响反应的进行。
常见的配体包括有机配体、配位聚合物和有机聚合物等。
有机配体是一种常见的配体类型,它与金属离子形成配位键,并催化配位聚合反应。
常见的有机配体包括二脉冠醚、亚胺和卡宾等。
高分子化学(第五版)第7章

2)丙烯的配位聚合动力学 对于均相催化剂体系,可参照阴离子聚合增长速率
方程: Rp= kp[C*][M] α-TiCl3-AlEt3是微非均相体系,其聚合速率~时间(
Rp~t)曲线有2种类型:
A-衰减型 B-加速型
-TiCl3-AlEt3引发的丙烯
聚合动力学曲线
28
曲线A由研磨或活化后引发 体系产生:第Ⅰ段增长期,在 短时间内速率增至最大;第II 段衰减期;第III段稳定期,速 率几乎不变。
CH CH2
空位
R
环状过渡态
CH CH2 R
TiCl3和AlR3络合物在Ti上形成活性 点(或空位),丙烯在空位上配 位,形成σ-π络合物,配位活化后 的单体在金属-烷基链中插入增长。
配位和增长反复进行,形成大分子。
δ-
δ+
CH CH2 CH CH2 Mt
R
R
5
配位聚合的特点:
单体首先在过渡金属上配位形成σ-络合物;
Cl
Ⅳ B族过渡金属,如锆(Zr)、钛(Ti)、铪(Hf) +
茂型配体:至少一个环戊二烯基(Cp)、茚基(Ind)、芴基 (Flu)或它们的衍生物 +
非茂配体,如氯、甲基、苯基等。
18
空间几何构型
Ti
Cl
Cl
Cl
非桥链型 普通结构
X
R'
M
X
桥链型
R
R
R
R2
R
L
MCl2 2
R3
限定几何构型
19
茂金属引发剂的特点: 高活性,几乎100%金属原子都形成活性中心; 单一活性中心,可获得分子量分布很窄、共聚物组成
R代表速率,t为时间,下标0为起始最大值, 为后 期稳定值,k为常数,与丙烯压力有关,与三乙基铝浓度 无关。
第五章配位聚合解析

第五章 配位聚合 习题参考答案1.举例说明聚合物的异构现象,如何评价聚合物的立构规整性?解答:(1)聚合物的异构现象:① 结构异构聚合物,如聚甲基丙烯酸甲酯与聚丙烯酸乙酯:CH 3|-[-CH 2-C-]n - -[-CH 2-CH-]n -| |CO 2CH 3 CO 2C 2H 5聚甲基丙烯酸甲酯 聚丙烯酸乙酯② 几何异构聚合物,汉分子链中由于双键或环形结构上取代基在空间排列方式不同造成的立体异构称为几何异构,也称顺-反异构。
如丁二烯聚合所形成的1,4-聚丁二烯,其结构单元有顺式结构和反式结构两种:~~~CH 2 CH 2~~~ ~~~CH 2 HC = C C = CH H H CH 2~~~ 顺式结构(顺-1,4聚丁二烯) 反式结构(反-1,4聚丁二烯)③ 光学异构聚合物,如聚环氧丙烷有一个真正的手性碳原子:H|~~~O-C *-CH 2~~~|CH 3④ 构象异构聚合物,当大分子链中原子或原子团绕单键自由旋转所占据的特殊空间位置或单键连接的分子链单元的相对位置的改变称构象异构。
构象异构可以通过单键的旋转而互相转换。
(2)当大分子链上大部分结构单元(大于75%)是同一种立体构型时,称该大分子为有规立构聚合物,或立构规整聚合物、定向聚合物。
反之,称为无规立构聚合物。
2.写出下列单体聚合后可能出现的立构规整聚合物的结构式及名称:(1)CH 2=CH-CH 3(2)CH 2-CH-CH 3O(3)CH 2=CH-CH=CH 2CH 3|(4)CH 2 =C-CH=CH 2 解答:(1) 聚丙烯全同聚丙烯(R 为甲基) 间同聚丙烯(R 为甲基)全规聚环氧丙烷 间规聚环氧丙烷 (3) 丁二烯~~~CH 2CH 2~~~ ~~~CH 2 HC = C C = CHH 2~~~ 顺式结构(顺-1,4聚丁二烯)反式结构(反-1,4聚丁二烯)R 为乙烯基)间同1,2-聚丁二烯(R 为乙烯基)(4) 异戊二烯~~~CH 2 CH 2~~~~~~CH 2 H C = CC = C CH 3CH 3 2~~~ 顺式结构(顺-1,4聚异戊二烯)反式结构(反-1,4聚异戊二烯) 全同3,4-聚异戊二烯(R 为-C(CH 3)=CH 2)间同3,4-32)全同1,2-聚异戊二烯(R 乙烯基)间同3,4-聚异戊二烯(R 为乙烯基)3.什么是配位聚合?主要有几类催化剂(或引发剂),各有什么特点?解答:(1)配位聚合:是指单体分子的碳-碳双键先在显正电性的低价态过渡金属的空位上配位,形成某种形式的络合物(常称σ-π络合物),经过四元环过渡态,随后单体分子插入过渡金属-碳键中进行增长的聚合过程。
配位聚合
3、立构规整性(重要概念) 立构规整聚合物:是指那些由一种或两种构 型的结构单元(即手性中心)以单一顺序重 复排列的聚合物。 立构规整度:又称为定向度或定向指数,指 立构规整性聚合物在整个聚合物中所占的重 量百分含量。
问题:在合成过程中,如何控制 聚合物的立构规整性?
配位聚合及其引发剂体系等
7.2 配位聚合和定向聚合
7.1 聚合物的立体异构
结构异构:元 素组成相同而 原子或基团键 接位置不同。
配位聚合所涉及的异构现象
1、几何异构(顺反异构)
(1)形成:取代基在双键或环形结构平面 两侧的空间排列方式不同而造成的。 (2)结构特点:主链上有“=”或“环” 顺式
CH CH2 CH CH2 CH2 CH CH CH2
不足 只解释了引发和增长,没有解释立 构的形成原因
(2)单金属机理 Ti上引发,Ti上增长
特点 解释了立体构型的形成原因 对共引发剂的考虑少 不足
单体在Ti-C键间插入与空位回跳交 替进行的可能性
乙丙橡胶的介绍
因为大量甲基的存在破坏了聚乙烯的高度结构对称性,
不结晶而成为橡胶。 分子链上不含双键,所以耐臭氧、耐化学品、耐老化、 耐候性最佳。 密度小,有优异的电性能和耐油性,广泛用于电线电 缆、汽车部件、耐热密封件、传送带和日用生活品。 也因为分子链上不含双键,所以只能采用过氧化物进 行自由基型链转移硫化,硫化速度慢,粘接性能差。 采用加入少量共轭双烯作为第三单体进行三元共聚来
碳-碳双键过渡金属引 自由基聚合、离子聚 发剂的活性中心的空位 合、配位聚合 上配位 有规或无规 络合聚合、插入聚合 有规 有规立构聚合
产物 别称 举例
Ziegler-Natta引发剂引 BuLi引发丁二烯聚合 发苯乙烯聚合
乙烯配位聚合课件
配位聚合的特点
可控制分子量、窄分子量 分布、易调变性等。
配位聚合的应用
制备高性能合成纤维、工 程塑料、功能性高分子材 料等。
02 乙烯配位聚合原理
乙烯的特性
01
乙烯是一种不饱和烃,具有较高 的反应活性,容易发生加成、聚 合等反应。
02
乙烯分子结构中存在π键,容易与 金属原子形成配位键,是配位聚 合的理想单体。
橡胶制品生产
乙烯配位聚合生产的橡胶具有良好的 加工性能,可以在轮胎、胶管、胶带 等橡胶制品的生产中广泛应用。
05 乙烯配位聚合的未来发展
新催化剂的研发
总结词
新催化剂的研发是乙烯配位聚合未来发展的关键之一,旨在提高聚合效率和产物性能。
详细描述
随着科学技术的不断进步,研究者们正在不断探索和开发新的催化剂体系,以提高乙烯 配位聚合的反应活性和选择性。这些新催化剂可能包括金属催化剂、非金属催化剂以及
乙烯配位聚合课件
contents
目录
• 引言 • 乙烯配位聚合原理 • 乙烯配位聚合的影响因素 • 乙烯配位聚合的应用 • 乙烯配位聚合的未来发展 • 结论
01 引言
聚合反应简介
01
02
03
聚合反应
由单体结合成大分子,释 放出小分子(如水、氯化 氢等)的过程。
聚合反应的分类
根据聚合机理,聚合反应 可分为连锁聚合和逐步聚 合。
催化剂的活性中心可以与乙烯分子形成稳定的配位键,从而 控制聚合反应的速率、聚合物链的分子量、分子量分布等参 数。
聚合过程中的能量变化
聚合过程中能量的变化主要表现在自由能的变化上。随着 聚合物链的增长,体系的自由能逐渐降低,因为聚合物链 中的π键相互作用能抵消部分金属与乙烯之间的相互作用 能。
配位聚合
19
7.2 聚合物的立构规整性
立构规整性与性能的关系
有规立构与非立构规整性聚合物间的性质差别很大。 性能的差异主要起源于分子链的立构规整性对聚合物结晶 的影响。 有规聚合物的有序链结构容易结晶,无规聚合物的无 序链结构则不易形成结晶,而结晶导致聚合物具有高的物 理强度和良好的耐热性和抗溶剂性,因此有规立构聚合物 更具有实际应用意义。
高 分 子 化 学
23
7.3 引发剂
Zieglar-Natta引发剂
广义 Ziegler-Natta 引发剂指的是由 IV~VIII 族过渡金 属化合物与I~III族金属元素的金属烷基化合物所组成的一 类引发剂。其通式可写为:
MtIV-VIIIX + MtI-IIIR 主引发剂 助引发剂 常用过渡金属化合物 :Ti、V、Cr、Co、Ni 的卤化 物(MtXn),氧卤化合物(MtOXn),乙酰丙酮基化合 物[Mt(acac)n],环戊二烯基卤化物(Cp2MtX2)。
高 分 子 化 学
22
7.3 引发剂
引发剂的类型和作用
类型: Zieglar-Natta 型。用于α-烯烃、二烯烃、环烯 烃的定向聚合; 烷基锂。在均相溶液体系中引发二烯烃和极性 单体,形成立构规整聚合物 π-烯丙基镍(π-C3H5NiX)。专供引发丁二烯的 顺式-1,4和反式-1,4聚合 茂金属引发剂。 作用: 提供活性中心; 引发剂残余部分(金属反离子)紧邻引发剂中 心,使单体分子按照一定的构型进入增长链, 使单体定位,起连续定向的模板作用。
目前,聚乙烯和聚丙烯已经成为生产量最大、用途最广 的合成材料。
高 分 子 化 学
3
7.1 配位聚合概述
配位聚合:烯类单体的碳-碳双键首先在过渡金属
31讲 第5章5 配位聚合
表5-16
聚合反应类型和聚乙烯的主要物性 自由基型 氧气 180 ~ 200 180 ~ 200 0.91 ~ 0.93 50 ~ 70 105 ~110 1938年 低 密 度 聚 乙 烯 LDPE高压聚乙烯 0.94 ~ 0.96 80 ~ 90 125 ~ 135 1953年 高密度聚乙烯HDPE 低压聚乙烯 配位型 TiCl4-AlEt3 50 ~ 70
如果两种构型的手性碳原子无规排列,即由两种构型 结构单元组成的链节以无规的顺序重复排列,这种聚合物 称为“无规立构聚合物”。 全同立构聚合物和间同立构聚合物都称有规立构聚合 物。 5)立构规整度及其测定方法: 立构规整度又称为定向度或定向指数,乃立构规整性聚合 物在整个聚合物中所占的重量百分含量。 立构规整度的测定方法最早采用溶剂溶解法,如用沸腾 的正庚烷萃取聚丙烯样品。目前多采用红外、核磁等方法。
条件和性质 引发剂 温度(℃) 压力(Mpa) 密度(g/cm3) 结晶度(%) 熔点(℃) 问世时间 俗 称
5.5.2 聚合物的立体规整性 1)结构异构:
_ _ _ ~ CH2 _ CH ~ ; ~ CH O ~ ; ~ CH2 CH2 O ~ OH CH3
聚乙烯醇; 聚乙醛; 聚氧化乙烯(聚环氧乙烷)
表5-17 不同立构异构体聚α烯烃和共轭二烯烃的物理性质 聚 烯 烃 高密度聚乙烯 无规聚丙烯 全同聚丙烯 全同聚1-丁烯 全同聚3-甲基-1-丁烯 全同聚4-甲基-1-戊烯 顺式1,4-聚丁二烯 反式1,4-聚丁二烯 全同1,2-聚丁二烯 间同1,2-聚丁二烯 1.01 0.97 0.96 0.96 146 126 156 相对密度 0.95 ~ 0.96 0.85 0.92 0.91 熔点(℃) 120 ~ 130 75 175 136 304 250
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
配位聚合反应的特征
配位聚合反应是一种重要的有机合成反应,它是通过配位键的形成和断裂来实现分子间的聚合。
这种反应具有许多独特的特征,包括选择性高、反应条件温和、反应产物易于纯化等。
本文将从这些特征入手,详细介绍配位聚合反应的机理、应用和发展前景。
一、反应机理
配位聚合反应的反应机理可以分为两个步骤:配位键的形成和断裂。
在第一步中,两个或多个分子通过配位键的形成结合在一起,形成一个配位化合物。
在第二步中,配位键断裂,产生新的化学键,从而形成聚合产物。
配位聚合反应的反应机理与传统的聚合反应有所不同。
传统的聚合反应是通过共价键的形成来实现分子间的聚合,而配位聚合反应则是通过配位键的形成和断裂来实现分子间的聚合。
这种反应机理使得配位聚合反应具有许多独特的特征,如选择性高、反应条件温和、反应产物易于纯化等。
二、应用
配位聚合反应在有机合成中有着广泛的应用。
它可以用于合成各种有机分子,如聚合物、配合物、天然产物等。
下面将分别介绍这些应用。
1. 合成聚合物
配位聚合反应可以用于合成各种聚合物,如聚酰胺、聚酯、聚醚等。
这些聚合物具有许多优良的性质,如高强度、高韧性、高耐热性等。
它们广泛应用于各个领域,如材料科学、医学、电子工程等。
2. 合成配合物
配位聚合反应可以用于合成各种配合物,如金属配合物、有机配合物等。
这些配合物具有许多独特的性质,如催化性、光学性、磁性等。
它们广泛应用于各个领域,如催化剂、光电材料、磁性材料等。
3. 合成天然产物
配位聚合反应可以用于合成各种天然产物,如生物碱、植物素等。
这些天然产物具有许多独特的生物活性,如抗癌、抗病毒、抗菌等。
它们广泛应用于医学、农业等领域。
三、发展前景
配位聚合反应是一种重要的有机合成反应,它具有许多独特的特征和广泛的应用。
随着有机合成技术的不断发展,配位聚合反应也在不断发展。
下面将从两个方面介绍配位聚合反应的发展前景。
1. 反应机理的研究
配位聚合反应的反应机理是目前研究的热点之一。
通过对反应机理的深入研究,可以更好地理解反应过程,从而设计出更加高效、选择性更好的反应体系。
同时,反应机理的研究也可以为新型反应的发展提供理论基础。
2. 新型反应的开发
配位聚合反应的发展还需要不断地开发新型反应。
通过开发新型反应,可以实现更加高效、选择性更好的反应体系,从而满足不同领域的需求。
同时,新型反应的开发也可以为有机合成技术的发展提供新的思路和方法。
配位聚合反应是一种重要的有机合成反应,它具有许多独特的特征和广泛的应用。
随着有机合成技术的不断发展,配位聚合反应也在不断发展。
通过对反应机理的深入研究和新型反应的开发,配位聚合反应将会在各个领域发挥更加重要的作用。
