(完整word)高中化学十字交叉法运用

??
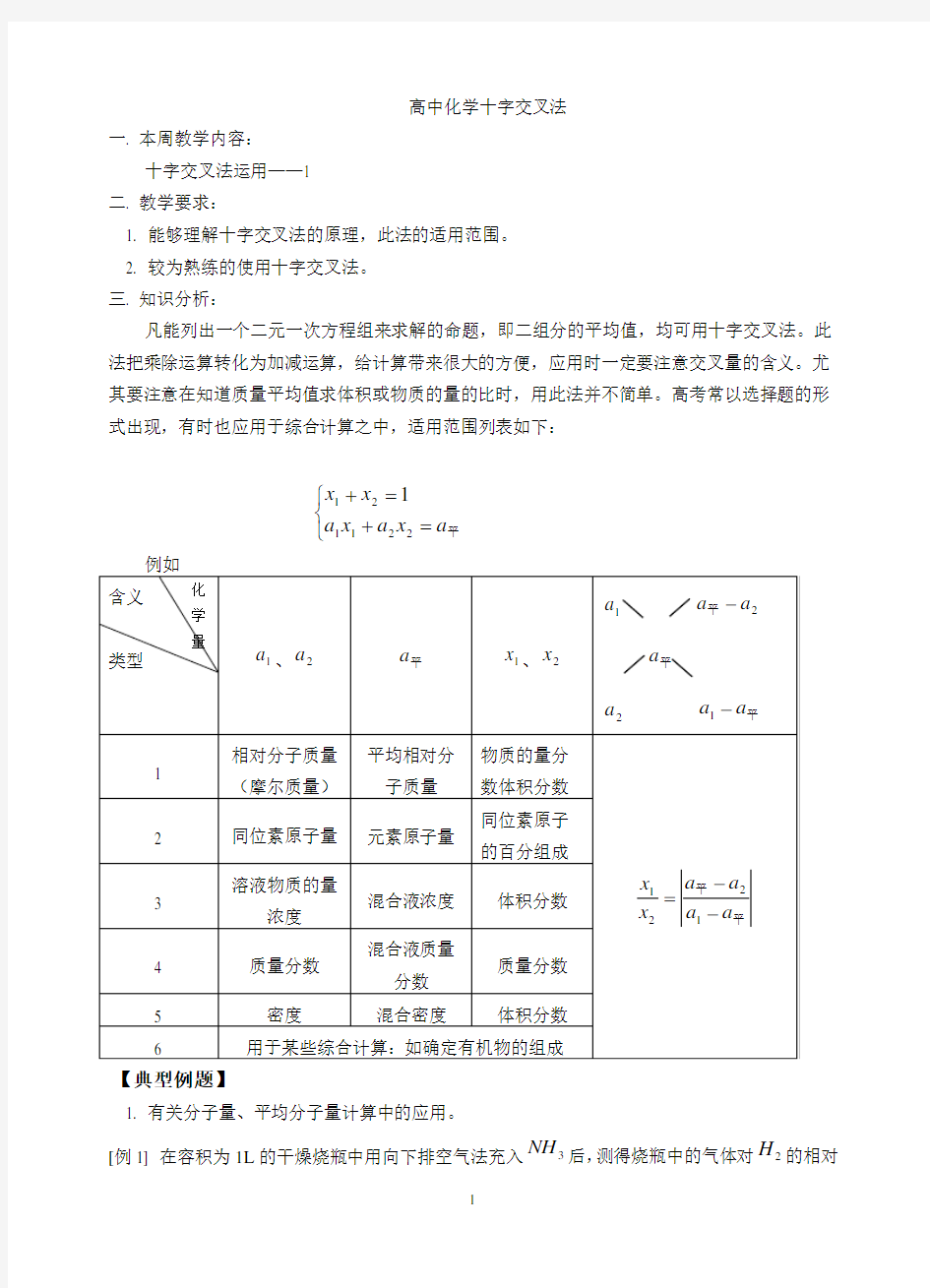
?=+=+平
a x a x a x x 2211211高中化学十字交叉法
一. 本周教学内容:
十字交叉法运用——1 二. 教学要求:
1. 能够理解十字交叉法的原理,此法的适用范围。
2. 较为熟练的使用十字交叉法。 三. 知识分析:
凡能列出一个二元一次方程组来求解的命题,即二组分的平均值,均可用十字交叉法。此法把乘除运算转化为加减运算,给计算带来很大的方便,应用时一定要注意交叉量的含义。尤其要注意在知道质量平均值求体积或物质的量的比时,用此法并不简单。高考常以选择题的形式出现,有时也应用于综合计算之中,适用范围列表如下:
【典型例题】
1. 有关分子量、平均分子量计算中的应用。 [例1] 在容积为1L 的干燥烧瓶中用向下排空气法充入
3NH 后,
测得烧瓶中的气体对2H 的相对
密度为7.9,若将此气体进行喷泉实验,当喷泉停止后进入烧瓶中溶液的体积为L
54,溶质的
物质的量浓度为 。
解析:4.197.92=?=M 17 6.9 4.19 14?
29 4.2 故烧瓶为含3NH 为:
L L 544141=+?
氢气不溶于水,当喷泉停止后,烧瓶内溶液应为L 54
L
mol L mol L L C /045.0544.22/54
1
=?=-
2. 有关同位素原子量及平均原子量的应用。 [例2]
晶体硼由B 10
5
和B 115两种同位素构成,已知g 4.5晶体硼与2H 反应全部转化为硼烷
)(42H B 气体,可得标况下426.5H B L ,则晶体硼中B 10
5和B 11
5两种同位素原子个数比为( )
A. 1:1
B. 3:1
C. 4:1
D. 2:1
解析:
mol
mol L L
H B n 25.04.226.5)(142=?=
-
由42222H B H B =+知: mol H B n B n 5.0)(2)(42==
B 的摩尔质量
mol
g mol g
/8.105.04.5==
即硼的相对原子质量为8.10
B 11
5
11 8.0
8.10 14?
B 105
10 2.0
故选C
3. 有关溶液的稀释,加浓及浓度计算的应用。
[例3] 某温度下,22%的3NaNO 溶液mL 150,加g 100水稀释后,其浓度变为14%,求原溶液的物质的量浓度?
解析:设原溶液的质量为x 22 14
14 100814x =
g x 175= 0 8
mol g NaNO M /85)(3=
L
mol L mol g g C /0.315.08517522.01
=??
=
-
4. 有关消耗量、差量计算。
[例4] 把NaCl 和NaBr 的混合物g 5.0溶于水后加入足量的3AgNO 溶液,把所得沉淀过滤、洗涤、干燥,最后得到卤化银g 10.1,求原混合物中NaCl 的质量分数是多少? 解析:NaCl —AgCl NaBr —AgBr 5.58 5.143 103 188 g AgX 10.1=
(1)若皆为NaCl ,可得沉淀
g g 227.15.585
.1435.0=?
NaCl 227.1 187.0 10.1 NaBr 913.0 127.0
∴
%
60%100127.0187.0187
.0%=?+=
NaCl
(2)若皆为NaBr ,可得沉淀
g g 913.0103188
5.0=?
【模拟试题】
一. 选择题:
1. 将金属钠在空气中燃烧,生成O Na 2和22O Na 的混合物,取该燃烧产物g 48.7溶于水制成mL 1000溶液,取出mL 10用L mol /1.0的盐酸中和,用去mL 20,由此可知该产物中O Na 2的物质的量分数为( )
A. %6.16
B. %20
C. %80
D. %4.78 2.
硅元素有
Si 2814、Si 2914、Si 3014三种同位素,硅的近似相对原子质量为81.2,自然界中Si 2814的
原子百分含量为%92,则Si 29
14和Si 30
14的原子个数比为( ) A. 5:3 B. 1:3 C. 3:2 D. 2:3
3. 今有34NO NH 和22)(NH CO 混合化肥,经设定含氮40%,则混合物中34NO NH 和
22)(NH CO 物质的量之比为( )
A. 3:4
B. 1:1
C. 4:3
D. 3:2 4. 已知下列两个热化学方程式
kJ l O H g O g H 6.571)(2)()(2222+=+
kJ l O H g CO g O g H C 0.2220)(3)(3)(5)(22283++=+
实验测得25H mol 和83H C 混合气体完全燃烧时放热kJ 3847,则混合气体中2H 与8
3H C 的体积比是( )
A. 3:1
B. 1:3
C. 4:1
D. 1:1
5. 在标准状况下,气体A 的密度为L g /25.1,气体B 的密度为L g /875.1,A 和B 的混
合气体在相同状况下对氢气的相对密度为8.16,则混合气体中A 与B 的体积比为( ) A. 2:1 B. 1:2 C. 3:2 D. 2:3
6. 3KHCO 与3CaCO 的混合物同与之等质量的3NaHCO 分别与酸完全反应时所消耗酸量相等。则3KHCO 和3CaCO 的质量比为( )
A. 4:17
B. 8:17
C. 1:1
D. 任意比 二. 填空题:
7. 把含431PO H mol 的溶液与含2)(25.1OH molCa 的石灰水混合,充分反应后,蒸干水得一固体,其组成为 (写成分的分子式及物质的量)。
三. 计算题:
8. %550g 的4CuSO 溶液配成%10的溶液,需%5.12的硫酸铜溶液多少克?
9. 32SO Na 部分氧化成42SO Na 后,S 元素占混合物%25,求32SO Na 和42SO Na 的物质的量之比。
10. 向体积为1L 的干燥容器里充入氯化氢气体,测出容器里的气体对氧气的相对密度为
082.1,若用此气体进行喷泉实验,当喷泉实验停止后,吸进容器里的液体的体积是多少?
11. 把%10100g KCl 溶液浓度变为%20,需加入多少克KCl ?或蒸发多少克水?或与多少克%25的KCl 溶液混合?
12. 已知Cl 的平均相对原子质量为5
.35,求Na 23
11
和Cl 357、Cl 37
17微粒组成的NaCl 晶体
g 25.29中含Cl 37
17的质量是多少?
13. 一定量的NO 和一定量的2O 混合,反应完全后,其气体密度是相同状况下氖气的两倍,求混合前NO 和2O 的物质的量之比为多少?
14. 32CO Li 和3BaCO 的混合物与盐酸反应所消耗盐酸的量同等质量的3CaCO 和同浓度盐酸反应所消耗的量相等,则混合物中32CO Li 和3BaCO 的质量比是多少?
【试题答案】
一. 选择题:
1. B
2. B
3. B
4. B
5. D
6. A
二. 填空题:
7. 243)(PO Ca mol 25.0 42HPO Ca mol 5.0
三. 计算题: 8. g 100 9. 1:7 10. L 75.0
11.
解:纯溶质的含量为100%,水的溶质含量为0 设需纯KCl xg ,蒸馏yg O H 2,需25%zg KCl 10 80 20 18?
x 100
18=
g x 5.12=
100 10 10 5 20 21?
z 100
21=
g z 200=
25 10 10 20
20
12?
y 10012= g y 50= 0 10 需加纯KCl g 5.12 或蒸发O H 2 g 50
或与质量为g 200%25的KCl 溶液混合 12.
解:mol
mol g g
NaCl n 5.05.5825.29)(1
=?=
-
Cl 3717
37 5.0
5.35 31?
Cl 3517
35 5.1
∵ NaCl mol 5.0中含-
Cl 为mol 5.0,则其中Cl 37
17的物质的量为:
mol mol 125.0311
5.0=+?
质量为g mol g mol 625.4/37125.0=? 13.
解:反应后混合气体的40220=?=M ∴ 混合气体可能是2NO 和NO 或2NO 与2O (1)若是2NO 与NO
2NO 46 40 35
?
NO 30 6 2222NO O NO =+ 2 1 2 转 5 5.2 5 余 3
5:165.2:8)(:)(2==NO n NO n
(2)若是2NO 与2O
2NO 46 8 40 43?
2O 32 6 2222NO O NO =+ 2 1 2 转 4 2 4 余 3 5:4)(:)(22=O n NO n
答:当NO 过量时:5:16)(:)(2=O n NO n
当2O 过量时:5:4)(:)(2=O n NO n 14.
解:可先求出混合物中32CO Li 和3BaCO 的物质的量之比 32CO Li 74 97 100 3BaCO 197 26
即
2697
)()(332=
BaCO n CO Li n ∴ 57
197
267497)()(332=
??=BaCO m CO Li m
