电化学基础ppt10(26份打包) 人教课标版1
合集下载
化学课件《电化学基础》优秀ppt9 人教课标版

――[阿萨·赫尔帕斯爵士] 115.旅行的精神在于其自由,完全能够随心所欲地去思考.去感觉.去行动的自由。――[威廉·海兹利特]
116.昨天是张退票的支票,明天是张信用卡,只有今天才是现金;要善加利用。――[凯·里昂] 117.所有的财富都是建立在健康之上。浪费金钱是愚蠢的事,浪费健康则是二级的谋杀罪。――[B·C·福比斯] 118.明知不可而为之的干劲可能会加速走向油尽灯枯的境地,努力挑战自己的极限固然是令人激奋的经验,但适度的休息绝不可少,否则迟早会崩溃。――[迈可·汉默] 119.进步不是一条笔直的过程,而是螺旋形的路径,时而前进,时而折回,停滞后又前进,有失有得,有付出也有收获。――[奥古斯汀] 120.无论那个时代,能量之所以能够带来奇迹,主要源于一股活力,而活力的核心元素乃是意志。无论何处,活力皆是所谓“人格力量”的原动力,也是让一切伟大行动得以持续的力量。――[史迈尔斯] 121.有两种人是没有什么价值可言的:一种人无法做被吩咐去做的事,另一种人只能做被吩咐去做的事。――[C·H·K·寇蒂斯] 122.对于不会利用机会的人而言,机会就像波浪般奔向茫茫的大海,或是成为不会孵化的蛋。――[乔治桑] 123.未来不是固定在那里等你趋近的,而是要靠你创造。未来的路不会静待被发现,而是需要开拓,开路的过程,便同时改变了你和未来。――[约翰·夏尔] 124.一个人的年纪就像他的鞋子的大小那样不重要。如果他对生活的兴趣不受到伤害,如果他很慈悲,如果时间使他成熟而没有了偏见。――[道格拉斯·米尔多] 125.大凡宇宙万物,都存在着正、反两面,所以要养成由后面.里面,甚至是由相反的一面,来观看事物的态度――。[老子]
87.当一切毫无希望时,我看着切石工人在他的石头上,敲击了上百次,而不见任何裂痕出现。但在第一百零一次时,石头被劈成两半。我体会到,并非那一击,而是前面的敲打使它裂开。――[贾柯·瑞斯] 88.每个意念都是一场祈祷。――[詹姆士·雷德非]
116.昨天是张退票的支票,明天是张信用卡,只有今天才是现金;要善加利用。――[凯·里昂] 117.所有的财富都是建立在健康之上。浪费金钱是愚蠢的事,浪费健康则是二级的谋杀罪。――[B·C·福比斯] 118.明知不可而为之的干劲可能会加速走向油尽灯枯的境地,努力挑战自己的极限固然是令人激奋的经验,但适度的休息绝不可少,否则迟早会崩溃。――[迈可·汉默] 119.进步不是一条笔直的过程,而是螺旋形的路径,时而前进,时而折回,停滞后又前进,有失有得,有付出也有收获。――[奥古斯汀] 120.无论那个时代,能量之所以能够带来奇迹,主要源于一股活力,而活力的核心元素乃是意志。无论何处,活力皆是所谓“人格力量”的原动力,也是让一切伟大行动得以持续的力量。――[史迈尔斯] 121.有两种人是没有什么价值可言的:一种人无法做被吩咐去做的事,另一种人只能做被吩咐去做的事。――[C·H·K·寇蒂斯] 122.对于不会利用机会的人而言,机会就像波浪般奔向茫茫的大海,或是成为不会孵化的蛋。――[乔治桑] 123.未来不是固定在那里等你趋近的,而是要靠你创造。未来的路不会静待被发现,而是需要开拓,开路的过程,便同时改变了你和未来。――[约翰·夏尔] 124.一个人的年纪就像他的鞋子的大小那样不重要。如果他对生活的兴趣不受到伤害,如果他很慈悲,如果时间使他成熟而没有了偏见。――[道格拉斯·米尔多] 125.大凡宇宙万物,都存在着正、反两面,所以要养成由后面.里面,甚至是由相反的一面,来观看事物的态度――。[老子]
87.当一切毫无希望时,我看着切石工人在他的石头上,敲击了上百次,而不见任何裂痕出现。但在第一百零一次时,石头被劈成两半。我体会到,并非那一击,而是前面的敲打使它裂开。――[贾柯·瑞斯] 88.每个意念都是一场祈祷。――[詹姆士·雷德非]
电化学基础ppt10(26份打包) 人教课标版5

第四章
电化学基础
第四章
电化学基础
热点一 [热点分析]
原电池的工作原理及其应用
以高科技或新型电池为背景考查原电池的工作
原理,是高考常见的切入点,题型以选择题、非选择题为主。 (1)选择题重点考查电极的判断、电子及离子的移动方向、电 极反应类型、电极附近或整个溶液的 pH 变化,以及判断电 极反应式的正误等。
- + +
第四章
电化学基础
(2015· 高考浙江卷)在固态金属氧化物电解池中, 高 温共电解 H2O-CO2 混合气体制备 H2 和 CO 是一种新的能 源利用方式,基本原理如下图所示。下列说法不正确的是 ( )
第四章
电化学基础
A.X 是电源的负极 B.阴极的电极反应式是 H2O+2e ===H2+O2
第四章
电化学基础
0~t1 时,原电池的负极是 Al 片,此时,正极的电极反应式 是____________________________________,溶液中的 H
+
向________极移动。t1 时,原电池中电子流动方向发生改变, 其原因是________________________________。
答案:NO3 +e +2H ===NO2↑+H2O
-
-
+
正 Al 在浓硝酸
中发生钝化,生成的氧化膜阻止了 Al 的进一步反应
第四章
电化学基础
热点二 [热点分析]
电解原理及其应用
该热点在高考考查中以选择题为主,有时也出
现在非选择题中以填空形式进行考查, 题型稳定、 难度不大, 考查的角度主要有: (1)电解原理、电极反应式的书写。 (2)离子放电顺序、电极产物的判断。 (3)电解质溶液 pH 的变化分析。
电化学基础
第四章
电化学基础
热点一 [热点分析]
原电池的工作原理及其应用
以高科技或新型电池为背景考查原电池的工作
原理,是高考常见的切入点,题型以选择题、非选择题为主。 (1)选择题重点考查电极的判断、电子及离子的移动方向、电 极反应类型、电极附近或整个溶液的 pH 变化,以及判断电 极反应式的正误等。
- + +
第四章
电化学基础
(2015· 高考浙江卷)在固态金属氧化物电解池中, 高 温共电解 H2O-CO2 混合气体制备 H2 和 CO 是一种新的能 源利用方式,基本原理如下图所示。下列说法不正确的是 ( )
第四章
电化学基础
A.X 是电源的负极 B.阴极的电极反应式是 H2O+2e ===H2+O2
第四章
电化学基础
0~t1 时,原电池的负极是 Al 片,此时,正极的电极反应式 是____________________________________,溶液中的 H
+
向________极移动。t1 时,原电池中电子流动方向发生改变, 其原因是________________________________。
答案:NO3 +e +2H ===NO2↑+H2O
-
-
+
正 Al 在浓硝酸
中发生钝化,生成的氧化膜阻止了 Al 的进一步反应
第四章
电化学基础
热点二 [热点分析]
电解原理及其应用
该热点在高考考查中以选择题为主,有时也出
现在非选择题中以填空形式进行考查, 题型稳定、 难度不大, 考查的角度主要有: (1)电解原理、电极反应式的书写。 (2)离子放电顺序、电极产物的判断。 (3)电解质溶液 pH 的变化分析。
应用电化学基础理论PPT课件

04
燃料电池的燃料可以是氢气、甲烷、乙醇等,氧化剂可以是氧气或空 气,通过控制反应条件可以实现高效、清洁的能源利用。
电镀与金属的电化学腐蚀防护
电镀是利用电解原理在金属表面镀上一层金属或合金 的过程,以提高金属的耐腐蚀性、耐磨性、装饰性和
功能性。
输标02入题
电镀过程中,阳极上的金属离子会通过电解作用沉积 在阴极表面形成镀层,可以控制镀层的厚度和成分。
反应和电解池反应。
电极反应
电子转移
电化学反应中,电极与电 解质溶液界面上的反应, 包括氧化和还原反应。
电化学反应中,电子从一 个原子或分子转移到另一 个原子或分子的过程。
离子转移
电化学反应中,离子在 电解质溶液中的迁移过
程。
电解质溶液
电解质
在水溶液或熔融状态下能导电的化合物。
电导率
衡量电解质溶液导电能力的物理量,与溶液 中离子的浓度和迁移率有关。
详细描述
电化学反应速率常数的大小反映了电化学反 应的快慢程度,其值越大,反应速率越快。 在一定条件下,可通过实验测定电化学反应 速率常数。
总结词
电化学反应的活化能是影响电化学反应 速率的重要因素之一,其大小与反应物
质的性质和温度等因素有关。
详细描述
活化能的大小决定了电化学反应的难易程度,活化能越高,反应越难以进行。在一定条件下,可通过实验测定电 化学反应的活化能。
目的
通过本PPT课件的学习,使学习者掌 握电化学的基本原理和应用,了解电 化学在解决实际问题中的重要性和作 用。
意义
通过深入了解电化学的应用,为解决 能源、环境、材料等领域的实际问题 提供理论支持和实践指导,促进相关 领域的发展和进步。
02 电化学基本概念
燃料电池的燃料可以是氢气、甲烷、乙醇等,氧化剂可以是氧气或空 气,通过控制反应条件可以实现高效、清洁的能源利用。
电镀与金属的电化学腐蚀防护
电镀是利用电解原理在金属表面镀上一层金属或合金 的过程,以提高金属的耐腐蚀性、耐磨性、装饰性和
功能性。
输标02入题
电镀过程中,阳极上的金属离子会通过电解作用沉积 在阴极表面形成镀层,可以控制镀层的厚度和成分。
反应和电解池反应。
电极反应
电子转移
电化学反应中,电极与电 解质溶液界面上的反应, 包括氧化和还原反应。
电化学反应中,电子从一 个原子或分子转移到另一 个原子或分子的过程。
离子转移
电化学反应中,离子在 电解质溶液中的迁移过
程。
电解质溶液
电解质
在水溶液或熔融状态下能导电的化合物。
电导率
衡量电解质溶液导电能力的物理量,与溶液 中离子的浓度和迁移率有关。
详细描述
电化学反应速率常数的大小反映了电化学反 应的快慢程度,其值越大,反应速率越快。 在一定条件下,可通过实验测定电化学反应 速率常数。
总结词
电化学反应的活化能是影响电化学反应 速率的重要因素之一,其大小与反应物
质的性质和温度等因素有关。
详细描述
活化能的大小决定了电化学反应的难易程度,活化能越高,反应越难以进行。在一定条件下,可通过实验测定电 化学反应的活化能。
目的
通过本PPT课件的学习,使学习者掌 握电化学的基本原理和应用,了解电 化学在解决实际问题中的重要性和作 用。
意义
通过深入了解电化学的应用,为解决 能源、环境、材料等领域的实际问题 提供理论支持和实践指导,促进相关 领域的发展和进步。
02 电化学基本概念
电化学基本概念ppt课件
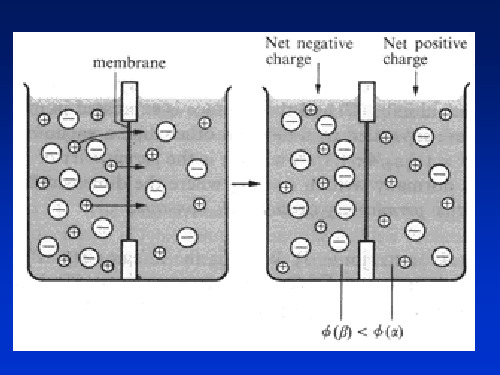
i i
两相间建立平衡电势
电极(Electrode)
电极材料/电解质
Zn|Zn2+, SO42Pt|H2,H+ Fe|Fe3O4|Fe2O3|水溶液
电极(Electrode)
电极材料/电解质 •传递电荷
Zn|Zn2+,SO42-,
•氧化或还原反应
Pt|H2,H+
的地点
•“半电池”
Fe|Fe3O4|Fe2O3|水溶液
法拉弟定律的几个要点
1. 电和化学反应相互作用的定量关系 2. 不受电极、外界条件的影响 3. 适用于多个电化学装置的多个反应(串联)
e-
i
H2
Cl2
Na+
Cl-
Ag
Ag+
ei
Ag+
Ag+
H+
OH-
阴极
阳极
H+
NO3-
银阴极 银阳极
法拉弟定律的几个要点
1. 电和化学反应相互作用的定量关系 2. 不受电极、外界条件的影响 3. 适用于多个电化学装置的多个反应(串联) 4. 适用于单个电化学装置的多个反应(并联)
I
负极 e
e 正极
-2e Pb
Pb2+ PbSO4
H2O H+
SO4= SO4= H+
硫酸
+2e PbO2
Pb2+ PbSO4
铅酸蓄电池 (1860年--)
充电
(吸收电能)
负极 e
e 正极
Pb2+ PbSO4
+2e
Pb
Pb2+
H2O
PbSO4
〔人教课标版〕高中化学电化学基础优质PPT 课件1 (3)

阳极:阳极材料是活泼电极时阳极材料放电,否则是溶液中阴离 子放电,放电顺序是:活泼金属>S2->I->Br->Cl->OH->SO24->F-。
阴极:一般是溶液中的阳离子放电,金属活动性顺序的逆顺序。 阳离子放电顺序:Ag+>Hg2+>Fe3+>Cu2+>H+(酸)>Pb2+>Fe2+>Zn2+>H+ (水)>活泼金属阳离子。
5
中一小时
铁丝表面已变得灰暗
6
将浸过氯化钠溶液的铁丝放在高于常 铁丝表面灰暗程度比实验 5
温的氧气流中一小时
严重
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是_3_、__4_、__5_、__6_(填实验序号); 在电化学腐蚀中,负极反应是_F_e_-__2_e-__=_=_=_F_e_2+__(或___2_F_e_-__4_e_-_=_=_=_2_F_e_2_+;) 正极反应是_2_H_2_O_+__O__2+__4_e_-_=_=__=_4_O_H__-。
书写注意事项:一看电极材料、二看电解质溶液、三看附加条件
与信息。
典例精析 [例 3] 如下图所示的电解池Ⅰ和电解池Ⅱ中,a、b、c 和 d 均为 Pt 电极。电解过程中,电极 b 和 d 上没有气体逸出,但质量均增大, 且增重 b<d。符合上述实验结果的盐溶液是( )
选项
A B C D
X
MgSO4 AgNO3 FeSO4 CuSO4
专题二 电解原理及应用 专题归纳
电解池中,阳极发生氧化反应,阴极发生还原反应。电解原理在 电解饱和食盐水制烧碱、氯气和氢气以及电镀、电冶金等方面有广泛 的应用。考纲中要求“了解氯碱工业反应原理”,所以电解 NaCl 水溶 液的相关内容是高考的热点。
第十一章电化学基础.ppt

④确定两半反应方程式得、失电子数目的最小公倍数。 将两个半反应方程式中各项分别乘以相应的系数,使得、 失电子数目相同。然后,将两者合并,就得到了配平的氧 化还原反应的离子方程式。有时根据需要可将其改为分e2(SO4)3 + K2SO4+ H2O
(3)若出现分数,可调整为最小正整数:
2 KMnO4 +10 FeSO4 + H2SO4 = 2 MnSO4 + 5 Fe2(SO4)3 + K2SO4 + H2O
(4) 配平各元素原子数(观察法)
先配平非H、O原子,后配平H、O原子。 1)配平K+、SO42-数目 SO42-:左11,应+7;右18
配平原则: ① 电荷守恒:氧化剂得电子数等于还原剂失电子数。
② 质量守恒:反应前后各元素原子总数相等。
配平步骤:
①用离子式写出主要反应物和产物(气体、纯液体、固 体和弱电解质则写分子式)。
②分别写出氧化剂被还原和还原剂被氧化的半反应。
③分别配平两个半反应方程式,等号两边的各种元素 的原子总数各自相等且电荷数相等。
3)配平(或核对)O的原子数目:已平衡。
对于电解质在溶液中的反应,也可通过“离子方程 式”表示(更简洁),配平步骤类似: MnO4- + Fe2+ + H+ Mn2+ + Fe3+ + H2O
MnO4- + 5 Fe2+ + H+ Mn2+ + 5 Fe3+ + H2O
MnO4- + 5 Fe2+ + 8 H+ Mn2+ + 5 Fe3+ + H2O
(3)若出现分数,可调整为最小正整数:
2 KMnO4 +10 FeSO4 + H2SO4 = 2 MnSO4 + 5 Fe2(SO4)3 + K2SO4 + H2O
(4) 配平各元素原子数(观察法)
先配平非H、O原子,后配平H、O原子。 1)配平K+、SO42-数目 SO42-:左11,应+7;右18
配平原则: ① 电荷守恒:氧化剂得电子数等于还原剂失电子数。
② 质量守恒:反应前后各元素原子总数相等。
配平步骤:
①用离子式写出主要反应物和产物(气体、纯液体、固 体和弱电解质则写分子式)。
②分别写出氧化剂被还原和还原剂被氧化的半反应。
③分别配平两个半反应方程式,等号两边的各种元素 的原子总数各自相等且电荷数相等。
3)配平(或核对)O的原子数目:已平衡。
对于电解质在溶液中的反应,也可通过“离子方程 式”表示(更简洁),配平步骤类似: MnO4- + Fe2+ + H+ Mn2+ + Fe3+ + H2O
MnO4- + 5 Fe2+ + H+ Mn2+ + 5 Fe3+ + H2O
MnO4- + 5 Fe2+ + 8 H+ Mn2+ + 5 Fe3+ + H2O
电化学基本知识ppt课件
电池过程
阴极
阳极
ZnSO4
CuSO4
Zn
Cu
盐桥
1.1 V
典型电化学过程
e
电化学过程的特点
Zn(s) + CuSO4(aq) ZnSO4(aq) + Cu(s) 半反应: Zn(s) Zn2+ + 2e- 阳极反应 Cu2+ + 2e- Cu(s) 阴极反应 电子不能在离子导体中运动 离子不能在电子导体中运动 即:电子与离子间必定在界面处发生了转化,这个转化就发生在离子导体和电子导体的界面处。
高频区为电极反应动力学(电荷传递过程)控制,低频区由电极反应的反应物或产物的扩散控制。
从图可得体系R、Rct、Cd以及参数,与扩散系数有关,利用它可以估算扩散系数D。由Rct可计算i0和k0。
扩散阻抗的直线可能偏离45,原因:
电极表面很粗糙,以致扩散过程部分相当于球面扩散; 除了电极电势外,还有另外一个状态变量,这个变量在测量的过程中引起感抗。
盐桥
1. 可以同时测量极化电流和极化电位; 2. 三电极两回路具有足够的测量精度。
三电极的优点
1.2.5.1 辅助电极的作用 实现WE导电并使WE电力线分布均匀。 1.2.5.2 辅助电极的要求 ①辅助电极面积大; 为使参比电极等势面,应使辅助电极面积增大,以保证满足研究电极表面电位分布均匀,如是平板电极: ; ②辅助电极形状应与研究电极相同,以实现均匀电场作用。
参比电极
常见的参比电极 ①甘汞电极; Hg|Hg2Cl2|Cl- 由于Hg+→Hg2+ (亚汞不稳定,高温时易变成Hg2+,受温度影响大。<70℃,另外,[Cl-]要饱和,防止 发生变化)。
高考化学复习课件:电化学基础
考试大纲要求
高考热点提示
1.了解原电池和电解 1.原电池的工作原理,电极反应
池的工作原理,能写 及电池反应方程式的分析与判断
出电极反应和电池反 的考查.
应方程式.
2.电解池的工作原理、电极反
2.了解常见化学电源 应、电池反应方程式的书写、电
的种类及其工作原 极产物的判断及结合两极电子守
理.
恒进行简单计算的考查.
C.总反应:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2.
(2)二次电池——铅蓄电池
①负极材料: 液.
,正极材料: Pb
②电极反应:A.负极:
,电P解bO质2 :H2SO4溶
C.总反应:Pb+PbO2+2H2SO4===2PbSO4+2H2O
(3)氢氧燃料电池
①H2SO4作电解质
解析:本题考查原电池的有关知识.在原电池中,活泼性较强的金属作负 极,活泼性相对较弱的金属或非金属作正极.在题给装置中,Zn作负极, 负极反应:Zn-2e-===Zn2+,Cu作正极,正极反应:2H++2e-===H2↑, 故A、B错;电子由锌片经导线流向铜片,电流方向与之相反,C错,D正 确.
负极:
,正极:
,电池反应:
.H2-2e-===2H+
O2+4e-+
②负K极O:H4作H+电=解==质2H2O
,正2极H2:+O2
===2H2O
,电池反应: .
2H2+O2===2H2O O2+4e-+2H2O===4OH-
2H2+O2===2H2O
1.关于如右图所示装置的叙述,正确的是( ) A.铜是阳极,铜片上有气泡产生 B.铜片质量逐渐减少 C.电流从锌片经导线流向铜片 D.氢离子在铜片表面被还原
高考热点提示
1.了解原电池和电解 1.原电池的工作原理,电极反应
池的工作原理,能写 及电池反应方程式的分析与判断
出电极反应和电池反 的考查.
应方程式.
2.电解池的工作原理、电极反
2.了解常见化学电源 应、电池反应方程式的书写、电
的种类及其工作原 极产物的判断及结合两极电子守
理.
恒进行简单计算的考查.
C.总反应:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2.
(2)二次电池——铅蓄电池
①负极材料: 液.
,正极材料: Pb
②电极反应:A.负极:
,电P解bO质2 :H2SO4溶
C.总反应:Pb+PbO2+2H2SO4===2PbSO4+2H2O
(3)氢氧燃料电池
①H2SO4作电解质
解析:本题考查原电池的有关知识.在原电池中,活泼性较强的金属作负 极,活泼性相对较弱的金属或非金属作正极.在题给装置中,Zn作负极, 负极反应:Zn-2e-===Zn2+,Cu作正极,正极反应:2H++2e-===H2↑, 故A、B错;电子由锌片经导线流向铜片,电流方向与之相反,C错,D正 确.
负极:
,正极:
,电池反应:
.H2-2e-===2H+
O2+4e-+
②负K极O:H4作H+电=解==质2H2O
,正2极H2:+O2
===2H2O
,电池反应: .
2H2+O2===2H2O O2+4e-+2H2O===4OH-
2H2+O2===2H2O
1.关于如右图所示装置的叙述,正确的是( ) A.铜是阳极,铜片上有气泡产生 B.铜片质量逐渐减少 C.电流从锌片经导线流向铜片 D.氢离子在铜片表面被还原
物理化学电子课件第七章电化学基础
第二节 电解质溶液
一、电导和电导率 图7-4所示为几种电解质溶液的电导率与浓度的关系。
第二节 电解质溶液
二、摩尔电导率
因为电解质溶液的电导率与浓度有关,因此不能用电导率来比较 不同浓度、不同类型的电解质的导电能力,需要引入摩尔电导率的概 念。
第二节 电解质溶液
三、电导的测定
电导是电阻的倒数,因此测量电解质溶液的电导实际上是测量其 电阻。测量溶液的电阻可利用惠斯通电桥,如图7-5所示。
第二节 电解质溶液
第三节 可逆电池及原电池热力学
一、可逆电池
(1)充电、放电反应必须可逆,即化学可逆和物质可逆,要求
(2)反应要在无限接近电化学平衡条件下进行,即可逆电池的 能量转移必须是热力学可逆的,要求电池必须在电流趋于无限小(即
I 0)的状态下工作。放电时对外所做的电功和充电时消耗的电功 大小相等,保证当系统恢复原状时环境也能复原,不留下任何变
第一节 电化学的基本概念
三、离子的电迁移和迁移数
3. 离子迁移数 t有多种测定方法,这里主要介绍希托夫(Hittorf) 法。其原理是:分别测定离子迁出或迁入相应电极区的物质的量及发 生电极反应的物质的量,然后通过物料衡算得到离子迁移数。实验装 置如图7-3所示。
第一节 电化学的基本概念
三、离子的电迁移和迁移数 实验测定中的物料衡算思路为:电解后某离子剩余的物质的量
二、法拉第电解定律
1833年,英国科学家法拉第(Faraday)在研究了大量电解过程后提出 了著名的法拉第电解定律——电解时电极上发生化学反应的物质的量与 通过电解池的电荷量成正比,简称为法拉第定律,其数学表达式为:
第一节 电化学的基本概念
三、离子的电迁移和迁移数
通电于电解质溶液后,溶液中承担导电任务的阴、阳离子分别向 阳极和阴极移动,同时在相应的两个电极界面上发生氧化或还原作用。 这种在电场作用下阴、阳离子分别向两极运动的现象称为电迁移。电 迁移是电解质溶液导电的必要条件。即
大学化学之电化学基础PPT讲稿
20
5.2.2 原电池的符号表示
1.书写要求 (1) 负极写在左边,正极写在右边; (2)正负极之间用盐桥“‖”相接; (3)电极固体标志用一竖线“│”表示; (4)同相之不同物质间用“,”间隔; (5)若为离子时应注明其活度(浓度亦可); (6)若电对不含金属导体,则需加一惰性导体; (7)纯气体、液体或固体与惰性电极名称之间以
17
5.2.1 原电池的概念
1.定义 原电池是利用氧化还原 反应产生电流的装置。
2.原电池的构成 ⑴电势不同的两个电极; ⑵盐桥; ⑶外电路(检流计)。
18
3.Daniell电池
e
—
+
图1 Daniell电池
电子由Zn极流向Cu极: Zn极电势低,为负极;Cu极电势高,为正极。
19
4.特征 正极:氧化剂(Cu2+)被还原,半电池反应为: Cu2+ + 2e → Cu 负极:还原剂(Zn)被氧化,半电池反应为: Zn → Zn 2+ + 2e 电池反应为: Cu2+ + Zn → Cu + Zn 2+
22
(2)电极组成:
正极:Pt│MnO4- (c1),Mn2+(c2),H+ (c3) 负极:Pt, O2 (p)│ H2O2 (c4), H+ (c3)
(3)电池符号:
(-)Pt, O2 (p)│ H2O2 (c4), H+ (c3)‖ MnO4- (c1),Mn2+(c2),H+ (c3) │ Pt(+)
①×5 + ② 得:
6Cl2(g)+ 12OH- = 10Cl- + 2ClO3-+ 6H2O 化简得:
3Cl2(g)+ 6OH- = 5Cl- + ClO3-+ 3H2O 3Cl2(g)+ 6NaOH = 5NaCl + NaClO3+ 3H2O
5.2.2 原电池的符号表示
1.书写要求 (1) 负极写在左边,正极写在右边; (2)正负极之间用盐桥“‖”相接; (3)电极固体标志用一竖线“│”表示; (4)同相之不同物质间用“,”间隔; (5)若为离子时应注明其活度(浓度亦可); (6)若电对不含金属导体,则需加一惰性导体; (7)纯气体、液体或固体与惰性电极名称之间以
17
5.2.1 原电池的概念
1.定义 原电池是利用氧化还原 反应产生电流的装置。
2.原电池的构成 ⑴电势不同的两个电极; ⑵盐桥; ⑶外电路(检流计)。
18
3.Daniell电池
e
—
+
图1 Daniell电池
电子由Zn极流向Cu极: Zn极电势低,为负极;Cu极电势高,为正极。
19
4.特征 正极:氧化剂(Cu2+)被还原,半电池反应为: Cu2+ + 2e → Cu 负极:还原剂(Zn)被氧化,半电池反应为: Zn → Zn 2+ + 2e 电池反应为: Cu2+ + Zn → Cu + Zn 2+
22
(2)电极组成:
正极:Pt│MnO4- (c1),Mn2+(c2),H+ (c3) 负极:Pt, O2 (p)│ H2O2 (c4), H+ (c3)
(3)电池符号:
(-)Pt, O2 (p)│ H2O2 (c4), H+ (c3)‖ MnO4- (c1),Mn2+(c2),H+ (c3) │ Pt(+)
①×5 + ② 得:
6Cl2(g)+ 12OH- = 10Cl- + 2ClO3-+ 6H2O 化简得:
3Cl2(g)+ 6OH- = 5Cl- + ClO3-+ 3H2O 3Cl2(g)+ 6NaOH = 5NaCl + NaClO3+ 3H2O
