第四节 金属的电化学腐蚀与防护(过关检测)
高二化学金属的电化学腐蚀与防护试题答案及解析

高二化学金属的电化学腐蚀与防护试题答案及解析1.下列物质的说法正确的是A.芳香烃可以来自于煤干馏产品中的煤焦油B.聚氯乙烯可用于制作食品包装袋C.镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀D.在铁的吸氧腐蚀中,负极是炭,电极反应为2H2O+O2+4eˉ=" 4OHˉ"【答案】A【解析】B聚氯乙烯是有毒物,C锌比铁活泼,可以起到保护铁的作用,而锡的活泼性比铁弱,不能起到保护铁作用。
D铁是负极,碳是正极。
所以答案选A【考点】考查化学的基本概念和基本理论的相关知识点2.如下图各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )A.④>②>①>③B.②>①>③>④C.④>②>③>①D.③>②>④>①【答案】A【解析】以①作参照物,进行比较。
在②中构成了原电池。
由于活动性Fe>Sn,所以Fe作负极,加快了Fe的腐蚀,因此②>①,在③中构成了原电池。
由于活动性Zn>Fe,所以Zn作负极,首先被腐蚀的的是Zn Fe得到了保护,腐蚀比原来慢。
因此腐蚀速率①>③。
④构成的是电解池,Fe是活性电极。
由于Fe与电源的正极连接,作阳极,发生反应:Fe-2e-=Fe2+.腐蚀的速率比作原电池的负极还要快。
因此腐蚀速率④>②。
所以铁在其中被腐蚀时由快到慢的顺序是④>②>①>③。
选项为A。
【考点】考查铁在不同情况下被腐蚀的快慢的顺序的知识。
3. [双选题]下列说法正确的是()A.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀B.原电池反应是导致金属腐蚀的主要原因,故不能用原电池原理来减缓金属的腐蚀C.钢铁电化学腐蚀的两种类型主要区别在于水膜的酸性不同,引起的正极反应不同D.无论哪种类型的腐蚀,其实质都是金属被氧化【答案】CD【解析】金属的腐蚀就是金属失电子被氧化的过程,因此D正确;析氢腐蚀和吸氧腐蚀是由于水膜酸性不同,正极反应就不同,C正确;原电池反应既可以加快金属的腐蚀,也可用于防止金属的腐蚀,如轮船外壳镶嵌锌块;不锈钢、镀锌铁等中的Fe均不易被腐蚀,A、B不正确。
人教版高二化学选修4 第四章第四节 金属的电化学腐蚀与防护 素养达标练
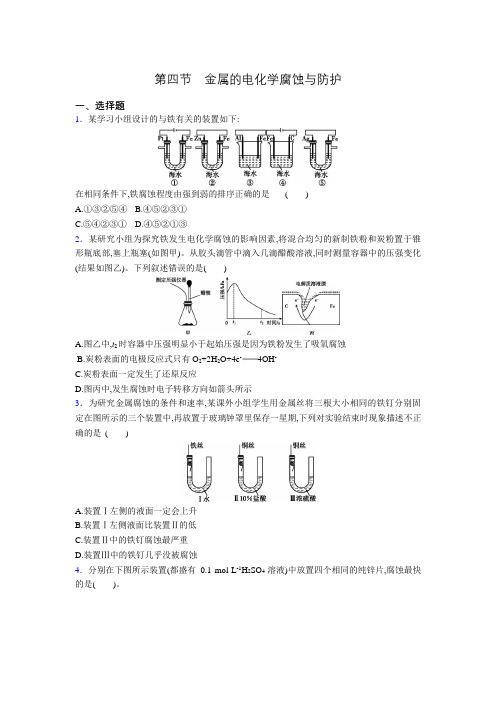
第四节金属的电化学腐蚀与防护一、选择题1.某学习小组设计的与铁有关的装置如下:在相同条件下,铁腐蚀程度由强到弱的排序正确的是()A.①③②⑤④B.④⑤②③①C.⑤④②③①D.④⑤②①③2.某研究小组为探究铁发生电化学腐蚀的影响因素,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图甲)。
从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化(结果如图乙)。
下列叙述错误的是()A.图乙中,t2时容器中压强明显小于起始压强是因为铁粉发生了吸氧腐蚀B.炭粉表面的电极反应式只有O2+2H2O+4e-4OH-C.炭粉表面一定发生了还原反应D.图丙中,发生腐蚀时电子转移方向如箭头所示3.为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在图所示的三个装置中,再放置于玻璃钟罩里保存一星期,下列对实验结束时现象描述不正确的是()A.装置Ⅰ左侧的液面一定会上升B.装置Ⅰ左侧液面比装置Ⅱ的低C.装置Ⅱ中的铁钉腐蚀最严重D.装置Ⅲ中的铁钉几乎没被腐蚀4.分别在下图所示装置(都盛有0.1 mol·L-1H2SO4溶液)中放置四个相同的纯锌片,腐蚀最快的是()。
5.糕点包装中常用的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。
下列分析正确的是()A.脱氧过程是吸热反应,可降低温度,延长糕点保质期B.脱氧过程中铁作原电池正极,电极反应为Fe-3e-Fe3+C.脱氧过程中碳作原电池负极,电极反应为2H2O+O2+4e-4OH-D.含有1.12 g铁粉的脱氧剂,理论上最多能吸收氧气336 mL(标准状况)6.下列与金属腐蚀有关的说法中,不正确的是()A.钢铁在潮湿空气中生锈属于电化学腐蚀B.电化学腐蚀一般可分为吸氧腐蚀和析氢腐蚀C.金属腐蚀的本质是金属原子失去电子被氧化D.铝具有很强的抗腐蚀能力,是因为其不易与氧气发生反应7.中国上海世博会澳大利亚馆的外墙采用的是特殊的耐风化钢覆层材料,外墙的颜色每天都在发生着变化,它会随空气中太阳、风雨、湿度的影响,逐渐从橙色转变成代表澳大利亚大漠的赭红色,这种转变运用了钢材锈蚀原理。
高中化学第四节金属的电腐蚀与防护试题880

高中化学第四节金属的电腐蚀与防护试题 2019.091,100mL浓度为2 mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是 ( )A.加入适量的6mol·L-1的盐酸B.加入数滴氯化铜溶液C.加入适量蒸馏水D.加入适量的氯化钠溶液2,熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气体为阴极助燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:阳极反应式:2CO+2CO32--4e-== 4CO2阴极反应式:_________________,电池总反应式:_______________。
3,氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。
氢镍电池的总反应式是:(1/2)H2+NiO(OH) Ni(OH)2根据此反应式判断下列叙述中正确的是( )A.电池放电时,电池负极周围溶液的pH不断增大B.电池放电时,镍元素被氧化C.电池充电时,氢元素被还原D.电池放电时,H2是负极4,钢铁发生电化学腐蚀时,负极发生的反应()A.2H++2e-==H2 B.2H2O+O2+4e-== 4OH-C.Fe-2e-==Fe2+ D.4OH-+4e-==2H2O+O25,镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:由此可知,该电池放电时的负极材料是( )A.Cd(OH)2 B.Ni(OH)2C.Cd D.NiO(OH)6,铜片和锌片用导线连接后插入稀硫酸中,锌片是( )A.阴极 B.正极 C.阳极 D.负极7,下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是 ( )A.a电极是负极B.b电极的电极反应为:4OH--4e-== 2H2O+O2↑C.氢氧燃料电池是一种具有应用前景的绿色电源D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置8,碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。
第四节金属的电化学腐蚀与防护(新授)

第四章 电化学基础
课后达标检测
栏目 导引
第四章 电化学基础
本部分内容讲解结束
按ESC键退出全屏播放
栏目 导引
栏目 导引
第四章 电化学基础
2.改变金属的内部结构,如制成合金、不锈钢等。 3.加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表 面钝化等方法。
栏目 导引
第四章 电化学基础
1.正误判断:正确的打“√”,错误的打“×”,并阐释错 因或列举反例。
语句描述
阐释错因或列举 正误
反例
(1)轮船的船壳水线以下常装有一些
栏目 导引
第四章 电化学基础
答案:(1)Fe-2e-===Fe2+ (2)O2+4e-+2H2O===4OH- (3)2Fe+O2+2H2O===2Fe(OH)2 (4)4Fe(OH)2+O2+2H2O===4Fe(OH)3 (5)2Fe(OH)3===Fe2O3·xH2O+(3-x)H2O
栏目 导引
第四章 电化学基础
题组一 金属腐蚀的理解和判断 1.下列关于金属腐蚀的说法正确的是( ) A.金属在潮湿空气中腐蚀的实质是 M+nH2O===M(OH)n +n2H2↑ B.金属化学腐蚀的实质是 M-ne-===Mn+,电子直接转移 给氧化剂 C.金属的化学腐蚀必须在酸性条件下进行 D.在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀
栏目 导引
第四章 电化学基础
学习小结 1.钢铁在酸性环境中主要发生析氢腐蚀,放出氢气。 2.钢铁在中性或弱酸性环境中主要发生吸氧腐蚀,最终生成 铁锈的主要成分是 Fe2O3·xH2O。 3.钢铁吸氧腐蚀的正极发生的电极反应为 2H2O+O2+4e- ===4OH-。 4.金属电化学防护的方法有牺牲阳极的阴极保护法和外加电 流的阴极保护法。 5.金属腐蚀快慢的规律 电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有 保护措施的腐蚀。
4.4金属的电化学腐蚀与防护(练习)(解析版)

4.4 金属的电化学腐蚀与防护1.(福建省永泰县第一中学2019-2020学年高二上学期期中考试)下列化学用语或说法正确的是()A .用铁作阳极电解熔融Al 2O 3生产金属铝B .钢铁吸氧腐蚀的正极反应:--22O +2H O+4e =4OHC .粗铜(含Zn 、Fe 、Ag 、Au 杂质)精炼阳极泥的成分只有AuD .石墨作电极电解饱和食盐水:+222H +Cl Cl + H 通电【答案】B【解析】A 、用铁作阳极电解熔融Al 2O 3,阳极反应式为:Fe -2e -=Fe2+,电极被损耗,不符合生产实际,故A 错误;B 、钢铁吸氧腐蚀的正极发生还原反应,其电极反应式为:O 2+2H 2O +4e -=4OH -,故B 正确;C 、粗铜(含Zn 、Fe 、Ag 、Au 杂质)精炼阳极泥的成分主要为失电子能力比铜弱的金属(Au 、Ag 等),故C 错误;D 、石墨作电极电解饱和食盐水,阳极上是Cl -失去电子生成Cl 2,阴极为水电离出的H +得到电子,其电解总反应为:2Cl -+2H 2O H 2↑+Cl 2↑+2OH -,故D 错误。
2.(江苏省邗江中学2019-2020学年高二上学期期中考试)下列叙述正确的是()①锌跟稀硫酸反应制H 2,加入少量硫酸铜溶液能加快反应速率②镀层破损后,白口铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀③电镀时,应把镀件置于电解槽的阴极④冶炼铝时,把氧化铝加入液态冰晶石中熔融后电解⑤钢铁表面常易腐蚀生成Fe 2O 3·nH 2OA.全部B.①③④⑤C.①②⑤D.②④【答案】B【解析】Zn+Cu=Cu+Zn,形成原电池,加快反①锌与硫酸铜溶液发生置换反应,其离子反应方程式为:2+2+应速率,①正确;②金属活动性:Zn>Fe>Sn,镀层破损后,白口铁(镀锌的铁)中Zn为原电池的负极,仍能保护Fe,而马口铁(镀锡的铁)中Fe为原电池的负极,加快Fe的腐蚀,马口铁(镀锡的铁)比白口铁(镀锌的铁)更易腐蚀,②错误;③电镀时,镀件金属为电解池的阴极,镀层金属为电解池的阳极,在阴极上析出镀层金属,③正确;Na AlF)熔融后电④冶炼金属铝,电解熔融的氧化铝,为了降低其熔点,氧化铝加入液态冰晶石(36解;④正确;⑤钢铁表面常因发生原电池而被腐蚀,由于Fe比杂质C活泼,所以Fe作原电池的负极被氧化,最终Fe O nH O),⑤正确。
高三化学金属的电化学腐蚀与防护试题答案及解析

高三化学金属的电化学腐蚀与防护试题答案及解析1.一定条件下,碳钢腐蚀与溶液pH的关系如下:A.在pH<4溶液中,碳钢主要发生析氢腐蚀B.存pH>6溶液中,碳钢主要发生吸氧腐蚀C.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e-=2H2OD.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓【答案】C【解析】A、酸性条件下,碳钢发生析氢腐蚀,Fe-2e-= Fe2+,正确;B、当pH>6溶液中,碳钢主要发生吸氧腐蚀,负极电极反应式为:Fe-2e-=Fe2+,正极上电极反应式为:O2+2H2O+4e-=4OH-,正确;C.在pH>14溶液中,碳钢腐蚀的正极反应O2+2H2O+4e-=4OH-,错误;D.在煮沸除氧气后的碱性溶液中,正极上氧气生成氢氧根离子速率减小,所以碳钢腐蚀速率会减缓,正确,答案选C。
【考点】考查金属的电化学腐蚀的种类与发生条件的判断2.铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。
下列说法不正确的是A.因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀B.若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小C.铜极上的反应是2H+ + 2e- ="=" H2↑,O2+ 4e- + 4H+ ="=" 2H2OD.在金属表面涂一层油脂,能防止铁铆钉被腐蚀【答案】B【解析】A、因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀,正确;B、若水膜中溶解了SO2,使溶液酸性增强,氢离子浓度增大,则铁铆钉腐蚀的速率变大,错误;C、从图中可看出,铁同时发生析氢和吸氧腐蚀,铜极是正极,发生的反应是2H+ + 2e- ="=" H2↑,O2+ 4e- + 4H+ ="="2H2O ,正确;D、在金属表面涂一层油脂,隔绝氧气,能防止铁铆钉被腐蚀,正确,答案选B。
【考点】考查金属腐蚀原理及防护3.下列说法不正确的是:A.通过煤的干馏可获得苯、甲苯等芳香烃B.在海轮外壳装上锌块,可减缓船体的腐蚀速率C.电渗析法、离子交换法中,只有后者可以应用于海水的淡化D.我国城市推广使用清洁燃料是压缩天然气类和液化石油气类【答案】C【解析】A、煤干馏可得煤焦油,煤焦油中含有苯、甲苯等芳香烃,正确;B、在海轮外壳装上锌块,形成原电池时,Zn为负极,Fe为正极,可减缓船体的腐蚀速率,正确;C、电渗析法、离子交换法都可用于海水的淡化,错误;D、压缩天然气类主要成分是甲烷,液化石油气主要成分是丙烷、丙烯、丁烷、丁烯,燃烧时产生污染物较少,是我国城市推广使用的清洁燃料,正确。
第四节金属的电化学腐蚀与防护同步试题.doc
第四节金属的电化学腐蚀与防护同步试题一、选择题:1、埋在地下的铸铁输油管道,在下列各种情况下被腐蚀的速度最慢的是()A. 在含铁元素较多的酸性土壤中B. 在潮湿疏松透气的土壤中C. 在干燥致密不透气的土壤中D. 含碳粒较多、潮湿透气的中性土壤中2、以下现象与电化学腐蚀无关的是()A. 黄铜(铜锌合金)制作的铜锣不易产生铜绿B. 生铁比软铁芯(几乎是纯铁)容易生锈C. 铁制器件附有铜制配件,在接触处易生铁锈D. 银制奖牌久置后表面变暗3、为了防止钢铁锈蚀,下列防护方法中正确的是()A. 在精密机床的铁床上安装铜螺钉B. 在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中C. 在海轮舷上用铁丝系住锌板浸在海水里D. 在地下输油的铸铁管上接直流电源的负极4、将Al片和Cu片用导线相连,一组插入浓硝酸中,一组插入稀氢氧化钠溶液中,分别形成原电池,则在这两个原电池中,正极、负极分别为()A.Al片、Cu片B.Cu片、Al片C.Al片、Al片D.Cu片、Cu片5、白铁皮(镀锌)发生析氢腐蚀时,若有0.2mol电子发生转移,下列说法正确的是()A.有6.5g锌被腐蚀B.在标准状况下有22.4L氢气放出C.有2.8g铁被腐蚀D.在标准状况下有2.24L气体放出6、黄金首饰的纯度通常用“K”表示,24K是纯金,标号为18K的首饰中黄金的质量分数是()A.25%B.75%C.18%D.36%7、2000年5月,保利集团在香港拍卖会上花费3000多万港币购回在火烧圆明园时流失的国宝:铜铸的牛首、猴首和虎首。
普通铜器时间稍久容易出现铜绿,其主要成分:Cu2(OH)2CO3。
这三件1760年铜铸的国宝在240年后看上去仍然熠熠生辉不生锈,下列对其原因的分析,最可能的是()A.它们的表面都电镀上了一层耐腐蚀的黄金B.环境污染日趋严重,它们的表面的铜绿被酸雨溶解洗去C.铜的金属活动性比氢小,因此不易被氧化D.它们是含一定比例金、银、锡、锌的铜合金8、不小心将水银温度计摔破,水银微小颗粒掉在地上.为防止水银蒸气中毒,可在水银表面撒一层( )A.石灰B.砂土C.食盐D.硫磺9、人体内含有多种元素,其中许多元素是人体必需的,但有些元素尚未证实其生理功能,相反,在食品中它们的含量稍高就会引起毒性反应,食品卫生法对它们的最高标准有极严格的规定.这些元素是:①Na,②Mg,③As,④Cd,⑤Ca,⑥Zn,⑦Hg,⑧Pb,⑨Cu,⑩K中的( )A.③④⑦⑧B.①⑥⑦⑧⑨C.②④⑧⑨⑩D;②④⑥⑦⑨10、废旧电池集中处理的首要原因是()A.回收电池中的石墨电极B.回收电池外壳金属材料C.防止电池中汞、镉等重金属污染土壤和水源D.防止电池中的渗出液腐蚀其它物品11、近年来,科学家正在探索利用铝粉作燃料的可能性,以期铝能成为一种石油的取代物。
人教版化学选修4 第四章 第四节 金属的电化学腐蚀与防护
…○……__班级:___…○……绝密★启用前 高二人教版选修4 第四章 第四节 金属的电化学腐蚀与防护 试卷副标题 xxx 注意事项: 1.答题前填写好自己的姓名、班级、考号等信息2.请将答案正确填写在答题卡上 第I 卷(选择题) 请点击修改第I 卷的文字说明 一、单选题 1.下列关于金属的腐蚀及防腐说法错误的是 A .马口铁(镀锡铁)镀层破损铁的腐蚀速率加快 B .为了防止钢铁设备腐蚀,利用外加电流的阴极保护法,应另附加一惰性电极,惰性电极作阴极 C .可以采用改变金属组成或结构的方法防止金属腐蚀 D .为保护海轮的船壳,利用牺牲阳极的阴极保护法,常在船壳上镶入锌块 2.埋在地下的铸铁输油管道在下列各种情况下,被腐蚀的速率最慢的是 A . 在含铁元素较多的酸性土壤中 B . 在潮湿疏松的碱性土壤中 C . 在干燥致密不透气的土壤中 D . 在潮湿透气的中性土壤中 3.钢铁生锈过程发生如下反应: ①2Fe+O 2+2H 2O=2Fe(OH)2; ②4Fe(OH)2+O 2+2H 2O=4Fe(OH)3; ③2Fe(OH)3=Fe 2O 3+3H 2O 。
下列说法正确的是 A . 反应①、②中电子转移数目相等 B . 反应①中氧化剂是氧气和水 C . 与铜质水龙头连接处的钢质水管不易发生腐蚀………○………○…………※※请※※装※※订※※线※※内………○………○…………○………………装………订……_________姓名:________考号:___○………………装………订……下列说法正确的是 A . 随pH 的升高,碳钢腐蚀速率逐渐加快 B . pH<4,发生析氢腐蚀C . pH 为14,其负极反应为2H 2O+Fe-3e -=FeO 2-+4H +D . 在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会加快 9.下列与金属腐蚀有关的说法正确的是 A . 图a 中,插入海水中的铁棒越靠近底端腐蚀越严重 B . 图b 中,开关由M 改置于N 时,CuZn 合金的腐蚀速率减小 C . 图c 中,接通开关时Zn 腐蚀速率增大,Zn 上放出其他的速率也增大 D . 图d 中,Zn-MnO 2干电池自放电腐蚀主要是由MnO 2的氧化作用引起的 10.研究电化学腐蚀及防护的装置如图所示。
(人教版)化学选修四思维导图:4-4金属的电化学腐蚀与防护(含答案)
第四章电化学基础第四节金属的电化学腐蚀与防护【思维导图】【微试题】1.关于下列各装置图的叙述中,不正确的是()①②③④A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ C.装置③中钢闸门应与外接电源的负极相连 D.装置④中的铁钉几乎没被腐蚀【答案】B2.下列说法正确的是()A. 金属腐蚀就是金属原子失去电子被还原的过程B.钢铁吸氧腐蚀时,负极反应式为:2H2O+O2+4e- = 4OH-C.镀锌铁皮的镀层损坏后,铁更容易腐蚀D.氯碱工业中,阳极发生的反应为:2Cl--2e-=C12↑【答案】D3.(2012·海南高考·10)下列叙述错误的是( )A.生铁中含有碳,抗腐蚀能力比纯铁弱B.用锡焊接的铁质器件,焊接处易生锈C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液D.铁管上镶嵌锌块,铁管不易被腐蚀【答案】C4.(2014山东卷理综30.(16分))离子液体是一种室温熔融盐,为非水体系,由有机阳离子、Al2Cl7—和AlCl4—组成的离子液体作电解液时,可在钢制品上电镀铝。
(1)钢制品应接电源的极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为。
若改用AlCl3水溶液作电解液,则阴极产物为。
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还原产物的物质的量为mol。
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有。
a.KCl b. KClO3 c. MnO2 d. Mg取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,(填“能”或“不能”)说明固体混合物中无Fe2O3,理由是(用离子方程式说明)。
【答案】(1)负 4Al2Cl7—+3e-=Al+7AlCl4— H2 (2)3(3) b、d 不能 Fe2O3+6H+=2Fe3++3H2O 2Fe3++ Fe=3Fe2+(或只写Fe+ 2Fe3+ =3Fe2+)【解析】(1)在钢制品上电镀铝时,即钢制品为镀件,电镀时作为阴极(与电源的负极相连);在电镀时,阴极生成Al单质,所以电极反应为4Al2Cl7—+3e-=Al+7AlCl4—;电镀时若用AlCl3作为电解液,则由水电离出的H+也能在阴极放点生成H2;(2)用NaOH溶液溶解钢制品表面的铝镀层时,发生反应的方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,该反应的还原产物是H2。
高中化学 第04章 电化学基础 4.4 金属的电化学腐蚀与防护试题 选修4
第四节 金属的电化学腐蚀与防护一、金属的电化学腐蚀 1.金属腐蚀:(1)概念:金属与周围的__________________物质发生氧化还原反应而引起损耗的现象。
(2)本质:金属本身失去电子变成阳离子的过程(发生________反应):M −ne− Mn+ 。
(3)金属腐蚀的类型。
①化学腐蚀 金属跟接触到的_______________(如SO2、Cl2、O2等)或_______________液体(如石油) 等直接发生化学反应而引起的腐蚀。
②电化学腐蚀 不纯的金属与电解质溶液接触时,会发生________反应,比较活泼的金属失去电子被 ________的腐蚀。
电化学腐蚀比化学腐蚀更普遍,危害更大。
2.钢铁的电化学腐蚀: (1)腐蚀类型图 类型钢铁的析氢腐蚀示意图 析氢腐蚀发生条件水膜酸性较强正极反应 负极反应2H++2e− H2↑ Fe−2e− Fe2+钢铁的吸氧腐蚀示意吸氧腐蚀 水膜弱酸性、中性或碱性O2+2H2O+4e− 4OH− 2Fe−4e− 2Fe2+总反应Fe+2H+ Fe2++H2↑2Fe+O2+2H2O 2Fe(OH)2最 终 生 成 铁 锈 ( 主 要 成 分 为 Fe2O3•xH2O) , 反 应 如 下 : _______________________, 2Fe(OH)3 Fe2O3•xH2O+(3−x)H2O(2)钢铁的吸氧腐蚀实验 实验操作实验现象实验结论装置中铁、碳和饱和食盐水 导管中____________________,构成原电池,铁钉发生 铁钉表面有________生成________腐蚀二、金属的防护 1.金属的电化学防护:(1)牺牲阳极的阴极保护法:利用________原理,让被保护金属作________,另找一种 活泼性较强的金属作________。
如图所示:用实验验证牺牲阳极的阴极保护法: 实验名称验证牺牲阳极的阴极保护法实验装置实验原理 锌电极:Zn-2e- Zn2+; 铁电极:2H++2e- H2↑。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四节 金属的电化学腐蚀与防护(过关检测) 一、选择题(每小题4分,共48分) 1、下列说法中不正确的是( )
A、用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,如锌、锡、铬、镍等,能够减缓金属的
腐蚀( ) B、把铬、镍等加入普通钢里制成不锈钢,就大大地增加了钢铁对各种侵蚀的抵抗力( ) C、给铁件通入直流电,把铁件与电池负极相连接以防止铁腐蚀( ) D、制成合金后均比纯金属耐腐蚀( ) 2、钢铁发生吸氧腐蚀时,正极上发生的电极反应是( ) A.2H++2e-===H2↑ B.Fe2++2e-===Fe C.2H2O+O2+4e-===4OH- D.Fe3++e-===Fe2+ 3、下列防护措施中属于电化学保护法的是( ) A.用氧化剂使金属表面生成致密稳定的氧化物保护膜 B.在金属中加入一些铬或者镍制成合金 C.在轮船的船壳水线以下部分,装上一锌锭 D.在金属表面喷漆 4、糕点包装中常用的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是( ) A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 B.脱氧过程中铁作原电池正极,电极反应:Fe-3e-===Fe3+ C.脱氧过程中碳作原电池负极,电极反应:2H2O+O2+4e-===4OH- D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) 5、如图所示,各烧杯中盛有海水,铁在其中被腐蚀的速率由快到慢的顺序为( )
A.②①③④⑤⑥ B.⑤④③①②⑥ C.⑤④②①③⑥ D.⑤③②④①⑥ 6、一定条件下,碳钢腐蚀与溶液pH的关系如下,下列说法不正确的是( ) pH 2 4 6 6.5 8 13.5 14 腐蚀快慢 较快 慢 较快 主要产物 Fe2+ Fe3O4 Fe2O3 FeO-2
A.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e-===2H2O B.在pH<4溶液中,碳钢主要发生析氢腐蚀 C.在pH>6溶液中,碳钢主要发生吸氧腐蚀 D.在煮沸除氧气的碱性溶液中,碳钢腐蚀速率会减缓
7、.下列有关钢铁腐蚀与防护的说法正确的是( ) A.钢管与电源正极连接,钢管可被保护 B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀 C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀 D.钢铁发生析氢腐蚀时,负极反应是Fe-3e-===Fe3+ 8.下列关于金属腐蚀的叙述正确的是( )
A.金属被腐蚀的本质是M+nH2O===M(OH)n+n2H2↑ B.马口铁(镀锡铁)镀层破损后,首先是镀层被氧化 C.金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀 D.常温下,置于空气中的金属主要发生化学腐蚀 9我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均值为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下铁的腐蚀的叙述不正确的是( ) A.此腐蚀过程有化学腐蚀也有电化学腐蚀 B.发生电化学腐蚀时,正极反应式为2H2O+O2+4e-===4OH- C.在电化学腐蚀过程中有氢气产生 D.发生电化学腐蚀时,负极反应式为Fe-2e-===Fe2+
10、近年来,我国南方大面积持续降雪使得融雪剂需求量大。“化冰盐”氯盐类(氯化钠、氯化钙等)融雪剂,对钢轨设施的腐蚀如图所示。下列有关说法中不正确的是( )
A.正极电极反应式为:2H++2e-===H2↑ B.此过程中还涉及反应:4Fe(OH)2+2H2O+O2===4Fe(OH)3 C.此过程为吸氧腐蚀原理 D.此过程中电子从Fe移向C 11、.铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图所示,下列说法正确的是( )
A.阳极电极反应式为2Al-6e-+6OH-===Al2O3+3H2O B.随着电解的进行,溶液的pH逐渐增大 C.当阴极生成气体3.36L(标准状况)时,阳极增重2.4g D.电解过程中H+移向铝电极
12、研究电化学腐蚀及防护的装置如下图所示。下列有关说法错误的是( )
A.d为石墨,铁片腐蚀加快 B.d为石墨,石墨上电极反应为O2+2H2O+4e-===4OH- C.d为锌块,铁片不易被腐蚀 D.d为锌块,铁片上电极反应为2H++2e-===H2↑
二、非选择(共52分) 13(14分)实验探究(如图所示)
(1)若棉团浸有NH4Cl溶液,铁钉发生________腐蚀,正极反应式为____________________,右试管中现象是______________。 (2)若棉团浸有NaCl溶液,铁钉发生________腐蚀,正极反应式为_____________________,右试管中现象是____________________________________________________________。
14(14分)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。 (1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为____________________________________________________________。 (2)为了降低某水库的铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在铁闸门上的固体材料R可以采用________。
A.铜 B.钠 C.锌 D.石墨 (3)如乙图所示方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________极上。
15(14分)某研究小组对铁生锈进行研究。
(1)甲同学设计了A、B、C一组实验(如上图),探究铁生锈的条件。经过较长时间后,甲同学观察到的现象是A中铁钉生锈;B中铁钉不生锈;C中铁钉不生锈。 ①通过上述实验现象分析,可得出铁生锈的外部条件是 ____________________________________________________________。 ②铁钉发生电化学腐蚀的正极电极反应式为____________________________________________________________ ____________________________________________________________。 ③实验B所用的水要经过____________________处理。植物油的作用是____________________________________________________________。 ④实验C中碱石灰的作用是________________________________________。 (2)乙同学为了达到同样目的,设计了实验D(如图),发现一段时间后,试管中的液面升高,其原因是________,该实验__________(填“能”或“不能”)说明水对铁钉生锈产生影响。 16、(14分)某实验小组欲探究牺牲阳极的阴极保护法的原理,设计如图实验装置: 实验Ⅰ:向烧杯中加入一定量的饱和食盐水,插入两个无底玻璃筒。将一根锌棒和一根铁棒用导线与电流计连接后,再分别插入两个玻璃筒中,电流表指针发生偏转。 (1)锌棒上发生的电极反应为_____________________________________; 铁棒上发生的电极反应为_______________________________________。 (2)向铁棒附近滴加K3[Fe(CN)6]溶液,无明显现象,这说明该实验中无________产生。 实验Ⅱ:该小组的同学将锌棒换为铜棒,并用导线将其与电流表连接。一段时间后,向插入铁棒的玻璃筒内滴入几滴K3[Fe(CN)6]溶液,向插入铜棒的玻璃筒内滴入几滴酚酞溶液。 (3)实验Ⅱ中电流计指针的偏转方向与实验Ⅰ________(填“相同”或“相反”)。 (4)在铁棒和铜棒附近可观察到的现象分别是____________________________________________________________、 ____________________________________________________________。 (5)上述两个实验表明,活泼性不同的两种金属作电极构成原电池时,一般是相对________(填“活泼”或“不活泼”)的金属被保护,根据此原理采取的金属防护方法称为____________________________________________________________ ____________________________________________________________。
第四节 金属的电化学腐蚀与防护(过关检测) 一、选择题(每小题4分,共48分) 1、下列说法中不正确的是( )
A、用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,如锌、锡、铬、镍等,能够减缓金属的
腐蚀( ) B、把铬、镍等加入普通钢里制成不锈钢,就大大地增加了钢铁对各种侵蚀的抵抗力( ) C、给铁件通入直流电,把铁件与电池负极相连接以防止铁腐蚀( ) D、制成合金后均比纯金属耐腐蚀( ) 答案:D 2、钢铁发生吸氧腐蚀时,正极上发生的电极反应是( )
A.2H++2e-===H2↑ B.Fe2++2e-===Fe
