温度对电沉积氢氧化镍电化学性能的影响
氢氧化镍三价沉淀颜色

氢氧化镍三价沉淀颜色1. 介绍氢氧化镍三价是一种无机化合物,化学式为Ni(OH)3。
它在化学实验中常用作沉淀剂,具有独特的颜色。
本文将详细讨论氢氧化镍三价沉淀的颜色以及相关的化学原理和应用。
2. 氢氧化镍三价的颜色氢氧化镍三价沉淀的颜色可以因多种因素而有所不同,主要取决于沉淀中存在的金属离子、pH值和其他配体的影响。
2.1 氢氧化镍三价的基本颜色一般情况下,氢氧化镍三价沉淀呈现出深蓝色或深绿色。
这种颜色是由于镍离子在氢氧化物配体的影响下形成了配位化合物。
2.2 pOH值对颜色的影响pOH值也会对氢氧化镍三价沉淀的颜色产生影响。
在较高的pOH值下,沉淀通常呈现出绿色,而在较低的pOH值下,沉淀可能呈现出蓝色。
这是因为pOH值的变化会改变氢氧化物配体与金属离子的配位方式。
2.3 其他配体的影响除了pOH值之外,其他配体的存在也可能影响氢氧化镍三价沉淀的颜色。
例如,某些配体可以使沉淀呈现出不同的色调或导致沉淀溶解。
3. 氢氧化镍三价的制备方法氢氧化镍三价可通过多种方法制备,如下所示:3.1 反应方程式首先,镍离子与氢氧化物配体发生反应,生成氢氧化镍沉淀: Ni2+ + 2OH- ->Ni(OH)2然后,通过在碱性条件下氧化氢氧化镍沉淀,可以得到氢氧化镍三价沉淀:2Ni(OH)2 + O2 + 2H2O -> 2Ni(OH)33.2 实验操作在实验室中,氢氧化镍三价沉淀可以通过向含有镍离子的溶液中加入氢氧化物配体来制备。
重要的是控制反应条件,如温度和pH值,以确保得到纯净的氢氧化镍三价沉淀。
4. 氢氧化镍三价的应用氢氧化镍三价沉淀在化学实验和工业生产中有许多应用。
4.1 作为沉淀剂氢氧化镍三价沉淀常用作沉淀剂,可用于分离和鉴定其他金属离子。
其特殊的颜色可用于确定金属离子的存在以及鉴定化合物的性质。
4.2 作为催化剂氢氧化镍三价沉淀也可以作为催化剂。
其表面具有较高的活性,对于某些有机化合物的加氢反应具有催化作用。
粗制氢氧化镍钴(mhp)成分

粗制氢氧化镍钴(MHP)成分概述在材料科学领域,粗制氢氧化镍钴(M HP)是一种重要的化学物质。
它由镍和钴的氢氧化物组成,具有多种应用领域。
本文将深入探讨M HP的成分、性质以及其在能源存储和催化领域的应用。
成分M H P由镍和钴的氢氧化物组成,化学式为N iC o(OH)2。
该化合物是一种层状晶体结构的金属氢氧化物,含有镍、钴和氧的元素。
其化学成分对其性质和应用具有重要影响。
性质层状结构-:M HP具有层状结构,是由一层层镍、钴和氧原子组成的。
这种结构赋予了M HP独特的电化学性质和催化活性。
可控性-:M HP的成分可以通过化学合成方法进行调控,例如不同的沉积时间和温度可以影响镍和钴的比例和分布,从而调节MH P的性质。
电化学性能-:M HP具有良好的电化学性能,可用于储能设备和催化反应中。
它具有较高的电导率、电化学稳定性和可逆的电化学反应。
催化活性-:M HP在催化领域具有广泛的应用。
由于其特殊的结构和成分,MH P表现出优异的催化活性,可用于水分解、氧还原反应和其他重要的电化学过程。
应用能源存储M H P作为一种重要的电化学材料,在能源存储领域具有广泛的应用。
它可以用作电池正极材料,在锂离子电池和镍氢电池中发挥重要作用。
M H P的层状结构和优良电导率有助于提高电池的能量密度和循环稳定性。
催化剂由于其良好的催化活性,MH P被广泛应用于催化反应中。
它可以用作氧还原反应(OR R)的催化剂,O RR是燃料电池和金属-空气电池等能源领域的重要反应。
此外,MH P在其他电化学反应中,如水分解和甲醇氧化等方面也显示出出色的催化性能。
结论粗制氢氧化镍钴(MH P)是一种成分为镍和钴的氢氧化物,具有层状结构和优异的电化学性质。
它在能源存储和催化领域具有重要应用,可以用作电池正极材料和催化剂。
M HP的独特成分和结构为其在能源转换和储存技术方面的应用提供了新的可能性。
随着技术的不断发展,MH P在能源科学领域的应用前景也将不断扩大。
电沉积镍(电流密度)

学号14091700375题目:镍电沉积实验作者XX级别2009 级系别化学化工专业化学师范指导教师XXX完成时间2012 年6 月1日创新性实验——镍电沉积实验摘要:电沉积镍的效果与溶液中镍离子的浓度、添加剂与缓冲剂的种类和浓度、pH、温度及所使用的电流密度、搅拌情况等因素有关。
本实验通过研究5~10 A/dm2电流密度范围内的电流效率,发现当电流密度为8.3 A/dm2左右时,电沉积镍的电流效率最高,达到66.9%。
关键词:电沉积镍;电流密度;电流效率AbstractElectrodeposition of nickel depend on the nickel ion concentration in the solution, the type and concentration of additives and buffer, pH, temperature and the use of current density, agitation and other factors. Through the study of 5~10 A/dm2 current density within the current efficiency, found that when the current density is about 8.3A/dm2, nickel electrodeposition current efficiency is the highest, reaching 66.9%. Keywords:Electrodeposition of nickel;Current density;Current efficiency前言电沉积镍,可以改变基底表面的特性,改善基底材料的外观、耐腐蚀性和耐磨损性。
电沉积镍过程的主要反应为:阴极:Ni 2+ + 2e = Ni 阳极:Ni +2e = Ni2+溶液中镍离子的浓度、添加剂与缓冲剂的种类和浓度、pH、温度及所使用的电流密度、搅拌情况等都能够影响电沉积的效果。
氢氧化镍形貌

氢氧化镍形貌氢氧化镍,化学式为Ni(OH)2,是一种重要的无机化合物。
它的形貌在材料科学中具有重要的研究价值。
本文将从氢氧化镍的形貌特征、制备方法、应用领域等方面展开阐述。
氢氧化镍的形貌特征是指其在微观尺度上的外部形状和结构。
氢氧化镍可以呈现出多种形貌,如纳米片状、纳米棒状、纳米颗粒状等。
这些形貌的差异主要来源于制备方法和条件的不同。
例如,采用不同的沉淀剂、溶剂和温度等因素,可以控制氢氧化镍的晶型、晶粒大小和形状。
通过调控这些因素,可以制备出具有特定形貌的氢氧化镍,进而赋予其特定的物理和化学性质。
氢氧化镍的制备方法多种多样,常见的方法包括沉淀法、水热法、电化学沉积法等。
沉淀法是一种常用的制备方法,通过将适量的镍盐与碱溶液反应,产生氢氧化镍沉淀。
水热法则是在高温高压的条件下,将适量的镍盐和碱溶液混合,通过水热反应形成氢氧化镍。
电化学沉积法是利用电化学原理,在电解液中施加电压,将镍阳极溶解并在阴极上沉积成氢氧化镍。
这些方法各有优劣,可以根据需求选择合适的制备方法。
氢氧化镍具有广泛的应用领域。
首先,由于其优异的电化学性能,氢氧化镍常被用作电化学储能器件中的重要电极材料。
以纳米片状的氢氧化镍为例,其具有较大的比表面积和较短的电子和离子传输路径,能够提高电极的反应活性和储能性能。
其次,氢氧化镍还可以用于催化剂、吸附剂、光催化剂等领域。
例如,纳米棒状的氢氧化镍可以作为催化剂用于有机合成反应中,提高反应速率和选择性。
此外,氢氧化镍还具有一定的光催化性能,可用于光催化水分解产氢等领域。
总结起来,氢氧化镍的形貌在材料科学中具有重要的研究价值。
通过控制制备方法和条件,可以制备出具有特定形貌的氢氧化镍。
其形貌特征对其物理和化学性质有重要影响,进而影响其在各个应用领域的性能。
未来,随着科技的不断发展,相信氢氧化镍的形貌研究将会有更多的突破和应用。
氢氧化镍生产三氧化二镍的温度

氢氧化镍生产三氧化二镍的温度氢氧化镍(Ni(OH)2)是一种无机化合物,是镍的氢氧化物。
它是一种淡绿色的固体,广泛应用于电池、催化剂、涂料等领域。
三氧化二镍(Ni2O3)作为氢氧化镍的产物,它的形成温度可以通过热分解反应得到。
热分解反应是指由于给定化合物的高温热分解产物而发生的反应。
对于氢氧化镍,其热分解反应方程式为:2 Ni(OH)2 → Ni2O3 + 3 H2O根据这个反应方程式,我们可以看到,氢氧化镍在高温下分解生成三氧化二镍和水。
那么,温度对于这个反应的进行起着重要的作用。
实际上,在研究过程中,温度是一个非常重要的因素。
温度可以显著地影响反应速率、平衡常数和反应产物。
因此,为了获得高纯度和高产率的三氧化二镍,研究者需要探索最适宜的温度条件。
根据相关的文献研究,氢氧化镍在不同温度下的分解反应速率和产物形成情况存在差异。
其中,一项研究发现,在氢氧化镍的分解反应中,温度从400℃上升到600℃时,反应速率显著增加。
此外,随着温度的继续上升,反应速率也随之增加。
因此,可以推测在高温条件下,氢氧化镍的分解反应速率会进一步提高。
另外一项研究表明,在氢氧化镍的热分解反应中,温度对于产物的形成也有显著影响。
随着温度的升高,三氧化二镍的产率会增加。
但是,当温度超过一定阈值时,产物的产率将开始下降。
这可能是因为在高温下,氧化镍(NiO)的形成速率增加,从而减少了三氧化二镍的生成。
总的来说,根据目前的研究结果,可以初步得出结论:在温度范围内,氢氧化镍的分解反应速率和三氧化二镍的产率随温度的升高而增加。
然而,温度超过一定阈值后,产物的产率将开始下降。
当然,这只是初步的研究结果,并不能代表所有情况。
未来仍需要更多的实验和研究来探究氢氧化镍热分解反应的温度条件。
另外,影响温度对于反应过程的影响还有其他因素,例如反应时间、反应系统的气氛等等。
通过综合考虑这些因素,我们可以更好地确定氢氧化镍生产三氧化二镍的最佳温度条件。
pem电解水制氢 温度

pem电解水制氢温度温度对于pem电解水制氢的影响引言:随着全球对可再生能源的需求不断增加,氢能作为一种理想的清洁能源备受关注。
而pem电解水制氢作为一种高效、环保的制氢方法,被广泛研究和应用。
然而,温度作为pem电解水制氢过程中的重要参数,对于制氢效率和产氢速率有着显著影响。
本文将从温度的角度探讨pem电解水制氢的相关问题。
一、温度对pem电解水制氢效率的影响1.1 温度对电解电压的影响在pem电解水制氢过程中,温度对电解电压有着直接影响。
一般来说,随着温度的升高,电解电压会降低。
这是因为在高温条件下,电解质膜的离子迁移速率加快,电解电压降低。
因此,提高温度可以降低电解电压,提高制氢效率。
1.2 温度对电解质膜的稳定性的影响温度对电解质膜的稳定性也有着重要影响。
在pem电解水制氢过程中,高温会使电解质膜发生膨胀、变形等问题,导致膜的性能下降,甚至失效。
因此,选择合适的温度范围是确保电解质膜稳定工作的关键。
二、温度对pem电解水制氢速率的影响2.1 温度对电解反应速率的影响温度对电解反应速率有着显著影响。
一般来说,随着温度的升高,电解反应速率会增加。
这是因为在高温条件下,电解质膜中的水分子活化能降低,离子迁移速率加快,电解反应速率增加。
因此,提高温度可以提高pem电解水制氢的速率。
2.2 温度对水的溶解度的影响温度对水的溶解度也有一定影响。
在pem电解水制氢过程中,高温会降低水的溶解度,从而减少电解质膜中的水含量。
而水的含量直接影响着氢气的产生速率。
因此,选择适当的温度可以调节水的溶解度,进而影响氢气的产生速率。
三、温度对pem电解水制氢的优化选择为了实现高效、稳定的pem电解水制氢,需要选择合适的温度。
一般而言,温度应该在一定范围内进行优化选择。
过低的温度会导致电解反应速率较慢,影响制氢效率;过高的温度则会引起电解质膜的失效,降低制氢稳定性。
因此,根据具体应用需求,需要在综合考虑制氢效率和稳定性的基础上选择合适的温度。
氢氧化镍沉淀ph

氢氧化镍沉淀ph氢氧化镍沉淀pH氢氧化镍是一种常见的无机化合物,具有广泛的应用领域。
在化学实验室中,我们通常使用氢氧化镍来调节溶液的pH值。
pH值是一个用来表示溶液酸碱性强弱的指标,其数值范围从0到14,其中7表示中性。
在调节溶液pH值的过程中,我们需要了解氢氧化镍的性质以及其与水的反应。
氢氧化镍是一种碱性物质,能够与水反应生成氢氧化镍溶液。
这个反应的化学方程式如下所示:Ni(OH)2 + H2O → Ni(OH)2(aq)根据这个方程式,我们可以看出氢氧化镍在水中完全离解,生成了Ni2+和OH-离子。
这些离子会影响溶液的pH值。
当我们将氢氧化镍加入到酸性溶液中时,溶液的pH值会增加。
这是因为氢氧化镍溶液中的OH-离子能够与溶液中的H+离子反应,生成水分子。
这个反应会导致溶液中H+离子的浓度减少,从而使溶液的酸性减弱,pH值增加。
相反,如果我们将氢氧化镍加入到碱性溶液中,溶液的pH值会减少。
这是因为溶液中的OH-离子与氢氧化镍溶液中的Ni2+离子反应,生成沉淀。
这个反应会导致溶液中OH-离子的浓度减少,从而使溶液的碱性减弱,pH值减少。
通过控制氢氧化镍的用量,我们可以精确地调节溶液的pH值。
例如,如果我们想要将酸性溶液中的pH值提高到中性,我们可以逐渐加入适量的氢氧化镍溶液,直到溶液的pH值达到7。
同样地,如果我们想要将碱性溶液中的pH值降低到中性,我们可以逐渐加入适量的酸性溶液,直到溶液的pH值达到7。
除了在实验室中调节溶液的pH值外,氢氧化镍还具有其他重要的应用。
例如,在电化学领域,氢氧化镍可用作催化剂,用于促进氧化还原反应。
此外,氢氧化镍还可用于生产金属镍、石墨烯等材料,具有重要的工业价值。
氢氧化镍沉淀pH是一种常见的化学实验现象。
通过控制氢氧化镍的用量,我们可以精确地调节溶液的pH值。
这个过程中,氢氧化镍与水反应生成Ni2+和OH-离子,影响溶液的酸碱性。
氢氧化镍不仅在实验室中有广泛的应用,还在电化学和材料科学领域具有重要的价值。
镍氢(镍镉)电池的特性e及曲线分析总括
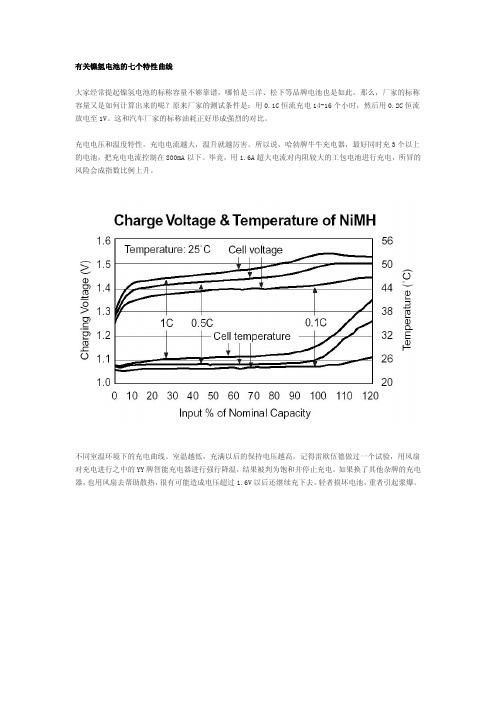
有关镍氢电池的七个特性曲线大家经常提起镍氢电池的标称容量不够靠谱,哪怕是三洋、松下等品牌电池也是如此。
那么,厂家的标称容量又是如何计算出来的呢?原来厂家的测试条件是:用0.1C恒流充电14-16个小时,然后用0.2C恒流放电至1V。
这和汽车厂家的标称油耗正好形成强烈的对比。
充电电压和温度特性。
充电电流越大,温升就越厉害。
所以说,哈勃牌牛牛充电器,最好同时充3个以上的电池,把充电电流控制在800mA以下。
毕竟,用1.6A超大电流对内阻较大的工包电池进行充电,所冒的风险会成指数比例上升。
不同室温环境下的充电曲线。
室温越低,充满以后的保持电压越高。
记得雷欧伍德做过一个试验,用风扇对充电进行之中的YY牌智能充电器进行强行降温,结果被判为饱和并停止充电。
如果换了其他杂牌的充电器,也用风扇去帮助散热,很有可能造成电压超过1.6V以后还继续充下去,轻者损坏电池,重者引起浆爆。
充电温度与效率。
摄氏27度左右,充电最饱和,充/放电效率最高。
放电容量与放电电流的关系。
0.2C小电流放电,比1C大电流放电,最终放电容量能多出10%左右。
放电容量与环境温度的关系。
用1C电流放电,环境温度为摄氏50度时候的放电容量,比环境温度为摄氏0度时候的放电容量,竟然要高出20%左右。
电池的存贮特性。
镍氢电池的自放电性能要好于镍铬电池,但是比锂电池还是要差一些。
质量再好的镍氢电池,充满以后在常温下搁置三个月,容量基本都会减少30%以上。
如果放进冰箱冷藏,那么即使搁置200天,也还有90%左右的容量。
如何提高镍氢电池的寿命(循环次数)?没有其他法宝,只有避免深度放电(过放电,放电电压低于1V)。
这一方面,DE1103的欠压保护做的很好,可惜是个电老虎。
另外,反向充电会极大地损害电池的寿命。
学而时习之,不亦晕乎?镍氢及镍镉特性曲线2009-04-16 10:20镍氢及镍镉特性曲线1、充 电建议用0.1C标准充电5小时或1C快速充电1.2-1.5小时,快充时,建议使用有终止电压控制开关或温度感应器的充电器,以保护电池。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第嘴绷0基燃VbIl26No.4
温度对电沉积氢氧化镍电化学性能的影响薛雷,王为(天津大学化工学院应用化学系,天津300072)摘要:在0.1mol/L的Ni(N03)2溶液中,采用电化学沉积法制
备出适用于锌镍微电池的氢氧化镍电极,研究了电沉积温度对Ni(OH)2电极的电化学循环伏安性能以及充放电性能的影响。测试结果表明,电沉积方法制备的Ni(OH):电极适合于微电池的制作。30oc下电沉积制备的Ni(OH)2电极具有优异的电化学}生能,其质子扩散系数为7.71×10J2cm2/s,放电比容量为1285pAh/cm2,
利用率达91.4%。
关键词:电沉积;氢氧化镍;电化学中图分类号:TM91l文献标识码:A文章编号:1004—227X(2007)04—0008—03Effectofelectrodepositiontemperature
on
electrochemical
performanceofNi(OH)2∥XUELei,W-ANG
W萌
Abstract:ANi(OH),electrode
usedforNi_Zimicrobatterywaspreparedbyelectrodepositionfroma0.1mol/LNi(N03)2solution.Theeffectofelectrodepositiontemperatureoncyclicvolmmmetryandcharge—dischargecapacityoftheelectrodewasstudied.ElectrodepositedNi(OH),iSsuitableformanufacturingZn—Nimicrobatteries.Ni(OH),depositedat30oCshowedgoodelectrochemicalperformance(protondiffusioncoefficient7.71×10“2cm2/s.specificdischargecapacityl285I.tAh/cm2andutilizationrate91.4%1.Keywords:electrodeposition;nickelhydroxide;electrochemislryFirst-author’saddress:DepartmentofAppliedChemistry,SchoolofChemicalEngineeringandTechnology,TianjinUniversity,Tianjin300072,Chinal前言氢氧化镍作为电池的正极活性物质应用于微电池已有报道【l七】。目前氢氧化镍的合成方法主要有:化学沉淀法、微乳液法、沉淀转化法、均匀络合共沉淀法、氧化法、电化学沉积法、离子交换树脂法等【3]。采用粉末氢氧化镍制作粘接性电极的工艺复杂,且不适用于收稿日期:20064)8—29修回日期:2006-09—18作者简介:薛雷(1982一),男,河北衡水人,在读研究生。作者联系方式:(Email)xuelei323@hotmail.com。·∥微电池。为了简化制造工艺,研究了采用电化学沉积法在微电池的正极集流体上直接制备氢氧化镍电极材料的技术,一次性制备出了氢氧化镍电极,并研究了不同温度下电沉积氢氧化镍电极的循环伏安特性以及充放电性能。2实验部分2.1材料的制备电解液采用0.1mol/L的Ni(N03)2溶液,以大面积高纯镍板作阳极,包含50个微区的镍基体为阴极(微区尺寸1000I.tm×1
000哪)。以10mA/cm2进行直
流电沉积,沉积时间15min,沉积温度分别为10。C,15。C,20oC,25。C,30oC,35oC,40oC,45oC,50。C。2.2循环伏安性能测试采用上海辰华CHl660B电化学工作站测试电极的循环伏安性能。测试体系为三电极两回路体系,研究电极为电沉积制备的包含50个微区的Ni(OH)2电极(以下简称微区Ni(OH)2电极),总面积O.5cm2,参比电极为Hg/HgO电极,辅助电极为铂网,电解液为6mol}LKOH+1mol/LLiOH溶液,扫描范围0.2~0.5V,测试温度25oC。
2.3充放电性能测试
充放电性能测试体系同2.2节。将电沉积制备的微区Ni(OH)2电极在6mol/LKOH+lmolTLLiOH电解液
中以2mV/s进行循环伏安扫描,扫描至稳定后,先以10C充电400S,静置50S后,再以10C放电至0V,
记录充放电曲线。2.4真实表面积的测定真实表面积测试体系同2.2节。采用恒电位阶跃法,阶跃幅值为5mV,通过测定电流一时间曲线计算出电极的电容值,并与标准微分电容值CN=20pF/cm2
比较,计算出电极的真实表面积。
万方数据3结果与讨论3.1沉积温度对材料循环伏安性能的影响对在不同温度下电沉积制备的微区Ni(OH)2电极进行了循环伏安测试,图l为扫描速度为1mV/s时测得的循环伏安曲线。由图1可知,不同电沉积温度下制备的微区Ni(OH)2电极的循环伏安曲线形状大致相同,存在明显的氧化峰和还原峰,且均为单峰。随着扫描电位的逐渐提高,阳极过程开始有析氧峰出现。
图l不同温度下电沉积制备的Ni(OH)z电极的循环伏安曲线(扫描速度1mV/s)
Figure1Cyclic
voltammetriccurvesofNi(OH)2electrodes
depositedatdifferenttemperatures(scanningrate1mV/s)
阴、阳极峰对应的反应可表示为:Ni(OH):+OH+焉㈣极放电xNiOOH+H:O+e(1)
说明电极反应是在Ni(OH)2/NiOOH之间进行。不同温度下制备的微区Ni(OH)2电极的氧化峰电位妒。与还原峰电位妒。及其差值△妒。,。列于表l。△妒。.。均大于59mV,约为120mV,这说明与反应(1)对应的氧化还原过程处于准可逆状态。由表1可以看出,
沉积温度对材料的妒。、妒。及△妒。,。的影响不大。表1沉积温度对Ni(OH)2的妒。,妒。和A妒。,。的影响Table1Effectofdepositiontemperatureon
妒a,伊candA妒_,cofNi(OH)2
3.2电沉积温度对Ni(OH)2质子扩散系数的影响质子扩散系数是Ni(OH)2电极反应动力学的重要参数。采用循环伏安法测定阳极过程的质子扩散系数。循环伏安峰电流与质子扩散系数存在如下关系【4]:L=2.69×105n3/2A(D.1,)"Co(2)
式中厶为电流峰值(A),”为电子转移数,A为电极面积(cm2),D为质子扩散系数(cm2/s),v为扫描速率(V/s),Co为反应物浓度(mol/cm3)。
Co=Mp(3)
式中P为Ni(OH)2的理论密度(g/cm3),M为Ni(OH)2的摩尔质量(g/m01)。30oC下电沉积制备的Ni(OH)2电极在不同扫描速
度下测得的循环伏安曲线如图2所示。随着扫描速度的增大,阴、阳极峰的电流值也随之增大,但基本形状不变。以图2的阳极峰电流密度对v¨2作图,根据所得直线的斜率,由公式(2)可计算出材料的质子扩散系数D为7.7l×10。2cmZ/s。
g.o.002≥0.000邑o
、0
图2300C下电沉积的Ni(OH)2在不同扫速下的循环伏安曲线Figure2CyclicvoltammetriccurvesofNi(OH)2electrodeat
differentscanningrates(deposition
temperature
30oc)
将其它温度下电沉积制备的微区Ni(OH)2电极的循环伏安曲线按上述方法进行处理,计算得到的质子
乡 万方数据扩散系数列于表2。随着电沉积温度的升高,Ni(OH)2电极的质子扩散系数先增后减。30oC下制得的Ni(OH)2的质子扩散系数最大,而10oC下制得的Ni(OH)2的质子扩散系数最小。表2沉积温度对Ni(olI)2质子扩散系数的影响Table2EffectofdepositiontemperatureOHprotondiffusioncoefficientofNi(OH)2厌沉积)/oC101520253035404550D/(x10"’2cm2/s)0.6464.004.455.407.715.793.643.373.343.3Ni(OH)2电极的充放电性能由于微锌镍电池主要工作在大电流场合,因此微区Ni(OH)2电极的大电流放电性能是其主要的电化学性能参数。图3为30。c下电沉积制备的Ni(OH)2电极的10C充放电曲线。充放电反应过程可用式(1)表示。由于采用大电流充放电,充电过程中电极电压上升很快,并在0.60v处出现析氧电压平台;而放电平台也很明显,出现在0.32V左右。图3Ni(o玛2的10C恒电流充放电曲线Figure3Charge-dischargecurveofNi(OH)2electrodeat10C在本文的制备条件下,可认为Ni(OH)2的电沉积效率为100%[51。由法拉第定律:矗=nZF(4)式中,为制备时的电极电流(A),t为通电时间(s),Z为制备反应的摩尔电子得失数(16/9),F为法拉第常数。计算出沉积量n为0.0524mmol/cm2。根据公式:C=HF/3.6(5)计算出电极的理论比容量为1406¨Ah/cm2,理论容量为703叫址。测试了不同温度下制备的微区Ni(OH)2电极在6moFLKoH+lmoFLLi0H电解液中的10C恒电流充放电曲线。不同温度下制备的微区Ni(OH)2电极的放电容量、比容量及利用率列于表3。随着温度的升高,电极的容量呈现先增大后减小的趋势,这与质子扩散系数的变化趋势是一致的。普遍认为Ni(OH)2的电化学反应过程受固相质子扩散控带lJt6"7]。质子扩散系数的增大,有利于提高Ni(OH)2在氧化还原过程中的利用率,从而提高Ni(OH)2电极的充放电性能。30。C下制得的电极的质子扩散系数最大,且该温度下制备的微区Ni(OH)2电极的放电容量也较大(642.5衅h),比容量为1285∥州cm2,利用
率达91.4%。上述结果表明,控制适当的制备温度,可制备出电化学性能很好的微区Ni(OH)2电极。表3电极的放电容量、比容量及利用率Table3Dischargecapacities,specificcapacitiesandutilizationratesofNi(OH)2electrodesdepositedatdifferenttemperatures
电极性能————————————!堕堕堕璺三——————————一101520253035404550
容量/rtAh556.5580.0638.6619.0642.5580.0589.7570.2580.0
