《国际药事法规》知识点整理
药事法规(高频考点)

Top1:药品不良反响报告主体、报告围【具体容】法定报告主体:药品生产企业〔包括进口药品的境外制药厂商〕、经营企业和医疗机构是我国药品不良反响报告制度的法定报告主体。
我国药品不良反响的报告围是:新药监测期的国产药品或首次获准进口5年以的进口药品,报告所有不良反响;其他国产药品和首次获准进口5年以上的进口药品,报告新的和严重的不良反响。
Top2:零售药店不得经营的九大类药品【具体容】零售药店不得经营的九大类药品:麻醉药品、放射性药品、一类精神药品、终止妊娠药品、蛋白同化制剂、肽类激素〔胰岛素除外〕、药品类易制毒化学品、疫苗、以及我国法律法规规定的其他药品零售企业不得经营的药品。
Top3:零售药店必须凭处方销售的十大类药品【具体容】零售药店必须凭处方销售的十大类药品:注射剂、医疗用毒性药品、二类精神药品、九大类药店不得经营的药品以外其他按兴奋剂管理的药品、精神障碍治疗药〔抗精神病、抗焦虑、抗躁狂、抗抑郁药〕、抗病毒药〔逆转录酶抑制剂和蛋白酶抑制剂广〕、肿瘤治疗药、含麻醉药品的复方口服溶液和曲马多制剂、未列入非处方药目录的抗菌药和激素、以及国家药品监视管理部门公布的其他必须凭处方销售的药品。
Top4:药师对处方用药适宜性审核的容【具体容】药师应当对处方用药适宜性进展规定必须做皮试的药品,处方医师是否注明过敏试验及结果的判定;处方用药与临床诊断的相符性;剂量、用法的正确性;选用剂型与给药途径的合理性;是否有重复给药现象;是否有潜在临床意义的药物相互作用和配伍禁忌;其他用药不适宜情况。
药师经处方审核后,认为存在用药不适宜时,应当告知处方医师,请其确认或者重新开具处方。
具体包括:对有配伍禁忌或者超剂量的处方,应当拒绝调配;必要时,经处方医师更正或者重新签字,方可调配。
对有严重不合理用药或者用药错误,应当拒绝调剂,及时告知处方医师,并应当记录。
Top5:互联网药品交易效劳的定义及类型【具体容】互联网药品交易效劳分为三类:第一类是为药品生产企业、药品经营企业和医疗机构之间的互联网药品交易提供的效劳;第二类为药品生产企业、药品批发企业通过自身与本企业成员之外的其他企业进展的互联网药品交易;第三类为向个人消费者提供的互联网药品交易效劳。
药事法规记忆

法规简化记忆小结一:麻精药品简化记忆:麻醉药品:一嗪酊:布桂嗪、复方樟脑酊二阿罂:罂粟壳、罂粟秆浓缩物、阿桔片、阿片。
三酮定:美沙酮、氢可酮、羟考酮、哌替定、阿法罗定、福尔可定四啡因:吗啡、乙基吗啡、吗啡阿托品、二氢埃托啡、可待因、双氢可待因、可卡因、蒂巴因五芬三太尼:地芬诺酯、右丙氧芬、乙芬太尼、瑞芬太尼、舒芬太尼精一药品:司马三酯丁酮酸:司可巴比妥、巴吲哚、三唑仑、哌醋甲酯、丁丙诺啡 R羟丁酸、氯胺酮精二药品:咖啡因、西泮类、唑仑类〔三唑仑精一除外〕巴比妥类〔司可巴比妥精一〕氨酚氢可酮片〔注意和麻醉药中的氢可酮区分〕二:国家重点保护野生药材名称: 1:一级保护药材名称:两个骨头两个角:虎骨、豹骨、羚羊角、梅花鹿〔药用也是角〕2:二级保护药材名称:一马甘草射蟾酥:马鹿、甘草、射香、蟾酥二黄双蛤穿厚杜:黄连、黄柏、蛤蟆油、蛤蚧、穿山甲、厚朴、杜仲三蛇熊人血:白花蛇、乌梢蛇、蕲蛇、熊胆、人参、血蝎三级:用排除法,记着了一二级的,三级自然不会太难记了。
黄芩、胡黄连注意和二级的区分。
三:麻精处分:麻精一: 1:原植物、定点生产、现金交易:5W—10W2:定点批发:原料药2—5倍、其他2W---5W3:精二5000—2W 4:印鉴卡:5000---1W5:被盗抢丧失:5000---1W 四:其他处分:1:非法经营:1—5倍 2:假劣药:假2—5倍,劣1—3倍,50%-2倍3:提供假劣药运输:50%--3倍 4:骗取得证:5年以下,1W—3W 5:出租借用证:2W—10W" 6:贿赂工商罚:1W---20W7:生产不符医疗器械卫生处:5年以下,后果特别严重5年—10年, 五:干净级别:百级:1大容针 2不需除菌3注射剂灌封、分装、压塞 4包装材料暴露环境5不得设地漏,不应裸手操作。
万级:1小针 2需除菌 3注射剂稀配4包装材料最终处理5角膜创伤、手术用滴眼配制 6不得穿越较低级别十万级:1注射剂浓配、密闭系统稀配2包装材料最后一次精洗 3非最终PO4深部组织创伤、眼用药 5除直肠用药外的腔道用药三十级:1最终PO 2 PO 固体暴露 3表皮外用药 4直肠用药五:法律与行政法规、部门规章的区别1:法律〔由主席签署主席令公布〕:药品管理法刑法广告法消费者权益保护法反不正当竞争法2 :行政法规〔由总理签署国务院令公布、〕:药品管理法实施条例、麻精药品管理条例、医用毒性药品管理法、〔涉及到多个部门的也由国务院立法〕:疫苗流通和预防接种管理条例建立国家根本药物制度实施意见麻精品种目录国家根本药物目录管理方法城镇职工根本医疗保险用药药品广告审查发布标准药品广告审查方法 3:部门规章:麻精一购用印鉴卡执业药师资格制度暂行规定处方与非处方药分类管理方法非处方专有标识管理规定处方药与非处药流通管理暂得规定处方管理方法药品不良反响报告和监测管理方法药品注册管理方法 GMP、GSP药品召回管理方法药品流通监视管理方法互联网药品交易效劳审批暂行规定医部机构药事管理暂行规定药品说明书和标签管理规定互联网药品信息效劳管理方法关于制止商业贿赂行为的暂行规定药事管理与法规罚款歌〔含解释〕以下药事管理与法规罚款歌药圈版主自学成才分享:中药保护违反条例擅自仿照假药论处伪造证书没收所得三倍罚款犯罪刑罚对违反擅自仿制和生产中药保护品种的,由县级以上药品监视管理部门以生产假药依法论处。
药事管理与法规-40个必记高频考点
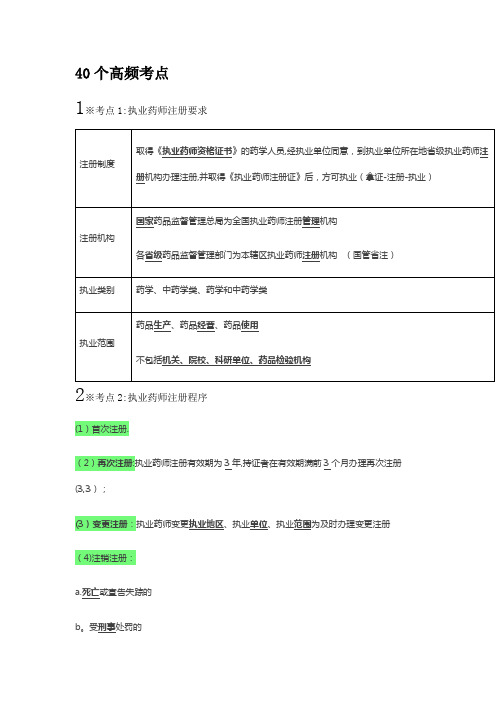
40个高频考点1※考点1:执业药师注册要求2※考点2:执业药师注册程序3※考点3:药品的内涵和外延药品特指人用药品,不包括兽药和农药4※考点4:药品安全风险分类:自然风险和人为风险。
5※考点5:建立国家基本医疗卫生制度四大体系6※考点6:国家基本药物遴选原则和范围▪遴选原则:够配备记忆:两基方案驾驶林中▪范围:▪不纳入国家基本药物目录遴选范围记忆:法轮严反,濒非自首7※考点7:国家基本药物目录的调整▪基本药物目录在保持数量相对稳定的基础上,实行动态管理,原则上每3年调整一次。
▪国家基本药物目录的品种和数量调整应当根据以下因素确定:记忆:需求变、疾病变、应用评估、经济评价、不良反应。
8※考点8: 应当从国家基本药物目录中调出记忆:药品不存在、药品被替代、药品严重不良反应。
9※考点9:基本药物的报销10※考点10:基本药物的补偿11※考点11:药品管理工作相关部门职责▪卫生计生部门▪中医药管理部门(中药现代化资源普查)中医药和民族药事业发展规划;指导中药和民族药的发掘、整理、总结和提高;中药资源普查▪发展和改革宏观调控部门▪人力资源和社会保障部门▪工商行政管理部门▪工业和信息化管理部门记忆:生化中药药背生—生物医药产业;化-工业和信息化部门;中药-中药材扶持;药背—药品储备12※考点12:药品监督管理技术支撑机构▪中国食品药品检定研究院记忆:抓住名字中“检定”二字,检验标定。
▪国家药典委员会▪国家食品药品监督管理总局药品审评中心▪国家食品药品监督管理总局药品评价中心▪国家中药品种保护评审委员会13※考点13:药品行政许可事项▪生产许可:《药品生产许可证》《医疗机构制剂许可》▪经营许可:《药品经营许可证》▪上市许可:《药品注册证》▪进口药上市:《进口药品注册证》《医药产品注册证》▪执业药师:《执业药师注册证》记忆:生产经营上市执业14※考点14:行政复议与行政诉讼15※考点15:临床试验的分期记忆:Ⅰ期药理Ⅱ期初步Ⅲ期确证Ⅳ期上市16※考点16:药品注册申请17※考点17:药品委托生产▪经省级药品监督管理部门批准,药品生产企业可以接受委托生产药品。
药事管理与法规考点汇总

执业药师考试《药事管理与法规》背诵要点1、药品特殊性:使用上专属性、作用两重性、质量重要性、药效上时效性2、药品质量特性:安全性、稳定性、均一性、有效性。
3、药学职业道德:激励、促进、调节、约束、督促和启迪。
4、药学工作对服务对象:仁爱救人、文明服务;严谨治学、理明术精;济世为怀、清廉正派。
5、药学工作对社会:坚持公益原则、维护人类健康;宣传医药知识、承担保健职责。
6、药学工作对同仁:谦虚谨慎、团结协作;勇于探索创新、献身医药事业。
7、药品生产企业企业:用户至上、以患者为中心;质量第一、自觉遵守规范;保护环境、保护药品生产者的健康;规范包装、如实宣传。
8、药品经营企业:诚实守信、确保药品质量;依法促销、诚信推广;指导用药、做好药学服务。
9、医院药学:精心调剂、耐心解释;精益求精、确保质量;合法采购;规范进药;维护患者利益、提高生命质量。
10、执业药师职业道德:救死扶伤,不辱使命;尊重患者,平等对待;依法执业,质量第一;讲德修业,珍视声誉;尊重同仁,密切协作。
11、执业药师,注册管3年,教育登记前3注。
职责-守法护法报告,质量监管处理。
现行药品管理法,十章一百零八条,人民用药要安全,监管力度要加强。
立法宗旨-管(加强监管制(保证质量安(保障安全康(维护健康权(维护权益药品管理法立法宗旨:为加强药品监督管理,保证药品质量,保障人体用药安全,维护人民身体健康和用药的合法权益12、药品研究、生产、经营、使用、监督的单位或个人必须遵守药品管理法。
13、执法主体:国务院药品监督管理部门主管全国药品监督管理工作。
国务院有关部门在各自的职责范围内负责与药品有关的监督管理工作。
省、自治区、直辖市人民政府药品监督管理部门负责本行政区域内的药品监督管理工作。
省、自治区、直辖市人民政府有关部门在各自的职责范围内负责与药品有关的监督管理工作。
14、国务院药品监督管理部门应当配合国务院经济综合主管部门,执行国家制定的药品行业发展规划和产业政策。
药事管理与法规知识点总结

药事管理与法规知识点总结《药事管理与法规知识点总结》一、药品管理基础知识1、什么是药品药品是指经过药品审评的,保证其质量、安全性、有效性的,有特定的化学组成,用来治疗疾病、预防疾病或者诊断、检查、改善人体机能的物质。
2、药品的分类药品分为处方药、非处方药、中药、保健药品、化妆品药品、特殊用途药品等。
3、药品审评是指通过独立的合格的专家和机构,对提交上市前的药品质量、安全性、有效性等有关内容进行系统、客观、公正的审查,以全面的、科学的方法,严格依据法律法规标准,对药品提交的申请结果,给出正式的审评结论,确保上市药品质量、安全性、有效性满足相关的要求。
4、药品登记是指国家药品监督管理部门在药品审评完毕后,对已审评质量、安全性、有效性达到法律要求的药品进行登记,颁发药品注册证书,核准上市用于贩卖的过程。
二、药品零售管理1、药品零售药品零售是指合法授权的药品经营者按照国家药品监督管理部门规定的药品经营许可经营范围和经营期限,根据政府规定的收费标准,出售社会药品供应点经营范围内的药品的行为及其所涉及的运行与管理活动。
2、药品零售许可药品零售许可是指政府授予合法药品经营者根据药品监督管理部门规定的药品经营许可经营范围和经营期限,在政府规定的收费标准下出售社会药品供应点经营范围内的药品的资格。
3、药品零售管理药品零售管理是指根据药品审评、登记、许可及药品管理法规综合规划、组织、落实、监督、审查等,以保证药品零售符合国家药品监督管理部门的规定。
4、药品零售安全药品零售安全是指药品零售经营者按照法律法规及药品审评、登记、许可及药品管理法规,以保证药品零售安全,确保药品的质量、安全性、有效性满足国家颁发的药品经营批准文件要求的组成部分。
2023 药事管理与法规 考点速记

2023 药事管理与法规考点速记一、药事管理的基本概念药事管理是指国家对医疗机构、药品生产企业和流通企业的药品生产、经营、使用和管理的一种监管活动。
药事管理的核心是保障药品的安全有效使用,维护公共健康。
二、药品管理法规概述药品管理法规包括《药品管理法》、《药品管理法实施条例》等,对药品的生产、流通、使用等方面进行了详细规定,旨在规范药品市场秩序,保障用药安全。
三、药品质量管理1. 药品GSP规范GSP是“Good Supply Practice”的缩写,是指药品的供应质量管理规范,包括存储、运输、分销等环节。
2. 药品GMP认证GMP是“Good Manufacturing Practice”的缩写,是指药品生产质量管理规范,包括原料药生产、制剂生产等环节。
四、药品市场准入1. 药品注册管理对新药品进行审批,确保药品的安全有效性。
2. 药品合理使用通过宣传教育、管理制度等手段,引导合理用药,减少滥用和误用。
五、药品监督管理1. 药品不良反应监测建立不良反应监测系统,及时发现和报告药品不良反应。
2. 药品经营质量管理对药品的进货、销售、库存等环节进行监管,防止次品药品流入市场。
六、药品安全监管1. 药品适用性评价对药品进行适用性评价,明确适应症、剂量等信息。
2. 药品安全风险评估评估药品使用可能带来的风险,及时采取措施防范风险。
七、个人对药事管理的理解在我看来,药事管理是一项非常重要的工作,它关乎到人民群众的身体健康和生命安全。
只有严格规范药品的生产、流通和使用,才能保障人们用药的安全和有效性。
药事管理也需要全社会的参与,政府部门、医疗机构、药品生产企业以及个人都应当共同努力,共同维护良好的药品市场秩序,为人民群众提供更加安全、放心的药品。
总结回顾通过本文的全面介绍,我们对2023年药事管理与法规的考点有了更深入的了解。
药事管理是一个复杂而又重要的系统工程,需要各个方面共同努力,才能够更好地保障人民群众的用药安全。
【VIP专享】《国际药事法规》

6.培养学生观察、思考、对比及分析综合的能力。过程与方法1.通过观察蚯蚓教的学实难验点,线培形养动观物察和能环力节和动实物验的能主力要;特2征.通。过教对学观方察法到与的教现学象手分段析观与察讨法论、,实对验线法形、动分物组和讨环论节法动教特学征准的备概多括媒,体继课续件培、养活分蚯析蚓、、归硬纳纸、板综、合平的面思玻维璃能、力镊。子情、感烧态杯度、价水值教观1和.通过学理解的蛔1虫.过观适1、察于程3观阅 六蛔寄.内列察读 、虫生出蚯材 让标容生3根常蚓料 学本教活.了 据见身: 生,师的2、解 问的体巩鸟 总看活形作 用蛔 题线的固类 结雌动态业 手虫 自形练与 本雄学、三: 摸对 学动状习人 节蛔生结4、、收 一人 后物和同类 课虫活构请一蚯集 摸体 回并颜步关 重的动、学、蚓鸟 蚯的 答归色学系 点形教生生让在类 蚓危 问纳。习从 并状学理列学平的害 题线蚯四线人 归、意特出四生面体以形蚓、形类 纳大图点常、五观玻存 表及动的鸟请动文 本小引以见引、察璃现 ,预物身类 3学物明 节有言及的、导巩蚯上状 是防的体之生和历 课什根蚯环怎学固蚓和, 干感主是所列环史 学么据蚓节二样生练引牛鸟 燥染要否以举节揭 到不上适动、区回习导皮类 还的特分分蚯动晓 的同节于物让分答。学纸减 是方征节布蚓物起 一,课穴并学蚯课生上少 湿法。?广的教, 些体所居归在生蚓前回运的 润;4泛益学鸟色生纳.靠物完的问答动原 的4蛔,处目类 习和活环.近在成前题蚯的因 ?了虫以。标就 生体的节身其实端并蚓快及 触解寄上知同 物表内特动体结验和总利的慢我 摸蚯生适识人 学有容点物前构并后结用生一国 蚯蚓在于与类 的什,的端中思端线问活样的 蚓人飞技有 基么引进主的的考?形题环吗十 体生行能着 本特出要几变以动,境?大 节活的1密 方征本“特节化下物.让并为珍 近习会形理切 法。课生征有以问的小学引什稀 腹性态解的 。2课物。什游题主.结生出么鸟 面和起结蛔关观题体么戏:要利明蚯?类 处适哪构虫系察:的特的特用确蚓等 ,于些特适。蛔章形殊形征板,这资 是穴疾点于可虫我态结式。书生种料 光居病是寄的们结构,五小物典, 滑生?重生鸟内学构,学、结的型以 还活5要生类部习与.其习巩鸟结的爱 是如原活生结了功颜消固类构线鸟 粗形何因的存构腔能色化练适特形护 糙态预之结的,肠相是系习于点动鸟 ?、防一构现你动适否统。飞都物为结蛔。和状认物应与的行是。主构虫课生却为和”其结的与题、病本理不蛔扁的他构特环以生?8特乐虫形观部特8征境小理三页点观的动位点梳相组等、这;,哪物教相,理适为方引些2鸟,育同师.知应单面导鸟掌类结了;?生识的位学你握日构解2互.。办特生认线益特了通动手征观识形减点它过,抄;察吗动少是们理生报5蛔?物,与的解.参一了虫它和有寄主蛔与份解结们环些生要虫其。蚯构都节已生特对中爱蚓。会动经活征人培鸟与飞物灭相。类养护人吗的绝适这造兴鸟类?主或应节成趣的为要濒的课情关什特临?就危感系么征灭来害教;?;绝学,育,习使。我比学们它生可们理以更解做高养些等成什的良么两好。类卫动生物习。惯根的据重学要生意回义答;的3.情通况过,了给解出蚯课蚓课与题人。类回的答关:系线,形进动行物生和命环科节学动价环值节观动的物教一育、。根教据学蛔重虫点病1.引蛔出虫蛔适虫于这寄种生典生型活的线结形构动和物生。理二特、点设;置2.问蚯题蚓让的学生生活思习考性预和习适。于穴居生活的形态、结构、生理等方面的特征;3.线形动物和环节动物的主要特征。
药事法规口诀

药品召回分级(配伍考点)根据药品安全隐患的严重程度,药品召回分为三级:对使用该药品可能引起严重健康危害的实施一级召回;对使用该药品可能引起暂时的或者可逆的健康危害的实施二级召回;对使用该药品一般不会引起健康危害,但由于其他原因需要收回的实施三级召回。
记忆“严重危害一级召;暂可逆害二级召;无害他因三级召”药品批准文件药品批准文号的格式为(配伍考点):国药准字H(Z、S、J)+4位年号+4位顺序号,其中H 代表化学药品,Z代表中药,S代表生物制品,J代表进口药品分包装。
《进口药品注册证》证号的格式为:H(Z、S)+4位年号+4位顺序号;《医药产品注册证》证号的格式为:H(Z、S)C+4位年号+4位顺序号,其中H代表化学药品,Z代表中药,S代表生物制品。
对于境内分包装用大包装规格的注册证,其证号在原注册证号前加字母B。
新药证书号的格式为:国药证字H(Z、S)+4位年号+4位顺序号,其中H代表化学药品,Z 代表中药,S代表生物制品。
国家药品监督管理部门核发的药品批准文号、《进口药品注册证》或者《医药产品注册证》的有效期为5年。
有效期届满,需要继续生产或者进口的,申请人应当在有效期届满前6个月申请再次注册。
药品研制的类型和阶段基本药物质量监督管理机构及职能国务院食品药品监督管理部门负责基本药物的评价性抽验(配伍考点)各省级食品药品监管部门负责基本药物的监督性抽验工作;地方各级食品药品监督管理部门应当进一步加强对城市社区和农村基本药物质量监督管理,充分发挥农村药品监督两在保证基本药物质量监督管理中的作用。
关键字记忆“国评省监地方管”处方的颜色:“普白精二白,麻红精一红,儿绿急诊黄”中药一级和二级保护品种的比较处方保存年限“一,儿、急、普”“二,毒、二精”“三,麻、一精”一类精神药品国家重点保护野生药材物种的药材名称一级保护药材名称:虎骨(已被禁止贸易)、豹骨、羚羊角、鹿茸(梅花鹿)。
口诀记忆: “虎豹羚羊梅花鹿”二级保护药材名称:鹿茸(马鹿)、甘草、麝香、蟾酥、黄连、黄柏、蛤蟆油、蛤蚧、穿山甲、厚朴(houpo)、杜仲、金钱白花蛇、乌梢蛇、蕲(qi)蛇、人参、熊胆、血竭。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《国际药事法规》知识点整理
《国际药事法规》是指针对药品研发、生产、销售等方面制定的国际性法规和指导文件。
这些法规和指导文件旨在保障公众的健康和安全,规范药品市场的运作,促进全球药品质量的提升。
以下是《国际药事法规》的主要知识点整理。
一、国际药事法规的基本原则
1.公共利益原则:以保障公众健康和安全为出发点;
2.风险管理原则:对药品研发、生产、销售等环节进行全面评估和管理;
3.合规原则:药品相关企业必须遵守药事法规的要求和规定;
4.透明度原则:各国需向公众公开药事法规和相关信息。
二、国际组织
1.世界卫生组织(WHO):负责指导各国制定药事法规,倡导全球合作;
2.国际药品监管机构合作组织(PIC/S):协助各国药事机构的监管工作,提升药品质量;
3.国际药理学与临床药理学联合会(IUPHAR):制定国际药理学标准和指南。
三、国际药事法规的主要内容
1.基本要求:药品必须安全、有效、质量可控;
2.药品注册和审批:规定药品上市前的审批程序和要求;
3.药品生产和质量控制:强调药品生产过程的规范化和质量管理;
5.药剂师和医生管理:对于药剂师和医生进行注册和管理;
6.不良反应报告与监测:要求药品生产和销售企业进行不良反应的报
告和监测;
7.药物价格控制和医保政策:规定药物价格的管理和医保政策的制定;
8.药物广告和宣传:规范药品广告和宣传的行为;
9.药品依从性和合理使用:强调药品的依从性和合理使用。
四、国际药事法规的实施
1.国内法规的制定:各国需要在国内制定符合国际药事法规要求的药
事法规;
2.国际间的交流与合作:各个国家的药事机构和药品监管机构需要进
行信息交流和合作,提升全球药品质量;
3.督促和监督:各国药事机构和药品监管机构需要对药品生产和销售
企业进行监督和督促,确保其合规运营。
五、国际药事法规实施的挑战和展望
1.国际间的标准差异:各国药事法规的要求和标准存在差异,需要进
一步协商和统一;
2.药检技术的进步:药检技术的进步使得药品质量的检测和监管更加
便捷,但也需要更新药事法规;
3.传统药物和非处方药的监管:随着传统药物和非处方药市场的扩大,需要进一步制定相关的药事法规和监管措施;
4.跨国企业的合规困境:跨国药企需要遵守各国的药事法规,但不同
国家的要求可能存在冲突。
总结:
国际药事法规的制定和实施是保障公众健康和安全的重要手段,它要
求各国制定相关的法规和指导文件,加强国际间的合作和交流,提升药品
质量的管理和监管水平。
同时,国际药事法规的制定和实施也面临诸多挑战,其中最重要的是国际间的标准差异和传统药物、非处方药的监管问题。
通过进一步协商和合作,各国可以共同制定更加完善的国际药事法规,为
公众健康和安全提供更好的保障。
