同济大学材料科学基础第六章S.ppt
同济大学材料科学基础第六章SPPT课件

反尖晶石 —— 一半三价离子与二价离子互 换位置
一半三价离子占据 V4 二价离子 + 另一半三价离子占据 V8 化学式 B(AB)O4
31
结构与性质 镁铝尖晶石是一种陶瓷材料的晶相 在一些耐火材料中也常存在这种晶相 反尖晶石则是一类氧化物铁氧体磁性材料,
23
(2)萤石的解理性 由于萤石结构中有一半的立方体空隙没有被
Ca2+填充,所以,在(111)面网上存在 着相互毗邻的同号离子层,其静电斥力将其 主要作用,导致晶体在平行于(111)面网 方向上容易发生解理,因此,萤石常呈八面 体解理。而NaCl晶体却无此性能。
24
25
(4)ABO3型晶体
第六章 无机非金属材料 的结构特征
1
标题添加
点击此处输入相 关文本内容
标题添加
点击此处输入相 关文本内容
总体概述
点击此处输入 相关文本内容
点击此处输入 相关文本内容
2
无机非金属材料的基本含义:
无机非金属材料是由指一种或多种金属元素同一种非 金属元素(如C、O、N等,通常为O)结合而成的 化合物,这些化合物主要是金属氧化物或金属非氧 化物,它几乎包含了除金属材料和高分子材料以为 的所有材料。
20
(2) AX2型晶体 (萤石型,CaF2)
21
AB2型化合物, rc/ra>0.732(0.85) 配位数:8:4 Ca2+作立方紧密堆积, F-填入全部四面体空隙中。 注意:所有八面体空隙都未被占据。萤石型结构的
氧化物在结构陶瓷和功能陶瓷方面具有重要的技术 应用。如CeO2、ZrO2、UO2等。萤石结构的衍 生结构如焦绿石(通式A2B2O7,Gd2Ti2O7)
起电介质的极化状态的改变不能及时被
同济材料科学基础6页

重点一、论述四种强化的强化机理、强化规律及强化方法。
1、形变强化形变强化:随变形程度的增加,材料的强度、硬度升高,塑性、韧性下降的现象叫形变强化或加工硬化。
机理:随塑性变形的进行,位错密度不断增加,因此位错在运动时的相互交割加剧,结果即产生固定的割阶、位错缠结等障碍,使位错运动的阻力增大,引起变形抗力增加,给继续塑性变形造成困难,从而提高金属的强度。
规律:变形程度增加,材料的强度、硬度升高,塑性、韧性下降,位错密度不断增加,根据公式Δσ=αbG ρ1/2,可知强度与位错密度(ρ)的二分之一次方成正比,位错的柏氏矢量(b)越大强化效果越显著。
方法:冷变形(挤压、滚压、喷丸等)。
形变强化的实际意义(利与弊):形变强化是强化金属的有效方法,对一些不能用热处理强化的材料可以用形变强化的方法提高材料的强度,可使强度成倍的增加;是某些工件或半成品加工成形的重要因素,使金属均匀变形,使工件或半成品的成形成为可能,如冷拔钢丝、零件的冲压成形等;形变强化还可提高零件或构件在使用过程中的安全性,零件的某些部位出现应力集中或过载现象时,使该处产生塑性变形,因加工硬化使过载部位的变形停止从而提高了安全性。
另一方面形变强化也给材料生产和使用带来麻烦,变形使强度升高、塑性降低,给继续变形带来困难,中间需要进行再结晶退火,增加生产成本。
2、固溶强化随溶质原子含量的增加,固溶体的强度硬度升高,塑性韧性下降的现象称为固溶强化。
强化机理:一是溶质原子的溶入,使固溶体的晶格发生畸变,对滑移面上运动的位错有阻碍作用;二是位错线上偏聚的溶质原子形成的柯氏气团对位错起钉扎作用,增加了位错运动的阻力;三是溶质原子在层错区的偏聚阻碍扩展位错的运动。
所有阻止位错运动,增加位错移动阻力的因素都可使强度提高。
固溶强化规律:①在固溶体溶解度范围内,合金元素的质量分数越大,则强化作用越大;②溶质原子与溶剂原子的尺寸差越大,强化效果越显著;③形成间隙固溶体的溶质元素的强化作用大于形成置换固溶体的元素;④溶质原子与溶剂原子的价电子数差越大,则强化作用越大。
同济大学材料科学基础绪论资料

一门新的综合性学科的诞生。
什么是材料科学 ?
• 材料科学是一门以材料为研究对象,介于基础科
学与应用科学之间的称之为应用基础科学的学科。
• 基本内容: • (1)从化学的角度出发,研究材料的化学组成、
键性、结构与性能的关系及其规律
• (2)从物理的角度出发,研究材料的组成原子、
材料科学学科形成的 深层次原因分析(4)
许多不同类型的材料可以相互代替和补充, 能更充分发挥各种材料的优越性,达到物 尽其用的目的。(复合材料的原理问题的 提出)
材料科学学科形成的 深层次原因分析(5)
• 最后,复合材料在多数情况下是不同类型
材料的组合,如果对不同类型材料没有一 个全面的了解,作为新材料发展之一的复 合材料的研究开发必然受到影响。对各类 材料有一个深入的了解是复合材料发展的 基础。
离子或分子等的排列形式或方式。
• (B)性质: • 赋予材料的价值和应用性.
• 指材料对电、磁、光、热、机械载荷的反应,
主要决定于材料的组成与结构。
• (C)使用性能: • 是材料在使用条件下应用性能的度量.
也指在使用状态下表现的行为,它与材料设计、工
程环境密切相关。实用性能包括可靠性、耐用性、寿
材料结构关系
• 材料的结构包括不同晶体结构和非晶体,以及显微镜下
的微观结构,哪些主要因素能够影响和改变结构?只有 了解了这些才能实现控制结构的目的。
• 材料的性能包括物理性能、化学性能、力学性能。 • 其内部结构包括四个层次:①原子结构;②结合键;③
原子的排列方式;④显微组织
• (A)组织结构: • 包含着决定材料性质和使用性能的原子、
材料科学学科形成的 深层次原因分析(2)
材料科学基础课件第六章第三节第四节第五节
凝固技术
凝固技术
二、单晶制取 单晶材料:功能材料,半导体、压电、光电、声
光、热电、红外遥感等 由单个晶核生长而成 制法:垂直提拉法,尖端形核法
凝固技术
福建鑫晶精密刚玉,2009年成立,顶部籽晶温度梯度法,人造蓝宝石; 用作蓝绿光半导体(LED)和大规模集成电路(SOS)最重要的衬底材
(Cu-Ag)、新亚稳相(Ag-Ge)、非晶体 (Au-Si(25%))、更多微晶(0.2~0.3μm), 抑制或减少偏析。
凝固技术
得非晶合金所需冷速:单元系金属≥1010K/s,多 元合金要小几个数量级。
产品:低维材料,粉末、细丝和薄膜(带)等 方法:喷射雾化、单辊、双辊
凝固技术
纯金属的结晶
②金属-非金属型:粗糙-光滑小平面,动态过冷
度相差几十倍,一个垂直生长,一个横向生长并
有取向性。在动态过冷度较小时.生长速率明显
不同,因此在生长过程中两相不能较好地合作、
协调及匹配长大,则其规则性差。这类共晶组织
形态必然与生长速度快的引领相的性质、生长形
态有关,而生长速度又与界面前沿的过冷度有关
(图6—12),它是由外界条件控制的,当过冷
共晶合金结晶
(2)动力学伪共晶区 由于共晶两相成核与生长动力学存在差异,使热
力学伪共晶区发生偏移或变形,熔点相差越大, E靠近低熔点相,低熔点相易于成核和生长, 成为领先相,按初生相方式长大,导致共晶合 金在非平衡冷却时得不到100%共晶组织,而 得到亚共晶组织,使伪共晶区向高熔点组元方 向偏移。
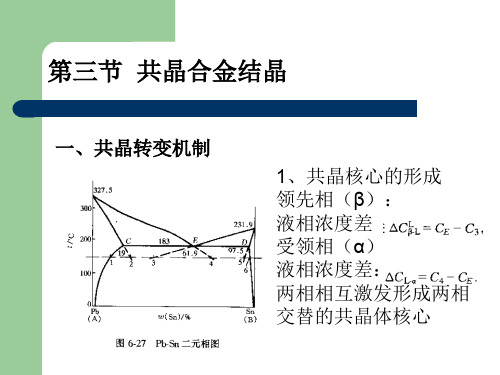
第三节 共晶合金结晶
一、共晶转变机制
1、共晶核心的形成 领先相(β): 液相浓度差 受领相(α) 液相浓度差: 两相相互激发形成两相 交替的共晶体核心
材料科学基础第六章 PPT课件

6.1 单元系相变 的热力学及相平衡
6.1.1 相平衡条件和相律
1. 相平衡的条件
多相体系中的吉布斯(Gibbs)自由能(G),是体系的 温度(T)、压力(P),以及各组元的物质的函数。
G=G(T,P,n1n2n3…)
d G SdT VdP idni
其中, idni 是i组元变化引起的体系自由能变化
11
0.294
Au
12
0.288
11
0.286
Al
12
0.286
10.6
0.296
Na
8
0.372
8
Sn 4+2+4 0.315,0.376
10
Bi
3+3
0.309,0.346
7~8
0.336 0.320 0.332
温度℃ 20 460 1100 700 390 280 240
比较固体与液体的有关数据可知: (1)液体中原子之间的平均距离比固体中略大。 (2)液体中原子的配位数比密排结构晶体的配位数小, 通常在8-11的范围内,故熔化时体积略微膨胀; 但对非密排结构的晶体如:Sb,Bi,Ga,Ge等,则液态 时配位数反而增大,故熔化时体积略为收缩。 (3)液态中原子排列混乱度增加。
固态的同素异构转变
纯铁相变
纯铁等压相变
纯铁的冷却曲线及晶体结构变化
SiO2相平衡图:化合物的多晶型转变
6.2 纯晶体的凝固
6.2.1 液态结构
一些常见金属衍射分析数据
金属
固态
液态
配位数 原子距离(nm) 配位数 原子距离(nm)
Hg
6+6
0.30,0.347
材料科学基础课程总结PPT课件

6
第6页/共65页
立方晶系常见的晶面族为:
{100} : (100)、(010)、(001)
{110} : (110)、(101)、(011)、(110)、(101)、(011)
{111} : (111)、(111)、(111)、(111)
立方晶系常见的晶向为:
100 : [100]、[010]、[001]
31
第31页/共65页
Байду номын сангаас
单晶体金属的塑性变形
滑移变形的特点 :
⑴ 滑移只能在切应力的作用下发生。临界分切应力! ⑵ 滑移常沿晶体中原子密度最大的晶面和晶向发生。 ⑶滑移时,晶体两部分的相对位移量是原子间距的整数倍. ⑷ 滑移的同时伴随着晶体的转动。 (5) 滑移是通过滑移面上的位错的运动来实现的。
当外力在某一滑移系中的分切应力达到 一定临界值时,该滑移系方向首先发生 滑移,该分切应力称为临界分切应力
小角度晶界 大角度晶界
共格 半共格 非共格
对称倾斜
不对称倾斜 扭转
29
第29页/共65页
晶界特性
1) 晶界能量高,原子处于不稳定状态
易于原子扩散,故新相易于在晶界处形核 杂质原子易于在晶界富集,导致晶界熔点低于晶内,加
热时晶界先熔化, 过热 晶界原子扩散速度高于晶内,且晶内腐蚀比晶内也快
2) 晶界原子排列不规则,且存在较多的缺陷,如空位和位错等
三种常见晶格的密排面和密排方向
体心立方晶格 面心立方晶格 密排六方晶格
密排面 {110} {111} 六方底面
数量 6 4 1
密排方向 <111> <110>
底面对角线
材料科学基础 ppt课件

(5)结合键与性能
材料结合键的类型及键能大小对某些性能 有重要影响,主要表现在以下两个方面:
1.物理性能: (1)熔点的高低代表了材料稳定性的程度。物 质加热时,当热振动能足以破坏相邻原子间的稳 定结合时,便会发生熔化,所以熔点与键能值有 较好的对应关系:共价键、离子键化合物的熔点 较高,其中纯共价键金刚石具有最高熔点,金属 的熔点相对较低,但过渡族金属有较高的熔点, 特别是难熔金属W、Mo、Ta等熔点都很高。而具 有二次键结合的材料的熔点一般很低,如聚合物
2.根据排列次序建立了元素周期表,各个周 期中的元素的性质呈现相同的周期变化规 律,元素在周期表上的位置不仅决定了单 个原子的行为,也决定了材料中原子的结 合方式以及材料的化学性能和物理性能。
第二节 原子结合键
一.原子结合键 1.存在状态:凝聚态(液态和固态) 分类 2.一次键:结合力较强,包括离子键、共 价键和金属键。 3.二次键:结合力较弱,包括范德瓦耳斯 键和氢键。
二. 一次键
1.离子键
(1)通过电子转移形成稳定结构,存在于大 多数盐类、碱类和金属氧化物,如NaCI、MgO 、CuO、Mg2Si、CrO2。
(2) 基本特点是以离子为基本结合单位。
(3)一般离子晶体中正负离子静电引力较强 ,结合牢固。因此。其熔点和硬度均较高。 另外,在离子晶体中很难产生自由运动的电 子,因此,它们都是良好的电绝缘体。但当
电子云
原子核
电子云
原子核 a)理论电子云的分布
b)原子偶极矩的产生
4.氢键
氢键是一种特殊的分子间作用力,本质上与
范德瓦耳斯键一样,它是由氢原子同时与两个电
