中考化学计算题(表格型)
中考化学二轮复习专题七化学计算题

11. (2018徐州)工业上采用离子交换膜电解槽电解饱和食盐水,可得到高 浓度的烧碱溶液(含NaOH 35%~48%),某兴趣小组欲验证一化工厂生 产的NaOH溶液是否达到了高浓度标准,进行了如下操作,请你参与计算: (1)用37%的浓盐酸配制200 g 7.3%的盐酸,需要加水(密度为1 g·mL-1) ________mL。(计算结果保留一位小数) (2)采集该化工厂电解槽中的NaOH溶液20 g,向其中滴入所配制的盐酸, 当溶液的pH=7时,消耗盐酸100 g,判断电解槽中NaOH溶液是否达到 高浓度标准。(写出计算过程)
(1)67.5% (2)解:设100 g硫酸溶液中硫酸的质量为x
Zn+H2SO4=== ZnSO4+H2↑
98
2
x
0.25 g
98 = x
x=12.25 g
2 0.25g
硫酸溶液中硫酸的质量分数为
12.25g
×100%=12.25%
100g
答:所用硫酸溶液的溶质质量分数为12.25%。
2. (2017徐州)徐州地区石灰石资源丰富。某化学兴趣小组称取4.0 g石灰
(1)溶解时玻璃棒的作用是_________________。 (2)实验中加入过量CaCl2溶液的目的是___________________________。 (3)通过计算判断该工业纯碱是否为合格品。(写出计算过程,结果精确 到0.1%)。 【提示】分析图中实验过程,判断“滤渣”的成分,找出代入化学方程式 计算的纯净物质量。
实验序号
①
②③Biblioteka 样品的质量/g10
20
30
生成气体的质量/g
0.1
0.2
0.25
试计算所用硫酸溶液的溶质质量分数(写出计算过程,结果精确到0.01%)。
【化学】初三化学化学计算题专项训练及答案

【化学】初三化学化学计算题专项训练及答案一、有关化学式的计算1、计算硝酸铵(NH₄NO₃)中氮元素的质量分数。
解:硝酸铵中氮元素的相对原子质量总和为:$14×2 = 28$硝酸铵的相对分子质量为:$14×2 + 1×4 + 16×3 = 80$氮元素的质量分数为:$\frac{28}{80}×100\%= 35\%$答:硝酸铵中氮元素的质量分数为 35%。
2、已知氧化铁(Fe₂O₃)的化学式,求其中铁元素与氧元素的质量比。
解:氧化铁中铁元素与氧元素的质量比为:$(56×2) :(16×3) = 112 : 48 = 7 : 3$答:氧化铁中铁元素与氧元素的质量比为 7 : 3。
二、有关化学方程式的计算1、加热分解 63g 高锰酸钾,可以得到多少克氧气?解:设可以得到氧气的质量为 x。
$2KMnO₄\stackrel{\triangle}{=\!=\!=} K₂MnO₄+ MnO₂+ O₂↑$$316 32$$63g x$$\frac{316}{32} =\frac{63g}{x}$$x =\frac{32×63g}{316} ≈ 06g$答:加热分解 63g 高锰酸钾,可以得到 06g 氧气。
2、用氢气还原氧化铜,要得到 32g 铜,需要多少克氢气?解:设需要氢气的质量为 y。
$H₂+ CuO \stackrel{\triangle}{=\!=\!=} Cu +H₂O$$2 64$$y 32g$$\frac{2}{64} =\frac{y}{32g}$$y =\frac{2×32g}{64} = 1g$答:需要 1g 氢气。
3、实验室用 100g 含碳酸钙 80%的大理石与足量的稀盐酸反应,能制得多少克二氧化碳?解:大理石中碳酸钙的质量为:$100g×80\%= 80g$设生成二氧化碳的质量为 z。
九年级化学表格综合计算测试题-中考复习(附答案)

九年级化学表格综合计算测试题-中考复习(相对原子质量:H-1 O-16 C-12 K-39 Na-23 S-32 Fe-56 Ca-40 Cl-35.5)【一】1.常温下,向盛有100.0g KOH溶液的烧杯中逐滴加入120.0g质量分数为7.3%的稀盐酸,用pH计(精确测定溶液pH的仪器)测定反应过程中溶液的pH,所得数据如表:加入稀盐酸的质量/g 60.0 80.0 100.0 120.0烧杯中溶液的pH 13.7 13.3 7.0 0.7 (1)恰好完全反应时,消耗稀盐酸的质量为g。
(2)求该KOH溶液中溶质的质量分数(结果精确到0.1%)。
2.某科学兴趣小组同学取8.5g铁,放到含少量硫酸的硫酸铜溶液中,完全反应后,最终得到9.2g固体。
为测定所得固体中各成分的含量,同学们将62.5g稀盐酸分五次加入到该固体中,得到数据如表:次数 1 2 3 4 5 加入盐酸溶液质量/g 12.5 12.5 12.5 12.5 12.5剩余固体质量/g 8.5 7.8 a 6.4 6.4 请分析计算:(1)表中a的值是。
(2)9.2g固体中铁的质量是。
(3)稀盐酸的溶质质量分数是多少?(4)与硫酸铜反应的铁的质量是多少?3. 小科用如图所示的装置来测量某石灰石样品中碳酸钙的质量分数,注射器水平放置,夹持装置未画出。
他在试管中加入lg石灰石样品和足量的稀盐酸(石灰石中其它成分不与稀盐酸反应产生气体),快速将连有注射器的橡皮塞塞紧试管口,实验结果如下表。
(忽略活塞与筒壁之间的摩擦及温度变化对实验的影响)反应时间/min 0 1 2 3 4活塞对应的刻度/mL 0 98 152 176 176(1)实验中判断石灰石和盐酸反应完的依据是。
(2)当时实验条件下二氧化碳的密度约为2g/L.请利用表格中的数据,根据化学方程式计算该石灰石样品中碳酸钙的质量分数。
*****4.某石灰厂为了测定某石灰石样品中CaCO3的质量分数,往盛有300g稀盐酸的烧杯中依次加入粉碎后的石灰石样品(杂质不与盐酸反应),充分反应后,实验数据记录如表:实验次数第一次第二次第三次石灰石样品/g 25 15 10 烧杯中物质总质量/g 316.2 326.8 m请回答:(1)CaCO3中钙、碳、氧三种元素的质量比为;(写最简比)(2)表中m=;(3)所用稀盐酸的溶质质量分数为;(4)求该石灰石样品中CaCO3的质量分数。
中考化学表格型计算专题
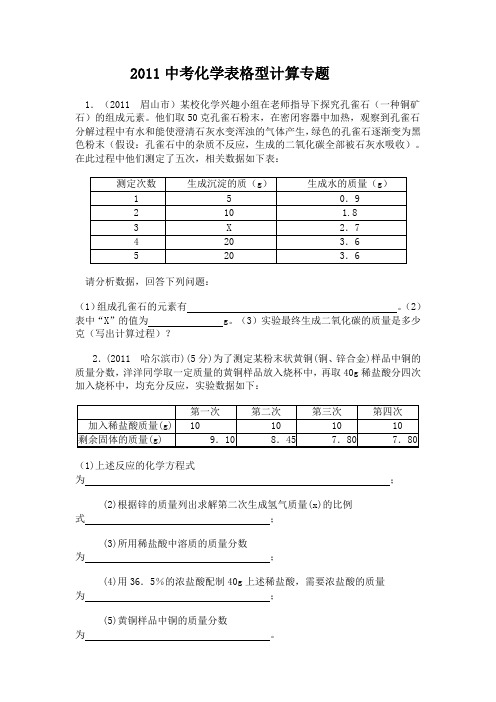
2011中考化学表格型计算专题1.(2011 眉山市)某校化学兴趣小组在老师指导下探究孔雀石(一种铜矿石)的组成元素。
他们取50克孔雀石粉末,在密闭容器中加热,观察到孔雀石分解过程中有水和能使澄清石灰水变浑浊的气体产生,绿色的孔雀石逐渐变为黑色粉末(假设:孔雀石中的杂质不反应,生成的二氧化碳全部被石灰水吸收)。
在此过程中他们测定了五次,相关数据如下表:请分析数据,回答下列问题:(1)组成孔雀石的元素有。
(2)表中“X”的值为 g。
(3)实验最终生成二氧化碳的质量是多少克(写出计算过程)?2.(2011 哈尔滨市)(5分)为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,洋洋同学取一定质量的黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:(1)上述反应的化学方程式为;(2)根据锌的质量列出求解第二次生成氢气质量(x)的比例式;(3)所用稀盐酸中溶质的质量分数为;(4)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量为;(5)黄铜样品中铜的质量分数为。
3.化学小组同学取某黄铜(铜和锌的合金)样品进行如下实验,他们取该黄铜样品碎屑50g,把200g稀硫酸分4次加入到该样品中,测得数据记录如下表:(1)当加入稀硫酸的质量为________g时,反应恰好完成.(2)铜锌合金中铜的质量分数为_________(3)计算生成氢气的总质量(写出计算过程).(4)计算(2)中生成物溶液中的溶质质量分数(写出计算过程).4.(2011.泸州市)小明同学将13.9g含杂质的的纯碱样品(碳酸钠与氯化钠的混合物)与90.5g稀盐酸相混合,充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据根据题目要求,回答下列问题:(1)碳酸钠完全反应后,生成CO2的质量为 g(2)请在下面的坐标图中,画出反应是生成气体的质量(m)随时间(t)变化的曲线。
(3)求完全反应后所得溶液中溶质的质量分数。
中考化学表格型计算题练习(附解析)
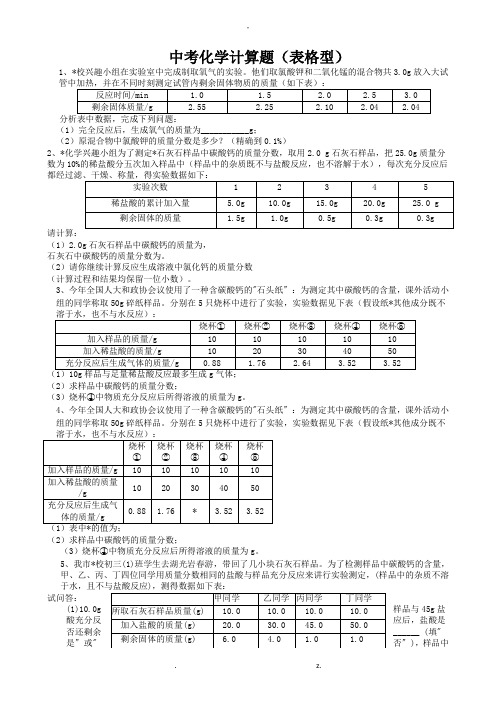
中考化学计算题(表格型)1、*校兴趣小组在实验室中完成制取氧气的实验。
他们取氯酸钾和二氧化锰的混合物共3.0g放入大试(1)完全反应后,生成氧气的质量为___________g;(2)原混合物中氯酸钾的质量分数是多少?(精确到0.1%)2、*化学兴趣小组为了测定*石灰石样品中碳酸钙的质量分数,取用2.0 g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后请计算:(1)2.0g石灰石样品中碳酸钙的质量为,石灰石中碳酸钙的质量分数为。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。
3、今年全国人大和政协会议使用了一种含碳酸钙的"石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。
分别在5只烧杯中进行了实验,实验数据见下表(假设纸*其他成分既不(2)求样品中碳酸钙的质量分数;(3)烧杯④中物质充分反应后所得溶液的质量为g。
4、今年全国人大和政协会议使用了一种含碳酸钙的"石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。
分别在5只烧杯中进行了实验,实验数据见下表(假设纸*其他成分既不(2)求样品中碳酸钙的质量分数;(3)烧杯④中物质充分反应后所得溶液的质量为g。
5、我市*校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品。
为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定,(样品中的杂质不溶试问答:(1)10.0g样品与45g盐酸充分反应后,盐酸是否还剩余______ (填"是”或"否”),样品中碳酸钙的质量分数是__________。
(2)10.0g 样品与足量稀盐酸反应后可产生二氧化碳多少克"(写出计算过程,计算结果精确到小数点后两位) 6、(鸡蛋壳的主要成分是碳酸钙,为测定鸡蛋壳中的碳酸钙含量,*同学将鸡蛋壳洗净、充分干燥并捣碎,展开了下列探究。
中考化学计算题及详细答案

有关化学式的计算题1、计算CuSO4·5H2O的式量______________________________2、计算NH4NO3中所含各元素的质量比_________________________________3、某黄铁矿中含FeS2为72%,计算该黄铁矿中硫元素的质量分数是()A.36%B.38.4%C.42.6%D.48%4、某元素R的单质跟氧气化合生成的氧化物中,R元素跟氧元素的质量比为21:8,原子个数比为3:4,又知氧元素的相对原子质量为16,则元素R的相对原子质量为()A.24B.27C.56D.655、在SO3和SO2的两种物质中,相同的是()A.氧元素的质量分数B.硫元素的质量分数C.元素种类D.原子个数比6、A、B两种化合物均由R和氧两种元素组成的,在化合物A和B中,R元素的质量分数分别为50%和40%,若A的化学式为RO2,则B的化学式为() A.R2O B.RO C.R2O3 D.RO37、在FeSO4和Fe2 (SO4) 3的混合物中,氧元素的质量分数为a%,则该混合物中铁元素的质量分数为()A.2a%B.1-a%C.1-0.5a%D.1-1.5a%8、甲、乙两种化合物x2y和yz2中,y元素的质量分数分别约为40%和50%,则在丙化合物x2yz3中y 元素的质量分数约为()A.20% B.25% C.30% D.35%(一)标签型化学式计算题:1、锌是人体健康必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫功能低下。
市售的葡萄糖酸锌口服液对治疗锌缺乏病具有较好的疗效。
下图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答:(1)葡萄糖酸锌中各元素的质量比;(3)某患者除正常饮食吸锌元素外,还需服用该品牌葡萄糖酸锌口服液。
若治疗一个疗程需补充104mg锌元素,而这些锌有75%来自该口服液,则患者共需服用支葡萄糖酸锌口服液?(简写出解题过程)(二)叙述型化学式计算题:1、蛋白质是由多种氨基酸[丙氨酸:CH3CH(NH2)COOH等]构成的极为复杂的化合物,人体通过食物获得蛋白质,在胃肠道里与水发生反应,生成氨基酸,试计算:(1)丙氨酸分子中氮原子与氧原子的个数比。
初中化学计算题大全(含答案及解析)
2024年中考化学《必考经典》计算题大全(含答案及解析)1.实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。
分析并计算:(1)a点溶液中含有的离子是_____。
(2)当pH=7时,消耗氢氧化钠溶液中NaOH质量为_____g。
(3)计算稀H2SO4中溶质的质量分数。
_____(4)计算恰好完全反应时所得溶液的溶质质量分数。
_____【答案】Na+、H+、SO42- 0.8 稀H2SO4的溶质质量分数是9.8%;恰好完全反应时所得溶液的溶质质量分数是5.5%。
【解析】【详解】(1)由图示可知,在a点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以,溶液中含有的离子为:Na+、H+、SO42-;(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;(3)10g稀硫酸样品含有H2SO4的质量为x,生成的硫酸钠的质量为y2NaOH+H SO=Na SO+2H O2424280981420.8g x y解得:x=0.98g y=1.42g稀H2SO4的溶质质量分数为:×100%=9.8%;(4)恰好完全反应时所得溶液的溶质质量分数:×100%≈5.5%。
2.某小组同学将530 g碳酸钠溶液加入到280 g石灰乳(水和氢氧化钙的混合物)中,使之恰好完全反应,所得溶液中溶质的质量分数为1%,计算加入的碳酸钠溶液中溶质的质量分数。
【答案】2%【解析】【详解】设原碳酸钠溶液中溶质的质量为xNa2CO3+ Ca(OH)2=CaCO3↓+ 2NaOH106 100 80X则解得x =10.6g所以加入的碳酸钠溶液中溶质的质量分数为答:加入的碳酸钠溶液中溶质的质量分数为2%。
3.取一定量的氯化钠与氢氧化钠的混合物,加一定量的水配成溶液,然后向其中滴加溶质质量分数为7.3%稀盐酸,直至恰好反应,共消耗稀盐酸50g。
初三化学化学计算题题20套(带答案)
初三化学化学计算题题20套(带答案)1. 假设有一块铁块,其质量为56克。
求该铁块中含有的铁原子数。
解答:我们需要知道铁的摩尔质量。
铁的摩尔质量约为56克/摩尔。
因此,该铁块中含有的铁原子数为56克 / 56克/摩尔 = 1摩尔。
由于1摩尔物质中含有6.022 x 10²³个原子,所以该铁块中含有的铁原子数为1摩尔x 6.022 x 10²³个/摩尔= 6.022 x 10²³个。
2. 某化学反应中,反应物A和反应物B的化学计量比为2:3。
如果反应物A的质量为24克,求反应物B的质量。
解答:我们需要根据化学计量比计算出反应物B的质量。
由于反应物A和反应物B的化学计量比为2:3,所以反应物B的质量为24克x (3/2) = 36克。
3. 在一定条件下,一定量的氧气与一定量的氢气完全反应,了36克水。
求反应中消耗的氧气和氢气的质量。
解答:我们需要根据水的化学式H₂O计算出水的摩尔质量。
水的摩尔质量为2 x 1.008克/摩尔 + 16.00克/摩尔 = 18.016克/摩尔。
因此,36克水的物质的量为36克 / 18.016克/摩尔 = 2摩尔。
由于水的化学计量比为2:1,所以反应中消耗的氢气的物质的量为2摩尔,质量为2摩尔 x 2.016克/摩尔 = 4.032克。
同样,消耗的氧气的物质的量为1摩尔,质量为1摩尔 x 32.00克/摩尔 = 32.00克。
4. 某溶液中,溶质的质量分数为10%。
如果该溶液的质量为500克,求溶质的质量。
数为10%,即溶质的质量占溶液总质量的10%。
因此,溶质的质量为500克 x 10% = 50克。
5. 在一定条件下,一定量的氢气和一定量的氧气完全反应,了水。
如果反应中消耗的氢气的质量为2克,求反应中消耗的氧气的质量。
解答:我们需要根据水的化学式H₂O计算出水的摩尔质量。
水的摩尔质量为2 x 1.008克/摩尔 + 16.00克/摩尔 = 18.016克/摩尔。
中考化学表格型计算题
在一烧杯中盛有22.3 g Na2CO3和 NaCl 构成的固体混淆物,加足量水溶解,配成溶液。
向此中渐渐滴加溶质质量分数为 10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线以下图。
请依据题意回答以下问题:(1)当滴加了73 g 稀盐酸时,放出气体的总质量为g。
(2)当滴加稀盐酸至图中B 点时,烧杯中溶液里的溶质是(写化学式)。
(3)当滴加了 146g 稀盐酸时(即点时),烧杯中为不饱和溶液,试经过计算求出此中溶液质量。
67、(济南市)在一烧杯中盛有 100gBaCl 2和HCl的混淆溶液,向此中渐渐滴加溶质质量分数为 10%的Na2CO3溶液,混淆溶液的质量与所滴入 Na2CO3溶液的质量关系曲线以下图:请依据题意回答以下问题:(1)在实验过程中,有气体放出,还能够看到的显然实验现象是。
(2)在实验过程中放出气体的总质量为g。
(3)当滴入 Na2 CO3溶液至图中 B 点时,经过计算求此所得不饱和溶液中溶质质量分数是多少?(计算结果精准到 0.1% )向盛有 22.3 g Na 2CO3和 NaCl 固体混淆物的烧杯中加入216.1 g稀盐酸恰巧反响,反响过程用精细仪器测得烧杯连同药品的质量(m) 与反应时间 (t) 的关系以以下图所示:烧杯连同药品的开端质量为 300 g 。
回答以下问题:(1)当固体混淆物与稀盐酸恰巧完整反响时,所需时间约为S。
(2) 完整反响后,产生二氧化碳气体质量g 。
(3)反响后,获得室温下的不饱和溶液。
所得溶液中溶质的质量分数为多少?例5:某同学为研究铜铁合金中铁的质量分数,先后进行了三次实验,实验数据以下表:第一次序二次序三次所取合金 /g 20 20 40所加稀硫酸 /g 100 120 80生成氢气 /g 0.4 0.4 0.4依据该同学的实验,试回答以下问题:(1)上表三次实验中,合金里的铁恰巧完整反响时,耗费稀硫酸溶液的质量是_____g。
(2)该铜铁合金中铁的质量分数是多少?(3)第三次实验所得溶液溶质质量分数为____________(结果保存至 0.1%)。
九年级化学中考复习专题表格计算
化学计算综合练习题第一次第二次第三次所取合金的质量/g 20 20 20所加稀硫酸的质量/g 100 120 80生成氢气的质量/g 0.4 0.4 0.4(1)上表三次实验中,有一次恰好完全反应,则合金里的铁恰好完全反应时,消耗稀硫酸溶液的质量是g.(2)该合金中铁的质量分数是多少?(3)第三次实验所得溶液的溶质质量分数为多少?(精确到0.1%)2、为了测定某石灰石样品中碳酸钙的含量,取20g此样品,将80g的稀盐酸分四次加入样品使之充分反应(石灰石中的杂质不溶于水,也不与盐酸及生成物反应),每次用盐酸次数一二三四加入盐酸的质量/g 20 20 20 20剩余固体的质量/g 15 10 5 5计算:(1)样品中碳酸钙的质量分数;(2)20g此样品与足量盐酸反应最多生成二氧化碳的质量;(3)加入的稀盐酸中溶质的质量分数.3、某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。
分四次取样品与稀硫酸反1 2 3 4取样品质量(g)50.0 50.0 50.0 50.0取稀硫酸质量(g)40.0 80.0 120.0 160.0产生气体质量(g)0.4 0.8 1.0 1.0(1)恰好完全反应的是第次实验。
(2)黄铜中铜的质量分数4、某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验;取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,充分反应后,实验数据记录如下:请你据此分析计算:(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是g.(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)(3)根据实验数据,在下边的坐标纸上绘制出所加稀盐酸的质量与生成的二氧化碳的质量关系的曲线.(不要求写出计算过程,只画出曲线即可)5、为了测定校舍建筑工地上石料中碳酸钙的质量分数,该校某化学兴趣小组先将石料粉碎,然后称取4份,分别逐渐加入到4份稀盐酸中(石料中的杂质不参与反应)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中考化学计算题(表格型)
1、(10江西)今年全国人大和政协会议使用了一种含碳酸钙的“石头纸”:为测定其中碳
酸钙的含量,课外活动小组的同学称取50g碎纸样品。
分别在5只烧杯中进行了实验,实验数据见下表(假
(1g
(2 )求样品中碳酸钙的质量分数;
(3 )烧杯④中物质充分反应后所得溶液的质量为________ g
2、(10南昌)今年全国人大和政协会议使用了一种含碳酸钙的“石头纸”:为测定其中碳
酸钙的含量,课外活动小组的同学称取50g碎纸样品。
分别在5只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,也不与水反应):
(1)表中X的值为________ ;
(2 )求样品中碳酸钙的质量分数;
(3 )烧杯④中物质充分反应后所得溶液的质量为________ g
3、(2010湛江)我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品。
为了检测样品中碳酸
钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
试问答:
(1)10.0g样品与45g盐酸充分反应后,盐酸是否还剩余________ (填“是”或“否”),
样品中碳酸钙的质量分数是____________ 。
(2)
10.0g 样品与足量稀盐酸反应后可产生二氧化碳多少克
?(写出计算过程,计算结果
精确到小数点后两位)
4、(衢州)鸡蛋壳的主要成分是碳酸钙,为测定鸡蛋壳中的碳酸钙含量,某同学将鸡蛋壳 洗净、充分干燥并捣碎,展开了下列探究。
(1) 将溶质质量分数为 35%的浓盐酸配制成10%的稀盐酸,操作步骤为: 步骤1:计算所需浓盐酸和水的体积;
步骤2:根据计算结果,用 ________ 分别量取所需的浓盐酸和水; 步骤3:将浓盐酸倒入水中并用玻璃棒搅拌得到稀盐酸。
(2) 测得各自的质量后,将鸡蛋壳置于如图所示的锥形瓶中,打开分
液漏斗中的活塞,使 其充分反应,直到不再产生气泡为止 (假设装置中的稀盐酸足量,鸡蛋壳中的其他
物
质不与稀盐酸反应)。
实验数据记录如下表:
第3 6题 图
5、( 10乐山)生铁是铁和碳的合金。
为测定某炼铁厂生产的生铁样品中铁的质量分数,
化
学兴趣小组的同学称得该生铁样品 6.0g ,放入烧杯中,向其中加入 65.0g 稀硫酸,恰 好完全反应(假设杂质不参与反应)。
测得的实验数据如下:
r
反应前 反应后 烧杯及其中物质的质量
97.0g
96.8g
请你完成有关计算(结果保留一位小数) (1)反应放出的氢气是多少?
(2 )生铁样品的质量分数是多少?
(3 )反应后所得溶液中溶质的质量分数是多少?
反应前
鸡蛋冗的质量
16克 装置和稀盐酸的总质量
220克 反应后
:装置及其内容物的总质量
231.6 克
请计算该鸡蛋壳中碳酸钙的质量分数。
6、( 10娄底)Cu 与Zn 的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零 件。
某化学兴趣小组的同学为了测定某黄铜的组成, 取20g 该黄铜样品于烧杯中, 向其中分
5次加入相同溶质质量分数的稀硫酸,使之充分反应。
每次所用稀硫酸的质量及剩余固体的 质量记录于下表:
(1) 上述表格中 m 的值为 ______________ ; (2) 黄铜样品中锌的质量分 — ; (3) 所用稀硫酸中硫酸的质量分数 — _____________
7、(10鞍山.63)我国钢铁产量居全球第一,占全球总产量的 30%以上。
某兴趣小组到钢铁
厂做社会调查,取钢样
(假设只含铁和碳)进行实验。
他们向组成完全相同的四份钢样粉 末中分别加入100g 稀H 2SO 4溶液,充分反应后,测得的实验数据如下表所示:
请计算:稀硫酸完全反应的实验中,反应后溶液中溶质的质量分数是多少
保留至0. 1)
?(结果
参考答案
3、(1)352
(2)解:设1鬼样品中碳酸钙的质量为X CaCOj + 2HC1 = CaCU + H30 + C02T
100 44
X 3.52 g
100 _ 44
IT _ 3.52g
X = 8g
"石头纸"样品中碳酸钙的质量分数为:寤甸00強=80% 10g
答:“石头纸"样品中碳酸钙的质量分数为30%
(3)44,4 S
4. (1) 2.64
(2) 解:设10g样品中碳酸钙的质量为x
CaCO3+2HCI==CaCI 2+H2O+CO2T
100 44
x 3.52g
100 X 352?
x=8g
-^xl00%=80%
此石头纸中碳酸钙的质量分数为:'..:!/
(3) 44.48
5. ( 1 )否90%
⑵解:10.0g样品中碳酸钙的质量是:10.0g-1.0g=9.0g 设生成二氧化碳的质量为x。
CaCO3+2HCI==CaCI 2+H2O+CO2T
100 44
9.0g x
100 : 44= 9.0g : x
X=3.96g
答:
6. 解:生成二氧化碳的质量为:
16 克+220 克-231.6 克=4.4 克
设鸡蛋壳中碳酸钙的质量为x。
CaCO3+2HCI==CaCI 2+H2O+CO2T
10044
X 4.4克
100
44= X:4.4 克
:
X=10.0克
答:7. 1)反应生成的氢气质量=97g —96.8g=0.2g
2)解:设生铁中铁的质量为X,生成硫酸亚铁质量为y,则
Fe + H 2SO4 = FeSO 4 + H 2 f
56 152 2
x y 0.2g
x=0. 2g X 56/2=5.6g
y=0.2g X 152/2=15.2g
Fe%=5.6/6 X 100%=93.3%
(3)不溶性杂质的质量=6g-5.6g=0.4g
FeSO4%=15.2/ (50+7-0.4-0.2 )X 100%=21.6%
答:(1)生成氢气0.2g , ( 2)生铁中铁的质量分数为93.3%,( 3)反应所得溶液中FeSO的质量分数约为21.6%。
&解:(1) 0.2
(2)设10g黄铜样品粉末中锌的质量为x。
Zn +2HCl == ZnCl 2 +
65 2
X 0.2g
65 : 2= X : 0.2g
X=6.5g
合金中铜的质量分数为:
[(10g-6.5g )- 10g] X 100%=35%
答:
9.( 1) 12.0 (或12)
(2) 40%
(3) 解:设所用稀硫酸中硫酸的质量分数为x,据题意得:
Zn + H2SO4 = ZnSO4 + H21
65 98
20g-17.4g
=2.6g 20g • x
65 _ 98
2.6g 20g * x
x=19.6%
答:所用稀硫酸中溶质的质量分数为19.6%。
10.解;设参抑反应的铁的质量为小生成bVSO;的质量为y
H 击0, —FeSO t+H a f
56 152 2
JL y0.
56 _ T
T_o72g
J= 5.
152_
2一0■如
15.宛
生成礎:S"溶液的溶质质量分数是亦縣幽=1&冷%答:生成F曲。
溶楝的陪质质量分数是14.4%*。
