第08章 镧系元素的性质及其性质变化规律性
镧系元素
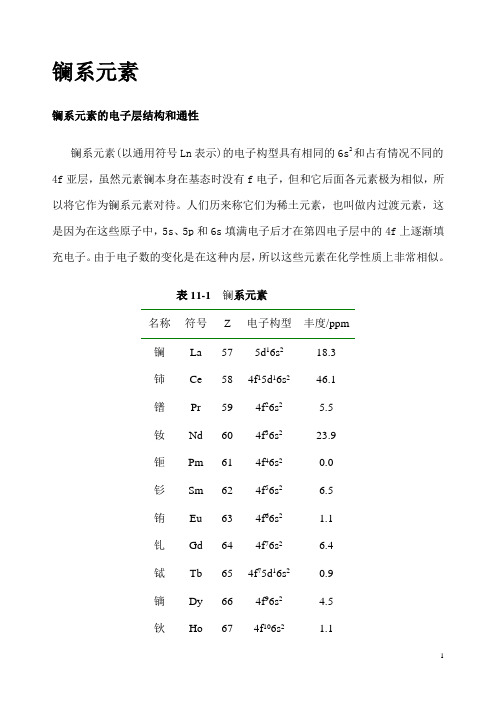
镧系元素镧系元素的电子层结构和通性镧系元素(以通用符号Ln表示)的电子构型具有相同的6s2和占有情况不同的4f亚层,虽然元素镧本身在基态时没有f电子,但和它后面各元素极为相似,所以将它作为镧系元素对待。
人们历来称它们为稀土元素,也叫做内过渡元素,这是因为在这些原子中,5s、5p和6s填满电子后才在第四电子层中的4f上逐渐填充电子。
由于电子数的变化是在这种内层,所以这些元素在化学性质上非常相似。
表11-1 镧系元素名称符号Z 电子构型丰度/ppm镧La 57 5d16s218.3铈Ce 58 4f15d16s246.1镨Pr 59 4f26s2 5.5钕Nd 60 4f36s223.9钷Pm 61 4f46s20.0钐Sm 62 4f56s2 6.5铕Eu 63 4f66s2 1.1钆Gd 64 4f76s2 6.4铽Tb 65 4f75d16s20.9镝Dy 66 4f96s2 4.5钬Ho 67 4f106s2 1.1铒Er 68 4f116s2 2.5铥Tm 69 4f126s20.2镱Yb 70 4f136s2 2.7镥Lu 71 4f145d16s20.8它们性质上的微小差别,主要是由“镧系收缩”引起的。
因为核内每增加一个质子,相应进入4f亚层的电子却太分散,不象定域程度更高的内层电子那样能有效地屏蔽核电荷,所以随着镧系元素原子序数的增加,原子核对最外层电子的引力就不断地增大,这就使得原子体积从镧到镥依次减小。
三价阳离子的收缩是十分规则的,从La3+的106pm收缩到Lu3+的35pm。
图11.1A所示金属半径,虽然总的趋向是减小,但Eu和Yb的半径比其余原子的要大得多。
它们是形成二价阳离子的倾向最大的两个镧系元素。
在固体中,这两种原子可能只将两个电子给予导带,而所形成的2+离子和其余镧系金属的3+离子相比,其半径较大、离子间的结合力较弱。
金属铕(Eu)和镱(Yb),与表中相邻的金属比,显然具有较低的密度,较低的熔点(图11.1B)和较低的升华能。
镧系元素和锕系元素知识总结

镧系元素和锕系元素知识总结
镧系元素是指的是镧(La)和镝(Dy)之间的元素,包括了镧、铈、镨、钕、钐、铕、钆、铽、镝、钬、铒和铥。
锕系元素是指镤(Pa)和铀(U)之间的元素,包括了镤、铀、镅、锔、锫、锎、锿、镄、钔、锘、铹和八氦。
这两个系列的元素都是内过渡金属元素,具有一些共同的特点和性质。
1. 化学性质:
- 镧系元素和锕系元素都具有较高的原子序数和较复杂的电子结构,因此在化学反应中表现出多样的化学性质。
- 这些元素的氧化态多种多样,一般有+2到+4的氧化态,也有较高的氧化态。
- 镧系元素和锕系元素都具有较强的还原性和氧化性。
2. 物理性质:
- 镧系元素和锕系元素都是铁磁性金属,具有较强的磁性。
- 这些元素的原子半径和离子半径较大,因此在金属中常以+3价状态存在。
- 镧系元素和锕系元素的原子核比较稳定,存在较多的同位素,包括放射性同位素。
3. 应用:
- 镧系元素和锕系元素在工业上有广泛的应用,尤其是镧、钇和铀等元素。
- 镧系元素广泛应用于电子产业、催化剂产业、照明产业等领域,如镧系金属在气体燃料电池中的应用和镧系氧化物作为催化剂的应用等。
- 锕系元素主要应用于核能产业,如铀和镅等元素被用作核燃料和核燃料后处理等。
镧系元素

镧系元素在周期系中,你知道什么是镧系元素?什么是稀土元素吗?它们的电子层结构和性质有什么特点?它们在科学技术和生产中扮演了什么样的角色?“镧系元素”在周期表中从原子序数为57号的镧到原子序数为71号的镥共15种元素,它们的化学性质十分相似,都位于周期表中第ⅢB族,第6周期镧的同一格内,但它们不是同位素。
同位素的原子序数是相同的,只是质量数不同。
而这15种元素,不仅质量数不同,原子序数也不同。
称这15种元素为镧系元素,用Ln表示。
它们组成了第一内过渡系元素。
“稀土元素”镧系元素以及与镧系元素在化学性质上相近的、在镧系元素格子上方的钇和钪,共17种元素总称为稀土元素,用RE表示。
按照稀土元素的电子层结构及物理和化学性质,把钆以前的7个元素:La、Ce、Pr、Nd、Pm、Sm和Eu称为轻稀土元素或铈组稀土元素;钆和钆以后的7个元素:Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu,再加上Sc和Y共10个元素,称为重稀土元素或钇组稀土元素。
“稀土”的名称是18世纪遗留下来的。
由于当时这类矿物相当稀少,提取它们又困难,它们的氧化物又和组成土壤的金属氧化物Al2O3很相似,因此取名“稀土”。
实际上稀土元素既不“稀少”,也不像“土”。
它们在地壳中的含量为0.01534,其中丰度最大的是铈,在地壳中的含量占0.0046,其次是钇、钕、镧等。
铈在地壳中的含量比锡还高,钇比铅高,就是比较少见的铥,其总含量也比人们熟悉的银或汞多,所以稀土元素并不稀少。
这些元素全部是金属,人们有时也叫它们稀土金属。
我国稀土矿藏遍及18个省(区),是世界上储量最多的国家。
内蒙包头的白云鄂博矿是世界上最大的稀土矿。
在我国,具有重要工业意义的稀土矿物有氟碳铈矿Ce(CO3)F,独居石矿RE(PO4),它们是轻稀土的主要来源。
磷钇矿YPO4和褐钇铌矿YNbO4是重稀土的主要来源。
我们从以下几个方面来讨论镧系元素的通性:1、价电子层结构2、氧化态3、原子半径和离子半径4、离子的颜色5、离子的磁性6、标准电极7、金属单质电子层结构这是目前根据原子光谱和电子束共振实验得到的镧系元素原子的电子层结构:根据电子填充的一般规律,由于4f能级的能量介于6s和5d之间,由表Ln-1中可见,从第57号元素镧开始,新增加的电子填充在4f能级上,应该4f能级充满后再填充到5d能级上去。
大学无机化学经典课件第八章+镧系与锕系

的习惯 。
根据 IUPAC 推荐,把 57 至 71 的 15 个元素称为
镧系元素,用Ln 表示 ,它们再加上 21 号的 Sc 和 39
号的 Y 称为稀土元素,用 RE 表示 。
稀土元素的分布、矿源及分组
由于稀土元素性质相似,所以常共生于同种矿物中。 按其存在形态,主要有三种类型的矿源: (1)稀土共生构成独立的稀土元素矿物。 (2)以类质同晶的形式分散在方解石、磷灰石等矿物中。 (3)呈吸附状态存在于粘土矿、云母矿等矿物中。
92 90
镧系收缩的原因:f电子 的屏蔽常数小于1,对核 电荷的屏蔽不够完全,使 有效核电荷增加,核对电 子的引力增大,使原子半 径、离子半径逐渐减少。
84
原子半径减少的趋势 不如离子半径,原因为: 原子的电子层比离子多一 层6s2 。
镧系收缩产生的结果:
(1)收缩缓慢是指相邻两个元素而言,两两之间的
3)酸性介质中,Yb和Eu的E明显稍高于各 自相邻的两个金属 Ln(s) 升华能 电离能 3+ 水合能 Ln(g) Ln (g) Ln3+(aq)
几种稀土元素在水溶液中 形成+3水合离子能量比较 Sm Eu Gd Tm Yb Lu
升华能+ +4095 +4230 +4165 +4294 +4366 +4356 电离能 水合能 -3562 -3617 -3632 -3779 -3812 -3838
57La58Ce59Pr60Nd
61Pm 62Sm 63Eu 64Gd
镧 铈 镨 钕
钷
钐
铕
钆
64Gd 65Tb 66Dy 67Ho68Er69Tm70Yb71Lu
钆
镧系元素的性质及其变化规律

这两种电子结构可以用来说明镧系元素化学性质的差异。 这些元素在参加化学反应时需要失去价电子,由于4f 轨道被 外层电子有效地屏蔽着, 且由于E4fE5d, 因而在结构为 4fn6s2 的情况下, f 电子要参与反应,必须先得由4f 轨道跃迁到5d 轨道。这样,由于电子构型不同,所需激发能不同,元素的 化学活泼性就有了差异。
原子序数是原子核内质子数的代表 ,偶原子序数的元素意味着核内质子数 为偶数。已经知道,核内无论是质子还 是中子,在基态时总以自旋相反配对存在,由于原子序数为偶数 的元素能满足这种自旋相反配对的要求,因而能量较低,所以就 特别稳定,既然该核特别稳定,那么它在地壳中的丰度就大。 稳定的原子核,吸收热中子后仍然很稳定,反之,奇原子序 数的核本身不稳定,吸收热中子后变得更不稳定,所以吸收热中 子的数目有限。
另一方面,激发的结果增加了一个成键电子,成键时可 以多释放出一份成键能。对大多数镧系的原子 , 其成键能大 于激发能,从而导致4f 电子向5d 电子跃迁, 但少数原子,如 Eu和Yb,由于4f 轨道处于半满和全满的稳定状态,要使4f 电子激发必须破坏这种稳定结构, 因而所需激发能较大, 激发 能高于成键能, 电子不容易跃迁, 使得Eu、Yb两元素在化学 反应中往往只以6s2电子参与反应。
2 镧系元素的价电子层结构
下表列出镧系元素在气态时和在固态时原子的电子层结构。
镧系元素气态原子的 4f 轨道的充填呈现两种构 型 , 即 4fn - 15d16s2 和 4fn6s2 ,这两种电子构型的相对 能量如图1所示: 其中 La、Ce、Gd、Lu 的基态处于4fn-15d16s2 时 能量较低,而其数的变 化作图,如左图所示。 一方面, 镧系元素原子半径从La的187.7 pm到Lu的173.4 pm,共缩小了14.3 pm,平 均每两个相邻元素之间缩小 14.3/14≈1 pm。 尽管平均相差只有1个pm,但其累积效应(共 14 pm)是很显著的。另一方面,原子半径不 是单调地减小,而是在 Eu 和 Yb 处出现峰和 在Ce处出现谷的现象。这被称为“峰谷效应 ”或“双峰效应”。
镧系元素和锕系元素

经过高温灼烧的 Ln2O3 在强酸
中的溶解性较差,灼烧温度较低的溶
解性较好。 镧系的氧化物与酸反应形成镧系
的盐类 。
例如
La2O3 + 6 HNO3 —— 2 La (NO3) 3 + 3 H2O Dy2O3 + 6 HCl —— 2 DyCl3 + 3 H2O 将溶液浓缩后,均可得到结晶水合物
具有 f3,f4,f5 和 f10,f11 结构的
+3 价离子呈现浅红色和黄色; 具有 f6,f7,f8 结构的 +3 价离子, 吸收峰全部或大部分在紫外区,所以 无色或略带粉红色。
镧系元素的一些简单化合物,如
Ln2O3 和 Ln (OH) 3 等的颜色基本与对
应的 Ln3+ 相同,这是因为它们的显色
HCl —— △
LnCl3 + 6 H2O
采用氧化物氯化的方法制备纯无 水盐,需要在反应体系中加入碳粉, 通过热力学耦合,使反应进行完全。
HCl Ln2O3 + 3 C + 3 Cl2 —— △
2 LnCl3 + 3 CO
制备无水氯化物的最佳方法 应是金属的直接氯化 。
(2) 含氧酸盐
硫酸与镧系金属,镧系氧化物、 氢氧化物反应,均可得到镧系的硫 酸盐。硫酸与镧系碳酸盐等弱酸盐 反应,亦可得镧系的硫酸盐。
化学反应的实质总是与酸或碱有关 。
氢氧化钠分解法和硫酸分解法
的反应实质分别为
△
LnPO4 + 3 NaOH ——
Ln (OH) 3↓ + Na3PO4
△ 2 LnPO4 + 3 H2SO4 ——
( )3 + 2 H3PO4 Ln 2 SO4
在周期系中,你知道什么是镧系元素?什么是稀土元素吗?它们的电子层结构和性质有什么特点?

在镧系收缩中,为什么原子半径的收缩比离子半径的收缩小得多呢?
想想看?这是因为离子比金属原子少一电子层,电子失去最外层6s电子之后,4f轨道则处于倒数第二层(倒数第一层为5s、5p轨道),这种状态的4f轨道比原子中的4f轨道(倒数第三层)对核电荷的屏蔽作用小,从而使得离子半径的收缩效果比原子半径明显。
我国稀土矿藏遍及18个省(区),是世界上储量最多的国家。内蒙包头的白云鄂博矿是世界上最大的稀土矿。在我国,具有重要工业意义的稀土矿物有氟碳铈矿Ce(CO3)F,独居石矿RE(PO4),它们是轻稀土的主要来源。磷钇矿YPO4和褐钇铌矿YNbO4是重稀土的主要来源。
我们从以下几个方面来讨论镧系元素的通性:
从表Ln-2所列镧系元素第三电离能I3的数据看,它们随原子序数的增加起伏较大,镧系元素由Ln2+
→Ln3+主要是由第三电离能I3决定的。I3的数值以Eu和Yb最大,其次为Tm和Sm,所以这些元素的+2价相对比较稳定。
另外从Ln-3可以看出,Eu2+和Yb2+的稳定性还与它们离子的电子层结构是半充满(Eu2+为4f7)和全充满(Yb2+为4f14)构型有关。Eu14和Yb2+就比Sm2+(4f6)和Tm2+(4f13)稳定。
从表Ln-8中的数据可见,镧系金属的密度、熔点除Eu和Yb以外,基本上随着原子序数的增加而增加。Eu和Yb的密度、熔点比它们各自左右相邻的两种金属都小。这是由于它们具有4f半充满和4f全充满的电子构型,使屏蔽效应增大,有效核电苛降低,导致原子核对外层6s电子的吸引力减小,而使它们的原子半径突然增大,以致它们的原子半径与碱土金属的原子半径相近,例如:
镧系锕系元素-内容要点

内容提要、重点难点、本章要求1.内容提要(1)镧系、锕系元素的名称、符号、电子层构型、氧化态及变化规律;(2)镧系收缩及后果;(3)镧系元素化合物;(4)稀土元素;(5)习题与测试;2.重点难点(1)镧系元素原子半径及离子半径变化规律;(2)镧系收缩及后果;3.本章要求(1)掌握镧系元素名称、符号、价电子构型及半径变化规律;(2)掌握镧系收缩及后果;(3)了解镧系元素性质;(4)了解稀土元素的用途;4.建议学时----2学时15.1 镧系、锕系元素的名称、符号、电子层构型、氧化态及变化规律1.名称和符号周期表中有两个系列的内过渡元素,即第六周期的镧系和第七周期的锕系。
镧系包括从镧(原子序数57)到镥(原子序数为71)的15种元素;锕系包括从锕(原子序数89)到铹(原子序数103)的15种元素。
2.电子层构型镧系、锕系电子层构型比较复杂,第三层4f、5f轨道上。
表15-1 镧系元素原子的电子层结构57镧La58铈Ce59镨Pr60钕Nb61钷Pm62钐Sm63铕Eu64钆Gd65铽Tb66镝Dy67钬Ho68铒Er69铥Tm70镱Yb71镥Lu从表15-1可知,除镧原子外,其余镧系元素原子的基态电子层结构中都有f电子。
镧虽然没有f电子,但它与其余镧系元素在化学性质上十分相似。
镧系元素最外两个电子层对4f轨道有较强的屏蔽作用,尽管4f能级中电子数不同,它们的化学性质受4f电子数的影响很小,所以它们的化学性质很相似。
【问题】为什么La最外层电子构型不是4f16s2,而是4f05d16s2; Gd最外层电子构型不是4f86s2,而是4f75d16s2?根据洪特规则,电子处于半满、全空时较为稳定。
表15-2 锕系元素原子的电子层结构原子序数元素名称元素电子层结构89锕Ac90钍Th91镤Pa92铀U93镎Np94钚Pu95镅Am96锯Cm97锫Bk98锎Cf99锿Es100镄Fm101钔Md102锘No103铹Lr3.氧化态镧系元素前三级电离势之和是比较低的,比某些过渡元素要低。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4 Ln3+离子的碱度
某种金属离子吸引电子或阴离子的能力被称为该金属 离子的“相对碱度”。引力越强,碱度越弱。 碱度的强弱可用金属离子的离子势φ(=Z/r)来量度, 离子势值越大(即半径小,电荷高)则碱度越弱。 对于镧系电荷相同的离子, 随着原子序数增加,离子半 径减小,离子势逐渐增大,离子的碱度减弱。
原子序数是原子核内质子数的代表 ,偶原子序数的元素意味着核内质子数 为偶数。已经知道,核内无论是质子还 是中子,在基态时总以自旋相反配对存在,由于原子序数为偶数 的元素能满足这种自旋相反配对的要求,因而能量较低,所以就 特别稳定,既然该核特别稳定,那么它在地壳中的丰度就大。 稳定的原子核,吸收热中子后仍然很稳定,反之,奇原子序 数的核本身不稳定,吸收热中子后变得更不稳定,所以吸收热中 子的数目有限。
单向变化
除离子半径外,属于镧系元素性 质单向变化的还有有效核电荷,标准 电极电势,配合物的稳定常数,一些 化合物的密度和熔点、溶解度,氢氧 化物沉淀的pH值,离子势等同离子状 态有关的物理、化学性质。此时镧系 元素性质的相似性大于相异性。性质 递变是以单调渐变为主。故称为单向 变化。
原子序数
镧系元素这些由离子制约的性质,其所以呈单向变化是因 为离子的电子结构的单向变化。即从La3+到Lu3+, +3价离子的 电子构型是4f0→4f14,由于4f电子对核的屏蔽不完全,使有效核 电荷单向增加,核对外面的引力逐渐增加之故。
187.7 106.1 182.4 103.4 182.8 101.3 182.1 99.5 181.0 97.9 180.2 111 96.4 204.2 109 95.0 180.2 93.8 178.2 92.3 177.3 90.8 176.6 89.4 175.7 88.1 174.6 94 86.9 194.0 93 85.8 173.4 84.8
另一方面,激发的结果增加了一个成键电子,成键时可 以多释放出一份成键能。对大多数镧系的原子,其成键能大 于激发能,从而导致4f 电子向5d 电子跃迁, 但少数原子,如 Eu和Yb,由于4f 轨道处于半满和全满的稳定状态,要使4f 电子激发必须破坏这种稳定结构, 因而所需激发能较大, 激发 能高于成键能, 电子不容易跃迁, 使得Eu、Yb两元素在化学 反应中往往只以6s2电子参与反应。
离子半径
离子半径
将镧系元素的离子半径随原子序数 的变化作图,如左图所示。 在上述镧系元素离子半径随原子序 数变化的图中一方面可以看到,镧系元 素+3价离子从f0 的La3+ 到f14 的Lu3+ , 依次增加4f电子(与原子的电子排布不一 样),因而随着原子序数的增加离子的 半径依次单调减小(没有峰谷现象),收 缩的程度比原子半径更大 , 由 La3 + 的 106.1 pm到Lu3+的84.8 pm,共缩小了21.3 pm,平均每两个相邻元 素间缩小了21.3/14≈1.5 pm。这是镧系元素性质的单向变化规 律。另一方面,离子半径的变化,在具有f7 的中点Gd3+ 钆处 ,微有不连续性,这是由于Gd3+具有f7半满稳定结构, 屏蔽稍 大, 半径略有增大之故。这是镧系元素性质的Gd断效应规律 。
镧系元素的原子,在固 态时的电子构型与气态时的 电子构型不尽相同。在固态 时,除Eu和Yb仍保持4fn6s2 以 外 , 其 余 原 子 都 为 4fn - 15d16s2的构型。 从气态变到固态,其实 质是原子间通过金属键的形 式结合成为金属晶体。成键 倾向于使用低能级轨道。镧 系元素气态原子在形成金属 键时的成键电子数,除Eu和 Yb为2、Ce为3.1外, 其余皆 为3。所以Eu和Yb只使用6s2 成键,气、固态一致,其余 元素在固态时减少一个f电 子,增加一个d电子。
Gd断效应
在镧系元素的离子半径的变化中,在具有f7的中点64Gd3+处 微有不连续性, 由其相邻离子半径的差值的大小可以看出: Pm3+ Sm3+ Eu3+ Gd3+ Tb3+ Dy3+ r/pm 97.9 96.4 95.0 93.8 92.3 90.8 1.5 1.4 1.2 1.5 1.5 rM 3+ K稳 △/pm
3 原子半径和离子半径
镧系元素的原子半径、离子半径
原子 元素 金属原子 离子半径/ pm 序数 符号 半径/pm RE2+ RE3+ RE4+
57 58 59 60 61 62 63 64 65 66 67 68 69 70 71
La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu
除原子半径外,原子体积、密度、原子的热膨胀系 数、第三电离子能、前三个电离能的总和、原子的电负 性、一些化合物的熔点、沸点等也出现这种峰谷效应。
峰谷效应 (双峰效应)
对峰谷效应的解释如下: 电子精细结构: 据计算,Eu、Gd、Yb、Lu Eu Yb 的电子精细结构分别为: Eu 4f75d0.52626s1.21476p0.2591 Ce Gd 4f75d26s1 Yb 4f145d0.26356s1.22516p0.5114 Lu 4f145d1.82356s16p0.1765 由于金属的原子半径与相邻原子之间的电 子云相互重叠(成键作用)程度有关。而Eu和Yb 只用少量 d 电子参与成键,成键电子总数为2,其他原子(如Gd、 Lu)能使用较多的 d 电子参与成键,成键电子总数为3 (Ce为3.1), 成键作用的差别造成了原子半径的差别 。 ●Eu和Yb的碱土性:Eu和Yb在电子结构上与碱土金属十分 相似,这种相似性使得Eu和Yb的物理和化学性能更接近于碱土金 属。其原子半径也接近于碱土金属。 ●洪特规则:Eu和Yb的 f 电子数分别为f7和f14,这种半满和 全满的状态能的是,若能利用Ln3+ 离子 与非+3价离子的化合物在性质上的较大差异来分离镧系元素比 纯粹利用Ln3+离子的碱性的微小差异来分离更为容易,例如: ●Ce4+比其他+3价Ln3+能在较低的pH下生成氢氧化物沉淀。 ●Ce4+ 在HNO3 溶液中用磷酸三丁酯萃取时,+4价的Ce4+ 比其他+3价镧系离子更易被萃取到有机相之中,因而能首先与 其他+3价镧系离子分离。 这当然是因为+4价Ce4+ 的离子势比其余+3价镧系的离子势 更大,碱度更弱,更易与OH- 离子生成氢氧化物沉淀和与磷酸 三丁酯生成萃合物而进入有机相之故。 总之,镧系离子的分离主要是根据各个离子的碱度的微小 差异,利用生成配合物或萃合物的能力上的差别以离子交换或 溶剂萃取的方法来进行的,有时还辅以溶解度,或氧化态的差 别。如控制pH值使氢氧化物分级沉淀或某些盐类的分级结晶, 将Ce3+氧化成Ce4+,Eu3+还原成Eu2+等来达到分组或分离成单 一元素的目的。
5 氧化态
下图示出镧系元素氧化态的周期性变化的规律。
可以看到: 镧系元素的特征氧化态是+3。这是由于镧系元素 的原子的第一、第二、第三电离能之和不是很大,成键时释放出 来的能量足以弥补原子在电离时能量的消耗,因此,他们的+3氧 化态都是稳定的。除特征氧化态+3之外,Ce、Tb以及Pr等还可显 +4氧化态,Eu、Yb以及Sm等可显+2氧化态。 这些显示非+3价氧化态诸元素有规律地分布在La、 Gd、 Lu 附近.这种情况可由原子结构的规律变化得到解释:La3+、Gd3+、 Lu3+分别具有4f轨道全空、半满、全满的稳定电子层结构,因而比 稳定结构多一个f电子的Ce3+和Tb3+有可能再多失去1个4f电子而 呈现+4氧化态,而比稳定结构少一个f电子的Eu3+和Yb3+有可能少 失去一个电子而呈现+2氧化态。显然镧系离子在氧化态变化周期 性规律正是镧系元素电子层排布呈现周期性规律的反映。
碱度呈现单向变化的规律。
利用Ln3+离子半径的微小差别, 亦即碱度的微小差别, 可以对镧系离子进行分离。
如Ln3+水 解生成 Ln(OH)3 沉淀的趋势随原 子序数的增加 ( 即碱度减弱) 而 增加,当加入 NaOH时, 溶解 度最小、碱度最 弱的Lu将最先 以Lu(OH)3的形 式沉淀出来,而 溶解度最大,碱 度最强的La将最 后以La(OH)3沉 淀。
64Gd
原子序数
类似的现象还出现在镧系元素的 配位化合物的稳定常数中。 这种现象被称之为Gd断效应。
64Gd位于15个镧系元素所构成的序列的正中央,其+3 价离子有半充满的f7 稳定结构,这种结构的电子屏蔽效应
大,有效核电荷相对较小,从而使半径收缩幅度减小,碱 度增加,导致配合物稳定常数等性质有所降低,从而出现 Gd断的现象。
2 镧系元素的价电子层结构
下表列出镧系元素在气态时和在固态时原子的电子层结构。
镧系元素气态原子的 4f轨道的充填呈现两种构 型 , 即 4fn - 15d16s2 和 4fn6s2 ,这两种电子构型的相对 能量如图1所示: 其中 La、Ce、Gd、Lu 的基态处于4fn-15d16s2 时 能量较低,而其余元素皆 为4fn6s2。
原子半径
将镧系元素的原子半径随原子序数的变 化作图,如左图所示。 一方面, 镧系元素原子半径从La的187.7 pm到Lu的173.4 pm,共缩小了14.3 pm,平 均每两个相邻元素之间缩小14.3/14≈1 pm。 尽管平均相差只有1个pm,但其累积效应(共 14 pm)是很显著的。另一方面,原子半径不 是单调地减小,而是在Eu和Yb处出现峰和 在Ce处出现谷的现象。这被称为“峰谷效应 ”或“双峰效应”。
92 90
84
左表示出镧系元素的原子半 径、离子半径。随着原子序数依 次增加,15个镧系元素的原子半 径和离子半径总趋势是减小的, 这叫“镧系收缩”。 研究表明:镧系收缩90%归 因于依次填充的(n-2)f电子其屏 蔽常数可能略小于1.00(有文献报 告为0.98),对核电荷的屏蔽不够 完全,使有效核电荷Z* 递增,核对 电子的引力增大使其更靠近核; 而10%来源于相对论性效应,重 元素的相对论性收缩较为显著。 由于镧系收缩的影响,使第 二、三过渡系的Zr和Hf、Nb与Ta、 Mo与W三对元素的半径相近,化 学性质相似,分离困难。
