氢氧化钠比热容
《常见碱主要性质及用途》 知识清单

《常见碱主要性质及用途》知识清单一、氢氧化钠(NaOH)1、物理性质氢氧化钠,俗称烧碱、火碱、苛性钠,是一种白色片状固体,易溶于水,溶解时放出大量的热。
暴露在空气中,容易吸收水分而潮解,也能与空气中的二氧化碳反应而变质。
2、化学性质(1)与酸碱指示剂作用:能使石蕊试液变蓝,酚酞试液变红。
(2)与酸性氧化物反应与二氧化碳反应:2NaOH + CO₂= Na₂CO₃+ H₂O(用于吸收二氧化碳)与二氧化硫反应:2NaOH + SO₂= Na₂SO₃+ H₂O(3)与酸发生中和反应与盐酸反应:NaOH + HCl = NaCl + H₂O与硫酸反应:2NaOH + H₂SO₄= Na₂SO₄+ 2H₂O(4)与某些盐反应与硫酸铜反应:2NaOH + CuSO₄= Cu(OH)₂↓ + Na₂SO₄(生成蓝色沉淀)与氯化铁反应:3NaOH + FeCl₃= Fe(OH)₃↓ + 3NaCl(生成红褐色沉淀)3、用途(1)用于造纸、纺织、印染等工业。
(2)在生活中,可用于除去油污,如炉具清洁剂中就含有氢氧化钠。
(3)在实验室中,用作某些气体的干燥剂,如干燥氢气、氧气等,但不能干燥二氧化碳、二氧化硫等酸性气体。
二、氢氧化钙Ca(OH)₂1、物理性质氢氧化钙,俗称熟石灰、消石灰,是一种白色粉末状固体,微溶于水,其水溶液俗称石灰水。
2、化学性质(1)与酸碱指示剂作用:能使石蕊试液变蓝,酚酞试液变红。
(2)与酸性氧化物反应与二氧化碳反应:Ca(OH)₂+ CO₂= CaCO₃↓ + H₂O(用于检验二氧化碳)(3)与酸发生中和反应与盐酸反应:Ca(OH)₂+ 2HCl = CaCl₂+ 2H₂O(4)与某些盐反应与碳酸钠反应:Ca(OH)₂+ Na₂CO₃= CaCO₃↓ + 2NaOH(用于制取氢氧化钠)3、用途(1)在农业上,用于改良酸性土壤。
(2)在建筑上,用石灰浆粉刷墙壁。
(3)在树木上涂刷含有硫磺粉等的石灰浆,可保护树木,防止冻伤,并防止害虫生卵。
2010热量衡算数据

(1—12)
qvb =Tb·(39.8lgTb-0.029Tb)/M kJ/kg 式中 Tb—液体的沸点 K;
M—液体的分子量。
(1—13)
3、熔融热的计算
不同物质的熔融热可根据以下公式求出:
元
素
qF =(8.4~12.6)TF
热量衡算中,过程热效应 Q3 的符号为:放热为正;吸热为负。 (1)、学反应热 QR 为计算各种温度下的反应热,规定当反应温度为 298K 及标准大气压时反应热的数值
为标准反应热,习惯上用 ΔH°表示,负值表示放热,正值表示吸热。这与在热量衡算中所 规定的符号正好相反,为避免出错,现用符号 q○r 表示标准反应热,放热为正,吸热为负, 则 q。r =-ΔH°。
2)、燃烧需氧原子数法标准燃烧热
里查德认为:有机化合物的燃烧热与完全燃烧该有机化合物所需的氧原子数成直线
关系。即:
q°c =∑a+x∑b kJ/mol
(1—19)
式中 a、b—常数,与化合物结构相关,其值见《药厂反应设备及车间工艺设计》(P213~217
表 6—6 和表 6—7);
X—化合物完全燃烧时所需的氧原子数。
无机化合物
qF =(20.9~29.3)TF
有机化合物
qF =(37.7~46.0)TF
其中:qF —— 熔融热 J/mol;
TF —— 熔点 K。
(1—14) (1—15) (1—16)
5
4、溶解热的计算
气态溶质的溶解热可取蒸发潜热的负值;固态溶质的溶解热则近似可取其熔融热的 值。
5、浓度变化热效应的计算
由无限稀释热可以求出浓度变化的热效应。本设计涉及到氢氧化钠、盐酸的水溶液浓
氢氧化钠理化性质

最大爆炸压力(MPa)
无意义
聚合危害
不聚合
稳定性
稳定
禁忌物
强酸、易燃或可燃物、二氧化碳、过氧化物、水
燃爆特性
与酸发生中和反应并放热。遇潮时对铝、锌和锡有腐蚀性,并放出易燃易爆的氢气。本品不会燃烧,遇水和水蒸气大量放热,形成腐蚀性溶液。具有强烈腐蚀性
灭火方法
可用水冷却未燃着的容器。消防人员必须穿戴全身防火防毒服。大火时,须在有防护措施的地方进行施救
灭火剂
抗溶性泡沫、干粉、二氧化碳灭火。用水灭火无效
毒性
LD50:40mg/kg(小鼠腹腔);LC50:无资料
对人体危害
侵入途径:吸入、食入
危害表现:本品有强烈刺激和腐蚀性。粉尘刺激眼和呼吸道,腐蚀鼻中隔;皮肤和眼直接接触可引起灼伤;误服可造成消化道灼伤,粘膜糜烂,出血和休克
急救
措施
皮肤接触:立即脱去被污染的衣着,用大量流动清水冲洗,至少15分钟。就医
饱和蒸气压KPa
0.13(739℃)
相对水密度(水=1)
2.12
临界温度℃
/
相对空气密度(空气=1)
无资料
临界压力MPa
/
燃烧热
无意义
燃烧
爆炸
危险性
燃烧性
不燃,无特殊爆炸性
燃烧分解产物
可产生有害的毒性烟雾
爆炸极限(V%)
无意义
闪点(℃)
无意义
引燃温度(℃)
无意义
自燃温度(℃)
无意义
最小引燃能量(mJ)
储运注意事项
储存于干燥清洁的仓库内。注意防潮和雨淋。应与易燃或可燃物及酸类分开存放。分装或搬运作业注意个人防护。搬运时要轻装轻卸,防止包装及容器损坏。雨天不宜运输
氢氧化钠

氢氧化钠(氢氧化钠片碱)氢氧化钠(NaOH),俗称烧碱、火碱、苛性钠,因另一名称caustic soda而在香港称为哥士的,常温下是一种白色晶体,具有强腐蚀性。
易溶于水,其水溶液呈性,能使变红。
氢氧化钠是一种极常用的碱,是的必备药品之一。
它的溶液可以用作。
氢氧化钠放大图英文名称:Sodium Hydroxide英文:Sodium Hydrate、Caustic Soda、Lye(液态):40.01摩尔质量:40CASRN:1310-73-2登录号:215-185-5:2.130克/厘米³:318.4℃:极易溶于水溶液呈无色:1390℃碱离解常数()= 3.0碱离解常数倒数对数()= -0.48致死量:40mg/kg中学鉴别氢氧化钠的方法:加入MgCl2,产生白色沉淀。
焰色反应,火焰呈黄色。
NaOH特性有强烈的腐蚀性,有,可用作,但是,不能干燥二氧化硫、二氧化碳、二氧化氮和氯化氢等酸性气体。
(会与酸性气体发生反应。
)且在空气中易而液化(因吸水而溶解的现象,属于物理变化);溶于水,同时放出大量热。
能使酚酞变红,使紫色石蕊试液变蓝,属于强碱。
腐蚀铝性物质,不腐蚀塑料。
只需放在空气中数分钟,就会吸收水分,成为液态毒药。
其熔点为318.4℃。
除溶于水之外,氢氧化钠还易溶于乙醇、甘油;但不溶于乙醚、丙酮、液氨。
其液体是一种无色,有涩味和滑腻感的液体。
氢氧化钠在空气中可与二氧化碳反应而变质!2NaOH + CO2==== Na2CO3 + H2O钠(Na)与水反应(与水反应时,应用烧杯并在烧杯上加盖玻璃片,反应时钠块浮在水面上,熔成球状,游于水面,有“嘶嘶”的响声,并有生成物飞溅),生成强碱性NaOH 溶液NaOH晶体放大图片,并放出氢气。
固体NaOH中OH以O-H共价键结合,Na与OH以强离子键结合,溶于水其解离度近乎100%,故其水溶液呈强碱性,可使无色的酚酞试液变成红色,或使PH试纸、紫色石蕊溶液等变蓝。
氢氧化钠理化性质

泄漏应急处理
隔离泄漏污染区;限制出入..建议应急处理人员佩戴自给式呼吸器;穿防酸碱工作服..不要直接接触泄漏物..小量泄漏:避免扬尘;用清洁铲子收集于干燥清洁有盖容器中;也可以用大量水冲洗;洗水稀释后放入废水系统..大量泄漏:收集回收或运至废物处理场所处置
灭火剂
抗溶性泡沫、干粉、二氧化碳灭火..用水灭火无效
毒性
LD50:40mg/kg小鼠腹腔;LC50:无资料
对人体危害
侵入途径:吸入、食入
危害表现:本品有强烈刺激和腐蚀性..粉尘刺激眼和呼吸道;腐蚀鼻中隔;皮肤和眼直接接触可引起灼伤;误服可造成消化道灼伤;粘膜糜烂;出血和休克
急救
措施
皮肤接触:立即脱去被污染的衣着;用大量流动清水冲洗;至少15分钟..就医
眼睛接触:立即提起眼睑;用大量流动清水或生理盐水彻底冲洗至少15分钟;就医
吸入:迅速脱离现场至空气新鲜处..保持呼吸道畅通..如呼吸困难;给输氧..如呼吸停止;立即进行人工呼吸..就医
食入:误服者用水漱口;给饮牛奶或蛋青..就医
防护
措施
工程控制:密闭操作..提供安全淋浴和洗眼设备
个体防护:可能接触其粉尘时;必须佩戴头罩型电动送风过滤式防尘呼吸器..必要时;佩戴空气呼吸器..穿橡胶耐酸碱服..戴橡胶耐酸碱手套
饱和蒸气压KPa
0.13739℃
相对水密度水=1
2.12
临界温度℃
/
相对空气密度空气=1
无资料
临界压力MPa
/
燃烧热
无意义
燃烧
爆炸
危险性
燃烧性ቤተ መጻሕፍቲ ባይዱ
不燃;无特殊爆炸性
氢氧化钠产品资料表
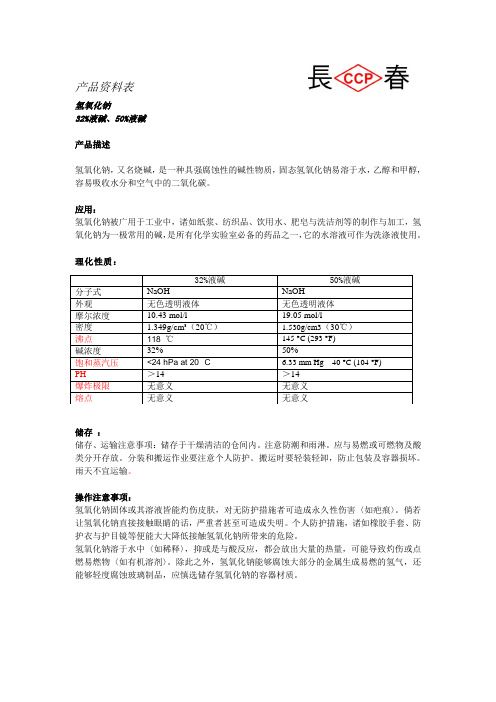
产品资料表氢氧化钠32%液碱、50%液碱产品描述氢氧化钠,又名烧碱,是一种具强腐蚀性的碱性物质,固态氢氧化钠易溶于水,乙醇和甲醇,容易吸收水分和空气中的二氧化碳。
应用:氢氧化钠被广用于工业中,诸如纸浆、纺织品、饮用水、肥皂与洗洁剂等的制作与加工,氢氧化钠为一极常用的碱,是所有化学实验室必备的药品之一,它的水溶液可作为洗涤液使用。
理化性质:储存:储存、运输注意事项:储存于干燥清洁的仓间内。
注意防潮和雨淋。
应与易燃或可燃物及酸类分开存放。
分装和搬运作业要注意个人防护。
搬运时要轻装轻卸,防止包装及容器损坏。
雨天不宜运输。
操作注意事项:氢氧化钠固体或其溶液皆能灼伤皮肤,对无防护措施者可造成永久性伤害〈如疤痕〉。
倘若让氢氧化钠直接接触眼睛的话,严重者甚至可造成失明。
个人防护措施,诸如橡胶手套、防护衣与护目镜等便能大大降低接触氢氧化钠所带来的危险。
氢氧化钠溶于水中〈如稀释〉,抑或是与酸反应,都会放出大量的热量,可能导致灼伤或点燃易燃物〈如有机溶剂〉。
除此之外,氢氧化钠能够腐蚀大部分的金属生成易燃的氢气,还能够轻度腐蚀玻璃制品,应慎选储存氢氧化钠的容器材质。
产品资料表盐酸无色液体、有刺激性气味、腐蚀性、极强的挥发性产品描述盐酸,学名氢氯酸,是氯化氢(化学式:HCl)的水溶液,是一元酸。
盐酸是一种强酸,浓盐酸具有极强的挥发性,因此盛有浓盐酸的容器打开后能在上方看见酸雾,那是氯化氢挥发后与空气中的水蒸气结合产生的盐酸小液滴。
盐酸是一种常见的化学品,在一般情况下,浓盐酸中氯化氢的质量分数在38%左右。
同时,胃酸的主要成分也是盐酸应用:人体用途:·使胃液保持激活胃蛋白酶所需要的最适合的pH值;·使食盐中的蛋白质变性而易于水解;·杀死随食物进入胃里的细菌的作用。
·盐酸可促进胰液、肠液的分泌以及胆汁的分泌和排放,酸性环境还有助于小肠内铁和钙的吸收。
日常用途:·制取洁厕灵,除锈剂等产品。
氢氧化钠cas编号

氢氧化钠cas编号
氢氧化钠,也称为苛性钠,化学式为NaOH,是一种强碱性化合物。
它的CAS号为1310-73-2。
氢氧化钠是一种重要的化工原料,在工业生产中广泛应用。
它可以用于制造纸张、化学纤维、塑料、肥料等产品。
此外,氢氧化钠也常被用作清洗剂、腐蚀剂、还原剂等。
由于氢氧化钠具有强碱性,对人体有较大的腐蚀作用,因此在使用时必须注意安全。
如果误食或接触到皮肤或眼睛,应立即用清水冲洗,并寻求医疗帮助。
总之,氢氧化钠是一种广泛应用的重要化工原料,它的CAS编号为1310-73-2。
在使用时必须谨慎,避免对人体造成危害。
- 1 -。
20wt%氢氧化钠比热容

20wt%氢氧化钠比热容
氢氧化钠(NaOH)的比热容是指单位质量物质在温度变化时吸
收或释放的热量。
具体到20wt%氢氧化钠溶液的比热容,首先要考
虑到溶液中溶质(NaOH)和溶剂(水)的比例。
一般来说,20wt%的
氢氧化钠溶液是指在溶液总质量中氢氧化钠的质量占20%。
在计算比热容时,需要考虑到溶质和溶剂的比热容以及它们的
质量比。
通常情况下,20wt%氢氧化钠溶液的比热容会介于纯水和纯NaOH的比热容之间,因为溶液的比热容受到溶质和溶剂的影响。
要准确计算20wt%氢氧化钠溶液的比热容,需要知道溶质和溶
剂的比热容数值,并考虑到它们在溶液中的质量分数。
一般来说,
可以通过实验测定得到溶液的比热容数值。
总的来说,20wt%氢氧化钠溶液的比热容是一个复杂的计算问题,需要考虑到多个因素的影响。
如果需要精确的数值,建议通过实验
或者查阅相关文献资料获取。
