万学海文2011年考研农学大纲详解:无机及分析化学(三)
0Zlzeg2011年考研农学备考指导:有的放矢有备无患

生活需要游戏,但不能游戏人生;生活需要歌舞,但不需醉生梦死;生活需要艺术,但不能投机取巧;生活需要勇气,但不能鲁莽蛮干;生活需要重复,但不能重蹈覆辙。
-----无名一、各科目备考指导2011年新大纲中考查目标、题型结构和分值以及知识点内容虽然没有发生变化,但从统考这几年来的考试情况和考生的复习备考情况来看,掌握各学科的特点和考查形式,有针对性的复习是十分有必要的。
无机及分析化学:基础是热化学、物质结构概念,重点为四大平衡原理(酸碱平衡、沉淀溶解平衡、氧化还原平衡和配位离解平衡),溶液分析可以作为贯穿知识点掌握和应用的连接主线,结合滴定分析、分光光度法、电势分析法等基础实验分析方法。
有机化学:有机化学是一门系统性较强的学科,各参考书中对知识点的阐述也较规律。
其中,基础是各类有机物的分类、结构、命名、物理性质,重点是有机物的化学性质、相应的特定化学反应过程,以及由此延伸的特征性、鉴定性反应,都是常考的知识点和重难点。
生物化学:基础是生物化学有关的基本概念、理论以及实验原理和方法,重点是白质、核酸、酶等生物大分子的化学组成、结构及功能,物质代谢及其调控,遗传信息的贮存、传递与表达部分。
植物生理学:基础是植物生理学的基本概念、基础理论知识和主要实验的原理与方法。
重点为光合作用、呼吸作用、有机物质的运输与分配、生长生理、生殖生理、休眠成熟和衰老生理等生命现象原理的解释、分析和利用。
动物生理:细胞的基本功能、血液循环、呼吸、消化、泌尿、神经系统与内分泌仍然是考察的重点和难点,动物生理学概述、血液、能量代谢与体温、生殖与泌乳这些考点多会以选择题的形式出现,占据比例较小,相对简单。
综上,我们以考试大纲为基准,结合历年真题分析,就可以发现考试的重点和难点,梳理出复习的主线,找到各个知识点之间的联系,使我们的复习更具有方向和目的。
二、各题型备考指导因两门专业课程的题型具体不同,我们分为客观题和主观题两类进行探讨。
客观题:主要有单项选择题、填空题、简答题。
《无机及分析化学》考试大纲

《无机及分析化学》考试大纲《无机及分析化学》考试大纲一、适用对象本考试大纲适用于报考应用技术大学化学工程与工艺专业“专升本”入学考试。
要求考生全面系统地掌握无机及分析化学的基本概念、基本理论、基本计算方法,并能很好地解释无机及分析化学中的一些现象和事实,具备较强的分析问题和解决问题的能力。
二、考试内容与要求第一章物质及其变化1.掌握理想气体状态方程式,混合气体分压、分体积定律,体积分数,物质的量分数及其计算。
2.掌握热力学第一定律,反应焓变,热化学方程式,盖斯定律,生成焓的概念及计算。
第二章化学反应速率和化学平衡1.了解化学反应速率的表示方法,平均速率。
2.掌握浓度对反应速率的影响(质量作用定律)、温度对反应速率的影响、催化剂对反应速率的影响,及其原因。
3.理解化学平衡及其特征,掌握化学平衡定律及其表达式,书写和应用标准平衡常数的规则,了解多重平衡规则。
掌握浓度,压力,温度对平衡的影响,理解其原因并能进行有关计算。
第三章电解质溶液和离子平衡1.了解强、弱电解质的区别。
2.掌握水的解离,一元弱酸、一元弱碱的离子浓度计算及pH值的计算。
3.掌握同离子效应对电离平衡的影响及计算,了解缓冲溶液的原理、选择和配制,掌握缓冲溶液pH值的计算。
4.了解不同盐类水解对溶液酸碱性的影响。
5.理解溶解-沉淀平衡,溶度积的原理,掌握溶度积规则的计算,沉淀生成的条件,沉淀完全的程度,同离子效应对沉淀的影响。
了解分步沉淀,沉淀的溶解及转化。
第四章氧化和还原反应1.了解氧化值的概念,化合物中各元素原子的氧化值,掌握用离子电子法配平氧化还原方程式。
2.理解氧化还原电对,掌握原电池的组成,表示方法。
3.掌握用原电池的标准电极电势来推断氧化还原反应能否进行(物质能否共存)及反应方向,原电池的电动势。
掌握非标准状态下上述计算(能斯特方程式,既影响电极电势的因素)。
4.掌握氧化还原反应进行程度的计算(平衡常数),了解元素电势图及其应用。
无机及分析化学大纲

一、课程说明1、课程简介《无机及分析化学》是生命科学系本科生必修的公共基础课。
它是一门基础理论课程,是培养生物专业学生具备无机及分析化学理论的重要课程,因此系统地传授无机及分析化学的基本理论是生物专业学生学好《有机化学》和《生物化学》课程及其它相关课程的基本保证。
《无机及分析化学》可分为化学热力学和动力学、四大平衡、原子结构和分子结构、配合物等;分析化学部分主要是误差及数据处理、四大滴定和一些仪器分析方法。
理论部分将由浅入深地做系统讲授,注重补充新知识,扩大信息量,加强化学与生命科学的联系;将四大滴定融入四大平衡,使无机化学与分析化学自然成为一体,实现两门课程的有机结合,并适当介绍一些与生命科学有关的分析方法。
随着生物学的发展,越来越多地需要运用化学概念和方法去解决生物学问题。
通过教学要求,学生能将化学基础与生物学知识相结合,应用分析化学的手段去研究化学元素和化学物质在生物体内的作用,及与生命的关系。
2、教学目的要求通过教学,使学生掌握无机及分析化学的基本概念、基本理论、基本技能,了解其最新成果和发展趋势。
(1)知识教学目标:理解原子结构和元素化合物的知识;理解化学键、杂化轨道理论与物质结构;掌握四大平衡及四种滴定分析方法;掌握分光光度分析方法;掌握重要的金属、非金属元素及其化合物。
(2)能力培养目标:具有运用化学科学理论知识解释和解决实际问题的能力;具有良好的学习方法和良好的学习习惯;具有较好的逻辑思维能力及分析综合能力;具有实验操作能力,综合分析问题解决问题的能力。
(3)思想教育目标:具有热爱科学、实事求是的学风,具有创新意识和创新精神;具有良好的职业道德和环境保护意识。
3、教学重点难点教学重点:化学平衡,解离平衡,氧化还原平衡,配位平衡,原子结构,分子结构,定量分析的误差和分析结果的数据处理,重量分析法,滴定分析法,分光光度法。
教学难点:化学平衡,解离平衡,氧化还原平衡,配位平衡的有关计算;原子结构,分子结构,滴定分析法。
无机及分析化学课程教学大纲

无机及分析化学课程教学大纲标题:无机及分析化学课程教学大纲一、课程简介无机及分析化学是是一门重要的基础科学,它涉及了化学的基础理论和实验技术。
本课程旨在为学生提供无机化学和分析化学的基本知识,培养学生的化学思维和实验技能,为后续的专业课程学习打下坚实的基础。
二、教学目标1、使学生掌握无机化学的基本概念、原理和方法。
2、培养学生掌握分析化学的基本原理和方法,包括定性、定量分析等。
3、使学生掌握化学实验技术,包括实验操作、实验设计和实验数据处理等。
4、培养学生的创新思维和解决问题的能力,提高学生综合素质。
三、教学内容1、无机化学基础:包括原子结构、分子结构、化学键、周期性现象、化学反应速率和化学平衡等。
2、分析化学:包括滴定分析、分光光度分析、色谱分析、电化学分析和质谱分析等。
3、实验技术:包括化学实验的基本操作、实验设计、实验数据处理和分析方法的建立等。
4、应用实例:结合实际应用,介绍无机及分析化学在环境、材料、生物和工业等领域的应用。
四、教学方法1、采用多媒体教学,通过图文并茂的方式使学生更好地理解抽象的化学概念和原理。
2、通过实例和案例教学,使学生更好地掌握化学实验技术和应用。
3、采用课堂讲解、小组讨论和实验实践等多种教学方式,提高学生的参与度和学习效果。
五、评估方式1、平时作业:布置与课程相关的作业,包括书面作业和实验报告等。
2、测验或考试:定期进行课堂测验和期末考试,检查学生对课程内容的掌握情况。
3、课堂表现:鼓励学生积极参与课堂讨论和提问,以评估学生的课堂表现。
六、实践环节1、基础实验:安排一系列基础化学实验,培养学生掌握基本的实验操作和技术。
2、综合实验:结合课程所学知识,安排一些综合性实验,培养学生解决实际问题的能力。
3、研究性实验:鼓励学生自主设计实验,探索化学领域的新知识,培养学生的创新能力和科学素养。
七、课程思政在课程教学中,注重融入思政教育元素,培养学生正确的世界观、人生观和价值观。
海文专业课内部资料与重要学习内容——农学

原题压中:万学海文2010动物生理学冲刺班讲义p55第二题
原题压中:万学海文2010年考前冲刺班预测卷一第20题
第21题
1、农学植物生理学冲刺复习关键点/a/20100108/000066.htm 2、万学海文2010植物生理强化班讲义 p5 “必需元素” 1、农学植物生理学预测核心考点/article/20 2、万学海文2010植物生理强化班讲义p12“同化物分配的一般规律” 3、万学海文2010植物生理冲刺班讲义p5页 “同化物分配机理” 4、万学海文2010年植物生理与生化考前冲刺模拟题三第20题 1、农学植物生理学考点预测/xueli/kaoyan/zhidao/zyk/ 2、万学海文2010年植物生理冲刺班讲义 p6 1、农学植物生理学冲刺复习关键点 /a/20100108/000066.html 2、万学海文2010植物生理冲刺班讲义 p4 “C3、C4、CAM植物在碳代谢途径上异 3、万学海文2010年植物生理与生化考前冲刺模拟题一第17题
海文命中出处 1、万学海文考前点题 /xueli/kaoyan/zhidao/zyk/20 2、万学海文钻石卡考前三套模拟题有机化学部分卷三 P49 1、万学海文考前点题 /zhuan_ye_ke_3974/20100108/t20100108_438285.shtml 2、万学海文农学化学强化班讲义有机化学部分P55
BJ-TK07-ZT 真题精讲班 BJ-TK07-CC BJ-TK07-JC BJ-TK07-QH BJ-TK07-QH 冲刺班 基础班 暑期强化班 国庆强化班
植物生理与 生化
BJ-TK07-ZT 真题精讲班 BJ-TK07-CC 冲刺班
所有研招专业均提供:专业课钻石卡高级辅导 专业课深度咨询专线:集团总部 010-62682299 北京 010-62682255 浙江 0571-87397373 重庆 023-65127542 大连 0411-84785055 湖南 0731-84133667 沈阳 024-23900799 陕西 029-85213835 河北 0311-89109907 四川 028-85483880 吉林 0431-85199309 山西 0351-7077676 湖北 027-51856666 考研专业课频道: 或 所有研招专业均提供:专业课全套备考资料 专业课 全套备考资料 全套备考资料咨询专线: TEL:010-82487329 QQ1:164650188 QQ2:574949229 江苏 济南 青岛 江西 福建 甘肃 025-51860025 0531-82397212 0532-85955666 0791-3802566 0591-23506644 0931-4810188 广东 020-85286398 安徽 0551-3662236 上海 021-55666892 天津 022-85681875 河南 0371-63396239 黑龙江 0451-86698985
无机及分析化学课程教学大纲(含创新创业教育)
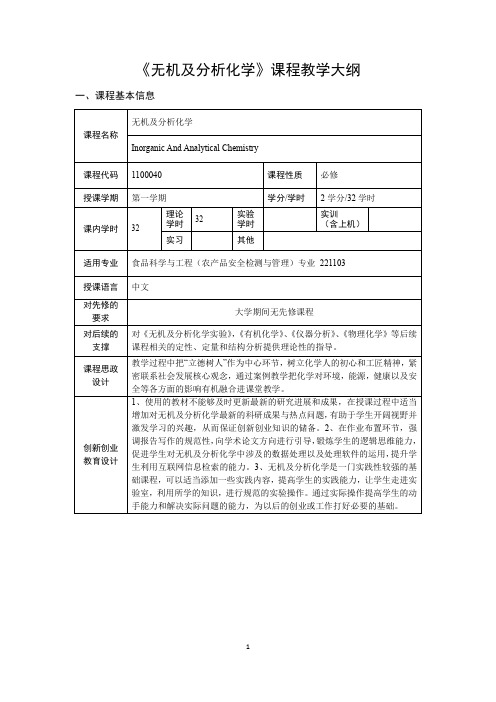
《无机及分析化学》课程教学大纲一、课程基本信息
二、课程目标及对毕业要求指标点的支撑
三、教学内容及进度安排
四、课程考核
注:各类考核评价的具体评分标准见《附录:各类考核评分标准表》
五、教材及参考资料
1.教材
《无机与分析化学》,商少明,化学工业出版社,2017第三版,978-7-122-29016-8。
2.主要参考书
1、《无机与分析化学》,陈若愚、朱建飞,大连:大连理工大学出版社,2007,第978-7-56-113764-2。
2、《无机与分析化学》,侯振雨、李英、郝海玲,北京:化学工业出版社,2016,第978-7-12-227545-5。
3、《无机与分析化学》,陈虹锦,北京科学出版社,2008,第二版,978-7-03-021961-9。
4、《分析化学》,武汉大学,北京:高等教育出版社,2006,第四版,978-7-04-007952-4。
5、《无机与分析化学学习指导》,谢少艾,陈虹锦,梁竹栖等,北京:科学出版社,2006, 第一版,7-03-017262-0。
6、《仪器分析原理及技术》,魏福祥,北京:中国石化出版社,2011,第一版,978-7-51-141066-5。
六、教学条件
多媒体教室。
附录:各类考核评分标准表
小测验评分标准
平时作业评分标准
课程考试评分标准。
2011年农学考研大纲(315化学,414植物生理生化,415动物生理生化)

2011年农学门类联考考试大纲化学Ⅰ.考察目标农学门类化学考试涵盖无机及分析化学(或普通化学和分析化学)、有机化学等公共基础课程。
要求考生比较系统地理解和掌握化学的基础知识、基本理论和基本方法,能够分析、判断和解决有关理论和实际问题。
Ⅱ.考试形式和试卷结构一、试卷满分及考试时间本试卷满分为150分,考试时间为180分钟。
二、答题方式答题方式为闭卷、笔试。
三、试卷内容结构无机及分析化学 50%有机化学 50%四、试卷题型结构单项选择题 30小题,每小题2分,共60分填空题 35空,每空1分,共35分计算、分析与合成题 8小题,共55分Ⅲ.考查范围无机及分析化学无机及分析化学考试内容主要包括:化学反应的一般原理、近代物质结构理论、溶液化学平衡、电化学等基础知识;分析误差和数据处理的基本概念,滴定分析、分光光度分析和电势分析等常用的分析方法。
要求考生掌握无机及分析化学的基础知识和基本理论,具有独立分析和解决有关化学问题的能力。
一、溶液和胶体考试内容分散系溶液浓度的表示方法稀溶液的通性胶体溶液考试要求1.了解分散系的分类及特点。
2.掌握物质的量浓度、物质的量分数和质量摩尔浓度的表示方法及计算。
3.掌握稀溶液依数性的基本概念、计算及其在生活和生产中的应用。
4.掌握胶体的特性及胶团结构式的书写。
5.掌握溶胶的稳定性与聚沉。
二、化学热力学基础考试内容热力学基本概念热化学及化学反应热的计算化学反应方向的判断考试要求1.了解热力学能、焓、熵及吉布斯自由能等状态函数的性质,功与热等概念。
2.掌握有关热力学第一定律的计算:恒压热与焓变、恒容热与热力学能变的关系及成立的条件。
3.掌握化学反应热、热化学方程式、化学反应进度、标准态、标准摩尔生成焓、标准摩尔生成吉布斯自由能、化学反应的摩尔焓变、化学反应的摩尔熵变、化学反应的摩尔吉布斯自由能变等基本概念及吉布斯判据的应用。
4.掌握化学反应的△r m r m r m r G m的计算。
《无机及分析化学》课程教学大纲

《无机及分析化学》课程教学大纲课程名称:无机及分析化学课程类别:专业基础课适用专业:生物科学/环境生态工程/生态学专业考核方式:考试总学时、学分:48学时3学分其中实验学时:0 学时一、课程教学目的本课程的目的是要求学生掌握元素周期律、物质结构理论基本知识、化学热力学、化学反应速率、化学平衡、酸碱平衡、沉淀平衡、配位平衡、氧化还原反应等基本理论。
并在上述理论的指导下,理解掌握溶液中四大平衡的相互关系和有关计算。
重点掌握平衡的原理、溶液中的各种化学平衡及其在分析化学中的应用,使学生建立准确的“量”的概念和掌握鉴定物质的化学结构和化学成分以及测定有关成分含量的化学分析方法及方法的原理。
通过分析化学理论和实验学习,培养学生实事求是的科学态度和严谨、细致的工作作风,为后继课程的学习和将来参加社会实践打下良好基础。
在完成该课程的学习之后,要求学生在掌握了无机分析化学基本原理的前提下,可以根据样品性质、分析对象,正确设计分析方案,精确测定组分含量,准确报告分析结果,培养学生分析问题和解决问题的能力,具备初步的实验技能。
能够运用所学知识解决生产生活中的实际问题,能将化学知识与专业实际相结合。
二、课程教学要求1、注意讲清本课程中的基本概念和基本理论,在保持课程的科学性及系统性的基础上,应突出重点、难点,并努力反映本学科的新成就。
2、因学时有限,内容较多,有一部分内容要求学生自学。
采用由教师提示,学生课后自学并提出问题,老师课后解答的方式。
3、必要时对重点章节,可在讲授基础上,引导学生查阅资料,并进行课后学习兴趣小组讨论,写出读书报告,以培养学生综合分析问题的能力。
4、教学过程中要充分利用微视频、直观教具、录像和计算机辅助教学软件、多媒体教学辅助设备。
三、先修课程高中化学四、课程教学重、难点课程教学重点是化学热力学基本概念及其应用,化学平衡原理,化学反应速率,酸碱平衡,氧化还原反应,原子结构,分子结构,配合物的组成、结构及价键理论,酸碱滴定分析法、氧化还原滴定分析法、配位滴定法、比色法和分光光度法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
生命是永恒不断的创造,因为在它内部蕴含着过剩的精力,它不断流溢,越出时间和空间的界限,它不停地追求,以形形色色的自我表现的形式表现出来。
--泰戈尔
万学海文2011年考研农学大纲变化详解:无机及分析化学(三)
解大纲立框架明详略
万学教育·海文考研专业课教研中心农学教研室瑞芳
一、无机及分析化学考查目标
该门学科在考查要求考生比较系统地理解和掌握无机化学、分析化学的基础知识、基本理论、基本方法和基本技能,能够分析、判断和解决有关理论和实际问题。
二、无机及分析化学考点解析
大纲中明确的考试内容主要包括化学反应的一般原理、近代物质的结构理论、溶液化学平衡、电化学等的基础知识;分析误差和数据处理的基本概念,滴定分析、分光光度分析和电势分析等常用的分析方法。
要求考生掌握无机及分析化学的基础知识和基础理论,具有独立分析和解决有关化学问题的能力。
本学科知识体系分为十一个章节,对大纲中各章节内容考点的总结归纳为七项,解析如下:
1、溶液和胶体
考试内容:溶液浓度的表示方法、稀溶液的通性、胶体溶液。
考点解析及复习建议:该部分内容属于基础概念,要求掌握物质的量浓度等基本内容,考查多以概念性描述的选择题为主,要求准确理解和描述。
2、化学热力学基础
考试内容:热力学基本概念、热化学及化学反应热的计算、化学反应方向的判断。
考试考点解析及复习建议:对热化学及化学反应热的计算,反应方向判断等是每年必考内容,也是重点,是化学平衡分析的基础。
该部分要求了解热力学能等名词概念,学会根据热力学定律分析化学反应过程中的热变化,及根据热变化分析化学反应方向等。
3、化学反应速率和化学平衡
考试内容:化学反应速率基本概念及速率方程式、反应速率理论、化学平衡及移动。
考试考点解析及复习建议:在名词概念理解的基础上,强调掌握计算、分析和判断。
分析计算题中要求正确书写化学反应速率方程式和化学平衡常数,判断浓度、温度等对化学平衡的影响,侧重分析,在单选、填空、计算题中均会出现。
4、物质结构
考试内容:核外电子运动状态、多电子原子核外电子排布、元素周期律及元素性质的周期性变化、离子键和共价键理论、杂化轨道理论、分子间力。
考试考点解析及复习建议:该部分内容概念性较强,较多,易混淆。
多以了解、理解为主,考查时以单选和填空为主,对此部分内容要求对名词概念的内容正确了解、理解物质组合结构规律,并根据规律学会分析判断杂化轨道、分子极性。
5、分析化学概论
考试内容:定量分析中的误差、有效数字及运算规则、滴定分析法概述
考试考点解析及复习建议:该部分是对实验原理及结果分析方法的考查,属于应用知识部分,要求较高,不仅有概念原理的理解,更有在此基础上的计算应用,多以计算等大题形式考查,考生应重点分析练习。
6、四大平衡和滴定法(酸碱平衡和酸碱滴定法、沉淀溶解平衡和沉淀滴定法、氧化还原反应和氧化还原滴定法)
考试内容:酸碱质子理论、酸碱平衡、缓冲溶液、酸碱滴定法;沉淀溶解平衡、溶度积原理、沉淀滴定法;氧化还原反应、电极电势及其应用、元素电势图及其应用、氧化还原滴定法;配合物基本概念、配合物化学键理论、配位平衡、配位滴定法。
考试考点解析及复习建议:该部分是该学科的重中之重、难中之难,不仅知识点多、考试分数比重大、考试形式多样,而且考查深度有潜有深,有对基础概念的了解,名词概念的考查,同时还有基本原理的应用及实验技能的考查。
针对此,首先要准确理解名词概念及基本原理,掌握反应原理,学会根据不同的平衡原理分析反应变化过程,同时还要根据原理设计分析实验。
在准确理解的基础上,灵活应用,重在分析。
7、分光光度法和电势分析法
考试内容:分光光度法概述、吸收定律、显色反应、分光光度计及测定方法;电势分析法基本原理、离子选择性电极。
考试考点解析及复习建议:该部分属于分析方法的学习应用,以了解、理解为主,在了解基本原理的基础上,学会分析化学变化,掌握实验分析测定方法。
对以上各章节考点进行进一步分析,提炼出其中的重点,总结概况如下:
无机及分析化学的各部分考点相互联系,前后形成统一的知识整体。
其中,基础是热化学、物质结构概念,重点为四大平衡原理(酸碱平衡、沉淀溶解平衡、氧化还原平衡和配位离解平衡),溶液分析可以作为贯穿知识点掌握和应用的连接主线,结合滴定分析、分光光度法、电势分析法等基础实验分析方法。
结合以上各章节知识点详细解析及重难点归纳,对该学科在考试内容及考试要求总结归纳为三个大框架:以对基础概念、公式、原理、理论的理解掌握为基础;理解性重点领悟化学平衡思想及其应用,同时掌握对热力学化学反应方向的判断、物质的结构特点、空间构型、化学反应速率、电极反应及其应用、分析化学三大平衡等基本知识点;使用物质、能量平衡的思想对分析化学原理进行应用和计算。
框架1:基本名词概念、基本反应原理、基础理论
1、热化学及化学反应速率
无机化学部分的基本名词较多,热化学、化学反应速率、化学反应平衡常数等基本概念及其计算公式是基础,在此基础上的反应平衡变化是重要的考查内容。
2、原子结构与元素周期律
核外电子运动的波粒二象性;用四个量子数对核外电子运动状态进行完整描述;多电子原子的能级以及能级交错的概念(造成能级交错现象的原因不作要求);多电子原子的核外电子的排布的三个规则。
3、化学键与分子结构
价键理论,杂化轨道理论。
价层电子对互斥理论以及理论的要点;分子几何构型的判断。
共价键的极性和分子极性的联系与区别;分子间力和氢键的概念以及三种分子间力的类型。
离子的极化概念以及对化合物性质的影响。
框架2:化学平衡思想的应用
1、酸碱反应
酸碱质子理论,酸碱平衡中有关浓度的计算。
分布系数、分布曲线的概念以及有关的计算。
物料平衡、电荷平衡、质子条件的概念以及各种体系PBE的正确写法。
两性物质的概念及其pH值的计算方法。
缓冲溶液、缓冲容量、缓冲范围的概念及其缓冲溶液pH值的计算方法。
2、沉淀反应
电解质的概念以及电解质强弱的概念;可溶、微溶、难溶电解质的概念;溶解度、溶度积的概念极其表示方法、相互之间的联系与区别和相关计算;同离子效应与盐效应的概念以及对沉淀溶解的影响和相关计算;分步沉淀原理、沉淀的溶解与转化以及相关计算。
3、配位反应
配位化合物的基本概念、配位化合物的基本组成以及与之相关的各种名词;配位化合物的命名和书写规则;配位化合物的价键理论。
螯合物的概念、EDTA与金属离子形成的螯合物的特征;配位化合物的稳定常数的概念;配位反应的副反应系数、条件稳定常数的概念及
其计算。
4、氧化还原反应
氧化还原反应方程式的配平、原电池和电极反应、氧化还原反应的方向、速度与程度、元素的电位图及用途。
利用能斯特方程式进行相关的计算;氧化还原反应的方向以及各种影响因素对之的影响;氧化还原反应进行的程度判断;氧化还原反应的速度以及各种影响因素对之的影响;元素电位图及其用途。
框架3:分析化学原理及应用
1、定量分析概论
定量分析过程和分析结果的表示、定量分析的误差、有效数字及计算规则。
分析结果的统计处理;可疑值的取舍(要求Q检验法)。
2、滴定分析法
对于不同强度的酸碱的滴定曲线,着重在计量点附近的pH突跃和根据pH突跃选择适应的指示剂;络合滴定法中主要以介绍EDTA滴定法为主,重点为络合平衡和络合滴定;氧化还原滴定法,根据氧化还原反应的这些特点,在讲解中应把重点放在滴定条件(溶液酸度、反应温度、试剂浓度和滴定速度)的选择上。
弱酸、弱碱(包括电离学说的弱酸、弱碱、弱酸盐和弱碱盐)被滴定的可能性,是酸碱滴定的难点,考生易混淆;氧化还原滴定结果的计算中,难点在于间接测定中氧化还原反应中各反应物间化学计量关系的确定。
3、分光光度分析法
朗伯—比耳定律是光吸收的基本定律,从物质对光的选择性吸收的基本原理出发,推导朗伯—比耳定律,同时讲解偏离朗伯—比耳定律的基本原因。
显色条件及测量条件的选择,影响显色反应的条件因素,重要的显色剂,入射光波波长和参比溶液的选择,掌握仪器测量误差对分析结果的影响,控制适宜吸光度范围。
4、电势分析法
重点结合副反应理论讲清条件电极电位及其在分析化学中的应用,氧化还原滴定曲线主要是掌握滴定过程中电极电位的变化规律。
氧化还原反应速度是该氧化还原反应能否用于滴定分析的关键之一,要求了解影响氧化还原反应速度的因素,特别要掌握催化反应和诱导反应的内容及作用。
氧化还原滴定法的应用,主要讲明KMnO4法、K2Cr2O7法和碘量法,掌握他们各自的特点、原理、结果计算等。
敬请关注万学海文2011大纲解析系列文章之(四)、(五)、(六)、(七)、(八)、(九),祝愿2011考研学子旗开得胜,马到成功!。
