第五章_金属有机化学-2.
有机化学 第五章旋光异构

旋光性
旋光仪(polarimeter)
旋光性的表示方法: • 旋光性--能旋转偏振光的振动方向的性质叫旋光性
• 旋光性物质(或叫光活性物质)--具有旋光性的物质.
• 右旋物质--能使偏振光的振动方向向右旋的物质. 通常用 “d” 或 “+” 表示右旋. • 左旋物质--能使偏振光的振动方向向左旋的物质. 通常用 “ l” 或 “-” 表示左旋. l • 旋光度-- 偏振光振动方向的旋转角度.用“”表 示.
(2)锲形式——比较直观 •将手性碳原子表示在纸面上,用实线表示在纸面 上的键,虚线表示伸向纸后方的键,用锲形实线表 示伸向纸前方的键。
2、构型的标记 (1)D—L法
(相对标记法)
甘油醛
D-(+)-甘油醛
L-(-)-甘油醛
目前,糖类、氨基酸的构型仍采用D、L标 记法,适合含一个C*的分子构型。
(2) R-S标记法
(补充). 螺环化合物
• 类似于丙二烯型化合物
a b
H HOOC
c a b ,c d 时, d 存在对映体
CH3 COOH
例2:联苯(邻位上有较大取代基时):
两个苯环不在一个平面 • 如果两个苯环上的取代基分布不对称,整个分子就具有 手性.(6,6’-二硝基-2,2’-联苯二甲酸)
HOOC
NO2
构造异构:分子式相同而分子中原子或 基团连接顺序不同 立体异构:分子中原子的结合顺序相同 而原子或基团在空间相对位置不同 对映异构:分子式和构造式相同,构型 不同并呈镜象对映关系的立体异构现象 称为对映异构,又称旋光异构或光学异 构。
一、 手性和对映体
生活中的对映体 (1)-镜象
沙漠胡杨
生活中的 对映体(2) -镜象
第五章 过渡金属有机化合物的基元反应

金属有机化学
配体的配位和解离反应
◎过渡金属和烯烃的配位
按照Chatt -Dewar -Duncanson模型,乙烯和过渡金属的 配位键包括: ● 烯烃的成键π轨道供给电子和金属的空d 轨道相重叠; ● 金属的满填d 轨道和烯烃的反键π* 轨道相重叠,即金 属的反馈。
金属有机化学
二、 氧化加成与还原消除
O OC CO Mn OC CO CO
14
CH3 +
14
OC CO OC
CO
C
CH3
Mn CO CO
金属有机化学
插入反应和反插入反应
不饱和化合物插入M—H键,如:
[R h (N H 3 ) 5 H ]
2+
+ C H 2=C H 2
[R h (N H 3 ) 5 C 2 H 5 ]
2+
如不饱和化合物插入M—R键则可表示为:
M
L
L
M
S
+
L
L
L
S
: S o lv e n t
M L3
+
L’ M L 3L ’
M L 3L ’
L
: lig a n t
K = M L3 L’
通常人们喜欢:易生成配位饱和的配合物而分离、纯化易, 而其中某个配体又极易在温和条件下解离,生成配位不饱和 的配合物而发生反应。
P d ( P P h 3) 4 P d ( P P h 3) 3 + PPh3
LnM R + C C LnM C C R
插入反应还有:
T i(N R 2 ) 4 + 4 C S 2 R 3P b R ' + S O 2 R 3S n -N R 2 + C O 2 T i(S 2 C N R 2 ) 4 R 3P b O S O R ' R 3S n O C O N R 2
第五章金属在各种环境中的腐蚀

8
2.4防止海水腐蚀的措施
• 1)研制和应用耐海水腐蚀的材料。 如:铁、镍、铜及其合金,耐海水钢。
• 2)阴极保护。 腐蚀最严重处采用护屏保护较合理,亦可采用简易可行的牺牲阳极法。
• 3)涂层。 除应用防锈油漆外,还可采用防止生物玷污的双防油漆,对于潮汐区和飞
溅区的某些固定的钢结构可以使用蒙乃尔合金包覆。
其寿命一般有几年。 *镍及其合金在碱液中的腐蚀
镍及其合金对于高温高浓度的碱耐蚀性很好,所以广泛用于制碱业。镍实际上 适合各种浓度和温度的碱液,其耐蚀性一般与合金含镍量成正比。 *两性金属在碱液中的腐蚀 铝、锌、锡等两性金属在碱溶液中不耐蚀。钛、钽、铌等在碱溶液中耐蚀性也 不好。在热碱中,钽的耐蚀性更差。
• (3)微生物引起的腐蚀。
11
3.3防止土壤腐蚀的措施
• 1)采用涂料或包覆玻璃布防水。 • 2)采用电化学保护,多采用牺牲阳极法,阴极保护与涂料联合使用效果更好。 • 3)采用金属涂层或包覆金属,镀锌层等。
12
第四节 金属在工业环境中的腐蚀
4.1金属在酸溶液中的腐蚀
• 氧化性酸与非氧化性酸对金属的腐蚀情况大不相同。 非氧化性酸的特点:腐蚀的阴极过程基本上是氢去极化过程,增加溶液酸度 相应地会增加阴极反应,并使金属腐蚀速度增加。
6
第二节 金属在海水中的腐蚀
2.1 海水腐蚀特点 • 1. 盐类及导电率 • 2. 溶解氧 • 3.海水的电化学特点
2.2影响海水腐蚀的因素
• 盐类 • 海水中溶解氧 • 海洋生物和腐烂的有机物 • 海水的温度、流速 • PH值
7
2.3海水中常用金属材料的耐蚀性
• 金属材料在海水中的耐蚀性差别很大,其中耐蚀性最好的是钛合金和Cr-Ni合金,而铸铁 和碳钢耐蚀性较差。不锈钢的均匀腐蚀速度虽然很小,但在海水中易产生点蚀。
金属有机化学 第5章 羰基配合物

过渡金属原子簇化合物的结构和性质
多核配位化合物,并不一定是原子簇化合物,因一般 的多核体系中,M 与 M 之间不一定存在 M-M 键。例如 Cr2O7= 并不是簇合物,因 Cr 与 Cr 之间由O来键合。上世 纪的60年代以前仅合成了几个簇合物,如 K3W2Cl9,Fe2(CO)9 等。但近年来发展非常迅速,已合成出了数百个结构新颖 的簇合物。
侧基配位的情况比较少, 此时, CO可认 为是一个四电子给予体, 它一方面以5孤 对电子同M1配位,同时又以1电子同M2 配位。
5σ
C :
O
1π
M1
M2
12
2) 边桥基配位 在双核或多核羰基化合物中,用符号“-CO” 表示,CO作为两电子配体,能够同时和两个金属原 子的空轨道重叠;另一方面金属原子充满电子的轨 道也能同CO的*反键轨道相互作用,形成反馈键。 结果是CO作为桥将两个金属联结到一起.
7
(2)与酸作用生成羰基氢化物
(3)配体取代反应 Fe2(CO)9+4NO
(4)氧化还原反应 Mn2(CO)10 +Br2
羰基配合物的成键: CO哪些分 子轨道上的电子能给予中心原子 形成配位键? (sp-sp反键)
(二重简并) (sp(C))
(二重简并)
(sp-sp成键) (sp(O))
8
4 轨道由于电子云大部分集中在CO核之间, 不能给予其它原子。 能给予中心金属原子电子对的只有3、1和 5电子。 3电子是 属于氧的孤对电子,由于氧的电负性比碳原子大, 除少数情况之外, 氧很难将3电子对拿出来给予中心金属原子, 因此,能与中心金 属原子形成σ 配键的分子轨道就只有1和 5了。
29
硼烷簇化合物的结构类型
structure type
有机化学第五章答案
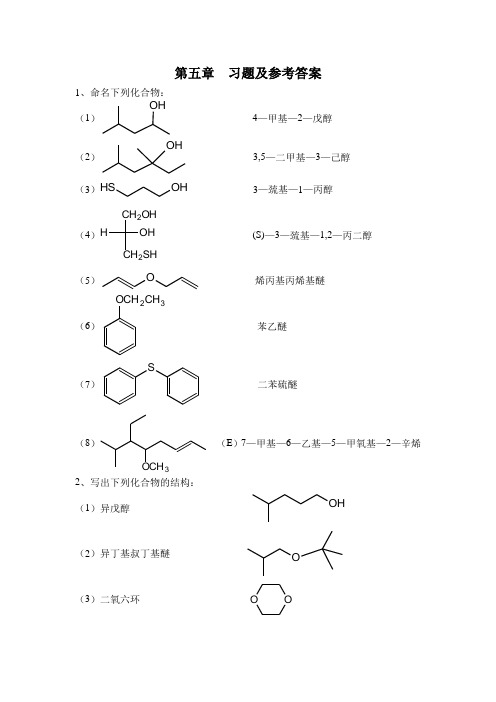
第五章 习题及参考答案1、命名下列化合物:(1)O H4—甲基—2—戊醇(2)O H3,5—二甲基—3—己醇(3)O H SH 3—巯基—1—丙醇(4)H O H CH 2OHCH 2SH(S)—3—巯基—1,2—丙二醇 (5)O烯丙基丙烯基醚(6)OCH 2CH3苯乙醚(7)S二苯硫醚(8)OCH3(E )7—甲基—6—乙基—5—甲氧基—2—辛烯2、写出下列化合物的结构:(1)异戊醇O H(2)异丁基叔丁基醚O(3)二氧六环 O O(4)DMSOC H 3SC H 3O(5)THFO(6)环氧丙烷 O3、按沸点从高到低顺序排列下列化合物:(1)正丁醇(2)正戊醇(3)异丁醇(4)叔丁醇(5)四氢呋喃 (2)﹥(1)﹥(3)﹥(4)﹥(5) 4、用化学方法区别下列各组化合物: (1)正丁醇、仲丁醇、叔丁醇取三支试管分别加入三种化合物少许,分别加入几滴Lucas 试剂,立即变浑浊的是叔丁醇,放置片刻变浑浊的是仲丁醇,室温下无变化,加热后变浑浊的是正丁醇。
(2)1,4—丁二醇、1,2—丁二醇取两支试管分别加入硫酸铜溶液少许,滴加氢氧化钠溶液至有氢氧化铜沉淀生成,一只试管中加1,4—丁二醇,另一只试管中加1,2—丁二醇,能生成将蓝色溶液的是1,2—丁二醇,则另一个是1,4—丁二醇 (3)苄醇和苄基溴高锰酸钾酸性溶液,步骤略 (4)O(CH2CH 2OH)2C H 2C H O HO HC H 3同(2)5(1)CH 2CH 3CH3O H H SOCC HC H 3C H(2)H 3CH2(3)(CH 3)3CCH 2OH+B r H H 3C C H 2C H 3B rC H(4)+OIH O H+CH 3I (Imol)(5)+IH +CH 3I OCH3O H(6)O33(7)O3+OO H(8)O HC C C H 3PhPh O HPh H 2SO4PhC C C H Ph O(9)O HO(CrO 3 /(C 5H 5N)2)或(CrO 3 /H 2SO 4/H 2O)或(MnO2/C 5H 12)6、将下列化合物按水溶解度由大到小排列成序:(1)丙三醇 (2)正丁醇 (3)甲乙醚 (4)甲硫醚 (1)﹥(2)﹥ (3)﹥ (4) 7、解释下列现象: (1)CH 2OHH 2SO4++(2)(CH 3)3C C H O HC H 334(CH 3)3C C HC H 2+(CH 3)2CH CC H 2C H 3+(CH 3)2C=C(CH 3)2(3)CH2OH24175℃(4)O HO HC H3C H3H2SO4OC H3C H3解释:(1)CH2OHH2SO4+C H2O+HH-H2OCH2+重排+++-H++(2)+(CH3)3C C HO HC H385%H3PO4(CH3)2CH C C H2C H3(CH3)2C=C(CH3)2(CH3)3C C HO+C H3H H-H2O(CH3)3C C H+C H3重排C H3C+C HC H3C H3C H3-H+(CH3)3C C H C H2-H+(3)+CH 2OHH 2SO4175℃CH 2O +H 2-H 2OCH2+-H +(4)+O H O HC H 3C H3H 2SO4OC H 3O H OH2+C H 3C H 3-H OO HC H 3C H 3重排3O +C H 3C H H-H +8、写出环氧丙烷与下列试剂反应的主要产物:(1)无水HBr (2)(CH 3CH 2)2NH (3)CH 3CH 2ONa/CH 3CH 2OH (4)CH 3CH 2MgBr (5)CH 3CH 2OH/H + (6)PhOH/OH -O(CH CH )NH3CH 2ONa/CH 3CH 2OHCH 3CH 2MgBrCH 3C H 3C B r C H 3O HC H 3COCH 2CH3C H 3O HC H 3C HC H 2O HC H 3C HC H 2OMgBrC H 2C H 3C H 3C HC H 2O HN(CH2CH 3)2C H 3C HC H 2O HOCH 2CH39、用指定原料合成:(1)由叔丁醇和乙醇合成乙基叔丁基醚C H 3C H 2O H H 3C H 2IC H 3CO HC H 3C H 3NaC H 3CO C H 3C H 3NaC H 3CO C H 3C H 3Na +C H 3C H 2IC H C H O HH 3COC H 3C H 3C 2H 5(2)由正丙醇和异丙醇合成2—甲基—2—戊醇C H 2C H 2O HC H 3C H 3C H O HC H 34C H 3C C H 3O+C H 2C H 2B C H 3Mg无水醚C H 2C H 2MgBrC H 3C H 3C C H 3O C H 2C H 2MgBrC H 3C H 3CC H 2C H 3C H 2C H 3OMgBr2C H 3C C H 2C H 3C H 2C H 3O H(3)由溴苯和异丙醇合成2—苯基—2—丙醇C H 3C H O HC H 34C H 3C C H 3O+Mg C H 3C C H 3O C H 3CC H 3OMgBr 2B rTHFMgBrMgBrC H 3CC H 3O H(4)由环己醇合成二环己醚+O HB rH B rO NaO N aB rO N aHO10、用高碘酸分别氧化四个邻二醇,得到的氧化产物如下: (1)只得到C H 3C C H 2C H 3O(2)得到CH3CHO 和CH3CH2CHO (3)得到HCHO 和C H 3C C H 3O(4)得到一个二羰基化合物C H 3C C H 2OC H 2C H 2CHO请根据氧化产物分别写出四个邻二醇的结构式。
第五章第2节高分子材料第2课时 课件 2021-2022学年高二化学人教版(2019)选择性必修3

B.CH2==CH—COOH
C.CH3—CH(OH)—COOH D.H2N—CH2—COOH
随堂巩固
3.X是一种性能优异的高分子材料,其结构简式为
,
已被广泛应用于声、热、光的传感等方面,它是由HC≡CH、(CN)2、CH3COOH三种 单体通过适宜的反应形成的。由X的结构简式分析合成过程中发生反应的类型有
很难溶解,但往往有一定程 度的胀大
性能
具有热塑性,无固定熔点
具有热固性,受热不熔化
强度大、绝缘性好、有可塑 特性 强度大、可拉丝、吹薄膜、绝缘性好
性
常见 物质
聚乙烯、聚氯乙烯、天然橡胶
酚醛树脂、硫化橡胶
小结
随堂巩固
1.手术缝合线、人造器官等人体用的功能高分子要求无毒且与人体有较好的相容性。
根据有关化合物的性质及生物学知识可知,下列高分子不宜用作手术缝合线或人造
②合成新的带有强亲水基团的高分子。
如CH2==CH—COONa —一交—定联—条—剂件→
聚丙烯酸钠(网状结构)
学习任务三:高吸水性树脂
3.性能: 不溶于水,也不溶于有机溶剂,与水接触后在很短的 时间内溶胀,可吸收其本身质量的数百倍甚至上千倍 的水,同时保水能力要强,还能耐一定的挤压作用。
《时代周刊》评出20世纪最伟 大的100项发明,其中“尿不 湿”榜上有名
器官材料的是 A.聚乳酸
B.聚氨酯
C
C.氯纶
D.聚乙烯醇
随堂巩固
2.用高分子塑料骨钉取代钛合金骨钉是医学上的一项新技术,这种塑料骨钉不仅具
有相当的强度,而且可在人体内水解,使骨科病人免遭拔钉的痛苦。合成这种塑料
骨钉的原料能与强碱溶液反应,也能在浓硫酸条件下形成环酯。则合成这种塑料骨
第5章-过渡金属有机化学基础

配体 CO 用碳原子的一个 σ 轨道同过渡金属未 填充电子的空d轨道发生重叠,电子由碳原子流向 过渡金属,形成σ配位键,又称σ给予键 过渡金属填充电子的d轨道与CO的2π*反键轨 道重叠形成 π 反馈键,电子从过渡金属流向 CO, 形成π反馈键,又称π接受键
金属有机化学
这种 σ 给予与 π 接受的作用是协同的。当碳原 子向过渡金属供给电子时,CO上的电子云相对密 度降低,并有利于通过反馈键从过渡金属获得电 子。 这样的结果导致CO中的碳氧叁键被削弱,接 近于双键性质;而过渡金属与碳之间的键加强, 也接近于双键。 从羰基的红外光谱和原子间的键长数据验证 了这些结果 。
非过渡金属有机化合物和过渡金属有机配合 物的合成方法有许多相似的地方,如用非过渡金 属有机化合物对过渡金属盐的烃基化,可引入 M—C σ键配位的配体 利用氧化加成反应引入 M-Cσ 键或 M-Cπ 键的 配体只在合成过渡金属有机配合物中才有
金属有机化学
5.3.1 钯有机配合物 1.合成钯有机配合物的初始原料 Pd(MeCN2)C12 、 Pd(PhCN)2C12 、 Pd(OAc)2 等是合成钯有机配合物的重要原料 氯化钯是合成钯配合物常用的初始原料,但 它在大多数有机溶剂中的溶解度很小,不便使用。
金属有机化学
就是将氯化钯转变成一个既能溶入有机溶剂,配 位的乙腈或苯甲腈又容易解离的过渡性钯配合物, 便于随后的反应 将氯化钯和过量氯化钙溶入甲醇中加入烯丙 基 氯 , 通 入 CO 能 得 到 烯 丙 基 钯 配 合 物 (C3H5)2Pd2Cl2
金属有机化学
2.用配体置换反应合成二价钯有机配合物 配体置换反应是合成过渡金属有机配合物的 重要方法之一 如Pd(acac)2就可以用Li2PdCl4和乙酰丙酮,在氢氧 化钠水溶液中,通过配体置换制备
第5章 过渡金属有机化学基础

R CC )R (IV
SO2 OC L Ir L Cl
R
L CO Cl Ir CO L
L Ir L Cl CO
图 5-5 Vaska配合物的氧化加成反应
• C-O键与过渡金属有机配合物的氧化加成反应
Ni(cod)2 + OAc C3H5)NiOAc C3H5)2Ni + Ni(OAc)2
• 还原消除反应 还原消除反应是氧化加成的逆反应。发生还 原消除反应时,配合物的氧化态及有效原子序 数均下降 "2",形成A-B型的消除产物。
• 还原消除经过一个非极性、非自由基的三中心过 渡态 。
图5-8 还原消除的三中心过渡态
由于还原消除反应按三中心过渡态机理 进行,发生消除反应的两个配体在过渡金 属有机配合物中必须处在顺位。
Ph2 P Me Pd P Me Ph2 DMSO, 80oC Me-Me
DMSO, 80oC NR Me Ph2P Pd P Ph2 Me
• 在反应过程中加入吸引电子的配体,如顺 丁烯二酸酐,丙烯腈等可加速还原消除反 应。
CN N Ni N Me N Me CN N Ni Me N Me CN CN N Ni CN + Me-Me
表5-3 有效原子序数的计算方法
• 5.3 过渡金属有机配合物的合成 • 5.4 过渡金属有机配合物的化学性质
(1),配体置换反应。(配位体的配位与解离) (2),氧化加成和还原消除反应。 (3),插入反应和消除(反插入)反应。 (4),过渡金属有机配合物配体上的反应。
• 5.4.1过渡金属有机配合物的配体置换反应 配位饱和的过渡金属有机配合物的配体 置换是它们的重要化学性质,也是它们实 现催化作用的首要条件。原有配体被另一 个配体---反应底物置换,使底物进入配位 圈,改变了底物的化学键状态而得到活化, 并接着在配位圈内发生反应。 这是配位催化中第一种反应底物进入配 位圈的途径。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
+ Mn(CO)6 +
Fe(CO)5
(C6H8)2Mn(CO)2+ 4 CO Fe(CO)3 + 2 CO
五元环的配体配合物常用环戊二烯钠和金属卤化 物反应制得。
2C5H6 + 2Na 2 NaC5H5 + H2
NiCl2 THF
[ (n5-C5H5)2Ni + NaCl
有时也可用环戊二烯和有机金属配合物作用,取代 掉两个其它的中性配体,然后再从环上脱去一个质子 得到环戊二烯键合的金属有机化合物。
b) 金属相同 1. R(Et)-M < Me-M < Ph-M < CF3-M 2. 烷 基 - 金 属 配 合 物 中 , 不 同 烷 基 其 稳 定 性 不 同 : 伯碳> 仲碳> 叔碳; 3. 对称性好的金属有机化合物稳定性大于对称性差的金属 有机化合物。 4. 金 属 - 碳 键 中 碳 的 电 负 性 越 强 , 如 杂 化 轨 道 中 S 成 分 越 多 或 碳 上 连 有 提 高 碳 的 电 负 性 的 基 团 , M-C 键 的 稳定性就增加。
同位素示踪表明反应可能有两种途径:a. 原来分子的羰 基插入Mn-CH3键机理;b. 甲基转移机理。研究表明:实际 的机理是甲基转移。 反应动力学指出反应的第一阶段包括甲基转移得到5-配 位的酰基络合物,然后受到进入的一氧化碳(或其他配位体) 的攻击得到最后的6-配位体产物。
(CH3)Mn(CO)5 (CH3CO)Mn(CO)4 CO (CH3CO)Mn(CO)5
HgEt2 + 2Li
△Hf (KJ/mol) +27.0 0
Hg + 2LiEt
0 -58.5
△Hf = -144 KJ/mol
这是第一个由于金属有机化合物本身的形成提供 反应推动力的例子。
R2Zn + 2Li R2Hg + 2Na 2C2H5Li + (CH3)2Hg
2RLi + Zn 2RNa + Hg (C2H5)2Hg + 2CH3Li
对于重主族元素(M = Tl, Pb, Bi, Hg),由于这些元 素的M-C键很弱,上述反应比较困难。但可以通过加 入电正性很强的金属来促进这个反应的进行。
2. 从金属有机试剂的交换反应制备
CH3Li + CuCl 2CH3Li + (PEt3)2PtBr2 CH3MgBr + (PEt3)2PtBr2 CH3Cu + LiCl (PEt3)2Pt(CH3)2 + 2LiBr (PEt3)2Pt(CH3)Br + MgBr2
反应通常是活泼金属有机试剂与一较为不活泼 的金属卤盐发生交换反应。 。
2LiEt + HgCl2
△Hf (KJ/mol) -58.5 -230.0
HgEt2 + 2LiCl
+27.0 -409.0
△Hf = -444 KJ/mol
可见,电正性较大的金属失去它的烷基而得到卤 素是反应的推动力。
羰基金属阴离子还可以与卤代烷反应生成金属有机 羰基金属阴离子 配合物。
14
CO
加热
加压
(CH3CO)Mn(CO)4(14CO)
(a) (b)
(CH314CO)Mn(CO)5
(CH3)Mn(CO)4(14CO)
+
CO
从反应式a可以看出,不用CO而用其它配位体也可使烷 基锰转化为酰基锰。
(CH3)Mn(CO)5 + L
L= NH3,PR3等
(CH3CO)Mn(CO)4L
b) 二价金属元素 二价金属元素与卤代烃反应可以制备有机金属化合 物。其中Grignard试剂的制备是最为主要的。
Mg + PhBr PhMgBr Grignard试剂 试剂 Zn + EtI EtZnI Hg + CH2 CH CH2I CH2 CH CH2HgI
这些金属没有一价金属活泼,通常需要加热, 反应才能发生。活性 RI > RBr > RCl
金属交换反应在有机合成中非常有用,可以高选择 高选择 性的制备活泼金属有机化合物。因为可以直接从金属本 性的制备活泼金属有机化合物 身制备的金属有机化合物太活泼,反应的选择性差,而 选择性高的金属有机试剂活性低,难以直接从金属制备, 所以只好用间接方法。
3. 烯(炔)烃的插入反应和取代反应
烯烃或炔烃可以通过插入金属与氢或金属与碳之间 的键中或取代某个配体而生成新的配位化合物。这是制 这是制 备金属-烷基化合物的重要方法之一 烷基化合物的重要方法之一。 备金属 烷基化合物的重要方法之一。
例:甲基五羰基锰(I)的羰基化反应
(CH3)Mn(CO)5 + CO 加压 (CH3CO)Mn(CO)5
特点: 1)把标记的CO引入反应,它不是成为酰基,而是顺式接到金 属上形成羰基(反应式a); 2)逆反应中,14C标记的酰基络合物不放出标记的一氧化碳(反 应式b)。
(CH3)Mn(CO)5 +
Na[Mn(CO)5] + CH3I (CH3)Mn(CO)5 + NaI
反应的推动力是生成不溶性的碘化钠。
Na[Mn(CO)5] + ClCH2CH
CH2
(CO)5Mn(CH2CH CH2)
Mn(CO)4
该反应先生成σ-烯丙基配合物,而后失去一分子CO并 重排成π-烯丙基配合物。
金属有机化合物还可以通过金属元素的交换反应制 备,电正性较小的金属烷基化合物和电正性较大的金属 反应时,烷基转移。
2. 反馈键
凡有反馈键形成的金属有机化合物, 凡有反馈键形成的金属有机化合物, 其稳定性相对 较高。 较高。 如果在过渡金属有机化合物中存在反馈键,则反馈 的π键增加了M-C之间键的多重性,提高了M-C之间σ键 的强度,从而提高金属有机化合物的稳定性,例如烯烃、 芳基就比烷基与过渡金属配位形成的化合物要在一定程 度上稳定。
RM + MX
M=Li, Na, K, Cs, X=Cl, Br, I
C2H5Cl (气) + 2Li
LiEt(固)+LiCl(固)
△Hf (KJ/mol)
-105
0
-58
-409
△Hf = -362 KJ/mol
可见,金属和卤代烷直接反应的成功不是取决于金 属-烷基键的生成焓,而是取决于金属-卤化物键的生成 焓:放热的金属 卤化物键的生成有利于反应的右行 放热的金属-卤化物键的生成有利于反应的右行 放热的金属 卤化物键的生成有利于反应的右行。
AlCl3
(C 6H6)Cr(AlCl4) I
除上面这些代表性的方法外,还可以用电解、裂解、重 排、还原、加成等方法得到各类金属有机化合物。
5.5 有机金属化合物稳定性和反应性的影响因素
与其他有机化合物一样,金属有机化合物的稳定性 与反应性,需视具体的反应类型、反应条件以及不同的 溶剂体系等各种因素而定。 金属有机化合物的稳定性越小, 一般规律:金属有机化合物的稳定性越小 , 其反应 金属有机化合物的稳定性越小 性就越大,稳定性越大,其反应性就越小。 性就越大,稳定性越大,其反应性就越小 金属有机化合物的反应性与金属原子的氧化态、 金属有机化合物的反应性与金属原子的氧化态 、 配 位数以及几何构型有密切的关系。 位数以及几何构型有密切的关系。
[ (PEt3)2PtHCl ]
+
C2H4
[ (PEt3)2Pt(C2H5)Cl ]
180℃,1大气压 ℃ 大气压
烯烃插入反应可逆性为烯烃的催化异构化提供基础。 烯烃插入金属-氢键的反应在工业上应用于烯烃催化加氢 反应,烯烃插入金属-碳键的反应在工业上应用于烯烃催 化聚合反应。
烯(炔)烃类金属化合物还可以由烯(炔)烃把 其它配位体取代而制得。
5. 分解反应
酰基、羰基、芳基磺酸基和重氮化合物等都可以发 生分解反应脱去一个小分子得到新的金属有机化合物。
N2 Cl
+
-
HgCl HgCl2
Cu
+
COCl
COMn(CO)5 NaMn(CO)5
-CO
Mn(CO)5
+
6. 碳环键合
绝大多数四碳键合的配位体是用四碳键配位体如丁 二烯、1,3-环己二烯等与金属有机化合物直接反应,取 代原来在金属上的配体如CO而直接生成新的配位化合 物。
H2O
Na2PtCl4
+
CH2=CH2
Na[(C2H4)PtCl3]
+
NaCl
CH2=CH2
+
(n5-C5H5)Mn(CO)3
紫外照射
(n5-C5H5)Mn(CO)2(C2H4) + CO
[Pt(PPh3)4]+Ph来自CPhCH2Cl2 25℃
[(PPh3)2Pt(PhC≡CPh)]
+
2PPh3
4. 小分子的配位反应 除了烯烃外,一些小分子化合物如CO、CO2、N2、 SO2、CS2等也可和金属进行配位。
>120℃ ℃ Al
插入反应与它的逆反应——消除反应 消除反应相互竞争,并 插入反应 消除反应 且在160℃左右时得到平均链长是C14的烷基铝化合物, 经氧化和水解反应得到需要的醇。
烯烃插入过渡金属-氢键反应的最主要特征是它的可 烯烃插入过渡金属 氢键反应的最主要特征是它的可 逆性。 逆性。
环己烷, ℃ 环己烷,95℃,40大气压 大气压
5.4 有机金属化合物的制备
许多金属有机化合物对氧和水是不稳定的。
2 CH3MgI + O2 CH3MgI + H2O 2CH3OMgI CH 4(气) + Mg(OH)I
