化工原理课后习题答案第七章吸收习题解答
化工原理1-7章习题答案

目录第一章流体流动与输送机械 (2)第二章非均相物系分离 (32)第三章传热 (42)第四章蒸发 (69)第五章气体吸收 (73)第六章蒸馏 (95)第七章固体干燥 (119)第一章 流体流动与输送机械1. 某烟道气的组成为CO 2 13%,N 2 76%,H 2O 11%(体积%),试求此混合气体在温度500℃、压力101.3kPa 时的密度。
解:混合气体平均摩尔质量kg/mol 1098.2810)1811.02876.04413.0(33--⨯=⨯⨯+⨯+⨯=∑=i i m M y M ∴ 混合密度333kg/m 457.0)500273(31.81098.28103.101=+⨯⨯⨯⨯==-RT pM ρm m2.已知20℃时苯和甲苯的密度分别为879 kg/m 3和867 kg/m 3,试计算含苯40%及甲苯60%(质量%)的混合液密度。
解:8676.08794.012211+=+=ρρρa a m混合液密度 3kg/m 8.871=m ρ3.某地区大气压力为101.3kPa ,一操作中的吸收塔塔内表压为130kPa 。
若在大气压力为75 kPa 的高原地区操作该吸收塔,且保持塔内绝压相同,则此时表压应为多少?解:''表表绝+p p p p p a a =+=∴kPa 3.15675)1303.101)(''=-==+(-+真表a a p p p p4.如附图所示,密闭容器中存有密度为900 kg/m 3的液体。
容器上方的压力表读数为42kPa ,又在液面下装一压力表,表中心线在测压口以上0.55m ,其读数为58 kPa 。
试计算液面到下方测压口的距离。
解:液面下测压口处压力 gh p z g p p ρρ+=∆+=10题4 附图m 36.255.081.990010)4258(30101=+⨯⨯-=+ρ-=ρ-ρ+=∆∴h g p p g p gh p z5. 如附图所示,敞口容器内盛有不互溶的油和水,油层和水层的厚度分别为700mm 和600mm 。
化工原理课后习题答案第七章吸收习题解答

第七章 吸 收7-1 总压101.3 kPa ,温度25℃时,1000克水中含二氧化硫50克,在此浓度范围内亨利定律适用,通过实验测定其亨利系数E 为4.13 MPa , 试求该溶液上方二氧化硫的平衡分压和相平衡常数m 。
(溶液密度近似取为1000kg/m 3)解:溶质在液相中的摩尔分数:50640.01391000501864x ==+ 二氧化硫的平衡分压:*34.13100.0139kPa=57.41kPa p Ex ==⨯⨯相平衡常数:634.1310Pa40.77101.310PaE m P ⨯===⨯7-2 在逆流喷淋填料塔中用水进行硫化氢气体的吸收,含硫化氢的混合气进口浓度为5%(质量分数),求填料塔出口水溶液中硫化氢的最大浓度。
已知塔内温度为20℃,压强为1.52×105 Pa ,亨利系数E 为48.9MPa 。
解:相平衡常数为:6548.910321.711.5210E m P ⨯===⨯ 硫化氢的混合气进口摩尔浓度:15340.04305953429y ==+若填料塔出口水溶液中硫化氢达最大浓度,在出口处气液相达平衡,即:41max 0.0430 1.3410321.71y x m -===⨯7-3 分析下列过程是吸收过程还是解吸过程,计算其推动力的大小,并在x - y 图上表示。
(1)含NO 2 0.003(摩尔分率)的水溶液和含NO 2 0.06 (摩尔分率) 的混合气接触,总压为101.3kPa ,T=15℃,已知15℃时,NO 2水溶液的亨利系数E =1.68×102 kPa ;(2)气液组成及温度同(1),总压达200kPa (绝对压强)。
解:(1)相平衡常数为:51311.6810Pa 1.658101.310Pa E m P ⨯===⨯ *1 1.6580.0030.00498y m x ==⨯=由于 *y y >,所以该过程是吸收过程。
化工原理吸收课后习题及答案

相组成的换算【5-1】 空气和CQ 的混合气体中,CQ 的体积分数为20%求其摩尔分数y 和摩尔比Y 各为多解 因摩尔分数=体积分数,y 0.2摩尔分数x 0.0105或 X 021061 x 1 0.0105【5-3】进入吸收器的混合气体中, NH 的体积分数为10%吸收率为 90%求离开吸收器时 NH的组成,以摩尔比 Y 和摩尔分数y 表示。
吸收率的定义为解原料气中NH 的摩尔分数y 0.1 W 0.1 Y 1 1 0.1111 y 1 0.1吸收器出口混合气中 NH 的摩尔比为少?时, 摩尔比 丫 —1 y 【5-2 】20 C 的 l00g 0251 0.2水中溶解IgNH s NH 在溶液中的组成用摩尔分数 x 、浓度c 及摩尔比X 表示各为多少?解摩尔分数x 1/17 1/17 100/18=0'0105浓度c 的计算20C, 溶液的密度用水的密度998.2 kg / m 3 代替。
溶液中NH 的量为 31 10 /17kmol 溶液的体积 101 10 3 / 998.2 m 33 1 10 /1733 ----------------- =0 281kmol/ mV 101 10 3/ 998.2[、. s998 23或 c -x .02105 0.582kmoJ/m 3M s18NH 与水的摩尔比的计算溶液中NH 的浓度c 摩尔比 摩尔分数y 2 ~^= 0.01110.010981 Y2 1 0.0111【5-4】l00g 水中溶解lg NH 3,查得 气液相平衡20C 时溶液上方 NH 3的平衡分压为798Pa 。
此稀溶液的气 液相平衡关系服从亨利定律,试求亨利系数 E(单位为kPa)、溶解度系数H[单位为kmol/(m 3 kPa)]和相平衡常数总压为100kPa 。
1/17解液相中NH 3的摩尔分数x 1/17 100/18-溶解多少克氧?已知 10C 时氧在水中的溶解度表达式为 衡分压,单位为kPa ; x 为溶液中氧的摩尔分数。
化工原理课后习题答案

第七章 吸收1,解:(1)(2) H,E 不变,则 (3)2,解:同理也可用液相浓度进行判断3,解:HCl 在空气中的扩散系数需估算。
现,故HCl 在水中的扩散系数.水的缔和参数分子量粘度 分子体积4,解:吸收速率方程1和2表示气膜的水侧和气侧,A 和B 表示氨和空气代入式x=0.000044m 得气膜厚度为0.44mm.5,解:查008.0=*y 1047.018100017101710=+=x 764.001047.0008.0===*x y m Pa mp E 451074.710013.1764.0⨯=⨯⨯==Pa m kmol E C H ⋅⨯=⨯==3441017.71074.75.55KPa P 9.301=2563.0109.3011074.734⨯⨯==P E m 0195.0109.301109.533=⨯⨯=*y 01047.0=x 862.101047.00195.0===*x y m Pa mp E 531062.5109.301862.1⨯=⨯⨯==Pa m kmol E C H ⋅⨯=⨯==-35510875.91062.55.5509.0=y 05.0=x x y 97.0=*09.00485.005.097.0=<=⨯=*y y 吸收∴atm P 1=,293k T =,5.36=A M ,29=B M 5.215.1998.1=+=∑AV()()smD G 25217571071.11.205.2112915.36129310212121--⨯=+⨯+⨯=L D ,6.2=α,18=s M (),005.1293CP K =μmol cm V A 33.286.247.3=+=()()s m s cm D L 29256.081099.11099.13.28005.1293136.2104.721---⨯⨯=⨯⨯⨯⨯=或()()()12A A BM A P P P P RTx D N --=3107.53.10105.0m kN P A =⨯=2266.0m kN P A =212.96065.53.101m kN P B =-=226.10066.03.101m kN P B =-=()24.986.1002.9621m kN P BM =+=()()()07.566.04.983.101295314.81024.01043-⨯⨯-=--x s cm D C 2256.025=为水汽在空气中扩散系数, 水的蒸汽压为,时间 6,解:画图7,解:塔低:塔顶:2.5N 的NaOH 液含 2.5N 的NaOH 液的比重=1.1液体的平均分子量:通过塔的物料衡算,得到如果NaOH 溶液相当浓,可设溶液面上蒸汽压可以忽略,即气相阻力控制传递过程。
化工原理吸收习题及答案

化工原理吸收习题及答案化工原理吸收习题及答案化工原理是化学工程专业的一门基础课程,主要涉及化学反应原理、物质转化和传递过程等内容。
其中,吸收是一种常见的分离和纯化技术,在化工生产中起到重要作用。
为了帮助学生更好地理解和掌握吸收原理,以下将介绍一些化工原理吸收习题及答案。
习题一:某化工厂需要将氨气从废气中吸收出来,工艺流程如下:氨气从废气中通过气体吸收塔进入吸收液中,吸收液中的氨气通过反应与溶液中的酸发生反应生成盐类。
请回答以下问题:1. 吸收液中的酸应选择什么样的性质?2. 如何选择合适的吸收液浓度?3. 吸收液中酸的浓度越高,吸收效果会如何变化?答案一:1. 吸收液中的酸应选择具有较强酸性的物质,例如硫酸、盐酸等。
这样的酸性物质可以与氨气快速反应生成盐类,实现氨气的吸收。
2. 吸收液的浓度应根据氨气的浓度和吸收效果要求来选择。
一般来说,如果氨气浓度较高,吸收液的浓度也应相应提高,以增加吸收效果。
3. 吸收液中酸的浓度越高,吸收效果会更好。
因为酸浓度越高,氨气与酸反应生成盐类的速率越快,吸收效果也就越好。
习题二:某化工过程中,需要从气体混合物中吸收二氧化硫。
已知气体混合物中的二氧化硫浓度为10%,请回答以下问题:1. 选择合适的吸收液时,应考虑哪些因素?2. 如果吸收液中的溶剂选择不当,会对吸收效果产生什么影响?3. 吸收液中的溶剂浓度选择应如何确定?答案二:1. 在选择合适的吸收液时,应考虑溶剂与待吸收气体的亲和力、反应速率、溶解度等因素。
合适的吸收液应能够与二氧化硫发生反应生成稳定的产物,并且具有较高的溶解度。
2. 如果吸收液中的溶剂选择不当,可能会导致吸收效果不佳甚至无法吸收。
例如,如果溶剂与二氧化硫反应生成的产物不稳定,会导致产物再次分解释放出二氧化硫,从而无法实现吸收的目的。
3. 吸收液中的溶剂浓度选择应根据二氧化硫的浓度和吸收效果要求来确定。
一般来说,如果二氧化硫浓度较高,吸收液的溶剂浓度也应相应提高,以增加吸收效果。
化工原理习题答案第七章

的平衡分压,kPa ; x 为溶液中氧的摩尔分数。
空气中氧的体积分数为 21%,试求 总压为101kPa 时,每m 3水中可溶解多少g 氧?(答:11.4gm",或 耐 m^3 )解:Pe = 0.21 101.3 =21.3kPa ,Pe7-3 .用清水吸收混合气中的 NH 3,进入常压吸收塔的气体含 NH 3体积分数为6%,吸收后气体含NH 3体积分数为0.4%,出口溶液的摩尔比为0.012kmolNH 3 kmol - 水。
此物系的平衡关系为 Y” =2.52X o 气液逆流流动,试求塔顶、塔底处气相推动 力各为多少?(答:顶 厶总= 0.00402,底=0.034 )塔顶气相推动力 Y 2二0.00402,塔底气相推动力 心第=第一丫叩=0.064 —0.03024 = 0.034。
7-4 .用水吸收空气中的甲醇蒸汽,在操作温度300K 下的溶解度系H =2 k m om ; k P a ,传质系数 kG 二 0.056kmol m ° h 二 kPa 」,k L = 0.075knol m h A kmol -1 m 3 o 求总传质系数K G 以及气相阻力在总阻力中所占常数m ,解: 总压力为 100kPa o (答:H = 0.59kmol m " kPa J , m = 0.943)1 17 Ac 0.582kmol m , 101 1000c 0.582 1 J3 H 0.59mol Pa m , Pe 0.98667.4 7 60 ccccc y 0.0099 1 0 01 0131 17 x 0.0 1 0 51 100 + 17 18 7-1 . 100g 水中溶解1gNH 3,从手册查得 20°C 时NH 3的平衡分压为 986.6Pa ,在此浓度以内服从亨利定律。
试求溶解度系数 H (单位为kmol mkPa _1 )和相平衡m 」-0.943o6.42 10“32 18 1000=11.4g0.0099 0.01057-2 100C 时氧在水中的溶解度的表达式P * =3.313 106x ,式中P”为氧在气相中21.3 3.313 10 =6.42 10^,解:0.004 1 - 0.004二 0.0402塔丫,=2.52X =2.52 0.012 =0.03024,塔丫,=2.52X =2.52 0 =0,= 0.064,丫2 =—-1- Y 20.06 1-0.061的分数。
【精品】化工原理第7章课后习题答案.doc
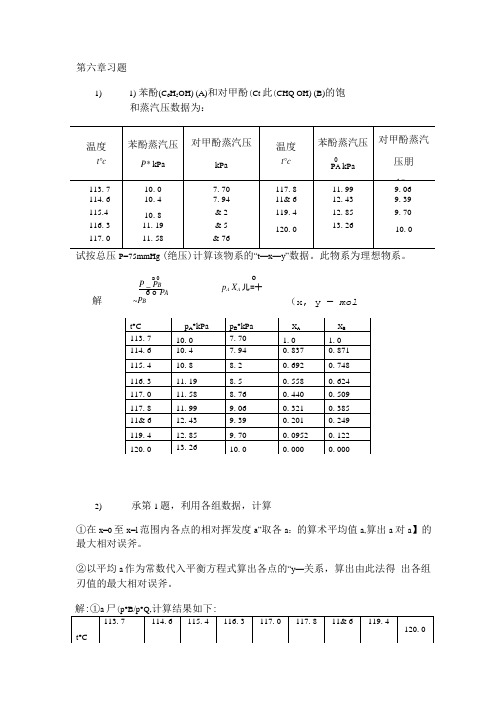
解:(x, y — mol第六章习题1)1) 苯酚(C 6H 5OH) (A)和对甲酚(Ct 此(CHQ OH) (B)的饱和蒸汽压数据为:P=75mmHg “t—x —y”2)承第1题,利用各组数据,计算①在x=0至x=l 范围内各点的相对挥发度a”取各a :的算术平均值a,算出a 对a 】的最大相对误斧。
②以平均a 作为常数代入平衡方程式算出各点的“y—关系,算出由此法得 出各组刃值的最大相对误斧。
D 0P _ P B 6 o - P A ~P B op A X A 儿=十"丝= 1.318最大误差= 1.318-1.299L299 =1.46%60-48.92 68.81-48.92 =0.5576&81x0.55760=0.639a x.y.= ---------------------'1 + ( or -1) x.Q按1.318计,结果如下:3)已知乙苯(A)与苯乙烯(B)的饱和蒸汽压与温度的关系可按下式算得: In 卩:=16.0195-3279.47/(7-59.95)In 加=16.0193-3328.57/(7-63.72)式中P°的单位是mmHg, T的单位是K。
问:总压为60mmHg (绝压)吋,A与B的沸点各为多少。
C ?在上述总压和65°C 吋,该物系可视为理想物系。
此物系的平衡汽、液相浓度各为多少摩尔分率?解:1)令= p,算得的/为A的沸点厶"60 = 16.0195 — 3279.47/( T — 59.95):.T A =334.95^ =61.8° CS B = p,算得的/为B的沸点Ln60 = 16.0193-3328.57/(7- 63.72).•.T B=342.85^=69.7°C2) p = 6QmmHg, t = 65°C = 33&15KLnp°A = 16.0195 — 3279.47 / (338.15 — 59.95)p°A = 68.81mmHgLnp°B = 16.0193 - 3328.57/(338.15-63.72) p°B = 4&92mmHg760-595.3 1436.7 —595.3 -0.19571436.7x0.1957760=0.374)苯(A)和甲苯(B)混合液可作为理想溶液,其各纯组分的蒸汽压计算式为log ^ = 6.906-1211/(/+220.8)log 巩=6.955-1345/0+219.5)式中P。
化工原理(下)课后习题解答

由于 1B A =+x x 故 2 B B A A B A A (d A d M x M x x M M w += (2 B B A A AA A M w M w M w x += 2 ( ( AdAdB BAAB AAA BB AA A1 1 ( 1 M w M w M M M w M w M w M w x +-
代入式(7-25,得 AA AAA AA AB A 2d d 2d d N p p z RT p N N y z c D N 总-=-= 分离变量,并积分得 总 总总 p p p z RT p D N A1 AB A 2ln 21+∆= 52521 1.8510101.3101.3222.5ln kmol/(m s 1.01210 kmol/(m s28.3142730.015101.3 --⨯⨯+⨯=⨯⋅ =⨯⋅ ⨯⨯ 5 2 5 2 B A 33 1.01210kmol/(m s 3.03610kmol/(m s N N --=-=-⨯⨯⋅ =-⨯⋅
0.2002 .99233S ⋅ =⋅ ⨯= = EM H ρ 2. 在温度为 25 ℃及总压为 101.3 kPa 的条件下,使含二氧化碳为 3.0%(体积分数的混合空气与含二氧化碳为 350 g/m 3 的水溶液接触。试判断二 氧化碳的传递方向,并计算以二氧化碳的分压表示的总传质推动力。已知操作条件 下,亨利系数 5 1066.1⨯=E kPa ,水溶液3350/1000 kmol/m 0.008kmol/m 44 c= = 对于稀水溶液,总浓度为 3t 997.8 k m o l /m 55.4318 c= =kmol/m 3 水溶液中 CO 2 的摩尔分数为
解:设 A -NH 3;B -H 2O 离界面 5 mm 处为点 1、两相界面处为点 2,则氨的摩尔分数为 085.0A1=x ,022.0A2=x 915.0085.01A1 1B1=-=-=x x 978.0022.01A2 1B2=-=-=x x 946.0915.0978 .0ln 915 .0978.0ln B1 B2B1B2 BM =-=-= x x x x x 点 1、点 2 处溶液的平均摩尔质量为 (kmol kg 92.17kmol kg 18915.01785.01=⨯+⨯=M (kmol kg 98.17kmol kg 18978.017022.02=⨯+⨯=M 溶液的平均总物质的量浓度为
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化工原理课后习题答案第七章吸收习题解答(总18页)-本页仅作为预览文档封面,使用时请删除本页-第七章 吸 收7-1 总压 kPa ,温度25℃时,1000克水中含二氧化硫50克,在此浓度范围内亨利定律适用,通过实验测定其亨利系数E 为 MPa , 试求该溶液上方二氧化硫的平衡分压和相平衡常数m 。
(溶液密度近似取为1000kg/m 3)解:溶质在液相中的摩尔分数:50640.01391000501864x ==+ 二氧化硫的平衡分压:*34.13100.0139kPa=57.41kPa p Ex ==⨯⨯相平衡常数:634.1310Pa40.77101.310PaE m P ⨯===⨯7-2 在逆流喷淋填料塔中用水进行硫化氢气体的吸收,含硫化氢的混合气进口浓度为5%(质量分数),求填料塔出口水溶液中硫化氢的最大浓度。
已知塔内温度为20℃,压强为×105 Pa ,亨利系数E 为。
解:相平衡常数为:6548.910321.711.5210E m P ⨯===⨯ 硫化氢的混合气进口摩尔浓度:15340.04305953429y ==+若填料塔出口水溶液中硫化氢达最大浓度,在出口处气液相达平衡,即:41max 0.0430 1.3410321.71y x m -===⨯7-3 分析下列过程是吸收过程还是解吸过程,计算其推动力的大小,并在x - y 图上表示。
(1)含NO 2 (摩尔分率)的水溶液和含NO 2 (摩尔分率) 的混合气接触,总压为,T=15℃,已知15℃时,NO 2水溶液的亨利系数E =×102 kPa ;(2)气液组成及温度同(1),总压达200kPa (绝对压强)。
解:(1)相平衡常数为:5131 1.6810Pa1.658101.310Pa E m P ⨯===⨯ *1 1.6580.0030.00498y m x ==⨯=由于 *y y >,所以该过程是吸收过程。
气相推动力为:*0.060.004980.0550y y -=-= 液相推动力为:*10.060.0030.03321.658y x x x m -=-=-=(2)相平衡常数为:5232 1.6810Pa0.8420010Pa E m P ⨯===⨯ *10.840.0030.00252y m x ==⨯=由于 *y y >,所以该过程仍是吸收过程。
气相推动力为:*0.060.002520.0575y y -=-=液相推动力为:*20.060.0030.06840.84y x x x m -=-=-=yx0.000.020.040.060.08y7-4 在某操作条件下用填料塔清水逆流洗涤混合气体,清水物理吸收混合气中的某一组分,测得某截面上该组分在气、液相中的浓度分别为 y = ,x = 。
在该吸收系统中,平衡关系为y = ,气膜吸收分系数k y = ×10-4 kmol / (m 2·s),液膜吸收分系数k x = ×10-5 kmol / ,试求:(1)界面浓度y i 、x i 分别为多少(2)指出该吸收过程中的控制因素,并计算气相推动力在总推动力中所占的百分数。
解:(1)对于稳定吸收过程,气、液两相内传质速率应相等,有: i i ()()y x k y y k x x -=-45i i 1.810(0.014) 2.110(0.02)y x --⨯⨯-=⨯⨯- (1) 在界面处气液两相达平衡,有: i i 0.5y x = (2)联立方程(1)、(2)得 i 0.0265x =,i 0.0132y =(2)气相传质阻力:324115.55610s m /kmol 1.810y k -==⨯⋅⨯ 以气相为基准的液相传质阻力:4250.5 2.38110s m /kmol 2.110x m k -==⨯⋅⨯ 因此,吸收过程为液膜扩散控制。
总气相传质推动力为:0.0140.50.020.004y mx -=-⨯= 气相推动力:i 0.0140.01320.0008y y -=-= 气相推动力在总推动力中所占比例:i 0.00080.20.004y y y mx -==-7-5 在吸收塔内用水吸收混于空气中的甲醇蒸气,操作温度为25℃,压力为105kPa (绝对压力)。
稳定操作状况下,塔内某截面上的气相中甲醇分压为 kPa ,液相中甲醇浓度为 / m 3。
甲醇在水中的溶解度系数H = kmol / (m 3·kPa),液膜吸收分系数k L = ×10-5 m / s ,气膜吸收分系数k G = ×10-5 kmol / (m 2·s·kPa.)。
试求:(1)气液界面处气相侧甲醇浓度y i ;(2)计算该截面上的吸收速率。
解:(1)对于稳定吸收过程,气、液两相内传质速率应相等,有: i i ()()G L k p p k c c -=-55i i 1.210(7.5) 2.110( 2.85)p c --⨯⨯-=⨯⨯- (1) 在界面处气液两相达平衡,有: i i 1p c H=i i 12.162p c =(2) 联立方程(1)、(2)得 3i 5.644kmol/m c =,i 2.611kPa p = 气液界面处气相侧甲醇浓度:i i 2.6110.0249105p y P === (2)该截面上的吸收速率:552A i () 1.210(7.5 2.611) 5.8710kmol/(m s)G N k p p --=-=⨯⨯-=⨯7-6 在及25℃的条件下,用清水在填料吸收塔逆流处理含的SO 2混合气体。
进塔气中含SO 2分别为 (体积分数),其余为惰性气体。
水的用量为最小用量的倍。
要求每小时从混合气体中吸收2000 kg 的SO 2,操作条件下亨利系数 MPa ,计算每小时用水量为多少(m 3)和出塔液中SO 2的浓度(体积分数) 7-7 此题的第二问修改成“出塔气中SO 2的浓度(体积分数)7-8 ”因条件不够计算不出来,原题第二问是计算出塔液中SO 2的浓度(摩尔分数)。
解:20X =,1110.040.417110.04y Y y ===-- 相平衡常数为:634.131040.77101.310E m P ⨯===⨯ 由于是低浓度吸收,有:40.77M m ≈= 由物料衡算得:122000()=31.25kmol/h 64V Y Y -=12min12()31.253055.31kmol/h 0.41740.77V Y Y L Y X M-===- min 1.54582.97kmol/h L L ==每小时用水量:34582.971882.494m /h 1000Q ⨯==由物料衡算得:121()4582.9731.25kmol/h L X X X -==10.00682X =出塔液中SO 2的浓度:1110.006820.00677110.00682X x X ===++7-9 用清水在吸收塔中吸收NH 3-空气混合气体中的NH 3,操作条件是:总压,温度为20℃。
入塔时NH 3的分压为,要求回收率为98%。
在 和20℃时,平衡关系可近似写为 Y * = X 。
试问:(1) 逆流操作和并流操作时最小液气比 (L / V )min 各为多少由此可得出什么结论(2)若操作总压增为 kPa 时,采用逆流操作,其最小液气比为多少并与常压逆流操作的最小液气比作比较讨论。
解:1 1.33320.0133101.3 1.3332p Y P p ===--, 21(10.98)0.020.01330.000266Y Y =-=⨯=20X =(1)逆流操作时最小液气比:12min 120.01330.000266() 2.6850.01332.742.74Y Y L V Y X --===-并流操作时最小液气比:12min 20.01330.000266()134.260.0002662.742.74Y Y L V Y --===由此可知:若完成相同的吸收任务,并流操作时的用水量比逆流操作时用水量大。
(2)由于亨利常数仅是温度的函数,若总压增加,相平衡常数会发生变化,又因为,该吸收为低浓度吸收,有:M m ≈ 11 2.74101.3277.562kPa E M P ≈=⨯= 22277.5620.913303.9E M P ≈== 加压后,逆流操作时的最小液气比:12min 1220.01330.000266()0.8950.01330.913Y Y L V Y X M --===- 由此可知,完成相同的吸收任务,加压后,逆流操作的用水量小于常压的用水量,但是加压会增加能耗,这是以增大能耗为代价来减少吸收操作的用水量。
7-10 在一逆流吸收塔中用吸收剂吸收某混合气体中的可溶组分。
已知操作条件下该系统的平衡关系为Y =,入塔气体可溶组分含量为9%(体积),吸收剂入塔浓度为1%(体积);试求液体出口的最大浓度为多少? 7-11 7-12 解:1110.090.0989110.09y Y y ===--由题可得,液体出口的最大浓度是与入塔气体浓度相平衡的液体浓度: 11,max 0.09890.0861.15Y X M === 液体出口的最大浓度:11,max 10.0860.0792110.086X x X ===++7-13 在填料塔内用清水逆流吸收某工业废气中所含的二氧化硫气体,SO 2浓度为(体积分数),其余可视为空气。
冷却后送入吸收塔用水吸收,要求处理后的气体中SO 2浓度不超过(体积分数)。
在操作条件下的平衡关系为Y * = 48X ,所用液气比为最小液气比的倍。
求实际操作液气比和出塔溶液的浓度。
并在Y -X 图上画出上述情况的操作线与平衡线的相互关系。
解:1110.080.0870110.08y Y y ===--,2220.0040.00402110.004y Y y ===--,20X = 逆流操作的最小液气比:12min 10.08700.00402()45.7820.087048Y Y L VY M--=== 实际操作液气比:min 1.6() 1.645.78273.251LL V V==⨯=由操作线方程可得: 121()0.08700.004020.0011373.251V Y Y X L --=== 出塔溶液的浓度:1110.001130.00113110.00113X x X ==≈++0.020.040.060.080.10YY 1Y *=48X7-14 常压()用水吸收丙酮——空气混合物中的丙酮(逆流操作),入塔混合气中含丙酮7%(体积),混合气体流量为1500 m 3 / h (标准状态),要求吸收率为97%,已知亨利系数为200kPa (低浓度吸收,可视M≈m )。
