7.3 气体的等容变化 查理定律
气体三大定律及状态方程

由玻意耳定律 p1V1=p2V2,得
0 +ℎ
解得 h=2 m。
答案:2 m
=
0.1m·
。
0.12m·
例2 一定质量的气体,在体积不变时,将温度由50
℃ 加热到100 ℃,气体的压强变化情况是( D )
A.气体压强是原来的2倍
50
B.气体压强比原来增加了273
C.气体压强是原来的3倍
50
C
p
查理定律:
C
T
V
盖-吕萨克定律:
C
T
p1V1 p2V2
pV
C 或
T1
T2
T
1.(多选)对于一定质量的理想气体,可能发生的过
程是( AC )
A.气体的压强增大、温度升高,体积增大
B.气体的压强增大、温度不变,体积增大
C.气体的压强减小、温度降低,体积不变
D.气体的压强减小、温度升高,体积减小
D.气体压强比原来增加了323
例3 (多选)一定质量的某种气体自状态A经状态C
变化到状态B,这一过程在V-T图上表示如图所示,
图象的应用
是( AD )
【例 3】
A.在过程AC中,气体压强不断变大
B.在过程CB中,气体压强不断变小
C.在状态A时,气体压强最大
D.在状态B时,气体压强最大
一定质量的某种气体自状态 A 经状态 C 变
5Pa,g取10m/s2)
为p
=1.0×10
0
以根据玻意耳定律问题即可解决。
解析:确定研究对象为被封闭的那部分气体,玻璃管下潜的过程
中气体的状态变化为等温过程。
设潜入水下的深度为 h,玻璃管的横截面积为 S。气体的初末状
高中物理:气体的等容变化和等压变化详解
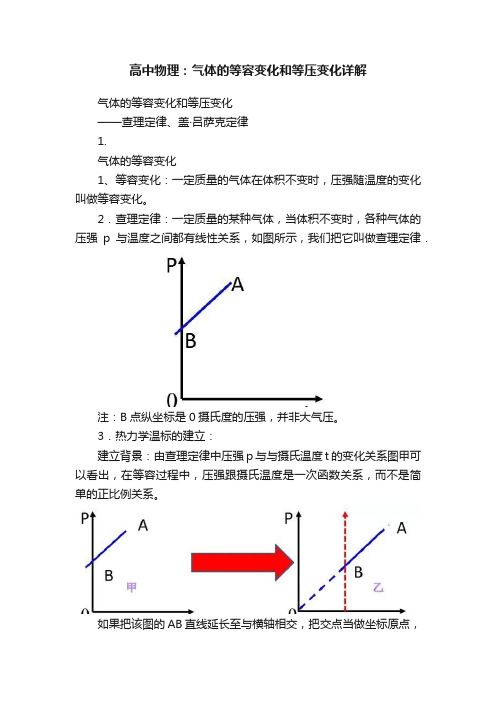
高中物理:气体的等容变化和等压变化详解气体的等容变化和等压变化——查理定律、盖·吕萨克定律1.气体的等容变化1、等容变化:一定质量的气体在体积不变时,压强随温度的变化叫做等容变化。
2.查理定律:一定质量的某种气体,当体积不变时,各种气体的压强p与温度之间都有线性关系,如图所示,我们把它叫做查理定律.注:B点纵坐标是0摄氏度的压强,并非大气压。
3.热力学温标的建立:建立背景:由查理定律中压强p与与摄氏温度t的变化关系图甲可以看出,在等容过程中,压强跟摄氏温度是一次函数关系,而不是简单的正比例关系。
如果把该图的AB直线延长至与横轴相交,把交点当做坐标原点,建立新的坐标系(图乙)此时压强与温度的关系就是正比例关系了。
图乙坐标原点的意义“气体压强为零时其温度为零”,由此可见,为了使一定质量的气体在体积不变的情况下,压强与体积成正比,只需要建立一种新的温标就可以了。
在现实中通过对大量的“压强不太大(相对标准大气压),温度不太低(相对于室温)”的各种不同气体做等容变化的实验数据可以证明“一定质量的气体压在强不太大,温度不太低时,坐标原点代表的温度就是热力学温度的零度,这就是热力学温度零点的物理意义。
由此可见:热力学的零点就规定为气体压强为零的温度。
在建立热力学温标之前,人们已经建立了华氏、摄氏温标,但这些温标都是与测温物质的热学性质有关,当采用不同的测温物质去测量同一温度时会产生一定差异,这种差异是不能克服的。
而由热力学温标的建立可知:热力学温度是在摄氏温度的基础上建立起来的,零点的确定与测温物质无关,因此热力学温标是一种更为简便科学的理论的温标,它的零度不可能达到。
又叫绝对零度。
4、查理定律的热力学温标描述:——查理定律:(1).查理定律:一定质量的某种气体,在体积不变的情况下,压强p与热力学温度T成正比。
(2).表达式:注:这里的C和玻意耳定律表达式中的C都泛指比例常数,它们并不相等。
这里的C与气体的种类、质量和压强有关。
气体的等容变化和等压变化

例2.将质量相同的同种气体A、B分别密封在体积不同 的两个容器中,保持两部分气体体积不变,A、B两部 分气体压强随温度t的变化图线如图所示,下列说法正 确的有( ABD ) A.A部分气体的体积比B部分小 B.A、B直线延长线将相交于t轴 上的同一点 C.A、B气体温度改变量相同时, 压强改变量也相同 D.A、B气体温度改变量相同时, A部分气体压强改变量较大 注意:同质量的气体在不同体积下的等容线中,斜 率大的体积小
P P2 P 1 T1 T2 T
注意:P与热力学温度T成正比,不与摄氏温度成正比,
但压强的变化P 与摄氏温度t的变化成正比.
3、适用条件:压强不太大,温度不太低
4、图象表述:
同一图像上的各点描述的气体状态参量中,气体的体 积相同,因此图像叫等容线。 注意:1、P-T图像是正比例函数,等容线与T轴交点 为0开. P-t图像是一次函数,等容线与t轴交点为273.15℃ 2、图像的斜率与体积的关系 斜率越小体积越大
习题
.对于一定质量的气体,在体积不变时,压强增大 到原来的两倍,则气体温度的变化情况是( B ) A.气体的摄氏温度升高到原来的两倍 B.气体的热力学温度升高到原来的两倍 C.气体的摄氏温度降为原来的一半 D.气体的热力学温度降为原来的一半
基本规律简单应用
例.如图所示,气缸中封闭着温度为100℃的空气,一 重物用绳索经滑轮跟缸中活塞相连接,且处于平衡状 态,这时活塞离气缸底的高度为10 cm,如果缸内空 气变为0℃。 ①重物是上升还是下降? ②这时重物将从原处移动多少厘米? (设活塞与气缸壁间无摩擦)
二、气体等压变化
1、盖·吕萨克定律: 一定质量的某种气体, 在压强不变的情况下,其体积V与热力学温度T 成正比。
《气体的等容变化和等压变化》 讲义

《气体的等容变化和等压变化》讲义一、引入在我们的日常生活和许多科学研究及工程应用中,气体的状态变化是一个非常重要的现象。
而气体的等容变化和等压变化,是研究气体性质时经常会遇到的两种典型情况。
二、气体的等容变化当一定质量的气体体积保持不变时,所发生的状态变化称为等容变化。
1、查理定律查理定律指出:一定质量的某种气体,在体积不变的情况下,压强p 与热力学温度 T 成正比。
数学表达式为:p/T = C(C 为常数)为了更好地理解查理定律,我们来举个例子。
假设一个密封的刚性容器中装有一定量的气体,容器的体积是固定的。
当我们给这个容器加热时,气体的温度升高,分子的热运动加剧,碰撞容器壁的频率和力度都会增加,从而导致气体的压强增大。
2、等容变化的图像图像是一条过原点的直线。
这条直线的斜率与气体的种类有关,不同的气体具有不同的斜率。
3、应用等容变化在实际中有很多应用。
比如,在汽车发动机的工作过程中,气缸内气体的燃烧会导致温度急剧升高,由于气缸的体积基本不变,所以气体压强会迅速增大,从而推动活塞做功。
三、气体的等压变化当一定质量的气体压强保持不变时,所发生的状态变化称为等压变化。
1、盖吕萨克定律盖吕萨克定律表明:一定质量的某种气体,在压强不变的情况下,体积 V 与热力学温度 T 成正比。
数学表达式为:V/T = C'(C'为常数)同样通过一个例子来理解。
想象有一个带有可移动活塞的气缸,里面充满了一定质量的气体,并且气缸与外界大气相通,保持压强不变。
当给气缸加热时,气体温度升高,分子热运动加剧,为了保持压强不变,活塞会向外移动,从而使气体的体积增大。
2、等压变化的图像出的图像也是一条过原点的直线。
这条直线的斜率同样与气体的种类有关。
3、应用等压变化在生活和工业中也十分常见。
例如,热气球的工作原理就利用了等压变化。
当对热气球内的气体加热时,气体体积膨胀,但由于外界大气压基本不变,热空气的密度变小,从而产生浮力使热气球上升。
气体三大定律以及状态方程

A.一定不变 B.一定减小 C.一定增加 D.不能判定怎样变化
4.一定质量的气体,经历一膨胀过程,这一过程可以
用图所示 的直线ABC来表示,在A、B、C三个状态 上
,气体的温度TA、TB、TC相比较,大小关系为( C )
A.TB=TA=TC B.TA>TB>TC C.TB>TA=TC D.TB<TA=TC
=
0.1m·������ 0.12m·������
。
解得 h=2 m。
答案:2 m
例2 一定质量的气体,在体积不变时,将温度由50
℃ 加热到100 ℃,气体的压强变化情况是( D )
A.气体压强是原来的2倍 B.气体压强比原来增加了25703
C.气体压强是原来的3倍 D.气体压强比原来增加了 35203
几何性质
力学性质
热学性质
体积V
压强p 三者关系
?
温度T 控制变量法
气体的等温变化
1.玻意耳定律 一定质量的某种气体,在温度不变 的情况下,压强p与体积V成反比。
pV=C 或
p1V1= p2V2
2.气体等温变化的p-V图
P 对于一定质量的
A 气体:T1<T2
B
T2
T1
0
V
气体的等容变化
1.查理定律 一定质量的某种气体,在体积不变的 情况下,压强p与热力学温度T成正比。
V C 或
T
V1 V2 T1 T2
2.气体等压变化的V-T图
V
p
P
0
T
0
V0
T
玻意耳定律的应用
例1 【粗例细2】均匀粗细的均玻匀璃的玻管璃内管封内闭封闭一一段段长长为为1122ccmm的的空空气气柱柱。. 一一个个人人手手持持玻璃玻管璃开管口向开下口潜向入下水中潜,当入潜水到中水,下当某潜深到度时水看下到某水 深 度 为进不以入变根度.p(0点玻据,=取时玻1璃玻拨水.璃看管意:0面由×管到口耳上于定1水内大2玻0律c气璃5m气进P问,压管a求体入,题强内人g即温玻取为气潜可璃度体入1p0解0温=水管视m1决度/中.0为口s。×不的212不)变0深c5,m变度P被,a。,封求,g (取闭玻人取气1璃潜水0体管m入面的/内s2质水上气) 量体中大也温的气不度深压变视,强所为
高中物理:气体的等容变化和等压变化

4.V-T 和 V-t 图象. (1)V-T 图象:一定质量的某种气体,在等压过程中, 气体的体积 V 和热力学温度 T 的图线是过原点的倾斜直 线,如下图左所示,p1<p2,即压强越大,斜率越小.
(2)V-t 图象:一定质量的某种气体,在等压过程中, 体积 V 与摄氏温度 t 是一次性函数,不是简单的正比例关 系,如上图右所示,图象纵轴的截距 V0 是气体在 0 ℃时 的体积,等压线是一条延长线通过横轴上-273.15 ℃的 倾斜直线,且斜率越大表示压强越小.
1.气体的等容变化. 气体的等容变化:气体体积保持不变的情况下所发 生的状态变化叫等容变化. 2.等容变化的规律. (1)实验条件: ①气体质量一定; ②气体体积不变.
(2)实验过程: ①在室温 t1 下将一定质量的气体封闭在烧瓶中,记 下气体的体积 V1 和压强 p1=p. ②把烧瓶放入冰水混合物的容器里,记下这时温度 为 t2=0 ℃,调整压强计保持气体体积不变,记下压强 p2=p-h.如图所示.
知识点一 气体的等容变化
提炼知识 1.等容变化:一定质量的某种气体在体积不变时压 强随温度的变化规律. 2.查理定律: (1)内容:一定质量的某种气体,在体积不变的情况 下,压强 p 与热力学温度 T 成正比.
(2)表达式:p=CT 或_T_p_11=__Tp_22__或pp12=TT12. (3)图象:一定质量的气体,在体积不变的情况下, 压强与热力学温度成正比.在 p-T 图上等压线为过原点 的倾斜直线,在 p-t 图上等容线不过原点,其反向延长 线与时间轴的交点为-273.15℃.
判断正误
1.气体在等容变化时,升高相同的温度所增加的压 强一定相同.(√)
2.由查理定律知,在体积不变的情况下压强与温度 成正比.(×)
气体的等容变化和等圧変化

解析:ABD
由P-t图像可知,图像的斜率表示 常数C,相同质量的同种气体,C与 气体的体积有关。P-t图像中,图像越 陡,体积越小A、B正确。由于A气体 的斜率较大,改变相同的温度,A气 体的压强变化较大,D正确。
作业:
固学案P11 7 ,9 题
学习目标:
1.掌握查理定律的内容及表达式(重点) 2.能理解P-T或P-t图像的问题(难点) 3.能运用查理定律解决生活中的一些问题。(难点)
气体的等容变化
1.等容变化:气体在体积不变的情况下压强随热力学温度的 变化。
2.查理定律:一定质量的某种气体,在体积不变的情况下, 压强p与热力学温度T成正比( p T ) 。
VA SA
15cm
故活塞N向右移动的距离是 S LA LA 5cm
②末解对态得压:BT中B强 气为pBpBT体B ,p4B00困K p活A ∴塞43tBM=10保15 P2a持7根℃在据原查位理置定不律动得,:TpBB
pB TB
小结:
1.查理定律的内容及表达式 2.表达式中各物理量的理解 3.查理定律的适用条件 4.对P-T,P-t图像的认识
①活塞N向右移动的距离是多少厘米? ②B气缸中的气体升温到多少摄氏度?
【解析】(1)5cm (2)127℃
试题分析:
①加力F后,A中气体a 3
对A中气体:由玻意耳定律:
则得 VA
pAVA pA
3 4 VA
pAVA pAVA
初态时, , LA
VA SA
气体的等容变化 查理定律

气体的等容变化查理定律北京第35中学郑人凯一、教学目标.物理知识要求:(1)知道什么是气体的等容变化过程;(2)掌握查理定律的内容、数学表达式;理解p-t图象的物理意义;(3)知道查理定律的适用条件;(4)会用分子动理论解释查理定律。
.通过演示实验,培养学生的观察能力、分析能力和实验研究能力。
.培养学生运用数学方法解决物理问题的能力——由图象总结出查理定律。
二、重点、难点分析.查理定律的内容、数学表达式、图象及适用条件是重点。
.气体压强和摄氏温度不成正比,压强增量和摄氏温度成正比;气体原来的压强、气体在零摄氏度的压强,这些内容易混淆。
三、教具.引入新课的演示实验带有橡皮塞的滴液瓶、加热装置。
.演示一定质量的气体保持体积不变时,压强与温度的关系查理定律演示器、水银气压计、搅棒、食盐和适量碎冰、温度计、保温套、容器。
四、主要教学过程(一)引入新课我们先来看一个演示实验:滴液瓶中装有干燥的空气,用涂有少量润滑油的橡皮塞盖住瓶口,把瓶子放入热水中,会看到塞子飞出;把瓶子放在冰水混合物中,拔掉塞子时会比平时费力。
这个实验告诉我们:一定质量的气体,保持体积不变,当温度升高时,气体的压强增大;当温度降低时,气体的压强减小。
请学生举一些生活中的实例。
下面我们进一步研究一定质量的气体保持体积不变,气体的压强随温度变化的规律。
(二)教学过程设计.气体的等容变化结合演示实验的分析,引导学生得出:气体在体积不变的情况下所发生的状态变化叫做等体积变化,也叫做等容变化。
.一定质量的气体在等容变化过程中,压强随温度变化的实验研究(1)实验装置——查理定律演示器请学生观察实物。
请学生结合实物演示,弄明白如下问题:①研究对象在哪儿?②当A管向上运动时,B管中的水银面怎样变化?③当A管向下运动时,B管中的水银面怎样变化?④怎样保证瓶中气体的体积不变?⑤瓶中气体的压强怎样表示?(当B管中水银面比A管中水银面低时;当B管中水银面比A管中水银面高时)(2)用气压计测量大气压强0= mmHg(注意水银气压计的读数方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
解:因为气体体积不变,故气体为等容变化。
初态:P1= 4× 10 Pa,T1=t1+273=27+273=300K。 末态:P2未知, 由查理定律可知: P1/T1=P2/T2 变形可得: P2=P1 (T2/T1) = 4× 10 310/300 =4.13×10 (Pa)
4 4 4
T2=t2+273=37+273=310K。
答:它的压强为4.13 ×10 Pa。
4
小
结
本节介绍一定质量的气体在压强不太大,温度不太低的情况 下,保持体积不变时,气体压强随温度的变化关系: 通过实验得出变化规律---查理定律: ( Ⅰ) 一定质量的气体,在体积不变的情况下, 温度 每升高(降低)1℃ ,气体的压强增大(减小)0℃ 时压强1/273 数学表达式: (Pt-P0) /t=P0/273 它的压强跟热力学温度成正比。
实验方法:
调节水银压强计的可动管A, 使B管水银面始终保持在同一水 平面上。改变气体温度,得到多 次压强值。
实验步骤一: 实验步骤一:
一只烧瓶上连一根玻璃管, 用橡皮管把它跟一个水银压强 计连在一起,从而在烧瓶内封 住一定质量的空气。 上下移动压强计,使得其 中的两段水银柱的高度在同一 水平面上。标记下B管水银柱 的高度。
℃
(Ⅱ) 一定质量的气体,在体积不变的情况下,
数学表达式:
P1 / T1 = P2 / T2
(T为热力学温度)
练一练
1.封闭在容器中的气体,当温度升高时,下面的哪 个说法是正确的( C )(不计容器的膨胀) A.密度和压强均增大; B.密度增大,压强减小; C.密度不变,压强增大; D.密度增大,压强不变。 .一个密闭容器里的气体,在0℃时压强8×104Pa, 2 5 给容器加热,气体的压强为1.0×10 Pa时温度升高到多少摄 氏度? 68.25℃
制作:徐旺苗
2000年5月26日
(Pt-P0)/t=P0/273℃
(II) 将上式变形得:Pt/(273+t)=P0/273
得公式:
P1/T1=P2/T2
( 气体压强与热力学温度成正比。)
实验图象: 实验图象:
实验图象可分为P—t图象和P—T图象 。但可用 下图一同表现出来。
图中以O为原点的是P ` -T图象,以O 为原点的 是P-t图象。 O`:坐标(273, 0)。 Po:0℃ 时气体的压强 大小。 θ :tgθ =P0/273 0℃时压强的1/273。 想一想:为什么O点附近用虚线?
将烧瓶放入某一温度的 热水中(水温可由温度计测 出T2),观察压强计中水银 柱的高度变化情况。 气体温度上升,A柱上 升,B柱下降,瓶内气体体 积增大。 上提A管,仍然使B管 水银柱的高度与开始时相同, 保证气体体积不变。再记录 下AB管水银柱高度之差H2, 以得出内外气体压强之差。
实验处理: 实验处理:
二.思考:
为什么隔夜的水杯( 半杯水 ) 难以打开?
可否认为气体的压强随温度的升高而升高,随温度的降低而降低?
实验目的
查 理 定 律
实验器材 实验方法 实验过程 数据处理 步骤一积保持不变的情况下,它的压强 怎样随温度的变化而变化。
实验仪器:
烧瓶(带软木塞),玻璃管, 橡皮连接管,水银压强计,温度计, 盛水容器,冰,冷水,(几种不同 温度的)热水。
7.3 气体的等容变化 查理定律
学校:霍邱二中 授课:徐旺苗 日期:二OOO年五月十六日
Back
一. 气体的等容变化
目 录
二. 查理定律 (实验定律) 三. 气体等容变化的图象 四. 查理定律的微观解释 五. 例题 六. 小结 七.练习
气体的等容变化
一.定义: 定义
质量一定的气体,在体积不变的情况下 所发生的变化过程.
微观解释:
一定质量的气体,在体积 不变时,它的单位体积内的分 子数不变,当温度升高时,气 体分子的平均动能增大,平均 速率增大,压强增大,反之, 压强减小。
例题精选:
1.封闭在容积不变的容器内装有一定质量的气体,当它的温度为27℃时, 其压强为4× 104Pa,那么,当它的温度升高到37℃ 时,它的压强为多大?
一.由水银压强计分别读出多次的压强P0,P1,P2,P3。 二.由温度计所测出相应的摄氏温度t0, t1,t2,t3 。 三.由以上数据得出气体压强和温度之间的定性关系
压强随着温度的升高而增大,随着温度的降低 而减小,但压强P和温度t不是正比关系。
查理定律
一定质量的气体,在体积不变的情况下, (I) 温度每升高 (降低)1℃ ,气体的压强增大(减 小)0℃时压强 的1/273。 数学表达式为:
实验步骤二: 实验步骤二:
将烧瓶放入纯净冰水混 合物中,观察压强计水银柱 的高度变化情况。 瓶中气温降低(温度为 T1),B柱上升,A柱下降。瓶 中气体体积减小。 A管下降,使B管中水银 柱高度与开始时相同,保证气 体体积不变. 记录下AB水银柱的高 度差H1,以得出内外气体压强 之差。
实验步骤三: 实验步骤三:
