EGFR信号通路在黑色素瘤中调节紫杉醇耐药及侵袭转移机制探讨
肿瘤药物耐药机制及对策研究进展如何

肿瘤药物耐药机制及对策研究进展如何肿瘤是严重威胁人类健康的疾病之一,而肿瘤药物治疗是对抗肿瘤的重要手段之一。
然而,肿瘤细胞对药物产生耐药性是导致肿瘤治疗失败的主要原因之一。
深入研究肿瘤药物耐药机制并寻找有效的对策,对于提高肿瘤治疗效果、改善患者预后具有重要意义。
一、肿瘤药物耐药机制(一)肿瘤细胞内在因素1、药物靶点改变肿瘤细胞可以通过基因突变等方式改变药物作用的靶点,使药物无法有效地与之结合发挥作用。
例如,某些肺癌患者在使用针对表皮生长因子受体(EGFR)的靶向药物治疗后,肿瘤细胞可能会出现新的EGFR 突变,导致药物失效。
2、细胞信号通路异常肿瘤细胞内的信号通路复杂且相互关联。
当一条信号通路被药物抑制时,肿瘤细胞可以激活其他代偿性的信号通路来维持其生存和增殖,从而导致耐药。
例如,PI3K/AKT/mTOR 信号通路在多种肿瘤中异常活跃,当使用针对其中某个节点的药物时,肿瘤细胞可能通过激活其他旁路来逃避药物的作用。
3、药物转运蛋白异常肿瘤细胞表面的药物转运蛋白可以将药物排出细胞外,减少细胞内药物的浓度,从而导致耐药。
例如,P糖蛋白(Pgp)是一种常见的药物外排泵,其过度表达会使肿瘤细胞对多种化疗药物产生耐药性。
4、细胞凋亡抵抗细胞凋亡是肿瘤细胞受到药物作用后的一种常见死亡方式。
然而,肿瘤细胞可以通过改变凋亡相关基因的表达或调控凋亡信号通路,从而抵抗药物诱导的凋亡,导致耐药。
(二)肿瘤细胞外在因素1、肿瘤微环境肿瘤微环境包括肿瘤细胞周围的基质细胞、细胞外基质、血管和免疫细胞等。
肿瘤微环境可以通过分泌细胞因子、生长因子等物质,为肿瘤细胞提供生存和耐药的条件。
例如,肿瘤相关巨噬细胞可以分泌一些因子促进肿瘤细胞的存活和耐药。
2、血管生成肿瘤组织的血管生成异常丰富,为肿瘤细胞提供了充足的营养和氧气供应。
同时,异常的血管结构也影响了药物在肿瘤组织中的分布和渗透,导致药物无法有效地到达肿瘤细胞,从而产生耐药。
EGFR基因突变及其检测方法的研究进展

EGFR基因突变及其检测方法的研究进展高云;陈嘉昌;朱振宇;彭焕玉【摘要】表皮生长因子受体(EGFR)属于酪氨酸激酶受体,它介导的信号转导途径调节细胞的生长、增殖和分化.在癌症中发现EGFR酪氨酸激酶区常发生各种突变,这些突变和酪氨酸激酶抑制剂的疗效密切相关.因此,EGFR突变的检测对癌症的个体化治疗具有重要的参考价值.目前常用的EGFR突变检测方法有测序法、PCR-SSCP、突变体富集PCR、ARMS、微数字PCR、HRM、DHPLC.【期刊名称】《分子诊断与治疗杂志》【年(卷),期】2011(003)001【总页数】7页(P51-57)【关键词】EGFR;突变;检测【作者】高云;陈嘉昌;朱振宇;彭焕玉【作者单位】中山大学中山医学院,广东,广州510080;中山大学达安基因诊断中心,广东,广州510665;中山大学中山医学院,广东,广州510080;中山大学达安基因诊断中心,广东,广州510665【正文语种】中文EGFR已成为近年来肿瘤治疗研究和抗肿瘤药物筛选的热点,有关EGFR突变与肿瘤发生以及EGFR突变在分子靶向治疗中的作用日益受到人们的关注。
EGFR突变是癌症患者是否对TKI敏感的强预测因子,因此EGFR基因突变的检测能为肿瘤靶向治疗提供依据。
现就EGFR基因突变及其主要检测方法做一综述。
1.1 EGFR的生物学特征人类表皮生长因子受体家族(epidermal growth factor receptor family, EGFR家族)属于酪氨酸激酶受体家族,也被称作HER家族或erbB家族。
EGFR家族由四个成员组成,分别是erbB1(EGFR/ HER1),erbB2 (neu/HER2),erbB3(HER3),erbB4(HER4)。
EGFR基因位于第七号染色体短臂上(7p12),长约118 kb,由28个外显子组成。
其转录形成的mRNA长约5.6 kb,编码的EGFR是分子量为170 kD的跨膜糖蛋白,编码蛋白由1186个氨基酸组成,具有酪氨酸激酶(tyrosine kinase, TK)活性,是传递胞外信号到胞内的重要途经蛋白。
EGFR信号通路

EGFR信号通路
18
1/3/2021
EGFR信号通路
19
1/3/2021
EGFR信号通路
20
• Thank you
1/3/2021
EGFR信号通路
21
1/3/2021
EGFR信号通路
5
Protein Function
Docking sites on EGFR
GRB-2 Adaptor
pY1068, pY1086
Nck
Adaptor
ND
Crk
Adaptor
ND
Shc
Adaptor
pY1148, pY1173
Dok-R Adaptor
pY1086, pY1148
1egfr信号通路egfr主要位于细胞质膜上属受体酪氨酸激酶家族受到egf等配体激活后通过二聚化引发胞内域形成酪氨酸激酶活性并进一步激活下游的细胞信号转导通路完成跨膜信号转导过程
EGFR主要 位于细胞质膜上,属受体酪氨酸激酶家族,受到 EGF等配体激活后通过二聚化引发胞内域形成 酪氨酸激酶活性,并进一步激活下游的细胞信号 转导通路,完成跨膜信号转导过程。
1/3/2021
EGFR信号通路
14
1/3/2021
EGFR信号通路
15
1/3/2021
EGFR信号通路
16
1/3/2021
EGFR信号通路
17
实验肿瘤学中EGFR的作用
1.促进肿瘤细胞的体内外增殖 2.促进肿瘤新生血管的生长 3.促进肿瘤的远处转移 4.保护肿瘤细胞不进入凋亡
1/3/2021
EGFR信号通路
8
• 硕士
1/3/2021
2012年度上海市自然科学基金面上项目立项清单
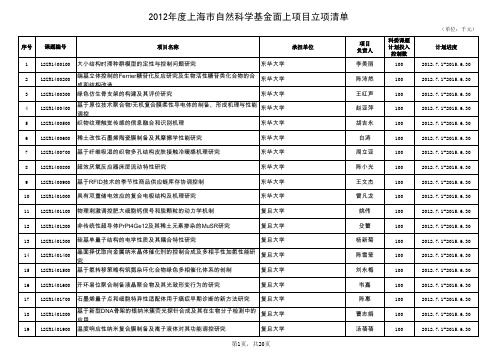
56 12ZR1405600 Relaxin-3在术后认知功能障碍中的作用及机制研究
复旦大学附属中山医院
57 12ZR1405700 姜黄素抗癫痫作用的γ氨基丁酸转运体机制及相关mTOR信号通路研究 复旦大学附属中山医院
58 12ZR1405800 癌旁肝细胞表达/分泌IL-2调节炎症免疫微环境抑制肝癌转移复发的分 复旦大学附属中山医院 子机制
34 12ZR1403400 1H MRS联合DTI新技术量化评估先天性心脏病新生儿脑发育的研究 复旦大学附属儿科医院
35 12ZR1403500 HCV与NK细胞上免疫模式识别受体介导的抗病毒固有免疫相互作用的 复旦大学附属儿科医院
机制研究 36 12ZR1403600 极低出生体重早产婴儿的神经运动发育早期筛查指标的研究:自发性 复旦大学附属儿科医院
进而参与动脉粥样硬化形成的研究
53 12ZR1405300 Smurf2调控结缔组织生长因子抑制肝纤维化的机制研究
复旦大学附属中山医院
54 12ZR1405400 新型经颈单孔内窥镜食管手术的实验研究
复旦大学附属中山医院
55 12ZR1405500 多肽HBSP肾脏保护作用信号通路的动态网络研究
复旦大学附属中山医院
制 31 12ZR1403100 应用家系iPS研究亨廷顿病中纹状体GABA能投射状神经元特异性损伤 复旦大学
的病理机制
32 12ZR1403200 星形胶质细胞瘤IDH1基因突变导致EMT发生相关蛋白筛选
复旦大学
33 12ZR1403300 含氮杂四元环骨架的新型Hedgehog通路抑制剂的设计、合成及抗肿 复旦大学 瘤活性研究
科委课题 计划投入
控制数 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100
EGFR—TKI在非小细胞肺癌中的耐药机制及治疗研究进展

EGFR—TKI在非小细胞肺癌中的耐药机制及治疗研究进展表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosine kinase inhibitor,EGFR-TKI)靶向治疗是非小细胞肺癌(NSCLC)治疗领域的里程碑,使晚期NSCLC的治疗从标准含铂双药的化疗时代迈进了靶向治疗时代。
但随着EGFR-TKI药物临床应用其耐药问题的出现不可避免,文章就NSCLC患者EGFR-TKI获得性耐药的分子机制及目前已知的治疗策略作一论述。
隨着全球工业化快速发展,空气污染越来越严重,肺癌已成为发病率和死亡率均居世界第一的恶性肿瘤,其中最常见的肺癌类型为非小细胞肺癌(non small cell lung cancer,NSCLC),占肺癌总数的80%~85%[1]。
目前,大多数患者确诊时已处于NSCLC晚期,失去了手术根治的机会,然而传统的放化疗似乎进入了平台期,无法满足进展期NSCLC的治疗需要。
表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosine kinase inhibitor,EGFR-TKI)靶向治疗是肺癌治疗领域的里程碑,能延长EGFR敏感突变NSCLC患者无疾病进展期(progression free survival,PFS),改善他们的生活质量。
随着EGFR-TKI 药物临床应用其耐药问题的出现不可避免,一般在8~10个月出现[2],耐药已成为限制EGFR-TKI临床应用的瓶颈。
因此阐明EGFR-TKI的耐药机制,寻找新的药物靶点,研发新的药物成为临床中亟待解决的问题。
1 获得性EGFR-TKI耐药机制表皮生长因子受体(epidermal growth factor receptor,EGFR)突变是肺癌最常见的驱动基因之一,尤其在亚裔人群的不吸烟肺腺癌患者中EGFR突变比例高达60%左右[3]。
乳腺癌抗-EGFR治疗的机制和临床进展

信 号传 导途 径 , 响 基 因表 达 , 制 细胞 分 化 和 增 殖 等 生 物 影 控 效 应 E 。T D含 有 活 化 位 点 可 以 结 合 酶 基 团 和 A P 从 而 4 K ] T,
使 酶基 团磷 酸 化 并 伴 随发 生 A P 水 解 。 ( ) 控 结 构 域 为 T 3调
吕宁 , 孔亚 楠 , 小明 ,韦尉 东 谢
中 山大 学 肿瘤 防治 中心 、 南肿 瘤 学 国 家 重 点实 验 室 乳腺 科 ( 州 50 6 ) 华 广 10 0 尽 管在 过 去 的 2 0年 中我 们 可 以使 用 一 系列 新 的 生 物 标 记 物和 广 为接 受 的临 床诊 疗指 引对 乳腺 癌 进 行 分 类 , 是 我 但
一
化 或 者 异 二 聚化 , 通过 位 于细 胞 内结构 域 的 特 殊 酪氨 酸 残 并 基 的转磷 酸化 机 制 使 其 自身 活 化 。 磷 酸 化 的 E F G R经 过 构 象改 变 , 而制 造 出接 头蛋 白 . 酶 和 细胞 内信 使 结 合 位 点 , 从 激
进 一 步 激 活 下 游的 R s P3 a 和 IK信 号传 导 通路 。
概括 的讲 , G R 可 以 分为 两 个 功 能 亚 结 构 。 细 胞 外 结 E F
。
该 家族 由 4 类 关 系 密 切 的 成 员 组 成 ,包 括 HER 一 1
( G R Eb 1 、 E 一 ( G R E F 或 rB ) H R 2 E F 2或 N u 、 E 3 Eb 3 e ) H R ( rB )
F 治 疗是 否 有 效 的标 准 … 。 因此 , 于 这 一 难题 我 们 必 须 R 基 强 化 乳腺 癌 的诊 断依 据 , 以提 高现 有 治 疗 策 略 的 疗 效 , 其 尤 是 改进 针 对 E F 的 单 克 隆 抗 体 和 小 分 子 酪 氨 酸 激 酶 抑 制 GR
靶向抗肿瘤药物的研究进展

靶向抗肿瘤药物的研究进展靶向抗肿瘤药物的研究进展近年来,随着肿瘤生物学及相关学科的飞速发展,人们逐渐认识到细胞癌变的本质是细胞信号转导通路的失调导致的细胞无限增生,随之而来的是抗肿瘤药物研发理念的重大转变。
研发焦点正从传统细胞毒药物向针对肿瘤发生发展过程中众多环节的新药方向发展,这些靶点新药针对正常细胞和肿瘤细胞之间的差异,可达到高选择性、低毒性的治疗效果,从而克服传统细胞毒药物的选择性差、毒副作用强、易产生耐药性等缺点,为此,肿瘤药物进入了一个崭新的研发阶段。
目前发现的药物靶点主要包括蛋白激酶、细胞周期和凋亡调节因子、法尼基转移酶(FTase) 等,现就针对这些靶点的研发药物做一综述。
1、蛋白激酶蛋白激酶是目前已知的最大的蛋白超家族。
蛋白激酶的过度表达可诱发多种肿瘤。
蛋白激酶主要包括丝氨酸/苏氨酸激酶和酪氨酸激酶,其中酪氨酸激酶主要与信号通路的转导有关,是细胞信号转导机制的中心。
蛋白激酶由于突变或重排,可引起信号转导过程障碍或出现异常,导致细胞生长、分化、代谢和生物学行为异常,引发肿瘤。
研究表明,近80%的致癌基因都含有酪氨酸激酶编码。
抑制酪氨酸激酶受体可以有效控制下游信号的磷酸化,从而抑制肿瘤细胞的生长。
酪氨酸激酶受体分为表皮生长因子受体(EGFR)、血管内皮细胞生长因子受体(VEGFR) 、血小板源生长因子受体(PDGFR) 等,针对各种受体的酪氨酸激酶抑制剂目前已开发上市的主要为表皮生长因子受体酪氨酸激酶(EGFR-TK) 抑制剂、血管内皮细胞生长因子受体酪氨酸激酶(VEGFR-TK) 抑制剂和血小板源生长因子受体酪氨酸激酶(PDGFR-TK)抑制剂等。
基于多靶点的酪氨酸激酶抑制剂目前已成为研究重点,具有广阔的发展前景,其中,包括舒尼替尼和索拉芬尼在内的几个上市新药均获得了良好的临床评价结果。
1.1 EGFR-TK抑制剂许多实质性肿瘤均高度表EGFR,EGFR-TK抑制剂是目前抗肿瘤药研发的热点之一。
第三代EGFR-TKI耐药后诊疗策略专家共识(2023)要点

第三代EGFR-TKI耐药后诊疗策略专家共识(2023}要点近年来,随着肺癌精准诊疗的快速发展,表皮生长因子受体醋氨酸激酶抑制剂(EGFR-T阳)已成为EGFR突变晚期非小细胞肺癌(NSC L C)患者的标准治疗选择,但EGFR-T阳耐药是难以避免的临床和科学难题,尤真以第三代EGFR-TKI治疗耐药最被临床所关洼。
第三代EGFR-TKI治疗后耐药机制多样化,墓于不同耐药机制探索个体化治疗方案,不仅可以进一步延长患者生存,还可以提升患者整体生活质量。
对于三代EGFR-TKI 耐药后治疗策略,既往临床实践中以传统化疗为主,但化疗疗效高限,远不能满足临床需求。
因此,重庆市肺癌精准治疗协作组(CPLOG)针对第三代EGFR-TKI治疗耐药后诊疗策略进行多次探讨,最终形成了第三代EGFR-TKI耐药后诊疗策略专家共识,旨在为临床实践中应对三代EGFR-TKI耐药提供参考及指导,规范临床诊疗实践,进一步改善EGFR 突变晚期NSCLC患者的生存及生活质量。
NSCLC重要的致癌驱动因素之一,表皮生长因子受体(EGFR)基因的发现,推动了以生物标志物为指导的晚期肿瘤患者的全新治疗模式。
伴随着EGFR酶氨酸激酶抑制剂(TKI)的研发迭代,与一/二代EGFR-TKI 相比,以奥希替尼为代表的第三代EGFR-TKI口显出更优的疗效和安全性,已成为EGFR突变晚期患者一线以及经-/二代EGFR-TKI治疗后存在T790M突变患者二线标准治疗优选。
使用第三代EGFR-TKI治疗后仍不可避免地会发生耐药,使得EGFR突变晚期患者的长期生存受限。
如何克服耐药,已成为第三代EGFR-T KI在||笛床进一步发挥作用,延长患者生存,提高患者生存质量的关键问题。
阳瞌点第三代EGFR-T阳的耐药机制,依据现高临床证据制定相应的耐药后处理策略,为临床在应对三代EGFR-T KI耐药后的临床诊疗f是供参考。
一、文献评价方法学二、耐药评估及机制探索EGFR突变主要是指EGFR基因第18~21号外显子上酷氨酶敷酶区域发生的突变其中第19号外显子的非移码缺失突变相21号外显子的L858R 错义突变为常见突变,约占EGFR突变的8S%~90%,真余10%~15%的类型则称之为罕见突变,包括G719X、L861Q、57681及20号外显子插入突变等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中国医科大学博士学位论文EGFR信号通路在黑色素瘤中调节紫杉醇耐药和侵袭转移机制探讨姓名:张晓晶申请学位级别:博士专业:肿瘤学指导教师:王舒宝20050501中国医科大学研究生学位论文独创性声明本人申明所呈交的学位论文是我本人在导师指导下进行的研究工作及取键的研究成果.据我所知,除了文中特别加以标注和致谢的地方外,论文中不包含其他人已经发表或撰写过的研究成果,也不包含为获得我校或其他教育机构的学位或证书而使用过的材料,与我一同工作的同志对本研究所做的任何贡献均已在论文中作了明确的说明并表示谢意.申请学位论文与资料若有不实之处,本人承担一切相关责任。
论文作者签名:啦出土逝日期:挫£:堑中国医科大学研究生学位论文版权使用授权书本人完全了解中国医科大学有关保护知识产权的规定,即:研究生在攻读学位期间论文工作的知识产权单位属中国医科大学。
本人保证毕业高校后,发表论文或使用论文工作成果时署名单位为中国医科大学,且导师为通讯作者,通讯作者单位亦署名为中国医科大学.学校有权保留并向国家有关部门或机构送交论文的复印件和磁盘,允许论文被查阅和借阅。
学校可以公布学位论文的全部或部分内容(保密内容除外),以采用影印、缩印或其他手段保存论文.论文作者签名:盈盛品指导教师戤:.五纭,~+—。
“…一、L一!型垒墅塑曼一,;EGFR信号通路在黑色素瘤中调节紫杉醇耐药和侵袭转移机制探讨目的黑色素瘤是高度恶性皮肤肿瘤,由于其对常规化疗药物敏感性低并易产生耐药,所以改善黑色素瘤预后的关键是控制黑色素瘤转移和解决化疗耐药问题。
探求黑色素瘤发生、发展、侵袭与转移机制,探求黑色素瘤化疗耐药机制,一直是肿瘤学者们关注的热点。
近年来人们发现,表皮生长因子受体(epidermalgrowthfactorreceptor,EGFR)在包含黑色素瘤在内的绝大多数肿瘤中表达或过表达,而且其表达程度与肿瘤的预后相关。
EGFR是由1186个氨基酸组成170KDa的单跨膜糖蛋白,具有酪氨酸蛋白激酶(tyrosineproteinkinase,TPK)活性;其分子结构由三部分组成,即:胞外与配子结合的氨基端,中间是单一及疏水的跨膜区,胞内为具有酪氨酸激酶活性的羧基端,能与ATP结合。
EGFR家族包括四个成员,即:EGFR/ErbBl,HER2/ErbB2,HER3/ErbB3和HER4/ErbIM;当生长因子与EGFR结合后即可诱导EGFR受体TPK激活,四个成员间形成活性较低的同源二聚体和活性较高的异源二聚体。
EGFR本身不仅有TPK活性,而且可作为TPK底物发生自身磷酸化后激活。
多细胞生物信号传导和调控是高等动物成长、发育、进化的必要条件之一。
如果信号传导控制失调,将导致细胞分裂由有控变成失控而无限增殖,最终导致肿瘤发生。
EGFR信号传导通路是一个重要的信号传导通路,目前发现其下游信号通路有:P13K/AKT、RAS—RAF—MAPKrct4/042和蛋白激酶c信号通路,EGFR信号通路的激活能导致细胞增殖、凋亡抑制、异质黏附性增强、侵袭转移能力提高等等。
已证实常规化疗过程中直肠癌、乳腺癌和卵巢癌细胞DNA损伤时能激活EGFR信号通路,使细胞产生耐药。
我们用紫杉醇和/或EGFR抑制剂AGl478、ERK抑制剂PD98059、P13K抑制剂LY290042分别作用黑色紊瘤A375细胞,探讨EGFR信号通路与紫杉醇耐药的关系及其作用机制;用EGF和/或EGFR抑制剂AGl478作用A375细胞,探讨EGFR信号通路调节黑色素瘤侵袭与转移的分子机制。
材料与方法1.常规细胞培养与稀释克隆筛选出EGFR高表达A375细胞株,取对数生长期细胞进行实验。
2.采用光镜、电镜、荧光显微镜观察细胞凋亡情况。
3.应用流式细胞术分析细胞周期(PI染色)和凋亡率(AnnexinV/Pl双染色)情况。
4.应用Matrigel胶和MTI'法进行体外黏附实验。
5.用Matrigel胶和Boyden小室进行体外侵袭实验。
6.用Westernblot方法检测P—EGFR,P—ERK,P—AKT,Bcl一2,Bax,Caspase一3蛋白表达。
7.用半定量RT—PCR检测MMP一2,MMP一9,TIMP一1。
TIMP一2mRNA表达。
实验结果1.紫杉醇以时间和剂量依赖方式抑制A375细胞生长0.001~1wmol/L紫杉醇以时间和剂量依赖方式抑制A375细胞生长(P<0.01)和诱导A375细胞凋亡(P<0。
05);IC5024h、48h、72h、96h分别为:9.5I.tJmol/L、3.7p.mol/L、0.06pmol/L、0.0079jnol/L(P<0.01);0.001、o.01、0.1、1肛moL/L紫杉醇24h细胞生长抑制率分别为:0.1%、10.8%、24.4%、32.5%(P<O.05)。
2.不同浓度紫杉醇通过不同途径诱导A375细胞凋亡0.001~lpmoVL紫杉醇作用h375细胞24h均可诱导细胞凋亡,但在细胞发生凋亡同时0.001p.mol/L紫杉醇并不改变细胞周期,0.01斗mol/L紫杉醇使Go/G。
期细胞含量明显减少,0.1、1l^mol/L紫杉醇使A375细胞发生明显的G2/M期阻滞。
但在蛋白水平上的变化是一致的,即:下调Bcl一2蛋白、上调Bax蛋白并激活Caspase一3。
3.紫杉醇通过激活EGFR—ERK/MAPK和EGFR—PDK/AKT信号通路产生耐药0.0l~0.1la,mol/L紫杉醇作用A375细胞24h,使P—EGFR、P—ERK和P—AKT蛋白表达均升高,当20pmol/LAGl478与紫杉醇联合作用细胞24h时使P—EGFR、P—ERK和P—AKT蛋白表达均下降,说明紫杉醇作用A375细胞使其发生凋亡同时能激活EGFR—ERK和EGFR—PBK/AKT二条信号通路使A375细胞产生耐药。
4.EGFR信号阻断剂与紫杉醇具有协同抗A375细胞生长和诱导细胞凋亡作用0.001~0.1ixmol/L紫杉醇与AGl478(20斗mol/L)联合应用时与紫杉醇单独作用相比细胞生长抑制作用明显增强(P<0.01)。
尽管AGl478(20la.mol/L)作用24h时没有表现诱导A375细胞凋亡作用,但与紫杉醇(0.001~0.1斗mol/L)联合应用时与紫杉醇单独作用相比早、晚期凋亡细胞比率均明显增加,早期凋亡率分别增加了2.7倍、2.8倍和1。
6倍(P<0.05),晚期凋亡细胞比率以0.01lzmol/L紫杉醇与AGl478联合作用效果最强,提高了6.8倍(P<O.01),而AGl478没有改善0.1la,mol/L紫杉醇诱导晚期凋亡细胞的作用。
由此推断EGFR信号阻断剂与紫杉醇联合应用具有协同抗黑色素瘤作用,而且这种作用不是简单的相加。
5.EGFR信号通路对A375细胞生长的影响外源性EGF作用A375细胞24h时使P—EGFR、P—ERK和P—AKT蛋白表达明显增加,而AGl478则能废弃外源性EGF的作用,使P—EGFR、P—ERK和P—AKT蛋白表达减少,并低于A375细胞正常表达水平。
外源性EGF在48h以内不影响A375细胞生长,当时间延长至72h以上时,EGF促细胞生长作用开始显现并逐渐增强,72h时细胞生长率达112.3%(P<0.05)。
AGl478、PD98059、SB203580和LY2940022分别封闭EGFR、ERK/MAPK、P38MAPK/JNK和PBK/AKT信号通路后使A375细胞生长均受到不同程度的抑制,24h时生长抑制率分别为24.9%、23.0%、17.8%和20.9%(P<0.01),而且每个阻断剂的抑制作用都呈时间效应关系。
说明EGFR信号通过至少MAPK和P13K/AKT二条下游信号通路调节黑色素瘤细胞生长。
6.EGFR信号通路对A375细胞黏附力的影响外源性EGF激活EGFR.活性后能明显地增加A375细胞对ECM的黏附性,相对黏附率是对照组的2.3倍(P<0.01);AGl478、PD98059和LY294002分别能抑制EGF的促异质黏附性的作用,使黏附率分别下降了65.5%、64.2%和65.O%(P<0.01);但SB203580则不能改变EGF的促黏附作用。
说明EGFR信号通过ERK/MAPK和P13K/AKT二条下游信号通路调节黑色素瘤细胞对细胞外基质的黏附性。
7,EGFR信号通路对A375细胞体外侵袭力的影响外源性EGF能明显地增加A375细胞穿透Matrigel体外侵袭能力,作用24h时过膜细胞数提高了26.4%(P<0.05);当AGl478、PD98059和LY294002分别封闭EGFR、ERKl/2和P13K基因后均能抑制EGF对细胞侵袭力的影响,使过膜细胞数分别下降了29.9%、25.1%和33.2%(P<0。
01);SB203580则不能改变EGF促细胞侵袭作用。
说明EGFR信号通过ERK/MAPK和P13K/AKT二条下游信号通路调节黑色素瘤细胞运动和侵袭能力。
8.EGFR活性改变对MMP一2、MMP一9、ⅡMP一1和‘nMP一2mlLNA表达的影响EGF作用24h时具有增加MMP一2、MMP一9mRNA表达,降低TIMP—l、TIMP一2mRNA表达的作用;而AGl478则具有抑制EGF的作用,使MMP一2、MMP一9mRNA表达明显减少,TIMP—lmRNA表达升高,但对TIMP一2mRNA表达影响不明显,结果MMP一2/TIMP一2和MMP一9/'lIMP一1的比值均明显下降(P<0.001)。
说嘎EGFR信号通过调节细胞外基质金属蛋白酶和其抑制剂的功能调节黑色素瘤细胞侵袭与转移能力。
讨论紫杉醇为有丝分裂抑制剂,通过与微管蛋白B亚单位结合使微管聚合加速、解聚抑制,进而形成异常稳定的微管,使细胞有丝分裂停止,阻滞细胳在G2/M期进而使细胞凋亡。
本实验结果显示,高剂量紫杉醇作用黑色素瘤.4375细胞时是通过作用微管、使有丝分裂失败进而发生G=/M期细胞阻滞和细胞凋亡,其作用机制与紫杉醇诱导骨肉瘤和卵巢癌细胞凋亡机制基本一致;而低剂量紫杉醇诱导黑色素瘤细胞凋亡时是通过作用G。
/G,期细胞而非G:/M期细胞所致,说明高低浓度紫杉醇抗黑色素瘤生长和诱导细胞凋亡是通过不同途径发挥作用的。
尽管紫杉醇作用机制独特,对常规化疗不敏感的肿瘤有效,但其本身副反应大和耐药性问题需亟待解决。
已证实EGFR信号通路与直肠癌、乳腺癌化疗耐药和放射治疗不敏感有关,当细胞DNA损伤时能够激活EGFR—PBK/AKT抗凋亡信号通路。
EGFR信号通路被激活后可通过多条下游信号通路传递信号至核内,促进或抑制特定靶基因,加速细胞增殖,抑制凋亡,增加肿瘤细胞的侵袭和转移能力。
