北京大学有机化学课件chapter13
有机化学第5版-李景宁-课件-13第13章羧酸衍生物

C H3 (C H3)2 C H C O C C O O C2 H5
C H3
不同酯的Claisen缩合反应:
• 对都具有α-H的酯:
O
O
OO E O tN a
C H 3 C O C 2 H 5 + C H 3 C H 2 C O C 2 H 5
CH3CCH2COC2H5
OO
+ CH3CH2CCHCOC2H5 +
C—O
N—H
≈1100cm-1
1100~1300cm-1 3300~3500cm-1(尖)
注意:
① 酰卤X的-I强,降低C=O的极性,增加双键性,
故波数高; ② 酸酐有两个C=O,双峰; ③ 酯与酮的羰基峰接近,但酯有2个C—O伸缩振
动; ④ 共轭使C=O下降; ⑤ N—H和O—H峰的区别:前者尖,后者宽。
C H O 2H
3. 酰胺的还原
催化氢化不易,但氢化锂铝可还原
C H3 C H2 C O N H C H3 LA i H l 4 C H3 C H2 C H2 N H C H3
四、酰胺的其他反应 1. 酸碱性
碱性减弱,酸性加强
2. 脱水
O
RCN H 2 + P 2 O 5
R C N+ H P O 3
第十三章 羧酸衍生物 (carboxylic acid derivatives)
第一节 命名与光谱性质
第五节 油脂和合成洗涤剂
一、命名
第六节 乙酰乙酸乙酯和丙二酸二乙酯
二、光谱性质
在有机合成上的应用
第二节 羧酸衍生物的化学性质
一、互变异构现象
一、取代反应
二、乙酰乙酸乙酯
二、羧酸衍生物与金属试剂反应
第13章高压喷射注浆法ppt课件

高压喷射注浆法所形成的固结体的形态与高压 喷射流的作用方向、移动轨迹和持续喷射时间
有密切关系。按喷射流移动轨迹分为旋喷、定 喷和摆喷三种。
旋喷法施工时, 喷嘴一面喷射一面旋转并提升, 固结 体呈圆柱状。主要用于加固地基, 提高土的抗剪强 度, 改善地基的变形性质, 也可组成闭合的帷幕, 用 于截阻地下水流和治理流砂。喷射法施工后, 在地 基中形成的圆柱体, 称为旋喷桩。
初期区域后为主要区域:轴向动压陡然减弱,喷射扩散 宽度和距离平方根成正比,扩散率为常数,喷射流的 混合搅拌在这一部分内进行。
主要区域后为终了区域:到此喷射流能量衰减很大,末 端呈雾化状态,这一区域的喷射能量较小。
喷射加固的有效喷射长度为初期区域长度和主要区域 长度之和,若有效喷射长度愈长,则搅拌土的范围愈 大,喷射加固体的直径也愈大。
高压喷射注浆法, 当时定名为CCP 工法
1972年铁道部科学研究院率先开发高压喷射 注浆法。1975年,我国冶金、水电、煤炭、建 工等部门和部分高等院校,也相继进行了试验 和施工。已成功应用于已有建筑和新建工程的 地基处理、深基坑地下工程的支挡和护底、构 造地下防水帷幕等。
高压喷射注浆
13.2 定义及其种类
第13章 高压喷射注浆法
Chapter 13 High Pressure Jet Grouting
13.1 概 述
13.1 Introduction
用高压水泥浆通过钻杆由水平方向的喷嘴喷 出,形成喷射流,以此切割土体并与土拌和形 成水泥土加固体的地基处理方法。
20 世纪60 年代末期, 日本NIT 公司在日本大阪 市地下铁道建设冻结法施工中, 由于冰冻融化, 造成严重事故, 后改为灌浆法施工。在灌浆过 程中, 浆液沿着土层交界面溢走很多, 不能完全 达到加固地基和止水的目的。在这关键时刻, 中西涉博士急中生智, 大胆引用了水力采煤技 术, 将高压水射流技术应用到灌浆工程中, 创造 出一种全新的施工法—— 高压喷射注浆法。
13 杂环化合物
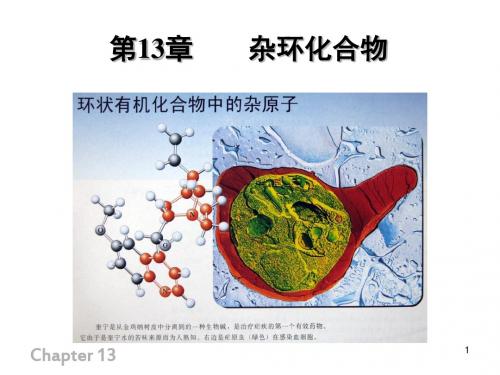
O 顺丁烯二酸酐
△
O+
苯炔
=
=
OO O 90%
OO
76%
Chapter 13
37
吡咯也可以与苯炔、丁炔二酸发生类似的反应 N-H
△
N-H +
C-COOH N-H +
△
C-COOH
N-H -COOH -COOH
噻吩的芳香性较大,环比较稳定,难发生双烯合成
Chapter 13
38
1. 物理性质
O
呋喃
子相邻的碳原子为α,依次β,γ……
(2)当环上有两个或多个杂原子时,应使杂原子的 位号最低,杂原子按O S N的次序给最低号。 (3)环上有不同取代基时,编号按最低系列原则和 顺序规则,使取代基所在的位次最低。
Chapter 13
10
O2N
CHO
O
5-硝基-2-甲酰基呋喃 α’-硝基-α-甲酰基呋喃 (5-硝基-2-呋喃甲醛)
N 吡啶 pyridine
N 喹啉 quinoline
Chapter 13
8
无特定名称的稠杂环化合物,选含特定名称的 杂环为基本环,用化学介词“并”表示稠合关系, 按衍生物命名 :
O
苯并呋喃
Chapter 13
9
2. 环上取代基的位置 基本环的编号原则如下: (1)从杂原子开始,定位1,依次2,3……或杂原
存在于松木焦油中 熔点-86℃ 沸点32℃
2. 定 性 鉴 别 遇浓HCl浸过的松木片,呈绿色反应
Chapter 13
39
3. 化 学 性 质
1) 亲电取代反应
Cl2 -40 oC
Cl + HCl O
有机化学(李景宁)13教材

O R -C X
O R-C-NH2
O R-C C C
IR
C=O
酰卤 ≈1800cm-1
C—O ≈1100cm-1
N—H
酸酐 ≈1820cm-1
≈1760cm-1
酯
≈1740cm-1 1100~1300cm-1
3300~3500cm-1(尖)
丙烯酸甲酯 methyl acrylate
二、羧酸衍生物的光谱性质 羧酸衍生物在结构上的共同特点是都含有酰基, 酰基与其所连原子或基团都能形成p-π共轭体系。
R C O L (X,O,N) p-π共轭
(1)与酰基相连原子的电负性都比碳大,故有-I 效应。 (2)和羰基碳相连的原子上都有未共用电子对, 故有+C效应。
+ H OH
(1)水解活性次序:酰卤>酸酐>酯>酰胺
(2)酰卤和酸酐的水解不需催化,而酯和酰胺的水 解需在酸或碱催化下进行,酯的酸性水解为可逆反应 ,碱性水解不可逆,可进行到底;酯的碱性水解称为 皂化反应。
2. 醇解——生成酯:
O R-C-X O O R-C-O-C-R' + H-OR'' O R-C-OR' HX O R-C-OR'' + R'COOH R'OH
O
amide
烃氨基取代:
R-C-NH2(R)
酰卤和酰胺的命名是根据酰基称为某酰某,
英文名:羧酸的词尾 “-ic acid”换成 “-yl halide” “-oic acid”或 “-ic acid”换成“amide” 酰胺。
CH3 C O Cl CH2 CH C O Br C O N(CH3)2 NH 戊内酰胺 pentanelactam
有机化学ppt课件完整版

重排反应通常发生在含有不稳 定结构或官能团的化合物中, 需要加热或加入催化剂。在重 排过程中,分子的骨架结构可 能发生变化。
重排反应在有机合成中具有重 要的应用价值,可以用于合成 具有特定结构或官能团的有机 化合物。同时,重排反应也是 研究有机化合物结构和性质的 重要手段之一。
08
有机化学在生活中的应 用
定义
特点
加成反应在有机合成中具有重要的应用价值,可以用 于合成各种烯烃、醇、醛、酮等有机化合物。
应用
加成反应通常发生在分子中的不饱和键上,需要一定 的反应条件和催化剂。
消除反应
定义
消除反应是指有机化合物分子中 失去一个小分子(如水、卤化氢
等),形成不饱和键的反应。
种类
包括脱水消除、脱卤化氢消除、 热消除等。
反应。此外,醇还可以与酸反应生成酯,是重要的有机合成原料。
酚类化合物结构与性质
结构特点 酚类化合物的分子中含有苯环和羟基(-OH)官能团,通 式为Ar-OH,其中Ar为苯基或其衍生物。
物理性质 酚类化合物一般为无色或淡黄色的固体或液体,具有特殊 的气味和较强的毒性。酚的熔点和沸点较高,易溶于有机 溶剂。
化学性质
03
可发生加成、氧化、还原等反应,如与氢气加成生成醇,被弱
氧化剂氧化成酸。
酮类化合物结构与性质
结构特点
羰基(C=O)两侧连接烃基或芳基,无双键性质。
物理性质
沸点较高、难溶于水、易溶于有机溶剂。
化学性质
主要发生加成和还原反应,如与氢气加成生成醇,被还原剂还原 成仲醇。
醌类化合物结构与性质
结构特点
04
醇、酚、醚类化合物
醇类化合物结构与性质
01
结构特点
有机化学碳负离子的反应
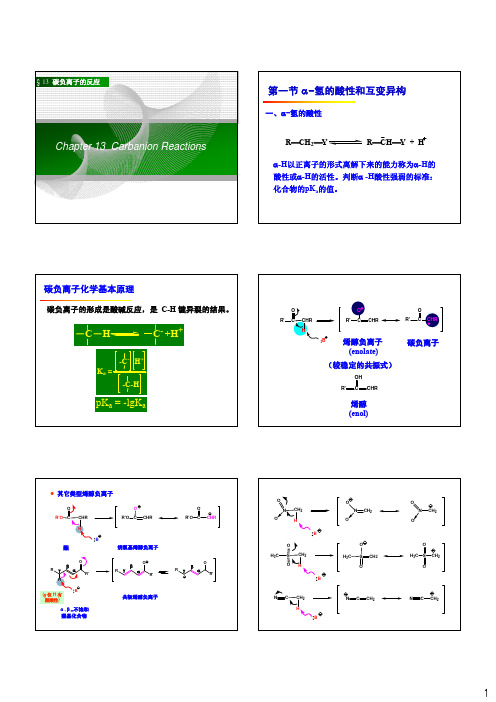
O R'O C
CHR
H
B
酯
O R'O C CHR
烷氧基烯醇负离子
O
β
Rγ
α
R'
H
B (γ 位 H 有
弱酸性)
α,β-不饱和 羰基化合物
β
O
Rγ
α
R'
共轭烯醇负离子
O R'O C CHR
O β
Rγ
α
R'
O
N CH2
O
H
B
O H3C S CH2
OH
B
N C CH2 H B
O N CH2
O
O
H3C
S CH2 O
¾芳醛中羰基化合物的反应活性受电子效应和空间结 构位置的影响,空间位阻较大时它将起主要的作用。
¾当苯环上为烷基时,由于烷基是给电子的基团,又 有位阻使反应物羰基活性下降,反应难以进行,产率 也低。
¾邻位甲基的位阻十分明显,导致不发生反应。
¾当苯环上有吸电子基团时有利于反应进行,不仅反 应的速度加快,并且产率也大大增加。
新型强碱
z 1. LDA 二异丙基胺锂 z 2. LHMDS六甲基二硅胺锂 z 3. LATMP四甲基哌啶锂
特点: z 1. 碱性强pKa大于33 z 2. 能溶解于非极性溶剂 z 3. 位阻大亲核性差
二、互变异构
O R' C CHR
H
O R' C CHR
B 烯醇负离子 (enolate)
(较稳定的共振式)
COOH
−CH=O + H2C
COOH
NH3,C2H5OH -H2O
COOH −CH=CHC
有机化学PPT课件

目录
• 有机化学简介 • 有机化学基础知识 • 有机化学反应 • 有机化学的应用 • 有机化学的未来发展
01 有机化学简介
有机化学的定义
总结词
有机化学是一门研究有机化合物 的组成、结构、性质、合成和反 应的学科。
详细描述
有机化学主要关注碳氢化合物及 其衍生物,即有机化合物,它们 是构成生命体的基本物质。
将有机化学与计算机科学、数学等学科交叉融合,利用计算机模拟和预测有机化学反应和 分子的性质,为有机化学研究和应用提供新的工具和手段。
THANKS FOR WATCHING
感谢您的观看
有机化学的发展历程
总结词
有机化学的发展经历了从天然有机化学到合成有机化学的演变,并不断推动着 人类社会的进步。
详细描述
早期的有机化学主要研究天然有机物,如动植物体内的化合物。随着科技的发 展,合成有机化学逐渐崛起,人们开始能够合成大量原本自然界不存在的有机 化合物,从而极大地丰富了人类的物质生活。
农业领域
1 2
农药合成
有机化学在农药合成中扮演着关键角色,通过设 计并合成新的农药分子,可以开发出更安全、更 有效的农药。
植物生长调节剂
有机化学也可用于合成植物生长调节剂,通过调 节植物生长代谢,提高作物产量和品质。
3
转基因作物
利用有机化学手段,可以修改作物的基因组,培 育出抗逆性更强、产量更高的转基因作物。
举例
乙醇被氧化生成乙醛。
04 有机化学的应用
医药领域
药物合成
有机化学在药物合成中发挥着重要作用,通过设计并合成新的有 机分子,可以开发出具有治疗作用的创新药物。
药物代谢
有机化学也涉及药物代谢的研究,了解药物在体内的代谢过程有助 于优化药物的疗效和降低副作用。
有机化学ppt课件完整版

有机化学ppt课件完整版目录•绪论•有机化合物的结构与性质•烃类化合物•烃的衍生物•有机合成与反应机理•生物活性有机化合物绪论碳氢化合物研究碳氢化合物(烃)的结构、性质、合成和反应机理。
碳氢化合物的衍生物研究烃的衍生物,如醇、醛、酮、羧酸、酯等有机化合物的结构、性质、合成和反应机理。
生命体系中的有机化合物研究生物体内的氨基酸、蛋白质、核酸、多糖等生命物质的结构、性质和功能。
经典时期19世纪初到20世纪初,以经验规律为指导,通过大量的实验总结出了许多有机化学的基本概念和原理。
萌芽时期从远古时期到18世纪,人们开始使用天然有机物,如木材、植物、动物等。
现代时期20世纪至今,以量子力学和统计力学为基础,发展出了现代有机化学的理论和方法,如分子轨道理论、价键理论、反应机理理论等。
环境领域有机化学在环境保护方面发挥着重要作用,如研究大气污染物、水体污染物的来源和治理方法等。
同时,有机化学也致力于开发环保材料和清洁能源。
材料领域合成纤维、塑料、橡胶等高分子材料广泛应用于服装、家居用品、交通工具等领域。
医药领域合成药物如抗生素、抗癌药物等对于治疗疾病具有重要意义。
同时,天然药物中提取的有效成分也是有机化学的研究对象。
农业领域合成农药和化肥对于提高农作物产量具有重要作用。
此外,生物农药和生物肥料的研发也需要有机化学的支持。
有机化学与生产生活的关系有机化合物的结构与性质碳原子通过四个共价键与其他原子或基团相连,形成复杂的有机分子结构。
碳原子的四价性键的极性空间构型碳原子与其他原子形成的共价键具有不同的极性,影响有机物的物理和化学性质。
有机化合物分子中的原子或基团在空间的排列方式不同,导致同分异构现象的产生。
030201有机化合物的结构特点03同分异构体的性质差异由于结构上的差异,同分异构体在物理性质、化学性质以及生物活性等方面表现出明显的不同。
01构造异构分子式相同但连接方式不同,如正丁烷和异丁烷。
02立体异构分子式相同、连接方式也相同,但空间构型不同,如顺反异构、对映异构等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
exit
本章提纲
第一节 羧酸衍生物的命名、物性和光谱性质 第二节 羧酸衍生物的结构和反应性能 第三节 羧酸及其衍生物的制备
第四节 羧酸衍生物的其它反应
第五节 与酯缩合、酯的烷基化、酰基化相类
似的反应
第六节 β-二羰基化合物的特性及应用
第一节 羧酸衍生物的命名、物性和光谱性质
一 羧酸衍生物的命名
CCl + SO2 + HCl
(bp 197oC)
实
O CH3CH2COH
PCl3 (bp 74.2oC)
O CH3CH2CCl + H3PO3
(bp 80oC) (200oC分解)
例
O CH 3(CH2)6COH
PCl5 (160oC升华)
O CH3(CH2)6CCl + POCl3
(bp 196oC) (bp 107oC)
CH3COOCMe3 Me3CCOOEt 0.01 CH3COOEt 1 ClCH2COOEt 296
V
相对
0.002
3. 形成的四面体中间体能量越低,反应速度越快。 (能分散负电荷的取代基对反应是有利的) 4. 酯的碱性水解是不可逆的。 5. 碱的用量要超过催化量。
*2. 酸性水解
O CH3CO18C2H5 + H2O
3oROH的水解只能用新的机理来解释。
*4 3o醇酯的酸性水解历程
反应式
O CH3CO18-C(CH3)3 + H2O
O
H+
CH3CO18OH + (CH3)3C-OH
+
反 应 机 理
CH3C O OH CH3C
+
18
H C(CH3)3
+
OH C(CH3)3
CH3C O18
SN1 O
18
C(CH3)3
4-氯甲酰苯甲酸
2 酸酐的命名
单酐:在羧酸的名称后加酐字; 混酐:将简单的酸放前面,复杂的酸放后面再加酐字; 环酐:在二元酸的名称后加酐字。
O O O CH3COCCH3 O O CH3COCCH2CH3 O Aceticpropionic anhydride Succinic anhydride O
普通命名法: 醋酸苯甲酯 IUPAC 命名法: 乙酸苯甲酯
-甲基--丁内酯 2-甲基-4-丁内酯
4 酰胺的命名
命名时把羧酸名称放在前面将相应的酸字改为酰胺即可;
O (CH3)CHCNH2 O CH3CH2CHCH2CN(CH3)2
常用英文命名 2-Methylpropanamide 普通命名法: 异丁酰胺 IUPAC 命名法: 2-甲基丙酰胺
CH3CO18OH + (CH3)3C+ H2O
+
关键 中间 体
(CH3)3COH + H+
(CH3)C 3COH2
通过同位素跟踪可以证明上述反应机制
*5 酯水解的应用
A 制备羧酸和醇 B 测定酯的结构
CH2OOCR CHOOCR' CH2OOCR'' NaOH H+ CH2OH CHOH CH2OH + RCOOH R'COOH R''COOH
O O RCOCR' + N+ H Cl -
2. 羧酸的脱水(甲酸除外)--制备单纯的羧酸
COOH (CH3CO)2O O C)2O + CH3COOH
(
3. 芳烃的氧化
CH 3 CH 3
O
+ 3 O2(空气)
V2O5
O O
400oC
4. 乙酸酐的特殊制法
O CH3CCH3
700-800oC
CH 3COO-H
H+
O CH3COH + C2H5O18H
同位素跟踪结果表明:酸性水解时,也发生酰氧键断裂。 反应机理
O RCOR'
H+
+OH
OH R-C-OR'
+
OH
H2O
RCOR'
R-C-OR' OH2
+
四面体中间体是正离子
OH R-C-OR' H HO
+
- R'OH
+OH
O
-H+
RCOH
RCOH
酸性水解的讨论
1 酰卤的命名:
在命名时可作为酰基的卤化物,在酰基后加卤素的名称即可。
Br O CH3CH2CHCBr HOOC COCl
常用英文命名 2-Bromobutyryl bromide
4-Chlorocarbonylbezioc acid
普通命名法: -溴丁酰溴 IUPAC 命名法: 2-溴丁酰溴
对氯甲酰苯甲酸
常用英文命名
3-Methylpentanenitrile
普通命名法: -甲基戊腈 IUPAC 命名法: 3-甲基戊腈
-氰基丁酸 2-氰基丁酸
己二腈 己二腈
二 羧酸衍生物的物性
低级的酰氯和酸酐是有刺鼻气味的液体,高级的为固体; 低级的酯具有芳香的气味,可作为香料;十四碳酸以下 的甲酯和乙酯均为液体; 酰胺除甲酰胺外,由于分子内形成氢键,均是固体; 而当酰胺的氮上有取代基时为液体; 羧酸衍生物可溶于有机溶剂; 酰氯和酸酐不溶于水,低级的遇水分解; 酯在水中溶解度很小; 低级酰胺可溶于水。
六 酯的制备
1. 酯化反应
2. 羧酸盐+卤代烷
3. 羧酸+重氮甲烷
参见羧酸一章
4. 羧酸对烯、炔的加成: (1) 酸催化 (2) 亲电加成反应机制 (3) 可以制备各种醇的酯 5. 羧酸衍生物的醇解反应
4. 羧酸对烯、炔的加成
eg1.
CH2(COOH)2 + 2(CH3)2C=CH2
浓H2SO4 室温
取代反应
该取代反应需要在碱或酸的催化作用下进行。
碱性催化的反应机制为:
O RCW + Nu R O
-
C W Nu
-W
-
O RCNu
酸催化的反应机制为:
O RCW + H+
+ +
OH Nu
OH R C W Nu
RCW
-W -
-H+ RCNu RCNu
OH
O
这是一个可逆反应,要使反应向右方进行,其条件是:
CH 2=C=O
O CH 3COH
700-740oC
乙烯酮
HO O CH2=COCCH3
O O CH3COCCH3
AlPO4
互变异构
五 羧酸的制备
1. 氧化法(参见羧酸一章)
2. 金属有机化合物与二氧化碳的反应
(参见羧酸一章)
3. 羧酸衍生物的水解反应
3. 羧酸衍生物的水解反应 (1) 水解反应的一般情况
烯丙位苯甲位的卤代
醇的卤化
NBS *1
SOCl2 PCl5 PCl3 PBr3
或X2+光照
自由基取代
亲核取代
HX (HI>HBr>HCl) X2 醛、酮、酸的-H卤化 羧酸羟基的卤化 SOCl2 PCl5 PCl3 *2 XX2, HX, HOX
PX3
烯醇化 加成
*3 醇能用HX取代,
卤代烃中卤素的交换
O CH 3CCl O O
HCl
O
CH3COCCH3
O CH3COC 2H5 + H2O
O CH3CNH2
CH 3COH
}
}
室温
O CH3COH + C2H5OH
加热 长时间回流
NH3 NH3
CH3C N
请同学考虑:
反应是否需要催化剂?需要什么催化剂?为什么?
亚硝酸在酰胺制酸中的作用
O CH3CNH2
同位素跟踪结果表明:
碱性水解时,发生酰氧键断裂。
反应机理
O RCOR + OH
' -
慢
OR-C-OR' OH
快
O RCOH + -OR'
四面体中间体 是负离子
O ROH + RCO
-
Na
+
O RCONa
碱性水解的讨论
1. 碱性水解速率与 [-OH]成正比。
2. 羰基活性越大,-C空阻越小,酯基空阻越小, 反应速率越快。
N,N-dimethylpentanamide
N,N-二甲基戊酰胺 N,N-二甲基戊酰胺
5 腈的命名
腈命名时要把CN中的碳原子计算在内,并从此碳原子开始编 号;氰基作为取代基时,氰基碳原子不计在内。
CH3 CH3CH2CHCH2CN CN CH3CH2CHCOOH 2-Cyanobutanoic acid NC(CH2)4CN 1,6-Hexanedinitrile
1. 酸在反应中的作用有二: ①活化羧基 羊 ②使OH、OR形成金 盐而更易离去。
2 在酯 (RCOOR’)中,R有吸电子基团虽能活化 羧羰基,但会使关键中间体正离子能量升高,R 为给电子基团亦有两种相反的作用,故表现不出 明显的影响。
3. 酯的酸性水解和酯化反应互为逆反应,平衡的 移动取决于反应的条件。体系中有大量水存在, 发生酯的水解。若有大量醇存在,并采取去水 措施,则有利于酯化反应。
第三节 羧酸及其衍生物的制备及互相转换 一 羧酸衍生物的羰基的亲核加成--消除机制 二 羧酸及衍生物的转换关系概貌 三 酰卤的制备 四 酸酐的制备 五 羧酸的制备 六 酯的制备 七 酰胺的酸碱性及制备
八 腈的制备
