费歇尔吲哚合成
5 吲哚的合成解析
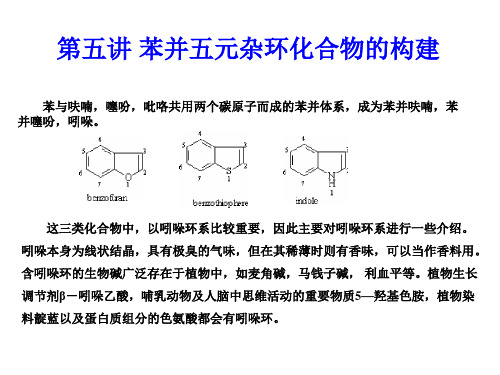
A. J. Peat and S. L. Buchwald, J. Am. Chem. Soc., 1996, 118, 1028.
K. Aoki, A. J. Peat and S. L. Buchwald, J. Am. Chem. Soc., 1998, 120, 3068.
2. Bartoli吲哚合成
4.Reissert吲哚合成
从邻硝基甲苯和草酸二乙酯合成吲哚及其衍生物。
用乙醇钾的反应效果较乙醇钠为好。 反应机理
首先邻硝基甲苯与草酸二乙酯反应生成邻硝基苯基丙酮酸乙酯,接下来用锌乙酸处理该产物,使之发生还原环化,得吲哚-2-羧酸。吲哚-2-羧酸还可脱羧产 生无取代的吲哚。
5.Bischler-Mohlau Indole Synthesis
三分子格氏试剂的作用:一 分子在第二步被消除,最终转化 为羰基化合物(6);一分子与氮上 的氢发生交换,生成烯烃 (11); 一分子成为吲哚环的C-2和C-3。
反应中的亚硝基芳烃中间体 (4)可以分离出来。它与两分子格 氏试剂反应,也可得到吲哚,说明它是反应的中间体。
Dobbs改进法
Adrian Dobbs 用邻位的溴作定位基成环,反应后再用偶氮二异丁腈和三丁 基锡烷将溴除去,生成 7-位无取代基的吲哚。
3.Leimgruber-Batcho吲哚合成
首先邻硝基甲苯与N,N-二甲基甲酰胺二甲缩醛和吡咯烷反应得到烯胺(2),然 后烯胺再发生还原环化,得到吲哚衍生物。
除上述提到的雷尼镍和肼外,钯碳加氢、氯化亚锡、连二亚硫酸钠以及铁-乙酸 都可用作还原一步的试剂。
反应机理
首先二甲基甲酰胺二甲缩醛受到吡咯烷的亲核进攻,二甲胺离去,产生一个活 性更强的试剂。它受到邻硝基甲苯甲基氢去质子化形成的碳负离子的进攻,失去甲 醇,得到上述烯胺。反应的此一步也可在无吡咯烷的条件下进行,这时反应经过 N,N-二甲基烯胺中间体,不过所需反应时间通常较长。这一步的产物烯胺类似于一 种分别在两侧连有吸电子和供电子取代基的烯烃,极性较强,而且常因分子中较大 的共轭范围而呈深红色。
吲哚的合成方法

吲哚的合成方法
嘿,朋友们!今天咱就来唠唠吲哚的合成方法。
这吲哚啊,可是个很有意思的东西呢!
你想想看,就好像搭积木一样,我们要把各种小零件巧妙地组合在一起,才能搭出我们想要的吲哚这个“小城堡”。
先说一个常见的方法,就像做菜一样,我们有了各种食材,通过一定的步骤就能做出美味佳肴。
比如费歇尔合成法,把苯肼和醛或酮放在一起,经过一系列反应,嘿,吲哚就慢慢出现啦!这就好像魔法一样神奇,不是吗?
还有一种方法呢,就像是走一条特别的小路。
通过邻硝基乙苯的反应,经过一些奇妙的变化,也能得到吲哚呢。
你说这是不是很有趣?就好像在一个神秘的化学世界里探险一样。
再说说从苯胺出发的方法,这就好比是从一个起点出发,沿着特定的路线前进,最终到达吲哚这个目的地。
这一路上啊,有各种反应和变化,就像我们在旅途中会遇到不同的风景一样。
有时候我就在想啊,这合成吲哚的过程,不就跟我们生活中的很多事情一样嘛。
需要耐心,需要技巧,还需要那么一点点运气。
就像我们要做成一件大事,得一步一个脚印,精心准备,才能迎来最后的成功。
而且啊,研究吲哚的合成方法,就像是打开了一扇通往奇妙世界的大门。
你能看到各种化学反应在那里奇妙地发生,就像一场精彩的演出。
咱可不能小瞧了这些合成方法,它们可是科学家们经过无数次尝试和探索才找到的呢。
就好像我们在生活中不断努力,才能找到属于自己的成功之路。
总之呢,吲哚的合成方法充满了神奇和魅力,让我们一起在这个化学的世界里尽情探索吧!不用去管什么复杂的步骤和困难,只要我们有热情,有好奇心,就一定能发现更多关于吲哚的奥秘!这就是我想说的,朋友们,你们觉得呢?。
吲哚的合成-060117

经典化学合成反应标准操作吲哚的合成目录2. Fischer 吲哚合成 (2)2.1 Fischer 吲哚合成反应示例 (2)3. 从硝基苯的衍生物出发合成吲哚 (3)3.1 邻甲基硝基苯衍生物合成吲哚 (4)3.1.1 邻甲基硝基苯衍生物合成吲哚示例 (4)3.2 邻甲酰基硝基苯衍生物合成吲哚 (4)3.1.2 邻甲酰基硝基苯衍生物合成吲哚示例 (5)3.3 邻氰甲酰基硝基苯衍生物合成吲哚示例 (5)3.4 邻乙烯基硝基苯衍生物合成吲哚示例 (6)3.5 邻位有氢的硝基苯衍生物直接用乙烯格氏试剂合成吲哚(Bartoli反应)示例74. 从苯胺的衍生物出发合成吲哚 (7)4.1苯胺经佛克烷基化再还原关环合成吲哚 (7)4.2 N-羟基苯胺DMAP催化下与丙炔酸酯缩合合成3-羧酸吲哚衍生物 (9)4.3 Nenitzescu吲哚合成 (9)5. 2-叠氮基-3-芳基丙烯酸酯环合合成2-羧酸吲哚衍生物 (10)5.1 2-叠氮基-3-芳基丙烯酸酯环合合成2-羧酸吲哚衍生物示例 (11)1. Introduction吲哚及其衍生物是一类非常有效的药物中间体。
已有不少相关综述报道其合成方法1。
我们将一些常用的合成方法简单的列举了出来,供大家在合成此类化合物的时候参考。
1 (a) G. W. Gribble, Contemp. Org. Synth., 1994, 145. (b) U. Pindur and R. Adam, J. Heterocycl. Chem., 1988, 25, 1. (c) C. J. Moody, Synlett , 1994, 681. (d) R. J. Sundberg, Indoles , Academic Press, San Diego, CA, 1996. (e) T. L. Gilchrist , J. Chem. Soc., Perkin Trans. 1, 1999, 2849. (f) G. W. Gribble, J. Chem. Soc ., Perkin Trans. 1, 2000, 1045.2. Fischer 吲哚合成Fischer 吲哚合成法是一个常见的吲哚合成方法。
Fischer吲哚合成法机理探究及其应用进展

e)在 18 r 83年 发 现 的 。反 应 是 用 苯 肼 与 醛 、酮 ( 一亚 甲 含
1 1 苯腙 的 烯肼化 .
关于烯肼 化 R bno o isn曾提 出这样 的假设 … :苯腙可能异 构
M e ha i m f Fi c e nd l y t e i nd is Ap lc to s c n s o s h r I o e S n h ss a t p i a i n
Z u n— u ,Y in HU G a h a ULa g—m n H NG Q ,Z A G Z i j ,L Xa i ,Z A i H N h - i a I i ( e a oa r f r eC e i r T er n eh ooy K yL brt yo i h m s y h o adT c n l ,Miir f d ct n o Ma n t y g ns o u ai , t y E o O enU i r t o hn ,S a dn ig a 6 10 hn ) ca nv sy f ia h n ogQn d o 6 0 ,C ia e i C 2
朱 官 花 ,于 良民 ,张 琦 ,张 智嘉 ,李 霞
( 中国海 洋大学海 洋化 学理论 与工程技 术教 育部 重点 实验 室 ,山 东 青 岛 2 6 0 ) 6 10
摘 要 :吲哚及其衍生物因其特殊的生物活性而广受关注,其合成方法很多,F ce法是合成该类化合物最经典和便捷的 i hr s
目前 被 广 泛 接 受 的 理 论 是 由 R bno ,G M 和 R bno , oi n . . s oisn R .在 12 提 出的 。可 简 要 概 括 为 三 步 : ( ) 苯 腙 的 烯 9 4年 1 肼 化 ; ( ) 新 C—C键 的 形 成 ; ( ) 释 放 氨 气 ,形 成 含 氮 五 元 2 3
吲哚合成方法

吲哚一词来源于印度的英文单词(India ):在十六世纪从印度进口的蓝色染料被称作靛篮。
将此染料化学降解可得到氧化的吲哚-吲哚酚和羟基吲哚。
吲哚在1866年通过在锌粉作用下蒸馏羟基吲哚第一次被制备出来。
吲哚可能是自然界中分布最广的杂环化合物。
色氨酸是必需的氨基酸,也是大多数蛋白质的组成部分。
它还可作为各种色胺、吲哚和2,3-二氢吲哚的生物合成前体。
2N H NH 2在动物中,存在于血液中的5-羟基色胺(5-HT )是中枢神经系统中非常重要的神经递质,在心血管和胃肠道中也起很大作用。
结构类似的激素褪黑素被认为能控制生理功能的昼夜节律。
NNH 2OH N H NHAcCH 3O植物王国中色胺酸衍生物包括3-吲哚基乙酸,它是一种有效的植物生长调节激素;以及大量不同结构的二级代谢产物-吲哚类生物碱,这一类化合物由于其有效的生理活性被广泛作为药物使用。
吲哚的结构单元也大量出现在许多人工合成的药物中,如具有消炎镇痛作用的环氧酶抑制剂吲哚美辛,止吐作用的5-HT 3受体拮抗剂昂丹司琼等。
NCH 3CH 3OOClCOOHNHON NMe由于吲哚在天然产物全合成和药物合成中的重要性,有机合成领域不断有大量关于吲哚环的全新合成方法和改进方法出现,已经形成了一个相当系统的合成框架,以下是一些目前可行的最重要的合成方法及示例。
1.通过醛和酮的苯腙的制备方法 (1) Fischer 合成法Fischer吲哚合成法发明于1883年,利用苯腙在酸或Lewis酸催化下通过重排反应,亲核关环,再消除氨而形成吲哚环N H NCH3NHPh1事实上,有时将醛或酮与苯肼在乙酸中一起加热即可发生“一锅煮”的反应2,生成的苯腙可不经分离直接发生重排反应。
甲基苯磺酸、阳离子交换树脂及三氯化磷都可有效地催化环化反应,有时在室温或更低的温度下反应也可进行3。
苯环上的供电基能提高Fischer环化反应的速率,而吸电基则降低反应速率。
但带有硝基的苯腙在合适的酸和反应条件下也可较好地发生反应,如甲苯与多聚磷酸的两相混合物4或三氟化硼的乙酸溶液5。
fisher吲哚合成法及反应机理

fisher吲哚合成法及反应机理
Fisher吲哚合成法是一种合成吲哚的方法,其反应机理如下:
首先,苯肼(或其衍生物)与含有两个α-氢的醛或酮在酸催化下缩合生成苯腙。
这个过程不需要分离,因为苯腙会立即在酸催化下发生异构化反应,生成烯胺。
烯胺又会发生一个[3,3]迁移反应,生成二亚胺。
之后,二亚胺芳构化后成环,得到一个缩醛胺(aminal)。
氨基质子化,放出氨,并失去一个质子生成芳香性的吲哚环。
在这个过程中,醛或酮必须是RCOCH₂R'类型的,其中R/R'为烷基、芳基或氢。
若醛酮的羰基有两个α-氢,则反应后一般得到两种产物的混合物。
此外,苯肼中的亚氨基氮原子(—NH—)在反应后转化为吲哚环中的氮,这一点已经得到同位素示踪实验的证实。
5-吲哚的合成-2011

维克多· 格林尼亚 1871 05.06 - 1935 12.13
反应机理 首先格氏试剂与硝基芳烃加成为中间体(3)。(3)自发分解为亚硝基芳烃(4)和醇 镁(5)。(5)在反应最后酸化时可以转化为羰基化合物(6)。(4)则与第二分子格氏试剂
加成为中间体(7),邻位取代基的位阻引发(7)的[3,3]-σ 迁移反应,使其转变为(8)。
Reaction mechanism The first two step involve the reaction of the α-bromo-acetophenone with molecules of aniline to form intermediate 4. The charged aniline forms a decent enough leaving group for an electrophilic cyclization to form intermediate 5, which quickly aromatizes and tautomerizes to give the desired indole 7.
The reaction mechanism is divided among three steps. The first step is the oxidation of the aniline 1 using (t-BuOCl) to give the chloramine 2. The second step is the addition of the ketone to give the sulfonium ion 3, and is typically done at low temperatures (-78 °C). The third and final step is the addition of a base, which in this case is triethylamine. Upon warming to room temperature, the base will deprotonate the sulfonium ion creating the sulfonium ylide 4, which quickly undergoes a [2,3]-sigmatropic rearrangement to give the ketone 5. The ketone 5 will undergo a facile condensation to give the desired 3thiomethylindole 6.
Fischer法合成2,5-二甲基吲哚的工艺研究

,
1 实验
1 . 1 试 剂与 仪器
在5 0 0 mL烧杯 中加 入 4 0 . 0 g ( 约0 . 2 5 oo t 1 ) 4 一 甲 基苯肼 盐 酸盐 ( 经 HP L C检测 纯度 为 9 7 . 2 9 , 6 ) 、 4 0 m除低沸点物
质, 即得 4 一 甲基 丙 酮 苯 腙 粗 品 3 O . 6 g , 不 经处 理 直 接
1 . 2 . 1 4 一 甲基苯 肼 的合成
收 稿 日期 : 2 0 1 3 —0 3 一O 2
作者简介 : 徐 小军( 1 9 7 2 一) ・ 男・ 湖 北红安人 。 工程师 。 研 究方向: 应用化 学; 通讯作者 : 喻 宗沅, 研究员 。 E - ma i l ; y u z y l s @g ma i lcom
亿
与 生 物 互程 2 0 1 3 , V o 1 . 3 0 N o . 4
Ch e mi s t r y & Bi o e n g i n e er i n g
囝
F i s c h e r法 合成 2 , 5 一 二 甲基 吲 哚 的 工艺 研 究
徐 小军 。 尤庆 亮I , Z 。 余朋 高 。 喻宗沅
关键词 : F i s c h e r法 ; 2 。 5 一 二 甲基 吲 哚 ; 合 成
中图 分 类 号 : TQ 2 5 1 . 3 4 0 6 2 6 . 1 3
文献标识码 : A
文章编号 : 1 6 7 2 —5 4 2 5 ( 2 0 1 3 ) 0 4 —0 o 5 9 一O 4
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
费歇尔吲哚合成
费歇尔吲哚合成是一种重要的有机合成反应,可以用于制备吲哚衍生物。
本文将从反应机理、反应条件和用途三个方面来介绍费歇尔吲哚的合成。
一、反应机理
费歇尔吲哚合成是一种经典的有机合成反应,形成吲哚骨架的过程中,酮类化合物通过酰亚胺中间体受亲核试剂的取代,最终生成吲哚结构。
反应机理如下:
首先酮类化合物与氨水或者胺发生加成反应,形成酰亚胺中间体。
然后中间体中的氮原子上的负电荷受到亲核试剂的攻击,形成一个新的碳-碳键,使酰亚胺环缩合成吲哚环。
最后通过水解反应,得到目标产物吲哚。
二、反应条件
1. 氨水或胺的使用量
氨水或胺的使用量直接影响到反应的效率和产率。
过多的氨水或胺会影响反应速率,而使用过少会产生杂质。
2. 催化剂
众所周知,催化剂可以提高反应速率和产物收率。
研究表明,不同的催化剂会对反应有不同的影响。
传统的催化剂有硼酸、三氯化铝、氧化铝等等,近年来,还有各种催化剂的开发和应用。
3. 反应溶剂
反应溶剂可以影响反应的效率和产率。
一般情况下,有机溶剂如乙醇、二甲基甲酰胺、二氯甲烷等可以作为反应溶剂。
4. 反应温度
反应温度也是影响反应速率和产物收率的重要因素。
一般反应温度在室温下或者略高于室温下进行,根据反应条件的不同,反应温度也会有所改变。
三、用途
1. 吲哚衍生物的合成
费歇尔吲哚合成是制备吲哚衍生物的重要方法。
吲哚及其衍生物在生物活性分子中具有广泛的应用。
2. 药物的合成
吲哚化合物在许多药物中被广泛应用,例如小檗碱、鹅观草碱等药物都是吲哚类衍生物。
利用费歇尔吲哚合成,可以合成具有特定结构和活性的药物。
3. 杂环化合物的合成
在特定的硬件条件下,费歇尔吲哚合成可用于获得不含氮或含氮杂环的化合物,从而制备出新的生物活性分子。
总结:
费歇尔吲哚合成是合成吲哚衍生物重要的方法之一,适用范围广泛,可以应用于合成化合物和杂环化合物等。
合成反应机理相对简单,但反应条件和催化剂等仍然需要根据实验的需要进行选择。
同时也可以进一步发展该反应来实现更广泛的应用,例如应用于特定类生物合成研究。
