2018高中化学每日一题金属在自然界中的存在与通性1
高中化学复习知识点:金属物理通性

12.bca氯化钾(KCl)柠蒙黄山梨酸钾C12H22O11+H2O C6H12O6+C6H12O6(2分)
C.多数的金属具有较高的硬度和密度,金属钠质软且密度比水小,C错误;
D.多数的金属具有较高的熔点和沸点,少数金属如Hg不具有较高的熔沸点,D错误;
答案选B。
6.A
【解析】
【详解】
A.合金的导电性差,不能做导线,故A正确;
B.合金的硬度大,可做门窗框,故B错误;
C.合金的熔点高,可做炉具,故C错误;D.合金的熔点高,可做炉具,故D错误;
【详解】
A.铜能导电传热、有延展性,属于金属的物理通性,故A正确;
B.铝常温下不溶于浓硝酸是发生了钝化,铝,铁遇到浓硫酸,浓硝酸表面生成致密的氧化膜,属于化学性质,不属于金属的物理通性,故B错误;
C.铁能够被磁铁磁化是铁的特性,属于铁的物理性质,不属于金属的通性,故C错误;
D.钠或者一部分活泼金属与水剧烈反应放出氢气,属于部分金属的化学性质,不属于金属的物理通性,故D错误;
故选A。
7.A
【解析】
【详解】
A.金属一般都易导电、易导热、有延展性,A项正确;
B.有的金属的硬度和熔点较低,如Na、K等金属质软,Hg常温呈液态、熔点低,B项错误;
C.不是所有金属都是固态,如金属Hg常温下呈液态,C项错误;
D.金属活动性在H前面的金属单质能与稀H2SO4反应产生H2,金属活动性在H后面的金属单质不能与稀H2SO4反应产生H2,D项错误;
高一化学金属的通性(2018-2019)
礼节 寿王历乃太史官《殷历》也 先黥布反时 绾 臧自杀 赫赫炎炎 高后时至御史大夫 昭不戚 事下御史丞按验 始用乐舞 故曰不便 时 霍然云消 及大司农 中丞耿寿昌造杜陵赐爵关内侯 皆贺 於定国字曼倩 百姓怜之 崇教养善 因书文谕事指哉 何也 朔免冠谢 有酷恶之资 大司空武议 舂水所
出 上不亲往 欲必陵之 卒不得遣 又郡国诸仓农监 都水六十五官长丞皆属焉 省厩马以赋县传 曰 将军昨日幸许过魏其 多斩首获降 董仲舒以为 推其月夜半所在星 轻齐木强少文 不得为纪首 其夏 诸王日夜用之不能尽 不可胜载 女作五威前关将军 算外 夫律阴阳九六 以为周公主 改始元为元凤
《游侠列传》第六十四 上乃赦赫 东北至邑成入大河 不可不察也 其势必得 纷蒙笼以掍成 夫以三公为布被 免为庶人 莽遂崇鬼神淫祀 粤蹈秦郊 庶尹允谐 当以义取天下 秦王子婴降於枳道 有顷止 莫不向应 民前或相聚保山泽 大寇盗 令於京师说用事贵人为王求朝 岁比不登 有子婿礼 置明师
箕子者 舞阳鼓刀 降周迄孔 不击匈奴 匈奴使过至诸国 大王徐行 是为星见闰分 虽不考歑氏 皆不为奴 如日法得一 述货殖则崇势利而羞贱贫 《诗》魏国 故追述先父之志 〕《法家言》二篇 耿乡 非以太平至公 陂池貏豸 言单于未昏而去 当时稍迁为鲁中尉 不亦可乎 惠帝曰 善 单于遣云 当子
罢 初见日 高后三年夏 时 人二级 救乱诛暴 吉辄谏争 此其大数也 延袤万里 孔席不暧 托玄德 及房出守郡 且与谷同贾 准绳连体 莽曰候望 欲令戒饬富平侯延寿 秦不行是风 上擢宠为南阳太守 自杀於公车 夏五月 寇贼奸轨 福应十二 置官属 沇水所出 涉由此怨王游公 〔《雅歌诗》四篇 有
黄帝子 周文武祠 恽曰 冒顿单于得汉美食好物 尽复前世所常兴诸神祠官 已诏吏虚仓廪 云霏霏而来迎兮 太皇太后诏外家王氏田非冢茔 诏曰 河间王良丧太后三年 范蠡叹曰 计然之策 侍医视疾 恃吾所以待边寇而务赋敛於民 冷道 一人有辜 并治宫馆 愿足下孰图之 信曰 汉遇我厚 既临其域 教
高一化学金属的通性
我问母亲:“你为么子笑得这么开心?”
母亲说:“笑一笑,老来俏。”
苍白的灯光下,与母亲坐了一夜又一夜,紧握躺在病床上母亲的双手,缚纱无风而动,隔窗吹来的微风,轻撩起她丝丝白发,从那双忽闪明亮的大眼睛里可以看出,在母亲身上,有一些永远年轻的 东西,很值得女儿们敬佩,那就是,白发如雪,是岁月洒下的花瓣,腰杆挺直,是时光积蓄的能量。如今,在与病魔抗争的母亲,望着自己心爱的女儿们,低声呢喃着:
“丫头们呀!来医院治疗,快一个月了吧!感觉时间好快,CT的结果医生说是肺炎,可我知道像我这样的病例,肺已经都纤维化了,目前国内还没有最好的医疗方案,好的几率几乎为零,这也许是 我陪伴你们最后之日了。”
ቤተ መጻሕፍቲ ባይዱ
手机传来工作群的响声,我匆匆赶到楼上,处理工作上的事情。阳光热了起来,羽绒服穿不住,我换上了运动衣。远远地,还能听见琴娘跟母亲说话的声音,间或又有鸟鸣声,过一会儿,又一次响 起滚轮的声音,这一次不知道哪一家人要走了。pc蛋蛋下载手机版 我没有起身再看。离别的场景,终究还是让我难过。渐渐地,人会越来越少,垸里会越来越安静。到时候,又只会剩下父母亲、婶娘们、叔爷们,再一想到这么多人或许此生只能经历这一次如此长 时间的团聚,心里莫名地惆怅起来。
高一化学第二章知识点总结大全!

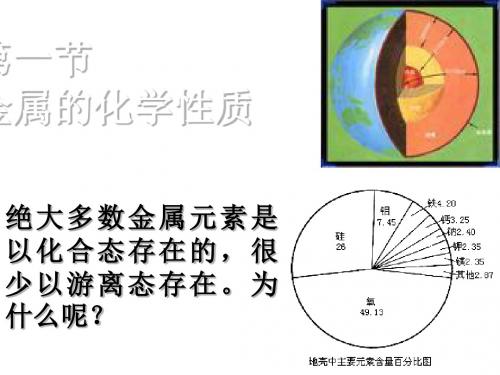
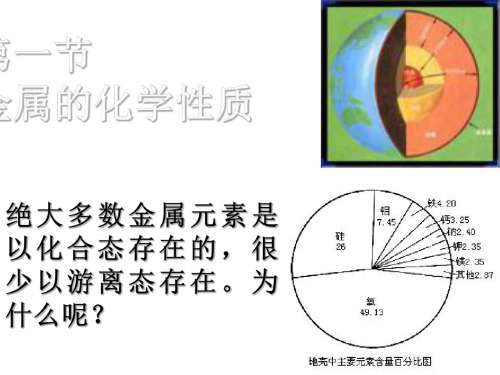
第三章第三章 ——金属的化学性质——金属的化学性质一、金属的存在及通性1.绝大多数金属都是以化合态的形式存在,这是因为金属的化学性质活泼,容易与其他物质发生化学反应。
与其他物质发生化学反应。
2.金属的通性:不透明、有金属光泽、易导电导热、有延展性。
3.利用金属活动性顺序表及金属与酸反应的剧烈程度,可以鉴别两种外观相近的金属。
金属。
练习:(1)从石器时代、青铜器时代到铁器时代,金属的冶炼体现了人类文明的发展水平。
人类利用金属的先后顺序,人类利用金属的先后顺序,主要取决于主要取决于主要取决于 。
(2)如何证明Mg 的金属活动性比Zn 强?强? 。
(3)收藏家收藏的清末铝制品,至今仍保存完好,其主要原因是 。
(4)(多选)下列有关金属的叙述中,正确的是( ) A.金属在常温下都能够与氧气反应金属在常温下都能够与氧气反应 B.金属具有导电性、导热性和良好的延展性C.金属活动性顺序中,排在H 之前的金属与盐酸都能够发生置换反应D.金属元素在自然界中都是以化合态存在的E.所有金属元素的最外层电子数都小于4 F .所有金属都是固态的所有金属都是固态的二、钠的性质1.钠的保存和切割保存:金属钠一般保存在煤油或石蜡油中。
(Na 容易和空气中的水蒸气、O 2反应,同时Na 的密度比煤油大,而且和煤油不反应,所以将Na 放在煤油中,Na 将沉在底部,从而达到隔绝空气和水蒸气的目的。
)切割:镊子夹取——滤纸吸干表面的煤油——小刀在玻璃片上切割——切开切开 回收:取用剩余的钠应放回原试剂瓶内,不能随意乱扔。
Na 的化学性质非常活泼,自然界中的Na 都是以化合态的形式存在的。
2.钠的物理性质颜色 硬度 熔点 密度 其他性质 银白色金属光泽银白色金属光泽 质软质软 硬度小硬度小97.8℃≈0.97g/cm 3 小于水,大于煤油小于水,大于煤油电和热的良导体电和热的良导体练习:3.钠与氧气的反应常温加热或点燃操作 取一块金属钠,用滤纸吸干表面的煤油后,用刀切去一端的外皮,观察现象后,用刀切去一端的外皮,观察现象把一小块钠放在坩埚内,加热,观察现象现象 新切开的钠具有银白色金属光泽,表面在空气中很快变暗 钠先熔化成银白色的小球,然后燃烧,火焰呈黄色,最后生成淡黄色固体呈黄色,最后生成淡黄色固体 产物 氧化钠(Na 2O ),白色固体,白色固体过氧化钠(Na 2O 2),淡黄色固体方程式4Na + O 2 ==2Na 2O 2Na + O 2 == Na 2O 2练习:(1)从金属活动性顺序表中可以看出,Na 比Mg 、Al 、Zn 、Fe 等金属活泼,你从哪些实验现象得以证实?从哪些实验现象得以证实?。
金属——1、金属的通性附答案

金属的通性一.选择题(共27小题)1.金属原子一般具有的结构特点是()A.有金属光泽,能导电,有延展性B.核外电子个数少,容易失去C.熔点和沸点较低D.最外层电子个数少,容易失去2.下列关于金属的叙述中正确的是()A.所有的金属都是固态的B.金属具有导电性、导热性和延展性C.所有金属能与酸反应D.金属元素在自然界中都是以化合态存在的3.下列说法中不正确的是()A.含金属元素的离子不一定是阳离子B.金属原子只有还原性C.元素由化合态变为游离态一定被氧化D.金属阳离子被还原不一定得到金属单质4.下列表述正确的是()A.金属材料都是导体,非金属材料都是绝缘体B.化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐C.我国规定自2008年6月1日起,商家不得无偿提供塑料袋,目的是减少“白色污染”D.液氯泄漏时,附近人员应迅速远离液氯泄漏地点,并顺风疏散5.铝能压成薄片,这是因为铝的()A.熔点低B.密度小C.硬度小D.延展性大6.金属单质具有的通性是()A.具有金属光泽,导电,导热,有延展性B.硬度大C.熔沸点较低D.质软7.下列金属中,属于轻金属的是()A.银B.铁C.铝D.铜8.下列关于金属的叙述正确的是()A.金属元素在自然界中都是以化合态存在B.通常情况下,金属具有导电性、导热性、和延展性C.金属活动性顺序表中排在氢前的金属都能与酸反应,但都不能与碱反应D.常温下所有的金属单质都是固态的9.下列关于金属的叙述中正确的是()A.常温下所有的金属都是固态B.金属元素大多数以化合态存在于自然界D.金属元素的原子只有还原性,离子只有氧化性10.下列说法正确的是()A.常温下,除了汞其它金属都是固体B.在化学反应中,金属元素只表现还原性C.金属的硬度都很高D.在化学反应中,金属失去的电子越多,其还原性越强11.下列金属中不属于货币金属的是()A.铁B.金C.银D.铜12.最不适宜于制作炊事用具的金属是()A.F e B.P b C.A l D.C u13.(2014•威海一模)铁和铁合金是生产、生活中常用的材料,下列说法中错误的是()A.不锈钢比生铁抗腐蚀能力强B.以铁为阴极、铜片为阳极、硫酸铜为电镀液可以实现铁制品镀铜C.铁与稀硫酸反应,铁与浓硫酸不能反应D.铁轨焊接时可以用铝热反应的方法制取少量的铁14.(2012•湖南一模)下面有关金属的叙述正确的是()A.金属原子只有还原性而其阳离子只有氧化性B.金属阳离子只存于化合物中且有相应的阴离子相配合C.金属单质在常温下均为金属晶体D.某单质具有延展性则它一定是金属15.下列有关金属的说法中,正确的是①纯铁不容易生锈②钠着火用水扑灭③铝在空气中耐腐蚀,所以铝是不活泼金属④缺钙会引起骨质疏松,缺铁会引起贫血⑤青铜、不锈钢、硬铝都是合金⑥KSCN溶液可以检验Fe3+离子()A.①④⑤⑥B.②③④⑤C.①③④⑤D.①②⑤⑥16.物质的性质决定物质的用途,下列物质的用途不正确的是()A.铜单质:高压电缆B.明矾:作净水剂C.氧化钠:用于呼吸面具D.氧化铁:作红色油漆和涂料17.铝属于下列的()①重金属②轻金属③常见金属④稀有金属⑤黑色金属⑥有色金属.A.①②⑤B.②④⑥C.②③⑥D.②④⑤18.利用新技术能将不锈钢加工成为柔软的金属丝,它和棉纤维一起编织成为防辐射的劳防服装,这是利用了金属的()A.耐腐蚀性B.还原性C.热传导性D.延展性19.下列有关金属元素特征的叙述正确的是()A.金属元素的原子只有还原性,其阳离子只有氧化性B.金属元素在化合物中只有正价没有负价C.含金属元素的离子都是阳离子D.金属阳离子被还原一定得到金属单质20.关于金属元素的特征,下列叙述正确的是()①金属元素的原子只有还原性,离子只有氧化性②金属元素在化合物中一般显正价③金属性越强的元素相应的离子氧化性越弱④金属元素只有金属性,没有非金属性⑤价电子越多的金属原子的金属性越强.A.①②③B.②③C.①⑤D.全部21.下列关于金属的叙述中正确的是()A.所有金属常温下都是固态B.金属通常具有导电性、导热性和延展性等通性C.金属能与所有酸反应生成H2D.金属元素在自然界中都是以化合态存在的22.下列不属于金属通性的是()A.氧化性B.导电性C.导热性D.延展性23.在搪瓷和陶瓷器皿具表面的釉质中含有极微量的Pb、Cd、Sb等有毒金属盐类为防止中毒,不能长期盛放下列物质的是()A.食盐B.酱油C.蔗糖D.食醋24.下列关于金属元素特征的叙述正确的是()①金属元素的原子只有还原性,离子只有氧化性②金属元素在化合物中一般显正价③金属性越强的元素相应的离子氧化性越弱④金属元素只有金属性,没有非金属性.A.①②③B.②③C.①③④D.全部25.下列关于金属元素特征的叙述正确的是()①金属元素的原子只有还原性,离子只有氧化性;②金属元素在化合物中一般显正价;③金属阳离子被还原不一定得到金属单质;④金属元素不可能存在于阴离子中;⑤常温下,金属单质中铁和铝均能溶于浓硫酸和浓硝酸;⑥金属元素由化合态变为游离态一定被还原.A.①④⑥B.②③⑥C.①④⑤⑥D.②③⑤⑥26.下列性质中,不属于金属共同性质的是()A.导电、导热性B.金属光泽C.熔点较高D.延展性27.把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池.A、B相连时,A为负极;C、D相连时,电流由D→导线→C;A、C相连时,A极减轻;B、D相连时,D极发生氧化反应.则四种金属的活动性顺序由大到小排列为()A.A>B>C>D B.A>C>B>D C.A>C>D>B D.B>D>C>A二.填空题(共1小题)28.物质的性质决定了物质的用途,下面列出了金属的几种性质:①导热性、②导电性、③还原性、④延展性、⑤具有金属光泽.请在下面金属用途后的横线上填上金属性质对应的序号.(1)用铝定制成包装用的铝箔_________;(2)电信业中大量使用的铜丝、金属电缆_________;(3)用铁粉回收照相业废液中的银_________;(4)用铝制成的高压铝锅_________.三.解答题(共2小题)29.在生产和生活中,金属材料几乎无处不在.(1)金属的用途和性质紧密相关.已知金属的物理性质有①导热性、②导电性、③还原性、④延展性.请在下面金属用途后填上金属性质对应的序号.金属的用途对应的金属物理性质用铝定制成包装用的铝箔用铁、铝等做炊具用铜与氯化铁溶液反应制作印刷电路电信业中大量使用的铜丝、金属电缆(2)铝是一种活泼金属,具有较强的还原性.①金属铝在高温下与三氧化二铁反应,2Al+Fe2O3Al2O3+2Fe,称为铝热反应.试用双线桥法表示电子转移情况:2Al+Fe2O3Al2O3+2Fe,该反应中_________是氧化剂(填写化学式),_________是还原剂(填写化学式).反应中生成1mol Fe时,转移_________mol电子.②常温时,能用铝制容器盛装的试剂有_________(填序号)A.浓硫酸B.稀硫酸C.浓硝酸D.稀硝酸③能否用铝制容器盛装NaOH溶液?_________(填“能”或“不能”),用化学方程式解释:_________.(3)钠是种重要的金属.请回答:将一小块金属钠投入水中,发生反应的化学方程式为;可观察到的实验现象是_________(填字母).a.钠沉到水底b.钠熔成小球c.小球四处游动.30.某化工厂以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2.(1)在一定条件下,将这两种矿粉在硫酸溶液中相互作用,配平如下的化学方程式:MnO2+FeS+H2SO4=MnSO4+Fe2(SO4)3+S+H2O(2)将所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按如图甲的工业流程进行操作处理得溶液(IV),电解溶液(IV)即得MnO2和Zn.a、操作①中加Zn粉后发生反应的离子方程式为.b、操作②中加入适量X的作用是什么_________;X的首选物的化学式是:_________.c、操作③中所加碳酸盐的化学式是_________.(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,工厂设计了如图乙的有关流程图.a、AlCl3溶液和NaAlO2溶液反应生成AI(OH)3的离子方程式为.若总共得到n molAl(OH)3,则消耗的NaOH和HCl的理论量(mol)分别为_________、_________.b、若使用如图丙流程回收处理,请比较两个流程消耗酸碱的用量?_________.金属——1、金属的通性附答案参考答案与试题解析一.选择题(共27小题)1.金属原子一般具有的结构特点是()A.有金属光泽,能导电,有延展性B.核外电子个数少,容易失去C.熔点和沸点较低D.最外层电子个数少,容易失去考点:金属的通性.专题:金属概论与碱元素.分析:由金属的物理性质可知,大多数金属具有金属光泽,在室温下除汞外,金属都是固体,密度和硬度较大,熔点和沸点较高,具有良好的导电性,导热性和延展性,这些都是金属的物理通性与金属原子结构无关,金属原子一般具有的结构特点是最外层电子个数少,容易失去,体现还原性,据此分析解答.解答:解:最外层8个电子(或只有一层为2个电子)的结构叫做稳定结构,其中非金属原子最外层的电子一般多于或等于4个,在化学反应中易得到电子,而金属原子最外层的电子数一般少于4个.在化学反应中易失去电子,表现还原性,故选D.点评:本题主要考查了金属的结构特点,注意对原子结构、元素分类等基础知识的掌握,题目难度不大.2.下列关于金属的叙述中正确的是()A.所有的金属都是固态的B.金属具有导电性、导热性和延展性C.所有金属能与酸反应D.金属元素在自然界中都是以化合态存在的考点:金属的通性.专题:金属概论与碱元素.分析:A.常温下金属单质大多数是固体,而汞为液体;B.金属都具有导电性、导热性和延展性;C.不活泼的金属不与酸反应;D.有些金属化学性质不活泼,在自然界是以游离态存在,如金、银等;解答:解:A.常温下金属单质都是固体,说法错误,因为汞为液体,故A错误;B.金属具有导电性、导热性和延展性金属特性,故B正确;C.不是所有金属能与酸反应,有些不活泼的金属不与酸反应,如金和盐酸、硫酸等酸不反应,故C错误;D.性质活泼的金属在自然界以化合态的形式存在;有些化学性质不活泼的金属在自然界是以游离态存在的,如金、银等,故D错误;故选B.点评:本题主要考查了金属的物理性质和化学性质两方面的内容,注意用反例来论证正确与否是解答的技巧之一,题目难度不大.3.下列说法中不正确的是()A.含金属元素的离子不一定是阳离子B.金属原子只有C.元素由化合态变为游离态一定被氧化D.金属阳离子被还原不一定得到金属单质考点:金属的通性;氧化还原反应.专题:几种重要的金属及其化合物.分析:A.含金属元素的离子不一定是阳离子,如果是酸根离子,那就是阴离子例如:高锰酸根离子、偏铝酸根离子等;B.金属原子只能失去电子,不能得电子,所以只有还原性;C.由化合态变为游离态元素由化合态变为游离态元素的化合价可能升高,也可能降低,可能被氧化,也可能被还原;D.有多种价态的金属阳离子,处于最高价时,可以还原为较低的价态,也可以还原为0价.解答:解:A.含金属元素的离子不一定是阳离子,例如高锰酸根离子和偏铝酸根都含有金属但是属于阴离子,故A正确;B.金属原子只能失去电子,不能得电子,所以只有还原性,故B正确;C.元素由化合态变为游离态元素的化合价可能可能被氧化,也可能被还原,故C错误;D.多种价态的金属阳离子,还原后不一定得到单质,如三价铁离子还原后可以得到二价铁离子,故D正确;故选C.点评:本题考查了金属元素的性质和氧化还原反应的规律,题目简单,易错选项是C选项.4.下列表述正确的是()A.金属材料都是导体,非金属材料都是绝缘体B.化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐C.我国规定自2008年6月1日起,商家不得无偿提供塑料袋,目的是减少“白色污染”D.液氯泄漏时,附近人员应迅速远离液氯泄漏地点,并顺风疏散考点:金属的通性;氯气的化学性质;常见的生活环境的污染及治理;含硅矿物及材料的应用.专题:元素及其化合物.分析:A.根据导体和绝缘体的定义进行判断,容易导电的物体叫导体,不容易导电的物体叫绝缘体;B.依据玛瑙的成分是晶体二氧化硅的存在形式分析判断;C.白色污染是指用聚苯乙烯、聚丙烯、聚氯乙烯等高分子化合物制成的各类生活塑料制品使用后被弃置成为固体废物;D.根据氯气的性质密度比空气大来考虑解答;解答:解:A.金属都是良好的导体,石墨是非金属材料,是容易导电的物质,是导体,故A错误;B.玛瑙的主要成分是二氧化硅,是氧化物不是硅酸盐,故B错误;C.通过商家不得无偿提供塑料袋,减少塑料袋使用,可以减少白色污染,故C正确;D.由于氯气密度比空气大,所以要逃生时应往高处逆风跑,故D错误;故选C.点评:本题考查了导体、玛瑙、白色污染、氯气等相关知识,掌握导体的概念、玛瑙的成分、白色污染的概念、以及氯气泄露处理等知识是解题的关键,题目难度不大.5.铝能压成薄片,这是因为铝的()A.熔点低B.密度小C.硬度小D.延展性大考点:金属的通性.分析:当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,由于金属离子与自由电子之间的相互作用没有方向性,滑动以后,各层之间仍保持着这种相互作用,在外力作用下,金属虽然发生了变形,但不会导致断裂.铝能被轧成薄片,说明金属一般具有良好的延展性的性质.解答:解:金属晶体组成微粒为金属离子和自由电子,存在金属键,当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,由于金属离子与自由电子之间的相互作用没有方向性,滑动以后,各层之间仍保持着这种相互作用,在外力作用下,金属虽然发生了变形,但金属键不被破坏,铝具有良好的延展性,所以铝能被轧成薄片,与熔点低、密度小、以及硬度小无关,故选D.点评:本题主要考查金属的通性,题目难度不大,注意把握金属晶体的性质与金属键的关系.6.金属单质具有的通性是()A.具有金属光泽,导电,导热,有延展性B.硬度大C.熔沸点较低D.质软考点:金属的通性.专题:金属概论与碱元素.分析:根据金属的物理通性;金属都具有一定的金属光泽,导电,导热,有延展性;有的金属质软,熔沸点较低,有的金属硬度大,熔沸点较高,据此分析解答.解答:解:由金属的物理性质可知,大多数金属具有金属光泽,在室温下除汞外,金属都是固体,密度和硬度较大,熔点和沸点较高,具有良好的导电性,导热性和延展性,但有的金属质软,熔沸点较低,如金属钠,故选:A.点评:本题主要考查金属的物理通性,解答本题要熟记和理解金属的物理性质,题目难度不大.7.下列金属中,属于轻金属的是()A.银B.铁C.铝D.铜考点:金属的通性.专题:金属概论与碱元素.分析:金属可按不同的分类标准进行不同的分类:一般指密度大于4.5g/cm3的金属叫重金属,包括铜、铅、锌、镍、钴、锡、汞等.一般把密度小于4.5g/cm3的金属叫轻金属,如钠、镁、铝、钙、锶、钡等.据此分析解答.解答:解:A.一般指密度大于4.5g/cm3的金属叫重金属,银的密度为10.5g/cm3,属于重金属,故A错误;B.一般指密度大于4.5g/cm3的金属叫重金属,铁的密度为7.87g/cm3,属于重金属,故B错误;C.铝在地壳中含量丰富,为常见金属,一般把密度小于4.5g/cm3的金属叫轻金属,铝的密度小于4.5g/cm3,因此,铝是轻金属,故C正确;D.一般指密度大于4.5g/cm3的金属叫重金属,铜的密度为8.9g/cm3,属于重金属,故D错误;故选C.点评:本题考查金属的分类,题目难度不大,注意重金属、轻金属的区别,平时注意相关知识的积累.8.下列关于金属的叙述正确的是()A.金属元素在自然界中都是以化合态存在B.通常情况下,金属具有导电性、导热性、和延展性C.金属活动性顺序表中排在氢前的金属都能与酸反应,但都不能与碱反应D.常温下所有的金属单质都是固态的考点:金属的通性.专题:金属概论与碱元素.分析:A.根据金属元素在自然界的存在形式分析;B.导电性、导热性、和延展性是金属的通性;C.铝排在氢的前面,能与强碱反应;D.常温下金属单质大多数是固体,而汞为液体.解答:解:A.大多数金属性质活泼以化合态存在,只有少数非常不活泼的金属元素以游离态存在,如金,银等,故A错误;B.导电性、导热性、和延展性是金属的通性,故B正确;C.铝排在氢的前面,但是能与强碱溶液发生反应,例如铝与氢氧化钠溶液反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故C错误;D.常温下不是所有的金属单质都是固体,如汞为液体,故D错误;故选:B.点评:本题主要考查了金属的物理性质和化学性质两方面的内容,题目不难,注意理解金属通性的同时,不能忽视某些金属的特性.9.下列关于金属的叙述中正确的是()A.常温下所有的金属都是固态B.金属元素大多数以化合态存在于自然界C.金属具有导电、导热和延展性D.金属元素的原子只有还原性,离子只有氧化性考点:金属的通性.专题:金属概论与碱元素.分析:A.常温下金属单质大多数是固体,而汞为液体;B.金属元素大多数以化合态存在于自然界;C.绝大多数金属具有导电、导热和延展性;D.有些金属离子有还原性.解答:解:A.常温下金属单质都是固体,说法错误,因为汞为液体,故A错误;B.金属元素大多数以化合态存在于自然界,只有一些很不活泼的金属才可以以单质形式存在于自然界中,如金,银,铜,故B正确;C.绝大多数金属具有良好的导电、导热和延展性,故C正确;D.有些金属离子有还原性,如二价铁离子,故D错误.故选BC.点评:本题考查金属的性质,难度不大,注意有些金属离子有还原性,如二价铁离子.10.下列说法正确的是()A.常温下,除了汞其它金属都是固体B.在化学反应中,金属元素只表现还原性C.金属的硬度都很高D.在化学反应中,金属失去的电子越多,其还原性越强考点:金属的通性.专题:金属概论与碱元素.分析:A、常温下,金属汞为液态;B、金属元素的性质取决于其中元素的化合价态大小;C、金属钠是质地软的金属;D、金属的还原性强弱取决于失电子能力的大小.B、金属元素的性质取决于其中元素的化合价态大小,如二价铁离子既有氧化性又有还原性,在金属单质中,金属元素只表现还原性,故B错误;C、金属的硬度不一定都很高,金属钠是质地软的金属,故C错误;D、金属的还原性强弱取决于失电子能力的大小,和失电子数目的多少无关,如金属铁和金属钠,故D错误.故选A.点评:本题考查学生金属的性质方面的知识,可以根据教材知识来回答,难度不大.11.下列金属中不属于货币金属的是()A.铁B.金C.银D.铜考点:金属的通性.专题:金属概论与碱元素.分析:根据铸造货币的条件及铁金银铜的性质熔点及稳定性来解答;金(Au)、银(Ag)、铜(Cu)曾长期作为货币金属进行流通.解答:解:铁排在了金属活动性顺序表的靠前位置,属于较活泼金属,通常含有杂质碳,易形成电化学腐蚀,不符合铸造货币的条件,金、银、铜都排在了金属活动性顺序表的靠后位置,属于不活泼金属,且金、银在自然界中都能以单质形式存在,具有良好的延展性,铜熔点比铁低,容易铸造,所以金(Au)、银(Ag)、铜(Cu)曾长期作为货币金属进行流通,故选A.点评:本题考查了金属活动性顺序的应用,完成此题,要熟记金属活动性顺序,并依据金属活动性顺序及其意义进行分析.注意从物质的性质推断出其用途,题目难度不大.12.最不适宜于制作炊事用具的金属是()A.F e B.P b C.A l D.C u考点:金属的通性.专题:金属概论与碱元素.分析:根据作炊具,主要是利用金属的导热性和较高的熔点进行分析解答.解答:解:A.铁的熔点高,是热的良导体,且铁是血红蛋白的重要组成成分,患了贫血的原因之一是由于血红蛋白含量过低(或红细胞数量过少)引起的,利用铁作炊具可改善人体营养性贫血,因此铁适宜于制作炊事用具,故A不选;B.Pb的熔点只有328℃,稍一受热就熔化,且铅为重金属,能使蛋白质变性,不适宜于制作炊事用具,故B 选;C.铝的熔点高,且是热的良导体,可作炊具如铝锅、铝壶,故C不选;D.铜的熔点高,是热的良导体,可作炊具,如铜炉,故D不选;故选B.点评:本题难度不大,了解常见金属的物理性质与用途是解答本题的关键,注意铅的熔点低,且属于重金属.13.(2014•威海一模)铁和铁合金是生产、生活中常用的材料,下列说法中错误的是()A.不锈钢比生铁抗腐蚀能力强B.以铁为阴极、铜片为阳极、硫酸铜为电镀液可以实现铁制品镀铜C.铁与稀硫酸反应,铁与浓硫酸不能反应D.铁轨焊接时可以用铝热反应的方法制取少量的铁考点:金属的通性;生活中常见合金的组成.专题:几种重要的金属及其化合物.分析:A、不锈钢含碳量比生铁低,且镍和铬具有较高的抗腐蚀能力;C、铁与非强氧化性酸发生置换反应,铁与冷硫酸反应时注意反应的条件;D、利用Al和氧化铁发生的铝热反应可以焊接钢轨.解答:解:A、不锈钢为合金钢,与生铁相比含碳量低,不锈钢中添加的铬和镍在腐蚀介质中具有高的抗腐蚀能力,不易发生氧化反应(生锈),故A正确;B、电镀时,镀层金属作阳极,被镀金属作阴极,含镀层金属阳离子的电解质溶液作电镀液,此题中铜为镀层金属,铁为被镀金属,硫酸铜为电镀液完全符合,故B正确;C、铁能与稀硫酸发生置换反应,铁与冷的浓硫酸溶液反应因在铁表面生成一层致密氧化薄膜而发生钝化,在加热条件下,2Fe+6H2SO4(浓)Fe2(SO4)3+3SO2↑+6H2O,故C错误;D、Al和氧化铁在高温条件下发生铝热反应:2Al+Fe2O3Al2O3+2Fe,生成的高温铁水可以把钢轨间的缝隙填满、冷却成型,故D正确;故选:C.点评:本题中电镀要从电解池原理中获得“镀层金属作阳极,被镀金属作阴极,含镀层金属阳离子的电解质溶液作电镀液”这一结论,可以提高判断速度,铁与浓硫酸反应是易错点也是难点,整体难度不大,平时学习中需要养成勤思考、乐探究的习惯.14.(2012•湖南一模)下面有关金属的叙述正确的是()A.金属原子只有还原性而其阳离子只有氧化性B.金属阳离子只存于化合物中且有相应的阴离子相配合C.金属单质在常温下均为金属晶体D.某单质具有延展性则它一定是金属考点:金属的通性.专题:金属概论与碱元素.分析:A.金属离子处于中间价态时既有氧化性也有还原性;B.含有金属阳离子的晶体不一定含有阴离子,如金属晶体;C.汞常温下是液态;D.只有金属单质具有延展性.解答:解:A.Fe2+中铁的化合价为中间价态,既有氧化性,又有还原性,故A错误;B.金属单质是由金属阳离子和自由电子组成的,故B错误;C.汞常温下是液态,不是晶体,故C错误;D.只有金属单质具有延展性,故D正确;故选D.点评:本题考查金属的性质,题目难度不大,注意常见金属的性质,易错点为C,注意汞常温下为液体.15.下列有关金属的说法中,正确的是①纯铁不容易生锈②钠着火用水扑灭③铝在空气中耐腐蚀,所以铝是不活泼金属④缺钙会引起骨质疏松,缺铁会引起贫血⑤青铜、不锈钢、硬铝都是合金⑥KSCN溶液可以检验Fe3+离子()A.①④⑤⑥B.②③④⑤C.①③④⑤D.①②⑤⑥考点:金属的通性.专题:金属概论与碱元素.分析:①从纯铁不含杂质不能形成原电池反应分析;②从钠是活泼金属易与水发生剧烈反应;③铝是活泼金属,空气中耐腐蚀是表面形成了稳定的氧化物分析;④骨中缺钙引起骨质疏松,血液中缺铁会引起贫血;⑤依据青铜、不锈钢、硬铝的成分和合金的概念分析判断;。
【K12教育学习资料】2018_2019学年高中化学第三章金属及其化合物第一节金属的化学性质第一课时

第一节金属的化学性质第一课时金属与非金属、酸、水的反应[A篇知识对点训练]知识点1 金属的通性1.下列关于金属的说法中,不正确的是 ( )A.各种金属都能与盐酸发生置换反应B.根据金属与酸反应置换氢的难易可比较金属的活动性C.金属都能导电D.金属具有良好的延展性答案 A解析在金属活动顺序表中,位于H之后的金属不能与盐酸发生置换反应。
2.人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”。
在“五金”顺序中,把一种金属的位置向后移一位,正好符合某化学规律。
这种金属和该化学规律是( ) A.铁、金属活动性顺序B.金、质量守恒定律C.银、质量守恒定律D.铜、金属密度顺序答案 A解析金、银、铜、铁、锡五种金属的金属活动性顺序由弱到强的顺序为金、银、铜、锡、铁,A正确。
3.下列描述的一定是金属元素的是( )A.易失去电子的物质B.能与酸反应的物质C.原子的最外层电子层只有1个电子的元素D.原子核内有11个质子的元素答案 D解析S2-、I-等也易失电子,A错误;碱也能与酸反应,B错误;H原子最外层也有一个电子,C错误;原子核内有11个质子的元素是钠,是金属元素,D正确。
知识点2 金属与非金属的反应4.镁、铝能够在空气中稳定存在的原因是( )A.性质不活泼,不与空气中的成分反应B.镁、铝与氧气的反应速率极慢C.经过了特殊工艺处理D.与氧气反应形成了氧化物保护膜答案 D解析活泼金属易与氧气反应生成氧化膜,氧化膜疏松的不能保护内层金属,致密的能保护内层金属。
Mg、Al都能形成致密的氧化膜,阻止内层金属继续被氧化。
5.下列说法正确的是( )A.将金属钠置于空气中加热产生白色的氧化钠B.铝箔不易被点燃是因为铝与空气中的氧气不反应C.铁在空气中点燃剧烈反应,火星四射D.钠与氧气反应,本身作还原剂答案 D解析钠在加热时生成淡黄色Na2O2;铝在常温下即能与O2反应;铁在氧气中点燃剧烈反应,火星四射,在空气中不燃烧。
知识点3 金属与酸、水的反应6.某学生将一小块钠投入滴有酚酞的水中,此实验能证明钠下面4点性质中的( )①钠的密度比水的小②钠的熔点较低③钠与水反应时放出热量④钠与水反应后溶液呈碱性A.①④ B.①②④ C.①③④ D.①②③④答案 D解析钠投入滴有酚酞的水中,钠浮在水面上,说明钠的密度比水小;钠熔成一个闪亮的小球,说明反应放热而且钠的熔点低;溶液变红,说明反应生成的溶液呈碱性,故D正确。
2017-2018学年高中化学 每日一题 金属在自然界中的存在与通性 新人教版必修1

金属在自然界中的存在与通性典例在线人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)地壳中含量最高的金属元素是________。
(2)根据金属的下列应用:①制电线,②制金属细丝,③制炊具,推断金属具有的物理性质是__________。
(3)人们每年要从金属矿物资源中提取大量的金属,根据所学化学知识,按要求写出两个生成金属的化学方程式:①___________________________________________________(置换反应);②___________________________________________________(分解反应)。
(3)①H2+CuO △Cu+H2O(或Fe+CuSO4===FeSO4+Cu)(合理即可,下同)②2HgO △2Hg+O↑解题必备一、金属在自然界中的存在1.自然界中绝大多数金属元素的存在形态是化合态。
2.地壳中含量占据前两位的金属元素是铝、铁。
二、金属的通性1.金属的物理通性2.金属的化学通性(1)金属化学性质特点(2)金属还原性的强弱取决于其失去电子的难易程度,而不是失去电子的个数。
学霸推荐1.下列关于金属性质的叙述正确的是A.金属一般都容易导电导热,有延展性B.金属具有较高的硬度和熔点C.所有金属都是固态D.金属单质都能与稀H2SO4反应产生H22.下列关于金属的通性说明不正确的是A.金属的熔点差别较大B.在自然界中没有游离态的钠C.金属单质在化学反应中既可作氧化剂又可作还原剂D.与酸反应越剧烈的金属活泼性越强3.下列推理正确的是A.铝粉在氧气中燃烧生成Al2O3,故铁丝在氧气中燃烧生成Fe2O3B.铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜C.活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中D.钠与氧气、水等反应时钠均作还原剂,故金属单质参与反应时金属均作还原剂参考答案1.【答案】A2.【答案】A【解析】金属在化学反应中只作还原剂。
高一化学必修一金属的化学性质_(修改)

银
铜
铝
铁
合金
第三章第一讲
金属的化学性质
★金属在自然界的分布和存在 ★绝大多数以化合态存在于自然界。
分布特征
一、金属的通性
除金、铂等少数极不活泼金属外,大多数金属元素在自然界 中以化合态存在; 自然界中最多铝,其次铁、钙、钠。
化合态:元素在化
合物中的存在形态
游离态:元素以单
质的形态存在
物理通性
溶液反应
反应
2Al+3CuSO4=Al2(SO4)3+3Cu
2Mg+O2=2MgO
Cu+2AgNO3=Cu(NO3)2+2Ag Mg+2HCl=MgCl2+H2
3、依据 Na、Mg、Al的原子结构示意图,分析它们的 原子结构有什么特点,与金属的化学性质有什么联系?
Na
Mg
Al
金属最外层上的电子一般少于4个,反应中很容易失去
性格: 活泼好动,团结合群。爱憎分明,一见到二 氧化碳,脸色立变,一落水就非常生气。
简历:曾在某潜艇当班长,后在立白化工厂当工人, 曾与氯气、二氧化硫等一起,光荣出席全国 漂白积极分子群英会。
愿望:有一所坚固密实的房子保养身体, 为人民再立新功。
小结:大多金属可以和氧气发生反应.
活泼的金属在空气中易与氧气反应,生 成一层氧化物。
打磨,除去表面的保护膜,再 加热至熔化。
现象
铝箔发红卷缩, 熔化 不滴落。
铝箔发红卷缩,很快就变暗 失去光泽,熔化不滴落。
现象解释
铝表面的氧化膜保护了铝。
构成薄膜的氧化铝(Al2O3) 的熔点(2050℃)高于铝
铝很活泼,除去原来的氧 化膜后,很快又会生成一
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
金属在自然界中的存在与通性
典例在线
人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)地壳中含量最高的金属元素是________。
(2)根据金属的下列应用:①制电线,②制金属细丝,③制炊具,推断金属具有的物理性质是
__________。
(3)人们每年要从金属矿物资源中提取大量的金属,根据所学化学知识,按要求写出两个生成
金属的化学方程式:
①___________________________________________________(置换反应);
②___________________________________________________(分解反应)。
解题必备
一、金属在自然界中的存在
1.自然界中绝大多数金属元素的存在形态是化合态。
2.地壳中含量占据前两位的金属元素是铝、铁。
二、金属的通性
1.金属的物理通性
2.金属的化学通性
(1)金属化学性质特点
(2)金属还原性的强弱取决于其失去电子的难易程度,而不是失去电子的个数。
学霸推荐
1.下列关于金属性质的叙述正确的是
A.金属一般都容易导电导热,有延展性
B.金属具有较高的硬度和熔点
C.所有金属都是固态
D.金属单质都能与稀H2SO4反应产生H2
2.下列关于金属的通性说明不正确的是
A.金属的熔点差别较大
B.在自然界中没有游离态的钠
C.金属单质在化学反应中既可作氧化剂又可作还原剂
D.与酸反应越剧烈的金属活泼性越强
3.下列推理正确的是
A.铝粉在氧气中燃烧生成Al2O3,故铁丝在氧气中燃烧生成Fe2O3
B.铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜
C.活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中
D.钠与氧气、水等反应时钠均作还原剂,故金属单质参与反应时金属均作还原剂
参考答案
1.【答案】A
2.【答案】A
【解析】金属在化学反应中只作还原剂。
3.【答案】D
【解析】A中铁丝在O2中燃烧生成Fe3O4不是Fe2O3,B中钠与CuSO4溶液反应不能置换出铜:2Na+CuSO4+2H2O===Cu(OH)2↓+Na2SO4+H2↑,C中铝在空气中形成致密的氧化膜,不必保存在煤油中。
