初中化学知识总结:图、表、线类试题
初中化学题型归纳总结

初中化学题型归纳总结 化学是初三才开始接触的,对于很多同学来说是⽐较难学的,为了帮助⼤家更好的学习化学,以下是店铺分享给⼤家的初中化学题型归纳,希望可以帮到你! 初中化学题型归纳 1.直选型选择题 例1 过氧化氢(H2O2,它的⽔溶液俗称双氧⽔)是常有的消毒剂,在实验室⾥可⽤它来制取氧⽓:2H2O2 MnO22H2O+O2↑,下列关于过氧化氢的叙述正确的是( ) A.每个过氧化氢分⼦由两个氢元素和两个氧元素构成 B.每个过氧化氢分⼦由⼀个氢分⼦和⼀个氧分⼦构成 C.由氢氧两种元素组成的化合的 D.由⼀个⽔分⼦和⼀个氧原⼦构成 审题与思路:由题给信息2H2O2MnO22H2O+O2↑可知,过氧化氢是⼀种具有⼀定组成结构的化合物,它的最⼩独⽴存在的粒⼦是分⼦,即它是由⼤量的过氧化氢分⼦构成。
故A、B、C是错误的说法。
总结:紧扣题⽬的已知条件(或信息)直接推论或计算出答案,从⽽做出选择。
真正做到平时总结,⽤时直接。
2.筛选型选择题 例2 分别将下列各组物质同时加到⽔中,得到⽆⾊透明溶液的是( ) A.CuSO4、HCl、KCl B.K2SO4、BaCl2、HCl C.Na2SO4、KCl、Na2CO3 D.FeCl3、KOH、NaCl 审题思路:此题根据筛选⽅法求解,思路较清楚,根据“⽆⾊”这⼀条可筛掉A。
因为含有Cu2+的溶液是蓝⾊;根据“透明溶液”这⼀条件可筛掉B和D,因为B中的K2SO4和BaCl2反应⽣成⽩⾊的BaSO4沉淀,D 中FeCl3和KOH反应⽣成红褐⾊的Fe(OH)3沉淀。
即只有C符合题意。
解答:选C 总结:根据题⽬所给的已知条件和提出的问题,对题⽬中给出的选项逐个进⾏甄别,可以做到去伪存真,排除不合题意的选项⽽得到正确的答案。
3.推断型选择题 例3 在等臂杠杆的两端分别挂着质量和体积都相同的铁球和铝球,这时杠杆平衡。
将两球分别浸泡在质量相同、溶质的质量分数也相同的稀硫酸中(如图所⽰),直⾄两个烧杯中均没有⽓泡产⽣为⽌。
初中化学最全知识点总结图

初中化学最全知识点总结图初中化学知识点总结图一、化学基本概念1. 物质的组成- 元素:物质的基本组成单位,不可分割。
- 化合物:由两种或两种以上元素以固定比例结合而成的纯净物质。
- 混合物:由两种或两种以上物质混合而成,各组成部分保持原有性质。
2. 物质的分类- 纯净物:具有固定成分和性质的物质。
- 混合物:由不同物质简单混合而成,没有固定成分和性质。
- 单质:由同种元素构成的纯净物。
- 氧化物:由氧元素和其他元素结合的化合物。
3. 化学反应- 反应物:参与化学反应的物质。
- 生成物:化学反应后生成的物质。
- 化学方程式:表示化学反应的式子,包括反应物和生成物的化学式以及反应条件。
二、化学实验基础1. 实验仪器- 试管、烧杯、量筒、滴定管、酒精灯、天平等。
2. 实验操作- 称量、量取、溶解、过滤、蒸发、结晶、蒸馏等。
3. 实验安全- 穿戴防护装备,如实验服、防护眼镜、手套。
- 了解化学品的性质和安全使用规则。
- 熟悉实验室紧急处理措施。
三、元素与化合物1. 常见元素- 金属元素:铁、铜、锌、钙等。
- 非金属元素:氢、氧、碳、氮等。
2. 常见化合物- 酸碱盐:硫酸、氢氧化钠、氯化钠等。
- 氧化物:水(H2O)、二氧化碳(CO2)等。
3. 元素周期表- 元素按照原子序数排列的表格。
- 包括元素名称、符号、相对原子质量等信息。
四、化学计算1. 摩尔概念- 物质的量,单位为摩尔(mol)。
- 1摩尔物质含有阿伏伽德罗常数(6.022×10^23)个粒子。
2. 质量守恒定律- 化学反应前后物质总质量不变。
3. 化学方程式计算- 根据化学方程式和已知物质的质量,计算反应物或生成物的质量。
五、溶液与溶解1. 溶液的组成- 溶质:被溶解的物质。
- 溶剂:溶解溶质的物质,常见的溶剂有水、酒精等。
2. 溶解度- 在一定温度下,某固体溶质在100克溶剂中的最大溶解量。
3. 溶液的性质- 浓度:溶液中溶质的质量分数或体积分数。
《易错题》人教版初中9年级化学第三章简答题专项知识点总结(专题培优)
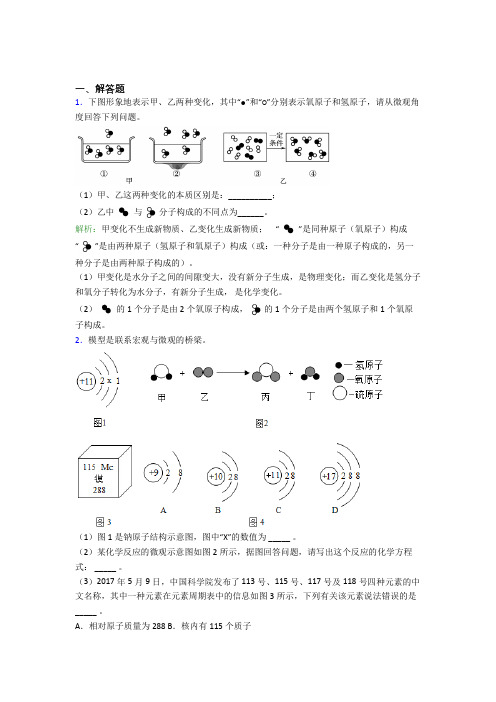
一、解答题1.下图形象地表示甲、乙两种变化,其中“●”和“○”分别表示氧原子和氢原子,请从微观角度回答下列问题。
(1)甲、乙这两种变化的本质区别是:__________;(2)乙中与分子构成的不同点为______。
解析:甲变化不生成新物质、乙变化生成新物质;“”是同种原子(氧原子)构成“”是由两种原子(氢原子和氧原子)构成(或:一种分子是由一种原子构成的,另一种分子是由两种原子构成的)。
(1)甲变化是水分子之间的间隙变大,没有新分子生成,是物理变化;而乙变化是氢分子和氧分子转化为水分子,有新分子生成,是化学变化。
(2)的1个分子是由2个氧原子构成,的1个分子是由两个氢原子和1个氧原子构成。
2.模型是联系宏观与微观的桥梁。
(1)图1是钠原子结构示意图,图中“X”的数值为 _____ 。
(2)某化学反应的微观示意图如图2所示,据图回答问题,请写出这个反应的化学方程式: _____ 。
(3)2017年5月9日,中国科学院发布了 113号、115号、117号及118号四种元素的中文名称,其中一种元素在元素周期表中的信息如图3所示,下列有关该元素说法错误的是_____ 。
A.相对原子质量为288 B.核内有115个质子C.是非金属元素 D.核内有173个中子(4)图4中ABCD四种粒子的结构示意图都具有 _____ 结构。
2H S+3O=2SO+2H O C 相对稳定(或最外层电子数相同)解析:2222【分析】(1)根据原子结构示意图的意义解答;(2)根据化学反应的微观示意图分析反应物、生成物写出反应的化学方程;(3)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析解答即可。
(4)根据最外层电子数都为8,属于稳定结构解答。
(1)原子结构示意图中质子数等于核外电子数,求得x=8;(2)由图2可知,反应物是H2S和O2,生成物是SO2和H2O,故反应方程式为:2H S+3O=2SO+2H O;2222(3)A、由图可知,相对原子质量为288,正确;B、核内质子数等于原子序数,故核内由115个质子,正确;C、由图可知,该元素为金属元素,错误;D、中子数=相对原子质量-质子数,288-115=173 ;正确。
人教版初中九年级化学上册第五单元《化学方程式》知识点总结(含答案解析)(1)
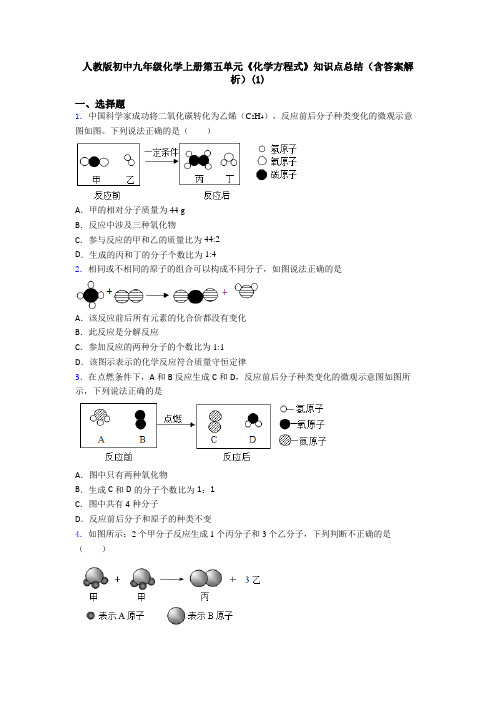
人教版初中九年级化学上册第五单元《化学方程式》知识点总结(含答案解析)(1)一、选择题1.中国科学家成功将二氧化碳转化为乙烯(C2H4),反应前后分子种类变化的微观示意图如图。
下列说法正确的是()A.甲的相对分子质量为44 gB.反应中涉及三种氧化物C.参与反应的甲和乙的质量比为44:2D.生成的丙和丁的分子个数比为1:42.相同或不相同的原子的组合可以构成不同分子,如图说法正确的是A.该反应前后所有元素的化合价都没有变化B.此反应是分解反应C.参加反应的两种分子的个数比为1:1D.该图示表示的化学反应符合质量守恒定律3.在点燃条件下,A和B反应生成C和D,反应前后分子种类变化的微观示意图如图所示,下列说法正确的是A.图中只有两种氧化物B.生成C和D的分子个数比为1:1C.图中共有4种分子D.反应前后分子和原子的种类不变4.如图所示:2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是()A .根据质量守恒定律可推知,1个乙分子中含有2个A 原子B .该反应前后一定有元素的化合价发生了改变C .该反应中甲、乙和丙的分子个数比是2:2:3D .该反应属于分解反应5.在一密闭容器中有A 、B 、C 、D 四种物质,一定条件下充分反应测得反应前后各物质的质量如表所示。
则下列说法中正确的是 物质 A B C D 反应前的质量/g 18 18 5 3 反应后的质量/g30待测9A .该反应一定是化合反应B .C 物质在该反应中一定是催化剂 C .反应后待测的C 物质的质量为0gD .参加反应的A 、B 、D 三种物质的质量比为3:2:16.当空气中受到 SO 2污染时,可通过飞机喷洒石灰石粉末,使空气中 SO 2含量降低,该过程发生反应为:32422CaCO +2SO +X=2CaSO +2CO ,则 X 的化学式为( ) A .CaO B .O 3C .O 2D .CO7.用和分别代表两种不同单质A 2和B 2的分子,A 2和B 2在一定条件下发生化学反应生成新物质X ,微观过程如下图所示。
初中化学流程题知识点总结含答案
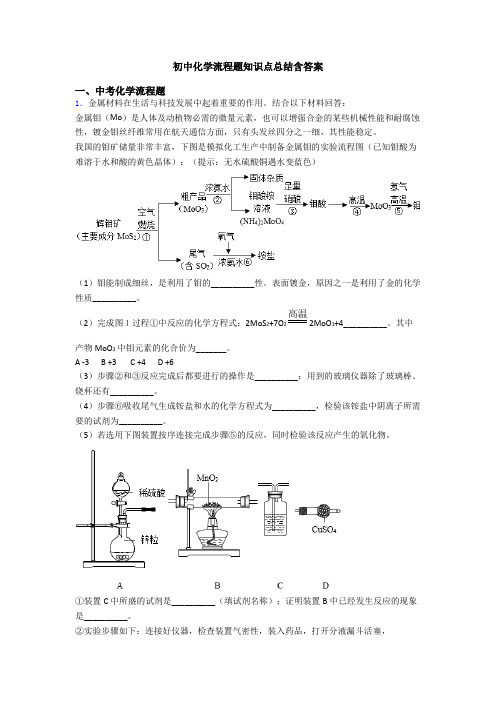
初中化学流程题知识点总结含答案一、中考化学流程题1.金属材料在生活与科技发展中起着重要的作用。
结合以下材料回答:金属钼(Mo)是人体及动植物必需的微量元素,也可以增强合金的某些机械性能和耐腐蚀性,镀金钼丝纤维常用在航天通信方面,只有头发丝四分之一细,其性能稳定。
我国的钼矿储量非常丰富,下图是模拟化工生产中制备金属钼的实验流程图(已知钼酸为难溶于水和酸的黄色晶体):(提示:无水硫酸铜遇水变蓝色)(1)钼能制成细丝,是利用了钼的__________性。
表面镀金,原因之一是利用了金的化学性质__________。
(2)完成图1过程①中反应的化学方程式:2MoS2+7O2高温2MoO3+4__________。
其中产物MoO3中钼元素的化合价为_______。
A -3B +3C +4D +6(3)步骤②和③反应完成后都要进行的操作是__________;用到的玻璃仪器除了玻璃棒、烧杯还有__________。
(4)步骤⑥吸收尾气生成铵盐和水的化学方程式为__________,检验该铵盐中阴离子所需要的试剂为__________。
(5)若选用下图装置按序连接完成步骤⑤的反应,同时检验该反应产生的氧化物。
①装置C中所盛的试剂是__________(填试剂名称);证明装置B中已经发生反应的现象是__________。
②实验步骤如下:连接好仪器,检查装置气密性,装入药品,打开分液漏斗活塞,_______→______→______→________。
(请按正确的先后顺序填入下列步骤的代号)a收集气体并检验其纯度 b停止加热,充分冷却c加热反应一段时间 d关闭分液漏斗活塞,停止通氢气2.某硫酸厂产生的烧渣(主要含 Fe2O3、FeO 及少量 SiO2)可用于制备FeSO4•7H2O和还原铁粉,其流程如图。
Ⅰ.写出“酸溶”中发生的任一反应的化学方程式___________。
Ⅱ.“滤渣”的主要成分是___________(填化学式)。
初中化学知识点总结(大全)

初中化学知识点总结一、基本概念:1、化学变化:生成了其它物质的变2、物理变化:没有生成其它物质的变化3、物理性质:不需要发生化学变化就表现出来的性质(如:颜色、状态、密度、气味、熔点、沸点、硬度、水溶性等)4、化学性质:物质在化学变化中表现出来的性质(如:可燃性、助燃性、氧化性、还原性、酸碱性、稳定性等)5、纯净物:由一种物质组成6、混合物:由两种或两种以上纯净物组成,各物质都保持原来的性质7、元素:具有相同核电荷数(即质子数)的一类原子的总称8、原子:是在化学变化中的最小粒子,在化学变化中不可再分9、分子:是保持物质化学性质的最小粒子,在化学变化中可以再分10、单质:由同种元素组成的纯净物11、化合物:由不同种元素组成的纯净物12、氧化物:由两种元素组成的化合物中,其中有一种元素是氧元素13、化学式:用元素符号来表示物质组成的式子14、相对原子质量:以一种碳原子的质量的1/12作为标准,其它原子的质量跟它比较所得的值某原子的相对原子质量=相对原子质量≈ 质子数 + 中子数 (因为原子的质量主要集中在原子核)15、相对分子质量:化学式中各原子的相对原子质量的总和16、离子:带有电荷的原子或原子团17、原子的结构:原子、离子的关系:注:在离子里,核电荷数 = 质子数≠ 核外电子数18、四种化学反应基本类型:(见文末具体总结)①化合反应:由两种或两种以上物质生成一种物质的反应如:A + B = AB②分解反应:由一种物质生成两种或两种以上其它物质的反应如:AB = A + B③置换反应:由一种单质和一种化合物起反应,生成另一种单质和另一种化合物的反应如:A + BC = AC + B④复分解反应:由两种化合物相互交换成分,生成另外两种化合物的反应如:AB + CD = AD + CB19、还原反应:在反应中,含氧化合物的氧被夺去的反应(不属于化学的基本反应类型)氧化反应:物质跟氧发生的化学反应(不属于化学的基本反应类型)缓慢氧化:进行得很慢的,甚至不容易察觉的氧化反应自燃:由缓慢氧化而引起的自发燃烧20、催化剂:在化学变化里能改变其它物质的化学反应速率,而本身的质量和化学性在化学变化前后都没有变化的物质(注:2H2O2 === 2H2O + O2 ↑ 此反应MnO2是催化剂)21、质量守恒定律:参加化学反应的各物质的质量总和,等于反应后生成物质的质量总和。
安徽宣城市人教版初中9年级化学第三章简答题专项知识点总结(含答案解析)

一、解答题1.下图①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
(1)氟元素的相对原子质量为____________,钙元素的原子序数为____________;(2)A、B、C、D属于同种元素的粒子是____________(填序号);(3)B粒子的化学性质与A、C、D中化学性质相似的是____________(填序号)。
解析:00 20 BC A【解析】本题考查了元素周期表的应用,原子结构示意图与离子结构示意图的运用。
(1)根据氟元素和钙元素在元素周期表中信息可知,氟的相对原子质量是19.00,钙元素的原子序数为20;(2)质子数相同的粒子属于同一种元素,由图可知BC两种粒子的质子数相同;(3)最外层电子数相同的粒子具有相似的化学性质,B粒子的最外层电子数为7,与其相同的是A。
2.浓氨水有一股难闻的刺激性气味,在老师指导下,同学们对原实验装置进行了改进,改进后的装置如图所示,回答下面问题。
(1)实验中观察到B、C试管内的溶液都变成红色,但C试管内液体变色速率较快,由此实验现象得出的结论是①___②___。
(2)E所起的作用是___。
解析:氨分子不断运动温度越高,氨分子运动越快对比实验(1)BC中的酚酞变为红色,说明AD中的氨气分子运动到了BC 中使酚酞变红,故说明分子做无规则的运动。
C中的酚酞比B中的酚酞变红较快,说明D中的氨气分子运动速率较快,故可得温度越高,氨分子运动越快。
(2)装置E是为了和装置BC对比。
3.如表是元素周期表中第1、2、3周期的元素,请回答有关问题(1)下列各组具有相似化学性质的元素是______(填字母序号)。
A O、SB Na、ClC F、ClD C1、Ar(2)写出一条第三周期元素原子的核外电子排布规律______。
(3)第7号元素与第12号元素的原子形成化合物的化学式为______。
Mg N解析:AC 从左往右,原子的最外层电子数依次增多32(1)下列各组具有相似化学性质的元素是AC,这是因为它们的最外层电子数相等;(2)第三周期元素原子的核外电子排布规律:从左往右,原子的最外层电子数依次增多;(3)第7号元素(氮元素)与第12号元素(镁元素)的原子形成化合物是氮化镁,氮化镁中镁元素化合价是+2,氮元素化合价是-3,根据化合物中元素化合价代数和为零可知,氮化镁化学式是Mg2N3。
2023-2024第一学期初中化学优秀试卷分析

2023-2024学年第一学期期末调研考试九年级化学试卷分析一、试卷分析本次期末试卷的命题是以《义务教育化学课程标准》为依据,重点考查学生化学基础知识和基本技能、基本方法,运用化学知识解决简单实际问题的能力等。
本次期末试卷覆盖面广,考试范围为初中化学教材一到八单元内容,题型没多大变化,共分四个大题,31道小题。
各个章节知识点分值情况统计如下:通过以上表格的统计,整体来看试卷结构合理,几乎能覆盖所有知识点,试题题量适中,难易适中,分值分配合理,符合《义务教育化学课程标准》规定的内容和要求,体现新课程理念。
具体特点分析如下:(一)注重双基考查基础知识和基本技能是学好化学的重要基础,也是激发兴趣,稳定兴趣,提高兴趣的根本。
本套试卷考查了物质的组成、结构、性质、变化、分类、用途、化学实验基本操作、简单的化学计算、书写化学式和化学方程式、气体制取的研究、能源利用与环境保护、金属材料等基础知识,面向全体学生,努力使不同层面的学生都展示自己的水平。
(二)注重能力考查本套试题在注重双基考查的基础上,又考查了学生阅读信息的能力、用化学知识解决问题的能力、知识迁移应用能力。
例如选择题第6、20题就是考查学生图文识别提取信息的能力。
填空题第25题的第(3)小题根据给出的反应物、生成物、反应所需条件来写未见过的化学方程式,这就是对学生灵活运用知识能力的考查。
第30题实验探究题考查了学生的支持迁移应用的能力、分析解决问题的能力等。
这些题目的设计体现了初中化学课程新理念,对核心素质教育的推进具有导向作用。
二、学生答题情况及成绩分析(一)学生成绩分析本学年我担任九年级7、8、12班3个班的化学教学,本次成绩如下表:表1 平均分、及格率、优秀率表2 总分分数段人数通过以上统计的数据来看,优秀生人数较少,低分学生较多,两级分化十分严重,学生的整体成绩堪忧。
(二)学生答题情况分析1.选择题选择题共20道小题,每题2分,总计40分。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
图、表、线类试题
一、坐标图像题
1.特点
坐标图像题的特点是借助于数学方法中的坐标图,把多个因素对体系变化的影响,用坐标图的形式直观地表示出来,考查学生看图、识图、发掘图形的隐含性质和相互联系的能力。
2.类型
坐标图像题的内容包括化学反应前后物质质量的变化、物质溶解时溶液的质量或溶质质量分数的变化、溶液的pH的变化等。
3.解题策略
(1)抓住图像特征认真分析坐标中纵、横坐标所表示的含义,图像的起始点、转折点、变化趋势、终点等。
(2)正确读取所需的数据或信息,弄清图像题中与曲线或直线变化的有关量的关系。
(3)认真解读题意,应用信息解答问题。
二、表格数据题
1.特点
表格数据分析题就是将物质的某组数据以表格的形式呈现。
根据表格中数据提供的信息对数据进行分析处理,从而解决问题的题型。
2.类型
主要包括给出化学反应前后的物质质量的表格数据,判断化学反应类型;根据多种物质的pH,判断溶液的酸碱性的强弱等;几种物质反应时,给出多次或多组物质的质量,依据化学方程式进行计算等。
3.解题策略
(1)正确解读表格中的数据或条件,审题时挖掘出数字中隐藏的规律,再依据规律排序,从而解决问题。
(2)若是多次或多组数据或条件,则需要通过比较、对比的方法,在比较中确定解题所需的有用信息,寻找出系列数据中的特殊数据,分析特殊数据的特点,从特点着手设计解题方案。
三、商标信息题
1.特点及类型
(1)利用标签中的信息(如化肥、农药、食品、药品或其他一些化学试剂),考查物质的组成和分类。
(2)利用标签中的信息考查物质的性质。
(3)利用标签中的信息考查化学实验中的危险品的安全标志。
(4)利用标签中的信息考查有关化学式的基本计算。
2.解题策略
(1)正确解读商标信息。
根据题意,从标签中找到解决问题的依据。
(2)记住常见商标中的图标及表示的意义。
四、溶解度曲线题
1.特点及类型
(1)给出某物质在不同温度时的溶解度,画出该物质的溶解度曲线。
(2)查出某物质在不同温度下的溶解度数值,并计算相应的溶质质量分数。
(3)比较不同物质在同一温度时的溶解度大小。
(4)确定物质溶解度受温度变化影响的大小。
(5)确定饱和溶液与不饱和溶液相互转化的措施。
(6)确定可溶性混合物分离的方法。
2.解题策略
(1)弄清楚溶解度曲线上的点、曲线的交叉点、曲线的变化趋势及涉及的“点”的位置的意义并分析“点”的变化趋势,如果“点”左右移动与温度有关,如果竖直上、下移动,则是恒温加减溶剂或加减溶质。
(2)根据溶解度曲线的变化趋势,可以确定该物质从溶液中获取时选择的适合方法。
如NaCl的溶解度受温度变化影响很小,可以采取蒸发溶剂的方法获取氯化钠晶体;而KNO3的溶解度随温度升高明显增大,因此,可采用冷却热饱和溶液的方法获取晶体。
