(完整版)初三化学习题精选(溶液的浓度)习题与答案
初三化学溶液的浓度单元测试题附答案(1)

初三化学溶液的浓度单元测试题附答案一、初中化学溶液的浓度选择题1.图是A、B、C三种物质的溶解度曲线,当等质量的A、B、C三种物质的饱和溶液同时从t=2℃降温到t=1℃时,其中溶质质量分数没有发生改变的是A.AB.BC.CD.AB【来源】2013届湖北省襄阳市襄州区中考适应性考试化学试题(带解析)2.氯化钠和硝酸钾两种固体的溶解度曲线如右图所示。
下列说法正确的是A.硝酸钾的溶解度大于氯化钠的溶解度B.常用冷却结晶的方法从氯化钠溶液中获得其晶体C.40℃时,将35 g硝酸钾晶体放入50 g水中,充分搅拌后,所得溶液的溶质质量分数为39.0%D.将20℃的硝酸钾饱和溶液升温至60℃,溶液的溶质质量分数增大(忽略水分蒸发)【来源】2017年初中毕业升学考试(江苏苏州卷)化学(带解析)3.甲、乙两种固体物质的溶解度曲线如图所示。
下列说法正确的是A.20 ℃时,甲溶液中溶质的质量分数一定比乙溶液的大B.将40 ℃时甲的一定量饱和溶液降温至20 ℃,溶液质量不变C.甲的溶解度大于乙的溶解度D.40 ℃时,分别在100 g水中各加入30 g甲、乙,同时降温至20 ℃,甲、乙溶液均为饱和溶液【来源】2017年初中毕业升学考试(山东临沂卷)化学(带解析)4.根据下表信息,相关说法正确的是()溶解度/g温度/℃NaCl KCl NH4Cl KNO32036.034.037.231.64036.640.045.863.96037.345.555.2110A.20℃时,NaCl 的溶液度为 36.0B.40℃时,KCl 饱和溶液的溶质质量分数为 40%C.40℃时,向 100g 水中加入 50gNH4Cl 充分溶解,溶液质量为 145.8gD.60℃时降温到 20℃时,KNO3和 KCl 的饱和溶液析出晶体较多的是 KNO3【来源】2017年初中毕业升学考试(四川成都卷)化学(带解析)5.甲、乙两种物质的溶解度曲线如图1所示。
初三化学溶液的浓度过关测试含答案解析
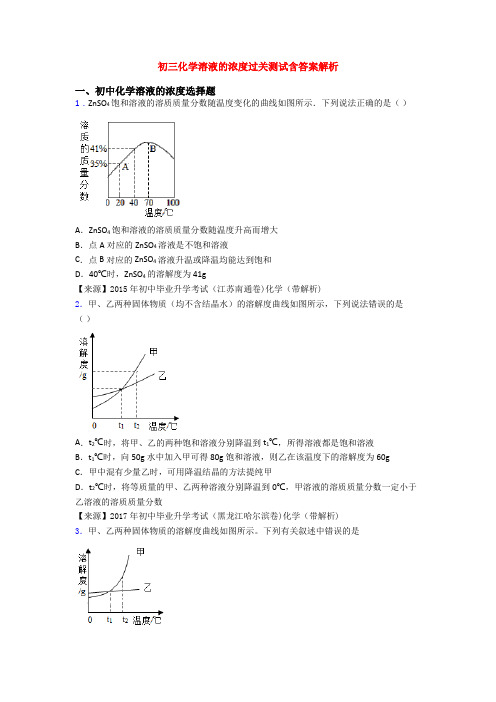
初三化学溶液的浓度过关测试含答案解析一、初中化学溶液的浓度选择题1.ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是()A.ZnSO4饱和溶液的溶质质量分数随温度升高而增大B.点A对应的ZnSO4溶液是不饱和溶液C.点B对应的ZnSO4溶液升温或降温均能达到饱和D.40℃时,ZnSO4的溶解度为41g【来源】2015年初中毕业升学考试(江苏南通卷)化学(带解析)2.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是()A.t2℃时,将甲、乙的两种饱和溶液分别降温到t1℃,所得溶液都是饱和溶液B.t1℃时,向50g水中加入甲可得80g饱和溶液,则乙在该温度下的溶解度为60g C.甲中混有少量乙时,可用降温结晶的方法提纯甲D.t2℃时,将等质量的甲、乙两种溶液分别降温到0℃,甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数【来源】2017年初中毕业升学考试(黑龙江哈尔滨卷)化学(带解析)3.甲、乙两种固体物质的溶解度曲线如图所示。
下列有关叙述中错误的是A.t2℃时甲的溶解度比乙的大B.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大C.升高温度可将甲的饱和溶液变成不饱和溶液D.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等【来源】2013-2014江苏省南京市鼓楼区中考一模化学试卷(带解析)4.20℃时,往100g硝酸钾溶液中加入20g硝酸钾,充分搅拌,硝酸钾部分溶解。
下列说法正确的是A.硝酸钾的溶解度变大B.溶质的质量分数保持不变C.所得溶液是饱和溶液D.所的溶液的质量为120g【来源】2014年初中毕业升学考试(福建莆田卷)化学(带解析)5.下图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法不正确的是A.10℃时,甲、乙两种物质的饱和溶液浓度相同B.保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液C.30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80gD.10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大【来源】2015年初中毕业升学考试(重庆B卷)化学(带解析)6.右图是a、b、c 三种物质的溶解度曲线,下列分析不正确的是A.t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>cB.t2℃时,将50ga物质放入100g水中充分溶解恰好得到a的饱和溶液(a物质不含结晶水) C.将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系b >c=aD.将c的饱和溶液变为不饱和溶液,可采用降温的方法【来源】[首发]山东省枣庄市薛城区2017届九年级中考模拟(5月)化学试题7.已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g.序号①②③④⑤固体种类NaCl NaCl NaNO3NaNO3NaNO3固体的质量/g3060306090水的质量/g100100100100100下列关于①-⑤实验操作所得溶液说法不正确的是A.溶质质量:①<②B.溶液质量:②<④C.溶质质量分数:①=③D.⑤中溶液质量:190g【来源】【市级联考】山东省齐河市2019届九年级下学期第一次练兵考试化学试题8.T1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后观象如图一所示。
中考化学复习---溶液的浓度计算题练习题(含答案解析)

中考化学复习---溶液的浓度计算题练习题(含答案解析)1、(2020•柳州)新冠肺炎疫情期间,可用体积分数为75%的乙醇(C2H5OH)消毒液进行手和其他皮肤的消毒。
如图为某品牌乙醇消毒液的标签。
(纯乙醇的密度约为0.8g/mL,水的密度约为1.0g/mL)。
请回答下列问题:(1)H2O的相对分子质量为18 ,H2O分子中H原子与O原子的个数比为2:1 。
(2)乙醇由C、H、O 元素组成,配制乙醇消毒液需要乙醇和水的体积比为3:1 。
(3)乙醇消毒液中乙醇的质量分数约为多少?(要求写出计算过程,结果精确到0.1%)【解答】解:(1)H2O的相对分子质量为:1×2+16=18,H2O分子中H原子与O原子的个数比为2:1;故填:18;2:1;(2)乙醇由C、H、O三种元素组成,配制乙醇消毒液需要乙醇和水的体积比为75:25=3:1;故填:C、H、O;3:1;(3)将75mL乙醇与25mL水混合,则消毒液中,乙醇的质量为:75mL×0.8g/mL=60g消毒液中,乙醇的质量分数为:≈70.6%答:乙醇消毒液中乙醇的质量分数约为70.6%。
2、(2020•枣庄)人体所需的维生素C(化学式为C6H8O6)主要从蔬菜、水果中摄取,计算:(1)维生素C中碳、氢、氧三种元素质量的最简整数比为9:1:12 。
(2)现有溶质质量分数为1%的维生素C的溶液300g,若配制成溶质质量分数为0.3%的维生素C的溶液,问需要加水的质量是多少。
(写出计算过程)【解答】解:(1)维生素C中,C、H、O三种元素的质量比为(12×6):(1×8):(16×6)=9:1:12,故填:9:1:12;(2)设需要加水的质量是x,根据题意可得:300g×1%=(300+x)×0.3%解得:x=700g。
答:需要加水的质量是700g。
3、(2020•海南)为了做好疫情防控,公共场所可用0.5%的过氧乙酸(化学式为C2H4O3)溶液来消毒。
中考化学溶液的浓度练习题附答案

中考化学溶液的浓度练习题附答案一、初中化学溶液的浓度选择题1.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是A.t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>cB.P点表示t1℃时,a、c两种物质的溶解度相等C.将c的饱和溶液变为不饱和溶液,可采用降温的方法D.t2℃时,将30g a物质加入到50g水中充分搅拌,得到80g a的饱和溶液【来源】2015年初中毕业升学考试(湖北孝感卷)化学(带解析)2.氯化钠和硝酸钾两种固体的溶解度曲线如右图所示。
下列说法正确的是A.硝酸钾的溶解度大于氯化钠的溶解度B.常用冷却结晶的方法从氯化钠溶液中获得其晶体C.40℃时,将35 g硝酸钾晶体放入50 g水中,充分搅拌后,所得溶液的溶质质量分数为39.0%D.将20℃的硝酸钾饱和溶液升温至60℃,溶液的溶质质量分数增大(忽略水分蒸发)【来源】2017年初中毕业升学考试(江苏苏州卷)化学(带解析)3.氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( )A.50℃时,氯化铵的溶解度大于硝酸钾B.a℃时,氯化铵与硝酸钾溶液的质量分数相等C.将60℃的硝酸钾饱和溶液降温会变为不饱和溶液D.40℃时,50g水中加入50g硝酸钾,充分搅拌,得到质量分数约为39%的硝酸钾溶液【来源】2015届山东省枣庄市薛城舜耕中学九年级学业水平模拟化学试卷(带解析) 4.下图是A、B、C三种物质的溶解度曲线,下列分析不正确的是()A.50℃时,A、B、C三种物质的溶解度由大到小的顺序是A>B>CB.50℃时,把50 g A放入50 g水中能得到A的饱和溶液,其中溶质与溶液质量比为1∶3 C.将50℃时,A、B、C三种物质的饱和溶液降温度20℃时,这三种溶液的溶质质量分数的大小关系是B>C=AD.将C的饱和溶液变为不饱和溶液,可采用降温的方法【来源】2013届北京市海淀区中考一模化学试卷(带解析)5.T1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后观象如图一所示。
初三化学溶液的浓度复习题及答案

初三化学溶液的浓度复习题及答案一、选择题1.下列关于溶液的说法中,正确的是 ( )A.饱和溶液一定是浓溶液B.溶液一定是无色透明的C.溶液一定是均一稳定的D.溶液中的溶剂只能为水【来源】吉林省长春市农安县东北学区三校2018届九年级下学期第一次月考化学试题答案:C【解析】A、饱和溶液不一定是浓溶液,错误;B、溶液不一定是无色的,比如硫酸铜溶液是蓝色的,错误;C、溶液一定是均一稳定的,正确;D、溶液中的溶解可能是水,也可能是其他的溶剂,错误。
故选C解析:C【解析】A、饱和溶液不一定是浓溶液,错误;B、溶液不一定是无色的,比如硫酸铜溶液是蓝色的,错误;C、溶液一定是均一稳定的,正确;D、溶液中的溶解可能是水,也可能是其他的溶剂,错误。
故选C。
【点睛】饱和溶液与不饱和溶液反映的是溶质能否继续溶解,浓溶液与稀溶液反映的是溶质的质量分数。
2.T1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后观象如图一所示。
硝酸钾和氯化钾的溶解变曲线如图二所示。
下列说法错误的是A.烧杯乙中上层清液是饱和溶液B.烧杯甲中溶解的溶质是氯化钾C.烧杯甲溶液中溶质的质量分数大于烧杯乙溶液中溶质的质量分数D.将温度由T1℃升高到T2℃,充分搅拌,烧杯乙中固体不一定全部溶解【来源】湖北省黄石市2018年中考理综化学部分试题答案:D【解析】根据所学知识和题中信息知,A、烧杯乙中上层清液一定是饱和溶液,有未溶解晶体,故A正确;B、烧杯甲中溶解的溶质是氯化钾,T1℃时氯化钾溶解度大于硝酸钾,故B正确;C、烧杯甲溶液中溶质的质解析:D【解析】根据所学知识和题中信息知,A、烧杯乙中上层清液一定是饱和溶液,有未溶解晶体,故A 正确;B、烧杯甲中溶解的溶质是氯化钾,T1℃时氯化钾溶解度大于硝酸钾,故B正确;C、烧杯甲溶液中溶质的质量分数大于烧杯乙溶液中溶质的质量分数,由于等质量的硝酸钾和氯化钾分别加入到100g水中,甲中全部溶解,乙中部分溶解,故C正确;D、将温度由T1℃升高到T2℃,充分搅拌,烧杯乙中固体一定全部容解,硝酸钾溶解度随温度的升高而增大,由于等质量的硝酸钾和氯化钾分别加入到100g水中,T1℃时氯化钾溶解度大于硝酸钾,氯化钾已全部溶解,T2℃时硝酸钾溶解度大于氯化钾,硝酸钾也一定会全部溶解,故D错误点睛∶溶解度曲线的意义①表示同一种物质在不同温度时的溶解度或溶解度随温度变化的情况;②表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的大小。
化学溶液浓度练习题

化学溶液浓度练习题一、浓度计算题1. 已知一溶液中含有30克NaCl溶解于250毫升水中,求该溶液的质量浓度。
解析:质量浓度(C)= 质量(m)/ 体积(V)质量(m)= 30克体积(V)= 250毫升 = 0.25升C = 30克 / 0.25升 = 120克/升2. 在500毫升溶液中,含有35克CuSO4,请计算该溶液的质量浓度。
解析:质量浓度(C)= 质量(m)/ 体积(V)质量(m)= 35克体积(V)= 500毫升 = 0.5升C = 35克 / 0.5升 = 70克/升3. 已知某溶液中含有2.5摩尔的HCl,体积为750毫升,请计算该溶液的摩尔浓度。
解析:摩尔浓度(C)= 摩尔数(n)/ 体积(V)摩尔数(n)= 2.5摩尔体积(V)= 750毫升 = 0.75升C = 2.5摩尔 / 0.75升 = 3.33摩尔/升二、溶解度计算题1. 已知CaCO3在25°C时的溶解度为0.1摩尔/升,问向100毫升水中加入多少克CaCO3可以形成饱和溶液?解析:饱和溶解度(C)= 摩尔数(n)/ 体积(V)饱和溶解度(C)= 0.1摩尔/升 = 0.1摩尔/1000毫升摩尔数(n)= 饱和溶解度(C) ×体积(V)= 0.1摩尔/1000毫升 × 100毫升= 0.01摩尔摩尔质量(M)= 相对分子质量(molecular weight)= 100.09克/摩尔质量(m)= 摩尔数(n) ×相对分子质量(M)= 0.01摩尔 × 100.09克/摩尔= 1克2. 已知某溶液中AgCl的溶解度为1.6×10^-3摩尔/升,问向200毫升水中加入多少克AgCl可以形成饱和溶液?解析:饱和溶解度(C)= 摩尔数(n)/ 体积(V)饱和溶解度(C)= 1.6×10^-3摩尔/升 = 1.6×10^-3摩尔/1000毫升摩尔数(n)= 饱和溶解度(C) ×体积(V)= 1.6×10^-3摩尔/1000毫升 × 200毫升= 3.2×10^-4摩尔摩尔质量(M)= 相对分子质量(molecular weight)= 143.32克/摩尔质量(m)= 摩尔数(n) ×相对分子质量(M)= 3.2×10^-4摩尔 × 143.32克/摩尔= 0.045克三、稀释计算题1. 已知一溶液的质量浓度为2克/升,现需要制备250毫升0.4克/升的溶液,问需要取多少毫升原溶液,并加入多少毫升纯水?解析:C1V1 = C2V2C1 = 2克/升 = 2克/1000毫升C2 = 0.4克/升 = 0.4克/1000毫升V1 = ?V2 = 250毫升C1V1 = C2V22克/1000毫升 × V1 = 0.4克/1000毫升 × 250毫升V1 = (0.4克/1000毫升 × 250毫升)/(2克/1000毫升)= (0.4克 × 250毫升) / 2克= 50毫升纯水的体积 = V2 - V1= 250毫升 - 50毫升= 200毫升取50毫升原溶液并加入200毫升纯水,可制备得到250毫升0.4克/升的溶液。
九年级下册化学《溶液的浓度》练习题(含答案及解析)

《溶液的浓度》练习题一、单选题(本大题共13小题,共26.0分)1.用60%的酒精溶液a和25%的酒精溶液b配制成45%的酒精溶液,所用a、b溶液的质量比为()A. 1:2B. 4:3C. 2:3D. 3:12.如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线。
根据图中信息判断,下列说法不正确的是()A. t1℃时,三种物质的溶解度的大小关系是Y=Z>XB. t3℃时,溶质质量分数为25%的X溶液属于不饱和溶液C. X中含有少量Y,采用冷却热饱和溶液结晶法提纯XD. t3℃时,等质量X、Y、Z的饱和溶液分别降温到t2℃,所得溶液中溶质质量分数大小关系是Y>X=Z3.甲、乙的溶解度曲线如图所示(不考虑水的变化)。
下列说法正确的是()A. 依据溶解度曲线可判断,甲的溶解度比乙的大B. t2℃时,甲的饱和溶液中溶质质量分数为40%C. 当甲中含有少量的乙时,可用蒸发结晶法提纯甲D. t1℃时,将甲、乙的饱和溶液分别升温到t2℃,两溶液中溶质质量分数相等4.如图是A、B、C三种物质的溶解度曲线,下列分析不正确的是()A. 50℃时,A、B、C三种物质的溶解度由大到小的顺序是A>B>CB. 50℃时,把50g A放入50g水中能得到A的饱和溶液,其中溶质与溶液质量比为1:3C. 将50℃时,A、B、C三种物质的饱和溶液降温度20℃时,这三种溶液的溶质质量分数的大小关系是B>A>CD. 将C的饱和溶液变为不饱和溶液,可采用升高温度的方法5.如图是A、B、C三种物质的溶解度曲线图,下列有关说法正确的是()A. A的溶解度最大B. t1℃时A、C的溶液质量相等C. t1℃时B的饱和溶液中溶质质量分数是40%D. 用升温结晶的方法从A与C的混合物中提纯C6.如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
下列说法正确的是()A. 三种物质的溶解度大小关系为甲>乙>丙B. t2℃时,将20g甲加入50g水中,得到70g溶液C. t3℃时,用等质量的甲、乙、丙固体配成饱和溶液,需要水的质量大小关系是乙>甲>丙D. 将t2℃的三种物质的饱和溶液分别降温到t1℃,所得溶液的溶质质量分数大小关系为乙>丙>甲7.溶液与人们的生产生活密切相关,其中溶解度是定量表示物质溶解性的一种方法。
初三化学习题精选(溶液的浓度)习题与答案

初三化学习题精选(溶液的浓度)习题与答案1、一定量溶液中溶质的含量称为浓度。
2、往100 g 20%的食盐溶液中加入100 g水后,溶液的质量不变。
3、一定温度下,某饱和溶液溶质的质量分数为A%,溶解度是S g/100g水,则A>S。
4、矿泉水属于溶液。
5、取水样后先进行过滤的目的是除去水样中的难溶性固体物质。
6、正确的说法是:在t℃时,90 g水中溶解10 g氯酸钾时达到饱和,所以氯酸钾在t℃时的溶解度是10 g/100 g水。
7、可乐等饮料中溶解有一定的二氧化碳,打开瓶盖会冒出许多气泡。
产生这一现象的原因是压力减小,导致二氧化碳的溶解度变小。
当气泡逸出后,瓶内的液体不是二氧化碳的饱和溶液。
8、40℃时,A物质的溶液中溶质质量分数为40%,B物质溶液的质量分数为20%,将两种溶液在温度不变的情况下蒸发等质量的溶剂,析出的晶体的质量无法确定。
9、使100 g 15%的NaNO3溶液浓度增大一倍可采用的方法是蒸发掉42.5 g水。
10、在一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原来温度后,溶液的pH值会升高。
1.在一定温度下,搅拌可以增加物质的溶解度,但不会改变溶液的浓度或溶质质量。
2.XXX的判断是正确的,因为溶液中溶质的质量增加了,但浓度和溶解度没有改变。
3.溶质的质量分数表示溶液中溶质的质量与溶液总质量的比值,通常用百分数表示。
4.加入8克食盐可以使NaCl的质量分数增加一倍,或者蒸发掉20克水也可以达到相同的效果。
5.答案是B,饱和溶液中NaCl的质量分数为26.5%,加入5克食盐后,溶液中NaCl的质量为31.5克,总质量为105克,质量分数为30%。
6.答案是B,稀释后溶液中NaOH的质量为4克,质量分数为20%,取出20克溶液中NaOH的质量为0.8克,加入NaCl后总质量为26克,NaCl的质量分数为6.15%。
7.加入300克水可以将溶液稀释成10%的浓度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初三化学习题精选(溶液的浓度)1、一定量的溶液里所含溶质的量叫做溶液的_______。
A. 浓度B. 密度C. 溶解度D. 溶解性2、往100 g 20%的食盐溶液中加入100 g水,则稀释前后________。
A. 溶剂的质量不变B. 溶液的质量不变C. 溶质的质量不变D. 溶液中溶质的质量分数不变3、一定温度下,某饱和溶液溶质的质量分数是A%,溶解度是S g/100g水。
从数值上看,A与S的关系是A____S(填“>”、“=”或“<”=。
4、矿泉水和蒸馏水在外观上都是无色、透明的,但矿泉水中含有对人体有益的矿物质。
按分散体系分类,矿泉水属于_______。
A. 悬浊液 B. 溶液 C. 纯净物 D. 化合物5、某研究小组对本地区河流的水质情况进行调查,取水样后先进行过滤,其目的是___。
A. 除去水样中的其它物质B. 除去水样中的难溶性固体物质C. 使水样变为纯净水D. 对水样进行消毒处理6、下列说法中正确的是_______。
A. 在t℃时,90 g水中溶解10 g氯酸钾时达到饱和,所以氯酸钾在t℃时的溶解度是10 g/100 g水B. 硝酸钾在60℃的溶解度是110 g/100g水,110 g硝酸钾溶解在90 g水里,可得到60℃的硝酸钾饱和溶液200 gC. 在100 g水里最多溶解A物质36 g,则A物质的溶解度是36 g/100g水D. 在10℃时,50 g水里溶解10.5 g硝酸钾就不能再溶解,则硝酸钾在10℃时的溶解度是21 g/100 g水7、可乐等饮料中溶解有一定的二氧化碳,打开瓶盖会冒出许多气泡。
产生这一现象的原因是____________,导致二氧化碳的溶解度变__ ____。
当气泡逸出后,瓶内的液体_____(填“是”或“不是”)二氧化碳的饱和溶液。
8、40℃时,A物质的溶液中溶质质量分数为40%,B物质溶液的质量分数为20%,将两种溶液在温度不变的情况下蒸发等质量的溶剂,析出的晶体的质量________。
A. A>BB. A<BC. A=BD. 无法确定9、有100 g 15%的NaNO3溶液,使其浓度增大一倍,可采用的方法是________。
A. 蒸发掉42.5 g水B. 蒸发掉50 g溶剂C. 加入15 g NaNO3D. 升高温度10、在一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原来温度。
下列说法中正确的是________。
A. 溶液浓度不变 B. 溶质质量增加 C. 溶剂质量不变 D. 溶解度变大11、“在一定温度时,搅拌不仅可以加速物质溶解,还可以增大物质的溶解度。
”判断这种说法是否正确,为什么?12、30℃时,老师在100 g饱和食盐水中加入8 g食盐,然后将其充分搅拌。
小敏认为溶液的质量增加了;小凤认为溶液的浓度增大了;小霞认为溶液中的溶质质量发生了改变;小娟认为溶液中溶质的溶解度发生了改变;她们的判断________。
一、填空题1.溶质的质量分数表示_______________________________。
2.现有100克质量分数为10%的食盐溶液,若使NaCl的质量分数增加一倍,应向此溶液中加入食盐_____克,或使溶液蒸发掉水_____克。
二、选择题1.在一定温度时,某溶质的溶解度为S克,则该温度时饱和溶液中溶质的质量分数()A 大于S%B 等于S%C 小于S%D 无法判断2.在20℃时,向100克饱和食盐水(食盐的质量分数是26.5%)中加入5克食盐,在温度不变的情况下溶液中食盐的质量分数为() A 24.5% B 26.5% C 28.5% D 无法计算3.把30克质量分数为20%的氢氧化钠溶液,加水稀释到100克,取出稀释后溶液20克,此溶液中NaCl的质量分数为() A 5% B 6% C 3% D 2%4.把400克质量分数为20%食盐水稀释成质量分数为10%的溶液,需加水()A 100克B 200克C 400克D 800克5.20℃时NaCl在水中的溶解度是36g。
在该温度下,50g水中放入20gNaCl,溶解后所得溶液中NaCl的质量分数为() A 28.6% B 26.5% C 40% D 30%6.将溶质的质量分数为a%的溶液mg,稀释成溶质的质量分数为b%的溶液,需加水的质量为()A am/b gB m(a-b)/b gC a/mb gD (a-b)/m g7.有xg20%A溶液,若要将浓度降到10%,应采取的措施是()A 加入一倍的溶剂B 加入的溶剂C 加入2xg5%A溶液D 加入xg20%A溶液9.20℃NaCl的溶解度是36g,在该温度下,将20gNaCl溶于100g水中配成溶液甲,取20g甲溶液,加入6gNaCl 晶体,得到乙溶液,则甲、乙两溶液的溶质质量分数正确的一组是()A 甲—16.7% 乙—35.9%B 甲—20% 乙—35.9%C 甲—20% 乙—26.5%D 甲—16.7%乙—26.5%10.在20℃时,A物质的不饱和溶液,浓度为10%,如再加入5gA或蒸发掉32.26g水,都可成为饱和溶液,则20℃时,A的溶解度为() A 13.4g B 15.5g C 16.7g D 无法计算11.在100g稀中加入20%的溶液100g后浓度为12%,则原稀的浓度为()A 2%B 4%C 8%D 10%12.现有40℃时KNO3的饱和溶液82.0g,当温度下降至10℃时,溶液质量为60.5g,此时需加水102.4g才能把析出的晶体全部溶解,则40℃时KNO3的溶解度是A 32gB 64gC 40.5gD 21.5g13.将60℃的硫酸铜饱和溶液100克,冷却到20℃,下列说法正确的是A 溶液质量不变B 溶剂质量发生变化C 溶液为饱和溶液,浓度不变D 有晶体析出,溶剂质量不变14.某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。
若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的溶质质量分数是 A 30% B ×100% C 26.5% D ×100%15.t℃时将一定质量的某物质的不饱和溶液分成三份,分别加热蒸发溶剂。
然后,把温度降至t℃。
已知从三份溶液中蒸发的溶剂分别为10g、20g、30g,析出晶体(不含结晶水)分别为a g、b g、c g,则a、b、c,三者的关系是() A c=2b-a B c=a+b C c=a+2b D c=2a+b三、判断题:下列说法是否正确?如不正确,结果应怎样改正?1.在20℃时,100克水溶解21克,这种溶液中溶质的质量分数是21%。
2.将50克质量分数为10%的NaCl溶液稀释成100克质量分数为5%的NaCl溶液,稀释后溶液中溶质是稀释前溶液中溶质质量的一半。
四、计算题1.蒸干15克NaCl溶液得到1.2克NaCl,计算原溶液中NaCl的质量分数。
2.在一定温度时,NaCl饱和溶液的质量是12g,把它蒸干后,得到3.2gNaCl,计算:(1)这一温度下NaCl的溶解度(2)该温度时NaCl饱和溶液中溶质的质量分数(3)配制该温度时NaCl饱和溶液1000g,需水和NaCl各多少g?3.在10℃时,,计算10℃时饱和溶液中溶质的质量分数。
在50℃时,饱和溶液中溶质的质量分数是33.3%,计算50℃时的溶解度。
4.在80g质量分数为15%溶液里加入20g水或20g,计算这两种方法制成的两种溶液中溶质的质量分数。
5.配500ml质量分数为10%NaOH(密度为),需NaOH和水各多少g?6.把100g质量分数为98%稀释成质量分数为10%,需水多少g?7.实验室需要配500g质量分数为10%的盐酸,需要质量分数为38%的盐酸(密度是)多少ml?8.100g某浓度的溶液恰好跟13g锌完全反应,试计算这种溶液中溶质的质量分数。
9.200ml质量分数为38%的盐酸跟足量的大理石反应,可生成多少L?(质量分数为38%盐酸的密度是,的密度按计算)。
10.30g可以跟150克溶液恰好完全反应,计算:(1)可制得多少g?把溶液蒸干,得到多少g?(2)这种溶液中溶质的质量分数是多少?(3)100g这种稀释成质量分数为20%的,需加水多少g?11.100g稀中滴入100g溶液,恰好完全反应,生成沉淀23.2g,求稀的百分比浓度,溶液的百分比浓度。
12.20℃时,把一定量20%的某物质的水溶液加热蒸发掉10g水,再降到20℃,析出2g溶质,溶液浓度变为24%,求20℃时,该物质的溶解度。
13.用60%的NaOH溶液与10%NaOH溶液混合,配制20%的NaOH溶液150g,求需60%的NaOH溶液和10%的NaOH溶液各多少g。
选择题答案答案:1.溶质质量与溶液质量的比值2.12.5 501.C 2.B 3.B 4.C 5.B 6.B 7.C 8.C 9.D 10.B 11.B 12.B 13.B 14.C 15.A (提示:第一份蒸发掉10 g水析出a g;第二份蒸发掉10 g水时,先析出a g,再蒸发掉10 g水时,又析出(b-a)g;第s三份蒸发掉10 g水时,先析出a g,又蒸发掉10 g水时,又析出(b-a)g,再蒸发掉10 g水时,再析出(b-a)g,所以共析出溶质c=a+(b-a)+(b-a)=2b-a )判断题答案:1.错:第一处错:指明溶液中溶质的质量分数时,无需给出温度条件第二处错:溶质的质量分数应改为:17.4%2.错:稀释前后,溶质的质量不变计算题答案1.8%2.(1)36.4g (2)26.7% (3)需要水733g,NaCl267g3.10℃时的溶质的质量分数为24.8%,50℃时溶解度为49.9g。
4.若加20g水,溶质的质量分数为12%若加20g,溶质的质量分数为32%5.需要NaOH55g,水495g6.880g 7.111mL 8.19.6% 9.27.6L10.(1)产生0.92g,得到74.3g (2)30% (3)50g 11.9.8%,20.8% 12.31.6g 13.30g 120g。
