(整理)尿沉渣试剂评估
尿沉渣计数板 计算方法

尿沉渣计数板计算方法尿沉渣计数板是一种用于观察尿液中颗粒状物质的装置。
该装置通常由一块玻璃片制成,上面有一个方形或长方形的孔洞,在孔洞附近有一些刻度线以帮助计数。
尿液通过孔洞滴在玻璃片上,然后用显微镜观察,并使用特定的计算方法进行计数。
尿沉渣计数板通常用于检测尿液中的红细胞、白细胞、上皮细胞、细菌等颗粒状物质的数量,以帮助判断患者是否存在尿路感染、泌尿系统疾病等情况。
下面介绍一种常用的尿沉渣计数板计算方法。
1.准备工作:a.将尿液收集到干净的容器中,确保样品新鲜。
b.在尿液样品中加入适量的尿沉渣计数板试剂悬浮液,使尿沉渣均匀分散。
c.使用移液器将悬浮液混匀,并将一滴尿液滴在玻璃片的透明孔洞上。
2.观察与计算:a.将玻璃片放在显微镜的载玻片上,并使用10倍或40倍镜头观察。
b.选择一个代表性的区域,如中央孔洞或孔洞附近的刻度线。
注意避免刀状细胞、颗粒物质等边缘区域。
c.使用尿液沉淀计数时,通常需要随机观察视场,并通过每个视场的计数估计总流量。
可以用标记笔进行记号,以便不重复数计。
d.观察并计数各种颗粒状物质的数量,如红细胞、白细胞、上皮细胞等。
根据孔洞的面积和深度,可以根据比例计算出单位体积内物质的数量。
e.每次观察一个尿样时,通常计数300-400个白细胞和红细胞。
如果含量较高,可以适当减少计数数量。
f.记录每个计数单位中的物质数量,并对不同类型的颗粒进行分类。
3.计算总体数量:a.确定尿样的体积和沉渣观察视野的面积,例如10μL和0.1mm^2。
b.使用下列公式计算总体数量:物质总量= (每个计数单位中物质数量的平均值/沉渣观察视野面积) *尿样总体积c.例如,在一个视野中平均计数到40个白细胞,尿样体积为10μL,观察视野面积为0.1mm^2:白细胞总数= (40 / 0.1) * 10 = 4000个白细胞4.结果的解释:a.通过计算得到白细胞、红细胞、上皮细胞等的总体数量。
b.尿沉渣计数板仅提供数量信息,并不能独立作出诊断结果。
尿沉渣分析报告

尿沉渣分析报告1. 引言尿沉渣分析是一种用于评估人体健康状况的常见方法。
通过观察和分析尿液中的沉渣物,可以获取关于肾脏功能、泌尿系统疾病、代谢异常等方面的重要信息。
本文将介绍尿沉渣分析的步骤和常见结果的解读。
2. 收集尿样进行尿沉渣分析的第一步是收集尿样。
最好的收集方法是早晨首次排尿,因为这时尿液中的沉渣物最为明显。
用干净的容器收集约50-100毫升的尿液,并尽快送至实验室进行分析。
3. 检查尿液外观在进行尿沉渣分析之前,我们首先观察尿液的外观。
正常的尿液应该是清澈透明的,没有异味。
混浊、浑浊的尿液可能是由于白细胞、红细胞、脓液、细菌等沉积物的存在。
4. 离心沉淀为了使尿液中的沉渣物沉淀到底部,我们需要使用离心机进行离心处理。
将收集的尿样在离心机中以适当的速度离心,通常为2000-3000转/分钟,持续约5-10分钟。
5. 观察沉渣物离心处理后,我们可以看到尿样中的沉渣物已经沉淀在离心管的底部。
用吸管或移液器将上层的尿液倒掉,留下底部的沉渣物。
将沉渣物转移到玻片上,并加一滴碘溶液进行染色。
6. 显微镜观察将染色后的沉渣物玻片放置在显微镜下,使用10倍和40倍物镜进行观察。
逐一检查沉渣物中的各种细胞和结晶物。
7. 分析结果解读根据观察到的沉渣物,我们可以得出一些结论和诊断:•红细胞:正常尿液中红细胞的数量较少,如果观察到异常增多的红细胞,可能暗示泌尿系统出血或其他疾病。
•白细胞:白细胞的增多可能表示泌尿系统感染的存在。
•上皮细胞:尿液中的上皮细胞通常来自尿道、膀胱等泌尿系统的上皮组织。
过多的上皮细胞可能暗示尿路感染或其他疾病。
•结晶物:尿液中的结晶物可以是尿酸盐、草酸钙、磷酸钙等,其存在可能与尿液酸碱度、代谢异常等有关。
8. 结论通过对尿沉渣的分析,可以帮助医生评估患者的肾脏功能和泌尿系统状况。
尿沉渣分析是一项简单而有效的检查方法,对于早期发现疾病和监测治疗效果具有重要意义。
因此,合理利用尿沉渣分析结果可以提高疾病的诊断准确性和治疗效果。
尿沉渣检验实验报告

一、实验目的通过尿沉渣检验,了解尿液中细胞、管型、结晶等有形成分的含量,以辅助诊断泌尿系统疾病。
二、实验原理尿沉渣检验是将尿液进行离心后,对沉淀物中的有形成分进行测定。
通过观察和计数细胞、管型、结晶等,可初步判断泌尿系统是否存在炎症、感染、结石、肿瘤等疾病。
三、实验材料1. 试剂:生理盐水、尿沉渣检测液、瑞氏染液、醋酸酒精固定液。
2. 仪器:离心机、显微镜、离心管、载玻片、盖玻片、滴管等。
四、实验方法1. 标本采集:采集新鲜晨尿,约10ml。
2. 尿液离心:将尿液置于离心管中,以每分钟2000转的转速离心5分钟。
3. 沉渣制备:弃去上清液,取约0.5ml沉渣,倾于载玻片上,覆以盖玻片。
4. 检测:(1)低倍镜观察:先用低倍镜将涂片全面观察一遍,寻找有无细胞、管型及结晶体。
(2)高倍镜观察:再用高倍镜仔细辨认,并进行计数。
5. 结果记录:记录细胞、管型、结晶等有形成分的数量。
五、实验结果1. 细胞:(1)红细胞:18个/HP;(2)白细胞:2125个/HP;(3)上皮细胞:46个/HP;2. 管型:无;3. 结晶:无。
六、实验分析1. 红细胞:正常尿液中红细胞数量很少,18个/HP可能提示有轻微的血尿,需进一步检查。
2. 白细胞:2125个/HP明显增多,可能提示泌尿系统感染,如急性肾盂肾炎、膀胱炎等。
3. 上皮细胞:46个/HP,属于正常范围。
七、实验结论本次尿沉渣检验结果显示,患者存在白细胞增多,可能存在泌尿系统感染。
建议患者进一步检查,如尿细菌培养、尿常规等,以明确诊断并采取相应治疗措施。
八、注意事项1. 标本采集时,应确保尿液新鲜,避免污染。
2. 离心过程中,注意保持离心速度和时间的稳定。
3. 观察和计数时,应仔细辨认细胞、管型、结晶等有形成分,避免误诊。
九、总结尿沉渣检验是泌尿系统疾病诊断的重要辅助手段。
通过观察和计数尿液中的有形成分,可初步判断泌尿系统是否存在炎症、感染、结石、肿瘤等疾病。
UF-100尿沉渣仪国产试剂的临床应用评价
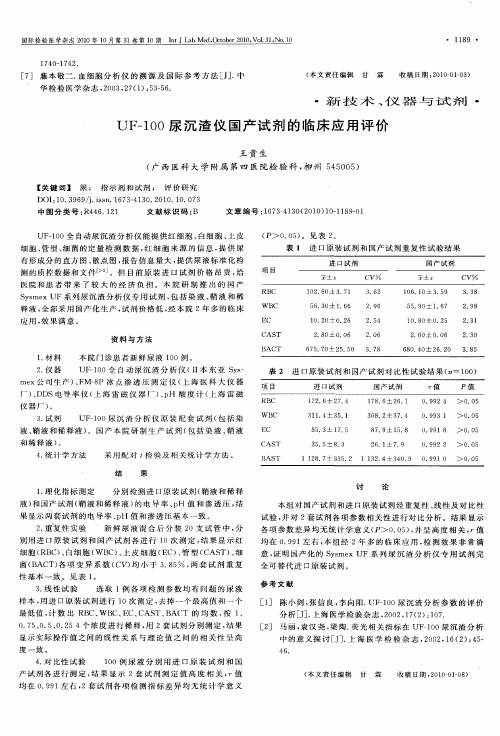
2 重复 性 实验 .
新鲜 尿液 混合后 分装 2 0支 试 管 中 , 分
别 用 进 口原 装 试 剂 和 国 产 试 剂 各 进 行 1 O次 测 定 , 果 显 示 红 结
细 胞 ( C) 白细 胞 ( RB 、 WBC) 上 皮 细 胞 ( 、 EC) 管 型 ( 、 CAS 、 T) 细
测 的质 控 数 据 和 文 件 n 一 ~ 。但 目前 原 装 进 口试 剂 价 格 昂 贵 , 给 医院 和 患 者 带 来 了 较 大 的 经 济 负 担 。本 院 研 制 推 出 的 国 产 S s x uF系 列 尿 沉 渣 分 析 仪 专 用 试 剂 , 括 染 液 、 液 和 稀 y me 包 鞘 释 液 , 部 采 用 国产 化 生 产 , 剂 价 格 低 , 本 院 2年 多 的 临 床 全 试 经
仪 器 厂 ) 。
RB C
1 2 6± 2 . 7. 74
3 1 4士 3 . 1 . 5 1
1 8 6± 2 . 7 . 6 1 3 8 2± 3 . 0 . 7 4 8 . 7 9± 1 . 5 8 2 . 士 7 9 6 1 .
0 9 24 . 9
> 0 0 . 5
菌 ( AC 各 项 变 异 系 数 ( ) 小 于 3 8 , 套 试 剂 重 复 B T) CV 均 .5 两
性 基 本 一 致 。见 表 1 。
3 线性 试 验 .
选 取 l例 各 项 检 测 参 数 均 有 问题 的 尿 液
样 本 , 进 宜原 装 试 剂 进 行 1 用 O次 测 定 , 掉 一 个 最 高 值 和 一 个 去 最 低值 , 数 出 R C wB E C T、 AC 的 均 数 , 1 计 B 、 C、 C、 AS B T 按 、 0 7 、 . 、 . 5 4个 浓 度 进 行 稀 释 , 2套 试 剂 分 别 测 定 , 果 . 5 0 5 0 2 用 结
尿沉渣检查——精选推荐

实验八尿沉渣检查Examination of urinary sediment非染色法尿沉渣显微镜检查实验原理尿液经离心沉淀后,置显微镜下观察其有形成分,如细胞、管型、结晶等。
试剂器材载玻片、盖玻片、滴管、10ml刻度离心管、离心机、普通光学显微镜操作步骤1.未离心直接涂片法(1)混匀将尿液标本混匀。
(2)制备涂片取混匀后的尿液1滴于载玻上,加盖玻片,避免产生气泡。
(3)观察计数先用低倍镜观察全片细胞、管型等成分的分布情况,再用高倍镜确认。
管型要观察计数至少20个低倍镜视野;细胞要观察计数至少10个高倍镜视野;结晶按高倍镜视野中分布范围估计报告。
(4)结果报告细胞以最低数∼最高数/HP、管型以最低数∼最高数/LP报告。
结晶以所占视野面积报告,无结晶为(-);结晶约占1/4视野为(+);约占1/2视野为(++);约占3/4视野为(+++);满视野时为(++++)。
如果细胞、管型数量过多难以计算时,则可按结晶的报告方式报告结果。
2.离心沉淀涂片法(1)离心刻度离心管,倒入混匀后的新鲜尿液10ml,相对离心力(RCF)500g离心5min。
(2)弃上清弃去上清液,留下0.2ml尿沉渣并混匀。
(3)涂片用微量吸管取混匀尿沉渣0.02ml,滴在载玻片上,用盖玻片覆盖。
(4)观察计数与未离心直接涂片法相同。
(5)结果报告与未离心直接涂片法相同。
3.定量尿沉渣分析板法定量尿沉渣分析板为特制的一次性使用的硬质塑料计数板(见图5-2),每块板上有10个计数池,每个计数池又有1个计数区,每个计数区有10个大方格,每个大方格又分为9或16个小方格,计数池的高度为0.1mm,每个大方格的面积为1mm2,故每个大方格的容积为0.1μl;10个大方格的总容积为1μl,每个样本用1个计数池。
(1)未离心法直接吸取混匀尿液1滴充入定量尿沉渣分析板计数池内,在低倍镜下计数10个大方格内管型总数,在高倍镜下计数10个大方格内细胞总数,此即每微升的尿液中某种有形成分的数量。
尿沉渣检查(UD-S仪器法)

尿沉渣检查(UD-S仪器法)⒈实验原理通过仪器自动实现取样、染色、清洗、混匀、稀释等动作,显微镜下的图象信息显示在计算机显示器上,可直接进行尿液有形成分的识别工作,并且计算机将尿分析定量板中已统计各有形成分数量自动换算成标准状态下数据,最后把干化学分析和尿沉渣分析的完整系统用真彩色图文报告。
⒉标本采集及运送2.1标本采集:实验室工作人员、医生、护士必须对病人留尿进行指导,务必使尿道口保持清洁。
随机尿液标本的留取无特殊时间规定,但病人必须有足够的尿量(10ml以上);晨尿指病人起床后第一次尿;收集“时段尿”时,应告病人时间段的起点和终点,起始时间先排空膀胱;三杯试验留尿时间要分段明确,做好标记。
送检单上应注明留尿时间、送检时间。
2.2 标本的运送:按上述要求留取尿液应在2小时内完成检验,如果标本收集后2小时内无法完成分析,可置2-8℃冷藏,6小时内完成检验;如仅作尿沉渣检查,可在尿标本中加适量防腐剂(大多使用400g/L的甲醛溶液,每升尿液加入5ml。
应注意甲醛过量时可与尿素产生沉淀物,干扰显微镜检查)。
2.3 标本的标记:标本容器必须有标记,包括:病人姓名、特定编码(或住院病人的病区、床号)、标本收集时间。
标签应贴在容器上,不可贴在盖上。
2.4 标本的接收:实验室应建立严格的标本接收制度,工作人员在接收标本时,必须检查标本容器是否符合要求;标记内容与医生所填写化验单是否一致;从留尿到接收标本的时间是否过长;标本是否被污染。
尿标本量不少于10ml,在特殊病例不可能达到此要求时(如小儿、烧伤、肾衰无尿期等),应在检验报告单上注明收到的尿量及检查方法(离心或未离心)。
⒊试剂3.1 染色液名称:阿一中染色液(生产厂家:北京国联在线医疗技术有限公司。
包装规格:250ml)3.2 清洁液(GLⅠ):尿沉渣仪清洁液(直接使用);生产厂家:北京国联在线医疗技术有限公司;规格:1L3.3 GLⅢ清洗液:用法:当计数池很脏或堵塞用GLⅡ清洗无效时,用该清洗液,可疏通并漂白管路。
尿沉渣 实验报告

尿沉渣实验报告
《尿沉渣实验报告》
尿沉渣是指尿液中沉淀下来的固体物质,通常包括细胞、蛋白质、细菌和晶体等。
通过观察尿沉渣的形态和成分,可以了解人体内部的健康状况,因此尿沉
渣实验成为一种常见的临床检测方法。
在进行尿沉渣实验时,首先需要收集患者的尿液样本。
然后将尿液置于离心机
中进行离心分离,离心后的上清液称为尿上清液,而沉淀下来的固体物质即为
尿沉渣。
接下来,可以通过显微镜观察尿沉渣的形态和结构,同时也可以进行
化学试剂的检测,以确定其中的成分。
通过尿沉渣实验,可以发现一些与健康相关的指标。
比如,尿中出现大量的白
细胞和红细胞可能表明患者存在泌尿系统感染或者肾脏疾病;尿中出现蛋白质
可能提示肾脏功能异常;尿中出现结晶体可能与尿液的pH值、饮食习惯等有关。
除了临床应用外,尿沉渣实验也被广泛运用于科研领域。
科研人员可以通过对
尿沉渣的分析,探究人体内部的代谢过程、疾病发生机制等。
同时,尿沉渣实
验也可以帮助医学研究人员开发新的诊断方法和治疗手段。
总的来说,尿沉渣实验是一种简单而有效的检测方法,它可以为医生提供重要
的诊断依据,也可以为科研人员提供宝贵的研究材料。
通过不断的实验和研究,相信尿沉渣实验将会在医学领域发挥更大的作用,为人类健康事业做出更大的
贡献。
三种尿沉渣检查方法的比较及评价

2 结
李爱香
朱 保 忠 刘俊 英 岳 晓 华
果
尿沉渣检验是 临床实验室常作 的检验 ,对于泌尿系统疾 病 的诊 断 和鉴别诊 断 有重 要 的参考价 值_ 1 J 研究 采用 直 。本 接 定 量 计 数 板 镜 检 法 、F _0 u _ l0型 尿 流 式 细 胞 分 析 仪 和 A E 6 A型全 自动智能 尿沉渣分析仪 3种方法对尿 中的 v 一7 3
09 , 和 检 验 U 21 ,> . 。 . 秩 4 = .2P 00 5 3 讨 论
1 . 分析 仪测 定 法 :严 格 按 仪 器 说 明 书操 作 步 骤 对 每份 充 .2 3
31 显 微 镜 检 测 技 术 : 红 细 胞 、 . 尿 白细 胞 的 显 微 镜 检 测 技术 ,
1 统计 学处 理 . 4 采 用 C IS统 计 软 件 进 行 秩 和 检 验 和 相 关 分 析 ,以 P HS < 0 5为差 异 有 统 计 学 意 义 。 . 0
有形成分定量分析的理想方法 ,但在现实中因效率低下和人
工误 差 而 不 实 用 。
3 全 自动尿沉渣分析仪 u — l0检测技术 : 自动尿沉渣 . 2 F o 全 分析仪 u . 10检测原理是直接对尿液标本染色后 , F.0 利用流
1 . 定量计数板镜检法 : .3 3 不离心标本 : 用一 次性塑料移液管 吸取 混匀尿液 , 滴入 2个 J S 次性 专用尿沉渣计数板 内 , A T一 稍待片刻 , 首先用低 倍镜 观察尿液 细胞分 布情况 , 再用 高倍 镜计 数 1 0大方格内红 细胞 、 白细胞数 。所有试验均在取样后 2h内完成 , 镜检结果脂肪滴等 因素导致 U 一 10尿液分析仪测定尿 白细胞 结 F o 果偏高。因此 , 虽然 u 一 10全 自动尿沉渣分析仪检测尿 液 F 0 定量分析具有快速 、 简单等优 势 , 但对 于“ 报警 ” 信息 的标 本 ,
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
SYSMEX UF-500i/UF-1000i尿沉渣分析仪试剂临床评价报告山东省xxx医院二零一一年十一月十七日尿沉渣SYSMEX UF500i/1000i试剂评价报告使用SysmexUF500i/1000i进行尿液常规检测,已经成为临床实验室最常用的方法之一,其检测结果的准确与否与使用的尿液分析仪用试剂有着非常密切的关系。
最近,我科对适用于SYSMEX公司UF500i/UF1000i尿沉渣分析仪的国产(STAC公司、BL公司、BRT公司)的尿沉渣分析仪配套试剂沉渣稀释液、沉渣染液、细菌稀释液、细菌染液、鞘液进行了临床试验,现将结果报告如下:目的国产尿沉渣分析仪用试剂应用于Sysmex尿沉渣分析仪的结果评价。
材料和方法一、材料1、仪器:SYSMEX UF1000i尿沉渣分析仪(仪器编号:11619)2、试剂:●SYSMEX UF1000i仪器原装试剂(简称原装试剂),1、沉渣稀释液UFII PACK-SED,批号:A10162、沉渣染液UFII SEARCH-SED,批号:A10083、细菌稀释液UFII PACK-BAC,批号:A10074、细菌染液UFII SEARCH-BAC,批号:A00255、鞘液UFII SHEATH,批号:G1082●原厂质控物U FⅡCONTROL ,批号:YS1004●国产尿沉渣试剂包括:1、STAC公司沉渣稀释液STAC-PACK-SED,批号:A0028沉渣染液STAC-SEARCH-SED,批号:A0015细菌稀释液STAC-PACK-BAC,批号:A0014细菌染液STAC-SEARCH-BAC,批号:A0016鞘液STAC-SHEATH,批号:G00132、BL公司沉渣染液URINE DYE-SED,批号:A1107细菌染液URINE DYE-BAC,批号:A1010沉渣稀释液URINE DIL-SED,批号:A1118细菌稀释液URINE DIL-BAC,批号:A1123鞘液II 批号:A10153、BRT公司沉渣染液UFII BRISEARCH-SED,批号:D2*******细菌染液UFII BRISEARCH-BAC,批号:E20111001沉渣稀释液UFII BRIPACK-SED,批号:B20111001细菌稀释液UFII BRIPACK-BAC,批号:C20111001鞘液UFII BRISHEATH,批号:A20110904标本:随机抽取尿样32例作为检验标本。
二、评价方法1、理化指标符合率2、空白计数:观察国产试剂上机后是否符合仪器的空白值要求。
3、质控检测:观察使用国产试剂后检测结果准确性。
4、检测结果相关性比较:观察使用国产试剂与使用原装试剂有无显著差异。
三、结果:1、理化指标小结:SYSMEX原装试剂与STAC试剂理化指标完全一致;BRT公司与BL公司则仅有个别指标与原装试剂一致,显而易见的是配方与原装有较大出入。
2、空白计数:按照仪器操作手册要求,对国产试剂和原装试剂分别进行空白检测,结果如下(表二):表二:空白结果由检测结果可以看出,使用国产试剂空白值和使用原装试剂空白值均在限值以下,说明国产的UF500i/UF1000i试剂在使用到UF500i/UF1000i仪器上时,测量的空白值均符合仪器的要求。
STAC公司生产的试剂在仪器上进行本底测量,测得的空白结果和使用原装试剂所测得的结果非常接近;BRT及BL公司试剂虽然测得空白结果符合仪器上限要求,但是比原装试剂的本底值高出了3~4倍;过高的本底则降低了仪器的灵敏度,对弱阳性标本影响较大,容易出现假阴性。
3、原装质控检测:使用国产试剂和原装试剂分别对尿质控进行测定,详细结果如下(表三-1、表三-2):表三-1:尿低值质控检测结果表三-2:尿高值质控检测结果Cond.(Ms/cm) 37.4±3.7 37.6 37 40.1 41.6 S-FSC 98.6-133.4 112 112.2 111.3 110.7 S-FSCW 23.6-28.8 26.2 26 27.0 27.0 S-FLH 14.9-34.7 21.4 20.9 14.0 19.1 S-FLL 89.2-208.2 127 110.4 168.8 154.9 S-FLLW 73.3-109.9 84.1 84 79.0 82.7 S-SSC 18.3-27.5 22.67 20.9 28.9 32.5 B-FSC 78.8-106.6 87 87.17 86.7 86.8 B-FSCW 61.8-83.6 67.5 68 68.2 68.8 B-FLH 82.5-153.3 147.73 140.8 97.9 131.7使用原装试剂和使用STAC试剂在测量高值质控和低值质控时,测量结果均在质控要求范围内,使用原装试剂和使用BL试剂在测量低值质控时,参数BACT和Cond.均超出了质控的要求,测量高值质控时,S-FLH和S-SSC参数超出了质控的要求范围。
使用原装试剂和使用BRT试剂在测量低值质控时,参数BACT和Cond.超出了质控的要求,测量高值质控时,Cond.和S-SSC参数超出了质控的要求范围。
通过观察尿质控检测的结果,使用国产试剂检测尿质控所得的结果中,STAC试剂所测结果均在在靶值范围内,STAC试剂可以保证检测结果的准确性;BL试剂所测结果中BACT、Cond.、S-FLH和S-SSC参数的测量值超出了质控的要求范围,BL试剂不能完全保证测量结果的准确性;BRT试剂所测结果中BACT、Cond.、S-SSC参数的测量值超出了质控的要求范围,BRT试剂不能完全保证测量结果的准确性。
4、统计学分析:使用成套国产试剂及成套SYSMEX公司原装试剂对同一标本组进行尿沉渣分析。
分析前,先用仪器配套质控品作质控,确认仪器的状态良好;对测定结果采用电脑程序的样本配对t检验和线性回归的统计学方法进行分析,详细结果如表四(分析数据线性图见附图):表四:原装试剂与STAC试剂测定结果比较(n=32)RBC(/µL)WBC(/µL)EC(/µL)CAST(/µL)BACT(/µL)Cond.(Ms/cm) 参数原装STAC 原装STAC 原装STAC 原装STAC 原装STAC 原装STAC x 9.69 9.48 7.86 7.79 6.70 6.73 1.04 1.03 184.4 183 6.29 6.25 R20.990 0.997 0.997 0.987 0.991 0.980t-检验P>0.05P>0.05P>0.05 P>0.05P>0.05P>0.05原装试剂与STAC试剂相关性比较使用原装试剂和使用STAC公司试剂进行标本测量比对,RBC测量结果的R2达到了0.990,RBC结果相关性良好,且无显著性差异结果高度相关。
使用原装试剂和使用STAC公司试剂进行标本测量比对,WBC测量结果的R2达到了0.997,WBC使用原装试剂和使用STAC公司试剂进行标本测量比对,EC测量结果的R2达到了0.997,EC结果相关性良好,且无显著性差异结果高度相关。
使用原装试剂和使用STAC公司试剂进行标本测量比对,CAST测量结果的R2达到了0.987,CAST 结果相关性良好,且无显著性差异结果高度相关。
使用原装试剂和使用STAC公司试剂进行标本测量比对,BACT测量结果的R2达到了0.991,BACT 结果相关性良好,且无显著性差异结果高度相关。
使用原装试剂和使用STAC公司试剂进行标本测量比对,Cond.测量结果的R2达到了0.980,Cond.表五:原装试剂与BL试剂测定结果比较(n=32)RBC(/µL)WBC(/µL)EC(/µL)CAST(/µL)BACT(/µL)Cond.(Ms/cm) 参数原装BL 原装BL 原装BL 原装BL 原装BL 原装BL x 9.69 9.3 7.86 7.7 6.70 6.9 1.04 1.05 184.4 191.8 6.29 6.25 R20.987 0.996 0.976 0.947 0.793 0.812t-检验P>0.05P>0.05P>0.05 P>0.05P<0.05P<0.05原装试剂与BL试剂相关性比较使用原装试剂和使用BL公司试剂进行标本测量比对,BACT测量结果的R2达到了0.793,BACT结果相关性不好,存在显著性差异。
使用原装试剂和使用BL公司试剂进行标量比对,Cond.测量结果的R2达到了0.812,Cond.结果相关性不好,存在显著性差异。
表六:原装试剂与BRT试剂测定结果比较(n=32)RBC(/µL)WBC(/µL)EC(/µL)CAST(/µL)BACT(/µL)Cond.(Ms/cm) 参数原装BRT 原装BRT 原装BRT 原装BRT 原装BRT 原装BRTx 9.69 9.4 7.86 7.6 6.70 6.8 1.04 1.05 184.4 214.9 6.29 6.4 R20.979 0.992 0.979 0.891 0.807 0.899t-检验P>0.05P>0.05P>0.05 P<0.05P<0.05P<0.05原装试剂与BRT试剂相关性比较使用原装试剂和使用BRT公司试剂进行标量比对,CAST测量结果的R2达到了0.891,CAST结果相关性不好,存在显著性差异。
使用原装试剂和使用BRT公司试剂进行标量比对,BACT测量结果的R2达到了0.807,BACT结果相关性不好,存在显著性差异。
使用原装试剂和使用BRT公司试剂进行标量比对,Cond.测量结果的R2达到了0.899,Cond.结果相关性不好,存在显著性差异。
四、结论从我科室试验过程及以上测试、分析数据来看,国产试剂中STAC试剂与原装试剂相比,有着良好的空白值、准确性且主要参数均无显著性差异,完全可以替代原装试剂用到SYSMEX-------------UF500i/1000i仪器上,而BL和BRT试剂与原装试剂相比,一些主要参数的准确性存在显著地差异,容易产生假阴性结果,不能替原装试剂用到SYSMEX UF500i/1000i尿沉渣分析仪上。
山东省xxx医院检验科二零一一年十一月十七日-------------。
