国际保健品管理的比较研究
国际保健品管理的比较研究(上)

第 4卷 第 7 期 20 0 8年 7 月
亚 太 传 统 医 药
Asa Pa i c" r d to a e ii e i- cf 1 a i n l i - i M dcn
V0. . 14No 7
J1 08 u.2 0
规、 管理机构 、 审批制度 、 标签声 明、 生产管理等 几方 面加 以介 绍和 比较 , 我 国保 健品行 业 的科 学管理和规 范发 为
展提供 借鉴 , 同时也为我 国保健品 生产企 业进 军 国际 市场提供 必要 的管理政策 支持 。
关 键 词 : 健 品 ; 理 ; 较 保 管 比
际上是 现代 工业 社会 中 的医 学 , 作 为现 代 科 技 文 化 的一 是
部 分 的医学 , 全 人 类 的 主 流 医 学 , 恰 当 的称 谓 应 当是 是 其 ‘ 代 医学 ’ 现 。相 比之 下 , 中国在 中世纪 比欧 洲更 发达 的“ 中
然科学层 面寻找突破 , 可能引发 中医飞跃 式发 展 的。 自 是不 然科 学 的发展 , 当驶 入 自然 科学 运 行 的轨 道 , 借现 代 就应 凭
医” 由于社 会长 期封 闭 、 守 、 滞 , , 保 停 没有 进 化 出现代 科 技
和工业革命 , 基本上是停 留在原来 的水平上 , 其恰当的称谓 应当是 ‘ 传统医学’ 。中国大百科全书在 19 年出版时, 92 医
学就 是 分成 两卷 —— 《 代 医 学卷 》 中 国传 统 医 学卷 》 现 和《 。
那就 是最 恰 当的分 类 和最科 学 的命名 。将现 在 的“ 医” ” 西 称
为“ 现代 医学” 并 非是 在有 意抬 高西 医 的身价 , 是采 用 了 , 而
保健品市场调查报告6篇

保健品市场调查报告6篇保健品,就是一种称之为蓝帽的保健食品。
大家做过保健品的市场调查报告吗?下面是为大伙儿带来的6篇《保健品市场调查报告》,亲确实定与共享是对我们最大的鼓舞。
保健品市场调查报告篇一随着近年来人们生活水平的不绝提高,以及人们健康保健意识的加强,保健品市场从原先的功能单一型发展到今日多元化保健,保健品功能层出不穷,种类也多种多样。
目前,市场上保健品层出不穷,人们使用最多的保健品紧要有五类:滋补类、养容养颜类、大脑神经类、补钙类、心血管类。
一、基本情况分析:1、从消费动机分析:一类城市“自我服用”,二类城市“馈赠亲友”,一类和二类城市“购买过但未服用过”的消费者是随年龄递增而下降的,而“服用过但未购买过”的则是上升的。
2、消费者购买群体:紧要集中在年轻人,而服用的紧要对象则紧要集中在中老年群体。
由此可见,保健品消费紧要是以“表达或传递感情”为目的。
3、消费季节:冬季虽为旺季,但季节性开始淡化冬令进补是中国人的传统,因此冬季无疑是保健品的销售旺季,这点仍旧表现得很明显,夏季是最少服用保健品的季节。
4、消费心理:关怀功效、价格、服用方便及口味保健品的服用者较为慎重,一、二类城市中按说明书的要求服用的人群比例分别实现81%和80%,表明保健品的消费种类目前仍然是以药品保健为主,此类产品的说明书的内容对消费者有确定的`引导作用。
5、购买紧要地方:超市、自选商场和药店超市自选商场和药店是消费者购买保健品的紧要地方,也是保健品比较集中的地区;医院则是消费者最少购买的地方(均不到5%)。
6、零售终端进货渠道分析:目前云南省将近全部的药店都有经营保健品,但是目前的市场情况都比较混乱,大部分(约70%)的终端客户进货渠道都是自身到昆明的保健品市场直接进货,有一部分(约30%)规模相对大的客户进货紧要集中在昆明几家保健品公司,如吉梦妮、长兴、奥妮等保健品公司。
二、结论:虽然生产厂家目前不绝推出各类保健品以满足消费者的多层次需求,各类产品的广告也打得铺天盖地,但由于保健品的种类多得将近已经可以掩盖全部人群,使得消费者保健品的消费进入成熟期,开始由冲动性购买转向理智型消费,消费群体也已由以前的单一型转向多元化。
最新保健食品管理制度

最新保健食品管理制度简介保健食品是指具有调节人体机能,适合普遍人群食用,不以治疗疾病为目的的食品。
随着人们对健康的关注度提高,保健食品市场也逐渐发展壮大。
然而,由于一些不负责任的企业存在,保健食品市场也暴露出一些问题,如虚假宣传、治愈疾病的不实承诺等。
为了保护消费者的权益,各国纷纷制定保健食品的管理制度。
本文将介绍最新的保健食品管理制度。
一、美国的保健食品管理制度美国的保健食品管理制度由联邦食品药品监督管理局(FDA)负责管理。
根据美国联邦法律,保健食品必须满足标准:1.不能以治疗疾病为目的:保健食品不能宣称可以治愈或预防疾病,不得进行虚假宣传。
2.不得含有药物成分:保健食品不能含有未经FDA批准的药物成分。
3.安全性要求:保健食品必须通过科学评估,确保其成分安全并符合标签上所示的用量。
另外,美国还对保健食品的标签要求进行了详细规定,包括成分表和营养成分表的标注等。
二、欧盟的保健食品管理制度欧盟对保健食品的管理主要通过食品安全局(EFSA)来进行。
欧盟的保健食品管理制度主要包括要求:1.成分安全和有效性:保健食品必须经过严格科学评估,证明其成分的安全性和有效性。
2.不能欺骗消费者:保健食品的宣传必须真实、准确,不得误导消费者。
3.标签要求:保健食品的标签必须清晰、准确,包括成分表、含量表等信息。
欧盟还规定了保健食品添加剂的使用限量以及对特定成分的禁用要求等。
三、中国的保健食品管理制度中国的保健食品管理制度由国家市场监督管理总局负责。
中国的保健食品管理制度主要包括要求:1.原料和配方要求:保健食品的原料必须符合国家标准,保健食品的配方必须经过科学评估。
2.安全性要求:保健食品必须经过国家食品药品监督管理部门的安全评估,确保安全性。
3.标签要求:保健食品的标签必须真实、准确,包括原料表、含量表、功能表等信息。
此外,中国还对保健食品的功能性成分作出了具体规定,禁止虚假宣传、医学化名等行为。
四、总结保健食品市场的管理制度对于保护消费者权益、维护市场秩序具有重要作用。
【推荐下载】PEST分析案例:保健品PEST分析案例

PEST分析案例:保健品PEST分析案例下面一篇介绍保健品PEST分析案例,所谓保健品行业“PEST”分析是指通过对政治、经济、社会和技术等因素进行分析,来确定这些因素的变化对保健品行业发展战略管理过程的影响。
PEST分析案例:保健品PEST分析案例 所谓保健品行业“PEST”分析是指通过对政治、经济、社会和技术等因素进行分析,来确定这些因素的变化对保健品行业发展战略管理过程的影响。
1.从政治法律角度看,政府主管部门的更迭也带来保健品行业新变化 保健品标准和规定缺失且相互矛盾,如我国卫生部制定的《食品添加剂使用标准》(B276196规定食品中不允许含过氧化氢(双氧水)但某些生产规章又订有保健食品的过氧化氢残留标准。
由于缺乏有关的行业管理和国家标准造成保健品行业目前假冒伪劣产品、虚假广告、·价格虚高等现象严重。
企业在现有法规下宣传自己的产品很容易违规。
法规规定,保健食品不能宣传治疗作用。
另一方面,保健食品中使用的中草药在药典中都有治疗作用。
可是一用到保健食品里就不能宣传了,似乎治疗作用全没了。
2003年3月7日,国务院公布机构改革方案决定成立国家食品药品监督管理局,原属卫生部管理的保健品划归sDA管理,自2003年6月1日起,卫生部已停止受理保健品的申报,同年1月10日,国家食品药品监督管理局完成交接,正式开展保健品的审批工作。
受非典、部门移交影响,当年度保健品报批工作停顿了半年之久。
从长期看,国家食品药品监督管理局接手保健品行业管理职责,有助于让保健品行业更规范、更健康的发展。
2,从经济的角度看,市场竞争日益激烈,跨国公司成为行业领头羊 保健品市场在过去的2年间,国外跨国公司一直鲜有涉足,市场被本土保健品企业牢牢占据,2003年在保健品行业陷入低潮之时,美国安利却凭借独特的销售模式异军突起,实现了年销售额3亿元的惊人业绩,尽管安利的营销模式颇有争议。
但不能否认,随着跨国保健品公司进军中国的步伐加快,国内保健业面临更大的市场竞争压力。
中韩人参研究的系统比较

中韩人参研究的系统比较人参,被誉为“生命之根”,是一种具有丰富营养价值和药用价值的植物。
中韩两国在人参研究方面都具有悠久的历史和丰富的经验。
本文将比较中韩两国在人参研究方面的系统差异,以期为未来中韩人参研究的合作与发展提供参考。
中国人参研究始于唐代,具有1500多年的历史。
自那时以来,人参在中医中一直被用作强壮剂和补药。
20世纪70年代以来,中国科学家开始对人参进行系统研究,探究其化学成分、药理作用、栽培技术等方面的知识。
目前,中国已经成为全球最大的人参生产国和出口国。
韩国人参研究始于20世纪50年代,比中国晚了约150年。
然而,韩国在人参研究方面发展迅速,成为全球最重要的人参研究力量之一。
韩国科学家在人参的栽培技术、化学成分、药理作用等方面进行了深入的研究,并开发了许多以人参为原料的保健品和药品。
研究机构:中国和韩国都拥有众多从事人参研究的科研机构。
在中国,主要有中国科学院、中国农业科学院、中国医学科学院等机构,而在韩国则主要有生命工学研究院、食品药品安全处等机构。
研究内容:中韩两国在人参研究内容方面有共同之处,但也存在一些差异。
中国在人参的栽培技术、化学成分、药理作用等方面进行了广泛的研究,而韩国则更加注重人参的产业化发展,如保健品、药品的开发等。
研究方法:中韩两国在人参研究方法方面有共同之处,如生物技术、化学分析等。
然而,韩国在人参研究的精细化方面较为突出,如在分子生物学、基因工程等领域的应用上较为活跃。
研究成果:中韩两国在人参研究成果方面均取得了显著的成绩。
中国在人参的栽培技术、化学成分、药理作用等方面发表了大量的学术论文和专利,而韩国则成功开发出多个人参保健品和药品,如高丽参粉、红参茶等,并在市场上取得了很大的成功。
随着科技的发展和人们对健康需求的提高,中韩人参研究将迎来更多的机遇和挑战。
未来,中韩两国在人参研究领域应加强合作与交流,互相学习和借鉴,共同推动人参研究的发展。
在此基础上,中韩两国应加强以下方面的研究与创新:人参栽培技术的进一步优化与提升。
德国著名保健品分析
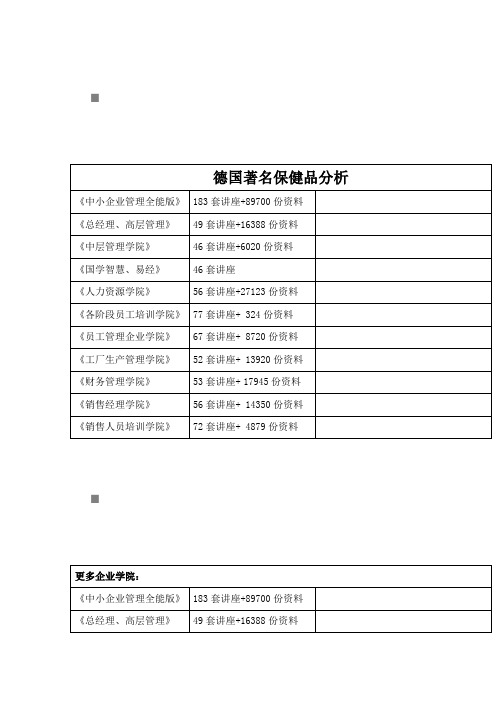
⏹⏹回国的送礼选择,德国著名保健品介绍保健品要紧有下列种类骨科- 骨胶原系列心脑血管,降血压血脂系列维生素软磷脂促进新陈代谢,增强体能,抗疲劳排毒养颜抗衰老护肤护发- 全天然药妆系列骨科及骨胶原系列1. 复合关节骨胶原德文原名: Gelenketabletten Plus要紧成分:葡糖胺Glucosamin sulfat ------ 700,00mg,骨胶原Chodroitin sulfat ------ 75,00mg,维生素E Vitamin E ------ 10,00mg (高达10毫克!) 维生素B6 Vitamin B6 ------ 2,00mg锌Zink ------ 5,00mg铜Kupfer ------ 0,20mg锰Mangan 0,20mg葡糖胺(Glucosamine)的作用:葡糖胺(Glucosamine)是一种人体用来制造粘多糖的氨基酸组合分子结构。
葡糖胺集中于关节软骨处,首先形成长链氨基酸粘多糖,然后形成更大的结构——蛋白聚糖。
蛋白聚糖的作用是汲取水分与液体到关节处用来在运动时润滑软骨。
骨胶原(Chondroitin)的作用:骨胶原又称之“软骨胶硫酸盐”,它大量地集中于动物关节邻近的软骨内,将体液引至关节内的细胞里,提供润滑作用,协助骨头随着各个动作来顺利滑动。
此外,骨胶原可与葡糖胺合作来制造软骨所需的胶原蛋白与其它成份。
多项研究说明,关节炎患者在服用骨胶原之后,疼痛症状不仅大为减轻,活动能力也增加,而且,停用之后很久仍感到效果。
骨胶原存在于我们平常食用的天然食物中。
研究证明,摄取骨胶原关于人体正常利用葡糖胺非常重要。
人体内含有多种消化酶,其中有些消化酶会“吃掉”软骨,导致软骨过早损坏,而软骨素就能够保护软骨免受这种侵害。
同时,“骨胶原能够抑制那些阻止营养素被输送到软骨的消化酶的活动……刺激蛋白聚糖、糖胺聚糖与胶原蛋白的产生,而他们正是软骨的基体分子,也就是构成健康新软骨的物质。
国际保健品管理的比较研究(下)

AR TG R数 码进 行识别 。如 处 方 药 , 些非 处 方药 和 医疗 某 仪 器 等 。 风 险 较 低 的 产 品 在 ART 中 作 为 登 记 产 品 G ( TG ) 绝 大多数 补充 药 品属 于此 类 。这 类产 品 T AR L, GA 不作上 市前 的安 全性 、 有效 性及 质量 评估 ( 种情况 仅适 用 这 于产 品所有 成分 均在先 前 已获得 T GA 同意作 为 低 风险 性
TGA和 新西 兰 医药 和 医疗 器械 安全 局 (h w Z aa d teNe eln ' s Me i n n dcl vcsS ft t oi ) 承担起监 dc ea dMe i ie aeyAu h r y , i a De t
补 充药 品 (o l etr d i s ( 被 认 为 是 传 cmpe na mein ) 也 m y ce
证据 材料 的指导 和规定 。考 虑 到 传统 药 品用 途 的依 据 , 包
括 医药书籍 、 参考 文献 和先前 的研究 报告 , 因此该 法规 对传 统草 药药 品的安全性 和有 效性 的评价 , 别是对 有效 性 , 特 比
其它药 品宽松许 多 。 4 3 管理机 构 .
T A 将 在 产 品上 市 前 对 其 安 全性 、 效 性 及 质 量 进 行 评 G 有
统药 品或替代 药品 ) 包括 维生 素 , 矿物质 , 草药 , 芳香 疗 法和
顺势疗 法用 品。
42 法规 .
管 两 国治疗用 物 品的质量 、 全 、 能或作用 等保 护公 众健 安 功
康 的责任 。一个 全新 扩展 的补 充 在起 草一 个共 同的议 案 , 一旦 通过 , 国协 两 议 开始实施 , 到时将 会 有 一个 专 门 的机 构 负 责补 充 药 品和 替代 药 品的管 理 。
医药保健品营销模式的比较研究

武 汉 职 业 技 术 学 院 学 报 二 O 一二 年 第
、
有关 概念 的界 定
营 销 模 式 是 指 企 业 在 营 销 价 值 链 中 各 环 节 发 生 的 一 系 列 业 务 活 动 或 因 素 的 组 合 , 它 是 以 企 业 为 中
收稿 日期 :0 1— 2 1 20 2 0 — 7
行 业 , 兴 营 销模 式 种类 较 多 , 要 有会 议 营 销 、 新 主 数
一
理 念 指 导 下 的 创 新 营 销 模 式 的 出 现 ,这 也 是 保 障 保 健 品 市 场 健 康 有 效 运 作 的关 键 。 保 健 品 营 销 模 式 的 创 新 关 系 着 企 业 发 展 的 命 脉 ,但 相 关 参 考 文 献 甚 少 ,本 文 将 其 具 体 归 为 三 大 类 :第 一 ,通 过 营 销 理 念 的 创 新 进 行 营 销 模 式 的 创 新 。 如 速 度 营 销 、 性 营 销 、 天 候 营 销 、 击 营 销 弹 全 游 等 。第 二 , 用 新 的 营 销 载 体 或 新 的 技 术 进 行 营 销 模 采 式 创 新 。如 拓 展 营 销 活 动 载 体 的 会 议 营 销 、 件 营 销 事 等 ; 用 现代 信 息 技术 的 网络 营销 、 据 库 营销 、 应 数 虚 拟 营 销 等 。 第 三 , 营 销 中 的 局 部 环 节 ( : 作 流 对 如 运 程 ) 行 优化 以及 对某 种 营销 要素 进行 创新 。 之更 进 使
模式相 比, 新兴 的营销模 式具有一定 的优越性 , 能够提供 个性化的服务 、 如 销售成本较低 、
信 息 沟通 具 双 向性 等 。
关键词 :医药保健品 ; 营销模 式; 会议营销 ; 数据库 营销
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
国际保健品管理的比较研究摘要:介绍了美国、加拿大、欧盟、澳大利亚、日本、韩国等国家或组织的保健品监管体系,主要从保健品范畴、法规、管理机构、审批制度、标签声明、生产管理等几方面加以介绍和比较,为我国保健品行业的科学管理和规范发展提供借鉴,同时也为我国保健品生产企业进军国际市场提供必要的管理政策支持。
关键词:保健品;管理;比较近年来,随着经济和科技的发展,人们生活水平的提高,人们的健康观念也发生了重大转变。
从疾病治疗转向疾病预防、注重保健,从单一依靠体育锻炼和通过一日三餐摄取营养转向间接强化输入营养。
随着人们追求健康和高质量的生活方式,以及人口老龄化的加剧,使得人们在营养保健品上的消费日益增长。
由于营养保健食品不仅能提供人体生存必需的基本营养物质,还能调节人体机能、促进健康,具备普通食品所不具备的第三功能,从而得到人们的广泛青睐。
在过去10年里,保健品行业发展迅速,其消费人群和市场销售额都有大幅增长。
2004年美国的功能食品市场规模达到245亿美元,全球膳食补充剂和功能食品的市场销售额为719亿美元,开发对人类健康有益的保健品已成为世界上最有前途、最有活力的行业之一。
为了规范行业的发展,确保消费者的健康和安全,各国政府纷纷出台了相关的法规和政策对保健品实施监督管理。
由于国际上关于保健品没有一个统一的定义,各国的提法略有差异。
在美国,这类产品称为膳食补充剂(dietary supplements),在澳大利亚,这类产品称为补充医药产品(complementary medicines),在日本称为特定保健食品(FOSHU)。
基于对保健品不同的认识和理解,各国采取了不同的监督管理办法。
本篇从范畴、法规、管理机构、审批制度、标签声明、生产管理等方面对世界主要国家和组织在该方面的情况作以介绍和比较。
1 美国[1,5]1.1 范畴膳食补充剂是一种旨在补充膳食的产品(而非烟草),它可能含有一种或多种膳食成分,如维生素、矿物质、草本(草药) 或其它植物、氨基酸、一种用以增加每日总摄入量来补充膳食的食物成分或以上成分的浓缩品、代谢物、成分、提取物或组合产品等。
产品形式可分丸剂、胶囊、软胶囊、片剂、粉剂或液状物等多种形式[2]。
须标识为“膳食补充剂”,不能代替普通食物或作为膳食的唯一品种。
1.2 法规1994年美国通过了《膳食补充剂健康与教育法》(DSHEA),1997年修订通过了《食品药品管理现代化法案》(FDAMA)其中包含了一些专门针对膳食补充剂和膳食补充剂食物成分的条款。
DSHEA 的条款首先确定了膳食补充剂和膳食成分的范畴,建立了确保其安全性的新框架,明确了产品销售时所标识的文字要求,例举了几种有关功能和营养的声明,指出了有关成分和营养标签的要求,并委托FDA 负责起草有关GMP 条例。
DSHEA 还要求在国家卫生院(National Institutes of Health) 建立一个膳食补充剂标签委员会和膳食补充剂办公室[6]。
1.3 管理机构政府对膳食补充剂的监管部门之一是FDA,负责产品标签上的健康声明,包括包装、插入物和其它的促销材料管理[7],另一部门是联邦贸易委员会(FTC),主要负责管理产品广告上的健康声明[8]。
1.4 审批FDA对药品和食品添加剂的管理非常严格,上市前必须报送全部实验资料,如理化、微生物、毒理等,临床试验需要几年时间才能获批准。
但对膳食补充剂则不同,只要生产商提出上市要求并保证安全就可以了。
只是如果该产品在作为膳食补充剂之前已作为药品销售(相同摄入途径和相同剂量),那么其安全性要经FDA 审核。
另外,在1994 年10 月15 日之前未曾在美国上市的膳食成分称为“新膳食成分”,凡含有新成分的膳食补充剂,生产商或经销商必须在上市前75天向FDA提供资料,证明其是安全的,无致病与危害作用[9]。
FDA收到材料90天后公布这些材料,厂家就可以上市。
同时,厂家可以委托FDA请有关单位对新原料制定一个安全使用条例。
虽然FDA不对食品补充剂评审,但是对食品补充剂的安全性有质疑的权利,如有质疑,可向消费者公布,供消费者参考。
根据DSHEA,某种膳食补充剂如果它本身或其中某些成分在标签指示下食用或在正常情况下食用(如无食用指示) 具有明显的或过度的引起疾病或损伤的危险,那么它就视为搀假产品。
某种膳食补充剂中所含有的新膳食成分如缺乏充分资料,不足以保证其不会引起明显或过度的疾病或损伤危险,那么它也被视为搀假。
美国卫生与人类事务部(SHHS) 公布哪些膳食补充剂或食物成分对人类健康和安全造成直接危害。
但如同其它食品一样,保证产品上市前的安全性和标签的正确标识是生产者的责任。
1.5 标签及声明[11]目前对食品补充剂的标签内容有:①食品名称(内含几种);②净含量;③功能简介(商家自已说明,未经FDA批准原则上不能标注疗效)④使用方法(不能按照医药品标注剂量,只能标注建议量)⑤食品补充剂营养成分表;⑥辅助成分按重要性递减列出;⑦生产及经销商。
在美国,可用于传统食品和膳食补充剂标签上的声明有三类:健康声明、营养素含量声明以及结构—功能声明。
确保这些声称合法性的责任在于生产商和FDA,就广告而言,责任在于联邦贸易委员会FTC。
1.5.1 健康声明健康声称是在表述某种食品、食品成分或者膳食补充剂成分与减少某种疾病或与健康相关症状的危害之间存在某种联系。
FDA 通过三种方式监管何种健康声明可以用于某种食品或膳食补充剂的标签之上或用于标示某种食品或膳食补充剂。
(1)根据1990年《营养标示和教育法案》(NLEA),FDA要求在申请书中提出的健康声明的科学证据必须经过FDA仔细审查才能授权认可该食品和膳食补充剂的健康声明。
(2)1997年《食品药品管理现代化法案》(FDAMA) 规定健康声明应该基于美国政府科研机构或国家科学院发表的权威结论,并且在使用该声明之前通告FDA。
(3)2003年FDA发布《促进消费者营养状况的健康信息》的文件中规定了有限健康声明(qualified health claims),所谓有限健康声明指当科学证据的质量和强度低于要求FDA授权条件的情况下的健康声明。
此种声明FDA作了详细的限制,以保证给消费者的信息必须是准确的,不具有误导性。
具有健康声明的膳食补充剂具有比较明确的适应证,因此健康声明必须经过FDA的批准。
目前FDA已经批准了11个食品健康声明,主要是补钙与骨质疏松、膳食纤维与癌症及必血管病、脂类与癌症及心血管疾病、钠与高血压的关系、叶酸与新生儿神经管畸形的关系等。
这些声明可用在符合要求的产品,做为标签的补充。
1.5.2 营养素含量声明NLEA容许使用标签说明一种食品中营养素的水平,即营养素含量声明。
营养素含量声明可以使用诸如无、高和低(free、high、low)这样的词汇,描述产品中营养素或营养物质的水平,或与其它某种食品中的某种营养素水平进行比较,使用多于、减少和清淡的(more,reduced and light)这样的词汇来描述。
准确的定量表达(如200mg钠)可用于表述任何存在的营养素含量。
但是,如果使用“只含200mg钠”这样的句子来说明产品的低钠水平是不太合适的,需要有一个比较[11]。
1.5.3 结构—功能声明结构—功能声称描述了一种营养素或膳食成分影响正常人体结构或功能的作用,例如“钙可构建强壮骨骼”。
另外,还可以描述一种营养素或膳食成分维持结构或功能的作用方式,例如“纤维素维持肠道平衡”,或“抗氧化剂维持细胞完整”或者描述摄入营养素或膳食补充剂可达到健康良好状态。
结构—功能声称也可描述对营养素缺乏疾病的益处(如维生素C 和坏血病),只要说明这种疾病在美国的普遍性。
结构功能声明可以明确或含蓄地与某种疾病或某种与健康关联的病状相联系。
生产商有责任确保这些声称的准确性和真实性,它们无需得到FDA 的批准,生产商只须在产品上市之后30天内向FDA提交一份通知。
包括这种声称的膳食补充剂标签,必须说明该声称未经过FDA 评估。
还必须说明该产品不用于“诊断、处理、治疗或预防任何疾病”,因为只有药物才可以合法地进行这些声称[12]。
1.6 生产管理[13]FDA为了帮助消费者获得准确标示的非假昌的膳食补充剂,2003年发表了新的行政规则建议《膳食补充剂和膳食成分的制造、包装或保存的现行生产质量管理规范》(Current Good Manufacturing Practice in Manufacturing,Packing,or Holding Dietary Ingredients and Dietary Supplements)。
这是FDA第一次建立标准以保证膳食补充剂和膳食成分不被污染或搀假,保证正确标示出产品中的活性成分和其他成分,保证草药产品每批次之间的一致性。
cGMP适用于所有制造、包装或保存膳食补充剂或膳食成分的机构,包括参与检测、质量控制、包装和标示以及批发销售产品的单位。
也适用于制造、包装或保存销往美国的膳食补充剂或膳食成分的外国公司。
2 加拿大[1]2.1 范畴天然健康产品的定义有两个要素:物质要素和功能要素。
物质要素包括允许以Natural Health Product Regulation(NHP)销售的多种成分或混合物、顺势疗法药品或传统药品。
如植物、藻类、细菌、真菌或非人类的动物材料及以上的提取物,氨基酸,必需脂肪酸,生态制品,矿物质,几种维生素,天然物质的合成仿制品。
但不能含有抗生素,通过刺破皮肤给药的物质,《烟草法案》管理的物质,还有《食品和药品法案》管理的几种物质如放射性药品,生物制品和毒品。
天然健康产品的功能要素包括:①诊断、治疗、缓解或预防人类的一种疾病、不适、非正常的身体状态或其症状;②恢复或纠正人类的器官功能;③调节人类的器官功能,以维持或促进健康。
2.2 法规2004年1月,加拿大提出了天然健康产品(NHP)这一名词,并应用《天然健康产品管理条例》(Natural health product regulations)对NHP的销售、生产、包装、标示、进口、分装及贮存等活动进行监管。
2003年发表的《天然健康产品成品的质量证据》则提出了加拿大天然健康产品的质量技术要求,主要涉及天然健康产品成品的品种鉴别,纯度,数量和效力以及容许限量,以制定成品的质量标准。
2.3 管理机构加拿大卫生部新设立的天然健康产品指导委员会(NHPD)进行管理。
2.4 审批在加拿大销售一种天然健康产品首先应获得必要的产品许可证(product license)和场地许可证(site license)。
产品许可证将给予产品识别号码(product identification number)。
