物化(上)期中考试试卷(0219)2004 3 28
沪教版(全国)化学上册期中试卷(含答案)

沪教版(全国)化学上册期中试卷(含答案)一、选择题(培优题较难)1.下图是金元素在元素周期表中的信息示意图。
从图中获取的信息正确的是A.金元素属于非金属元素B.一个金原子的中子数为197C.一个金原子的核外电子数为118D.一个金原子中粒子总数为2762.下列滴管使用图示正确的是()A.取液时挤入空气B.代替玻璃棒进行搅拌C.向试管中滴加液体D.将残留溶液的滴管倒持3.质量守恒定律是自然界基本的规律之一。
下列装置及实验(天平未画出)能用来验证质量守恒定律的是()A.B.C.D.4.下列关于CO2的实验室制法及性质实验的说法不正确的是()A、制CO2的药品B、发生装置C、收集装置D、比较CO2与空气的密度A.A B.B C.C D.D5.在进行“氧气的实验室制取与性质”实验时,某同学制得的氧气不纯。
你认为可能的原因是( )A.用排水法收集O2时,集气瓶装满水B.用向上排空气法收集O2时,导管伸入到集气瓶的底部C.用排水法收集O2时,导管口冒出气泡,立即收集D.用排水法收集O2,收集满后,在水下盖上玻璃片6.某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如下图所示,下列关于该过程的说法正确的是()A.c代表氧气B.t2时刻,O2开始产生C.t1时刻,KMnO4开始分解D.起催化作用物质的质量一直保持不变7.逻辑推理是一种重要的化学思维方法,下列推理合理的是()A.在同一化合物中,金属元素显正价,则非金属元素一定显负价B.化学变化伴随着能量变化则有能量变化的一定是化学变化C.单质含有一种元素,则含有一种元素的纯净物一定是单质D.催化剂的质量在反应前后不变,则在反应前后质量不变的物质一定是该反应的催化剂8.现有 18.6g NaOH 和 Na2CO3固体混合物,已知钠元素与碳元素的质量比 23:3,则原混合固体中含有钠元素的质量为()A.9.2 g B.6.9 g C.4.6 g D.2.3 g9.如图所示有关二氧化碳的实验中,只与二氧化碳物理性质有关的实验是()A. B. C. D.10.下列微观模拟图中●和○分别表示不同元素的原子,其中表示单质的是A.B.C.D.11.关于碳循环和氧循环,下列说法不正确的是A.碳循环和氧循环分别是指二氧化碳和氧气的循环B.碳循环和氧循环过程中均发生了化学变化C.绿色植物的生长过程,既涉及碳循环,又涉及氧循环D.碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定12.下列实验操作正确的是A.塞紧胶塞B.贮存氧气C.过滤D.吹灭酒精灯13.下列关于燃烧现象的解释或分析正确的是()A.图a中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间B.图b中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点C.图c中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动D.由图d中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火14.科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为 CH2O),该反应过程的微观示意图如下。
上册期中化学试卷(word解析版)

上册期中化学试卷(word解析版)一、选择题(培优题较难)1.正确记录实验数据是一项实验基本技能,某同学记录的实验数据错误的是A.用托盘天平称取2.9gNaCl固体B.用10mL量筒量取8.3mL蒸馏水C.在10mL试管中倒入约3mL蒸馏水进行加热D.用温度计测得水温为25.15C2.豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其中含量最多的是亮氨酸(C6H13NO2),关于亮氨酸的说法正确的是()A.亮氨酸是氧化物B.亮氨酸中碳元素的质量分数为27.3%C.一个亮氨酸分子由22个原子构成D.亮氨酸中碳、氢、氮、氧四种元素的质量比为6:13:1:23.下列实验操作正确的是A.塞紧橡皮塞B.加热液体C.取用液体D.读出液体的体积4.下列有关氧气的说法,错误的是()A.氧气能支持燃烧B.细铁丝在氧气中燃烧,生成氧化铁C.在通常状况下,氧气的密度比空气大D.氧气的化学性质比较活泼,能跟许多物质发生反应5.如图是四种粒子的结构示意图,下列有关说法正确的是()A.④表示的粒子属于金属元素B.①表示的粒子在化学反应中易失电子C.①②③④表示四种不同元素D.②④所表示的粒子化学性质相似6.下列关于CO2的实验室制法及性质实验的说法不正确的是()A、制CO2的药品B、发生装置C、收集装置D、比较CO2与空气的密度A.A B.B C.C D.D7.下列关于空气的说法中,不正确的是( )A.工业上采用分离液态空气法获得氧气B.二氧化硫是空气污染物之一C.空气中氧气质量占空气质量的21% D.空气中的氧气来源于绿色植物的光合作用8.在密闭容器内,有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法错误的是()A.该反应符合质量守恒定律B.生成的甲,丙两物质的质量比为8:1C.乙可能是该反应的催化剂D.参加反应的丁的质量等于生成的甲和丙的质量之和9.在一密闭的容器中,一定质量的碳粉与过量的氧气在点燃的条件下充分反应,容器内各相关量与时间(从反应开始计时)的对应关系正确的是( )A.B.C.D.10.下列符号中,表示两个氧分子的是A.2O B.O2C.O2―D.2O211.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是A.参加反应的甲和乙质量比为2:7 B.丙可能是该反应的催化剂C.丁一定是化合物D.x的值是712.根据图中提供的信息判断,下列说法正确的是A.③④属于同种元素B.②表示的元素在形成化合物时化合价为+1 价C.①③的化学性质相似D.硒元素的相对原子质量为 78.96 g13.科学理论在传承中不断发展,科学家们传承前人的正确观点,纠正错误观点,形成科学理论,关于原子结构的学说有:①在球体内充斥正电荷,电子镶嵌其中②原子是可分的③原子呈球形④原子中有带负电的电子⑤原子中有带正电的原子核⑥原子核很小,但集中了原子的大部分质量其中经过卢瑟福传承和发展后形成的观点是()A.②③④⑤⑥B.①②③④C.④⑤⑥D.⑤⑥14.从水分子分解示意图中获得以下信息,其中不正确的是()A.水是由氢元素和氧元素组成的B.化学反应前后元素的种类不变C.在化学变化中,分子可分,原子也可分D.一个水分子由两个氢原子和一个氧原子构成15.民间常用川乌、草乌泡制药酒。
上海市化学上册期中试卷(解析版)
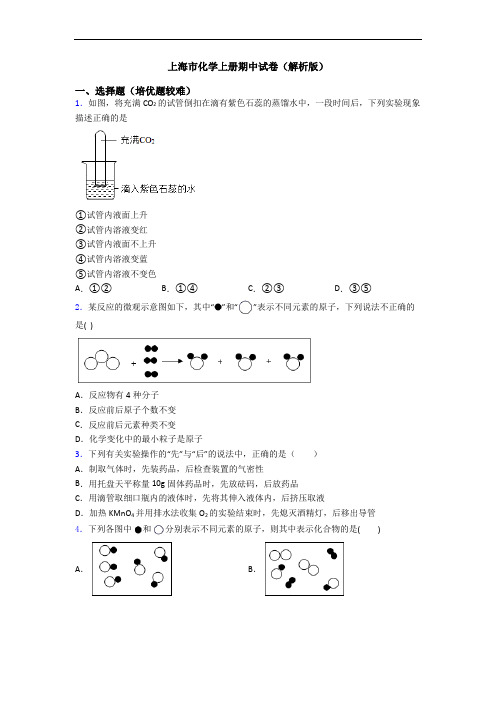
上海市化学上册期中试卷(解析版)一、选择题(培优题较难)1.如图,将充满CO2的试管倒扣在滴有紫色石蕊的蒸馏水中,一段时间后,下列实验现象描述正确的是①试管内液面上升②试管内溶液变红③试管内液面不上升④试管内溶液变蓝⑤试管内溶液不变色A.①②B.①④C.②③D.③⑤2.某反应的微观示意图如下,其中“”和“”表示不同元素的原子,下列说法不正确的是( )A.反应物有4种分子B.反应前后原子个数不变C.反应前后元素种类不变D.化学变化中的最小粒子是原子3.下列有关实验操作的“先”与“后”的说法中,正确的是()A.制取气体时,先装药品,后检查装置的气密性B.用托盘天平称量10g固体药品时,先放砝码,后放药品C.用滴管取细口瓶内的液体时,先将其伸入液体内,后挤压取液D.加热KMnO4并用排水法收集O2的实验结束时,先熄灭酒精灯,后移出导管4.下列各图中和分别表示不同元素的原子,则其中表示化合物的是( )A.B.C.D.5.最近,我国科学家成功合成新型催化剂,将CO2高效转化为甲醇(CH3OH)。
这不仅可以缓解碳排放引起的温室效应,还将成为理想的能源补充形式。
该化学反应的微观过程如下图所示。
下列说法正确的是A.该反应中四种物质均为化合物B.反应前后H元素的化合价不变C.参加反应的甲、乙分子个数比为1:3D.反应前后原子数目发生改变6.碳12是指含6个中子的碳原子。
下列对氧16和氧18两种氧原子的说法正确的是A.质子数相同B.质量相同C.电子数不相同D.16和18表示原子个数7.“天宫二号”太空舱利用NiFe2O4作催化剂将航天员呼出的二氧化碳转化为氧气。
已知Fe元素的化合价为+3价,则Ni元素的化合价为()A.+1 B.+2 C.+3 D.+48.下列加热高锰酸钾制取氧气的部分操作示意图中,正确的是A.检查装置气密性B.加热立即收集C.收满后移出集气瓶 D.结束时停止加热9.元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,其中X、Y、Z 代表三种不同的元素。
大学化学专业《大学物理(上册)》期中考试试卷 附答案

大学化学专业《大学物理(上册)》期中考试试卷附答案姓名:______ 班级:______ 学号:______考试须知:1、考试时间:120分钟,本卷满分为100分。
2、请首先按要求在试卷的指定位置填写您的姓名、班级、学号。
一、填空题(共10小题,每题2分,共20分)1、一长直导线旁有一长为,宽为的矩形线圈,线圈与导线共面,如图所示. 长直导线通有稳恒电流,则距长直导线为处的点的磁感应强度为___________;线圈与导线的互感系数为___________。
2、长为的匀质细杆,可绕过其端点的水平轴在竖直平面内自由转动。
如果将细杆置与水平位置,然后让其由静止开始自由下摆,则开始转动的瞬间,细杆的角加速度为_____,细杆转动到竖直位置时角加速度为_____。
3、气体分子的最可几速率的物理意义是__________________。
4、若静电场的某个区域电势等于恒量,则该区域的电场强度为_______________,若电势随空间坐标作线性变化,则该区域的电场强度分布为 _______________。
5、一电子以0.99 c的速率运动(电子静止质量为9.11×10-31kg,则电子的总能量是__________J,电子的经典力学的动能与相对论动能之比是_____________。
6、真空中有一半径为R均匀带正电的细圆环,其电荷线密度为λ,则电荷在圆心处产生的电场强度的大小为____。
7、一根长为l,质量为m的均匀细棒在地上竖立着。
如果让竖立着的棒以下端与地面接触处为轴倒下,则上端到达地面时细棒的角加速度应为_____。
8、一个质点的运动方程为(SI),则在由0至4s的时间间隔内,质点的位移大小为___________,在由0到4s的时间间用内质点走过的路程为___________。
9、两个相同的刚性容器,一个盛有氧气,一个盛氦气(均视为刚性分子理想气体)。
开始他们的压强和温度都相同,现将3J的热量传给氦气,使之升高一定的温度。
上海第四中学化学初三化学上册期中化学试卷

上海第四中学化学上册期中化学试卷一、选择题(培优题较难)1.下列关于燃烧现象的解释或分析正确的是()A.图a中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间B.图b中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点C.图c中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动D.由图d中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火2.下列实验设计不能达到其对应实验目的的是( )A.测定空气里氧气的含量B.检查装置的气密性C.验证质量守恒定律D.证明CO2密度比空气的大3.化学是在分子、原子的层次上研究物质的性质、组成、结构与变化规律的科学。
下图是某化学反应的微观示意图,下列说法正确的是A.反应前后分子的个数不变B.生成物有三种C.反应前后汞原子和氧原子的个数不变D.是保持氧气化学性质的最小粒子4.某纯净物3g 在氧气中完全燃烧,生成8.8g 二氧化碳和5.4g 水。
下列说法不正确的是 A .该纯净物中含有C 、H 元素,不含O 元素B .该反应中2O 和2CO 的质量比为14:11C .该反应中2O 和2H O 的分子数之比为7:6D .该纯净物中C 、H 原子的个数比为1:45.甲、乙、丙、丁四位同学分别进行了有关化学反应A +B =C 的四组实验,各物质的质量如下表所示,已知四位同学取的A 和B 的总质量均为10g ,且反应均完全进行。
下列选项不正确的是A/g B/g C/g 甲7 3 9 乙6 4 9 丙X Y 6 丁 5 5 ZA .Y 可能等于8B .X 可能等于4C .X 可能等于8D .Z 一定等于7.56.运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )A .因为化学变化都遵循质量守恒定律,所以质量不发生改变的变化一定是化学变化B .水和过氧化氢的组成元素相同,则两者的化学性质相同C .Na +、Mg 2+、Cl -的最外层电子数均为8,由此得出离子的最外层电子数均为8D .过氧化氢溶液加催化剂的反应速率快,说明催化剂可以改变反应速率7.化学实验操作应严谨规范,下列操作符合要求的是A .看B .听C .闻D . 吹8.正确记录实验数据是一项实验基本技能,某同学记录的实验数据错误的是A .用托盘天平称取2.9gNaCl 固体B .用10mL 量筒量取8.3mL 蒸馏水C .在10mL 试管中倒入约3mL 蒸馏水进行加热D .用温度计测得水温为25.15C9.硼是作物生长必需的微量营养元素,硼元素的相关信息如图所示。
高二年级化学上学期期中试卷

高二年级化学上学期期中试卷世界是由物质组成的,化学那么是人类用以看法和改造物质世界的主要方法和手腕之一,小编预备了高二年级化学上学期期中试卷,希望你喜欢。
一、选择题(每题只要一个正确答案,每题3分,此题共54分)1、以下电池任务时,O2在正极放电的是2、以下说法中,正确的选项是A.反响产物的总能量大于反响物的总能量时,△H 0B.在其他外界条件不变的状况下,运用催化剂,可以改动化学反响停止的方向C.0、0的反响在温度低时不能自发停止D.一个化学反响的△H仅与反响的起始形状和反响的最终形状有关,与反响途径有关3、以下说法正确的选项是A.Al-Mg合金焊接进程中运用的维护气为N2B.工业上可采用电解熔融NaCl的方法制备金属钠C.将0.5molN2和1.5molH2充入一密闭容器中充沛反响,放出热量19.6KJ,那么该热化学方程式为N2(g) + 3 H2(g) 2NH3(g)△H=-39.2 KJmo-1D.:2H2(g) + O2(g) 2H2O(g) △H= 486 KJmol-1 ,那么H2 的熄灭热△H为243 KJmol-14、以下各组物质的颜色变化,可用勒夏特列原了解释的是A.新制的氯水在光照条件下颜色变浅B.H2、I2、HI平衡混合气加压后颜色变深x kb 1C.氯化铁溶液加铁粉振荡后颜色变浅D.参与催化剂有利于氨的催化氧化5、只改动一个影响要素,平衡常数K与化学平衡移动的关系表达错误的选项是A.K值不变,平衡能够移动B.K值变化,平衡一定移动C.平衡移动,K值能够不变D.平衡移动,K值一定变化6、某反响进程能质变化如图所示,以下说法不正确的选项是A.反响进程b有催化剂参与B.该反响为放热反响,热效应等于△HC.参与催化剂,可改动该反响的活化能D.有催化剂的条件下,反响的活化能等于E1+E27、:C(s)+O2(g)=CO2 (g) △H1CO2(g)+C(s)=2CO(g) △H22CO(g)+O2(g)=2CO2(g) △H34Fe(s)+3O2(g)=2Fe2O3(s) △H43 CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s) △H5以下关于上述反响焓变的判别正确的选项是A.△H10,△H3B.△H20,△H30C.△H1=△H2+△H3D.△H3=△H4+△H58、:C(s)+H2O (g)=CO(g)+H2(g) H=akJmol-12C(s)+O2(g)=2CO(g) H= -220kJmol-1H-H、O=O和O-H键的键能区分为436、496和462kJmol-1,那么a为A.-332B.-118C.+350D.+1309、以下表达错误的选项是A.生铁中含有碳,抗腐蚀才干比纯铁弱B.用锡焊接的铁质器件,焊接处易生锈C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液D.电解精炼铜时,电解质溶液中铜离子浓度减小10、有A、B、C、D、E五块金属片,停止如下实验:①A、B 用导线相连后,同时浸入稀硫酸溶液中,A为负极;②C、D用导线相连后,同时浸入稀硫酸溶液中,电流由D导线③A、C相连后,同时浸入稀硫酸溶液中,C极发生少量气泡;④B、D用导线相连后,同时浸入稀硫酸溶液中,D极发作氧化反响;⑤用惰性电极电解含B离子和E离子的溶液,E先析出。
物化上册期中考试试卷

1. 对于热力学能是系统状态的单值函数的概念,下列哪种说法是错误的 (C )A. 系统处于一定的状态,具有一定的热力学能B. 对应于某一状态,热力学能只能有一个数值不能有两个以上的数值C. 状态发生变化,热力学能也必然变化D. 对应于一个热力学能,可以有多个状态2. 对于任一循环过程 ( C )A. W = 0B.Q = 0C. Q + W = 0D. Q = W3. 实际气体的节流膨胀过程中,下列哪一组的描述是正确的 ( A )A. Q=0 △H=0 △P <0 △T≠0B. Q=0 △H <0 △P >0 △T >0C. Q >0 △H=0 △P <0 △T <0D. Q <0 △H=0 △P <0 △T≠04. 热力学第一定律中的 W 是指_CA. 体积功B. 非体积功C. 各种形式功之和D. 机械功5. 公式“ pV γ = 常数” 适用于( D )A. 任何气体的绝热过程B. 理想气体的绝热过程C. 理想气体的可逆过程D. 理想气体的绝热可逆过程6. 公式“ W = C V (T 2-T 1) ”适用于( B )A. 任何气体的绝热过程B. 理想气体的绝热过程C. 理想气体的任何过程D. 理想气体的绝热可逆过程7. 下列各量中哪个是偏摩尔量( A )(A ) (B ) (C ) (D ) 8.熵是系统混乱度的量度,下列说法不正确的是( D )(A )同一种物质的S m (g) > S m (l) > S m (s)(B )同种物质温度越高熵值越大(C )分子内含有原子数越多熵值越大(D )0 K 时任何物质的熵值为零9.25℃时,将11.2升O 2与11.2升N 2混合成11.2升的混合气体,该过程( C )(A)、∆S > 0,∆G < 0 (B)、∆S < 0,∆G < 0(C)、∆S = 0,∆G = 0 (D)、∆S = 0,∆G < 010.在一个绝热刚瓶中,发生一个放热的分子数增加的化学反应,那么( C )(A) Q > 0,W > 0,∆U > 0 (B) Q = 0,W = 0,∆U < 0(C) Q = 0,W = 0,∆U = 0 (D) Q < 0,W > 0,∆U < 011. 冬季建筑施工中,为了保证施工质量,常在浇注混凝土时加入少量盐类,其主要作用是?( C )(A) 增加混凝土的强度 (B) 防止建筑物被腐蚀(C) 降低混凝土的固化温度 (D) 吸收混凝土中的水份12.液体A 与B 混合形成非理想溶液,当A 与B 分子间作用力大于同种分子之间的作用力时,该混合物对拉乌尔定律而言产生( B )(A )正偏差 (B )负偏差 (C )不产生偏差 (D )无法确定13. 在隔离体系中发生一个自发过程,则ΔG 应为 ( D )一、单项选择题(每小题2分,共30分),,C B B T p n S n ≠⎛⎫∂ ⎪∂⎝⎭,,C B B T V n F n ≠⎛⎫∂ ⎪∂⎝⎭,,C B T p n H V ≠∂⎛⎫ ⎪∂⎝⎭,,C BB B T p n n μ≠⎛⎫∂ ⎪∂⎝⎭(A) ΔG < 0 (B) ΔG > 0 (C) ΔG =0 (D) 不能确定14. (1) 溶液的化学势等于溶液中各组分的化学势之和 D(2) 对于纯组分,则化学势等于其Gibbs 自由能(3) 理想溶液各组分在其全部浓度范围内服从Henry 定律(4) 理想溶液各组分在其全部浓度范围内服从Raoult 定律上述诸说法正确的是:( D )A 、 (1),(2)B 、 (2),(3)C 、 (2),(4)D 、 (3),(4)15. 盐碱地的农作物长势不良,甚至枯萎,其主要原因是: ( D )(A) 天气太热 (B) 很少下雨 (C) 肥料不足(D) 水分倒流1. 焦耳-汤姆孙系数def T J -μ ,μJ-T >0表示节流膨胀后温度将降低 。
第一学期期中物理化学试卷及答案

第一学期期中考试《物理化学》卷一、选择题(每小题3分,共10题,共30分)1、一定量的理想气体从同一初态分别经历等温可逆膨胀、绝热可逆膨胀到具有相同压力的终态,终态体积分别为V1,V2,则:( )(A) V1> V2(B) V1< V2(C) V1= V2(D) 无法确定2、关于热和功, 下面的说法中, 不正确的是( )(A) 功和热只出现于系统状态变化的过程中, 只存在于系统和环境间的界面上(B) 只有在封闭系统发生的过程中, 功和热才有明确的意义(C) 功和热不是能量, 而是能量传递的两种形式, 可称之为被交换的能量(D) 在封闭系统中发生的过程中, 如果内能不变, 则功和热对系统的影响必互相抵消3、下列过程均为等温等压过程,根据公式d G = -S d T + V d p计算得ΔG = 0,此结论能用于下述何过程( )(A) -5C、pθ、冰→-5C、pθ、水(B) 等温、等压下,W f= 0 的化学反应 A + B→C + D(C) 等温、等压下食盐溶解于水(D) 100C、pθ、水→100C、pθ、水气4、在下列五个物理量中:(1) (V/n B)T,p,n c b≠(2) (B/n B)T,p,n c b≠(3) (H/n B)s,p,n c b≠(4) (A/n B)T,p,n c b≠(5) (G/n B)T,p,n c b≠(A) (1)、(4)、(5) 是偏摩尔量;(1)、(3) 是化学势(B) (1)、(4)、(5) 是偏摩尔量;(3)、(5) 是化学势(C) (1)、(4)、(5) 是偏摩尔量;(2)、(5) 是化学势(D) (1)、(2)、(4) 是偏摩尔量;(3)、(5) 是化学势上述结论正确的是( ) 5、在101325 kPa 压力下,mol H2O(l) 由10C升至50C,已知H2O(l)的平均摩尔定压热容为J·K-1·m ol-1,则此过程中体系的熵变为:( ) (A) J·K-1(B) 18225 kJ·K-1(C) J·K-1(D) J·K-16、石墨(C)和金刚石(C)在25C,101325Pa下的标准燃烧焓分别为kJ·mol-1和$(金刚石, 298 K)为:( )kJ·mol-1,则金刚石的标准生成焓Δf Hm(A) kJ·mol-1(B) kJ·mol-1(C) kJ·mol-1(D) kJ·mol-17、下列叙述中,不具有可逆特征的是:( )(A) 过程的每一步都接近平衡态,故进行得无限缓慢(B) 沿原途径反向进行时,每一小步系统与环境均能复原(C) 过程的初态与终态必定相同(D) 过程中,若做功则做最大功,若耗功则耗最小功8、恒温下,单一组分的过冷液体的化学势比其固体的化学势:( )(A) 高(B) 低(C) 相等(D)不可比较9、两只烧杯各有1 kg水,向A杯中加入mol蔗糖,向B杯内溶入mol NaCl,两只烧杯按同样速度冷却降温,则有( )(A) A杯先结冰(B) B杯先结冰(C) 两杯同时结冰(D) 两杯都不会结冰10、当溶液中溶质浓度采用不同浓标时,下列说法中哪一个是正确的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物理化学期中考试试卷(02019)2004 3 28姓名 学号 分数一、选择题(每小题2分,共26分):请将一个正确答案写在括号内。
1、下列过程中H ∆为零的是( ) (1)绝热恒压没有非体积功时发生化学反应; (2)绝热恒容没有非体积功时发生化学反应; (3)实际气体不可逆循环过程; (4)理想气体不可逆恒温压缩。
A 1、2、3;B 2、3、4;C 3、4、1;D 4、1、2。
2、下列说法中正确的是( )(1)不做功的封闭体系未必是隔离体系; (2)吸热又做功的体系是封闭体系;(3)与环境有化学作用的体系是敞开体系;(4)封闭的透热壁容器内,用只能允许水透过的半透膜将高分子水溶液与纯水隔开,高分子水溶液为敞开体系,而高分子水溶液与纯水合在一起则是封闭体系 A 1、2、3; B 2、3、4; C 3、4、1; D 4、1、2。
3、对下列关系的描述正确的是( )(1) O∆m c H (石墨,s )=O∆m f H (2CO ,s );(2) O∆m c H (2H ,g )=O∆m f H (O H 2,g );(3) O∆m c H (2SO ,g )=0;(4) ())(),(,525252OH H C H l OH H C H g OH H C H m vap m f m f OOO∆+∆=∆A 1、2、3;B 2、3、4;C 3、4、1 ;D 4、1、2。
4、下列过程中当温度升高时G ∆增加的是( )(1)MgCO 3 (s) → MgO (s) + CO 2 (g); (2)NH 3 (g) + HCl (g) → NH 4Cl (s); (3)NaOH (s)溶于水; (4)N 2 (g) 与O 2 (g)的混合。
A 1、2、3; B 2、3、4; C 3、4、1 ; D 4、1、2。
5、下列偏微分中属于化学势的是( ) A ij n P T i nU ≠⎪⎪⎭⎫ ⎝⎛∂∂,,; B ij n P T i n H ≠⎪⎪⎭⎫ ⎝⎛∂∂,,; C ij n P T i n F ≠⎪⎪⎭⎫⎝⎛∂∂,,; D ij n P T i n G ≠⎪⎪⎭⎫ ⎝⎛∂∂,,6、下列偏微分中属于偏摩尔量的是( ) A ij n V S i nU ≠⎪⎪⎭⎫ ⎝⎛∂∂,,; B ij n P S i n H ≠⎪⎪⎭⎫ ⎝⎛∂∂,,; C ij n V T i n F ≠⎪⎪⎭⎫⎝⎛∂∂,,; D ij n P T i n G ≠⎪⎪⎭⎫ ⎝⎛∂∂,,7、对于双原子分子的理想气体,SV T ⎪⎭⎫⎝⎛∂∂等于( )A VT 35; B VT 52-; CTV 35; D VT 57-8、公式.const pV=γ适用于( )A 任何气体的绝热变化;B 理想气体的任何绝热变化;C 理想气体的任何可逆变化;D 理想气体的绝热可逆变化。
9、在理想气体的S ~T 图上,任一条恒容线与任一条恒压线的斜率之比为( )A()()0=∂∂∂∂pT S VT S ; B()()∞=∂∂∂∂pT S VT S ; C()()Vp pT S V T S C C =∂∂∂∂; D()()pV pT S VT S C C =∂∂∂∂10、一个由气相变为凝聚相的化学反应在恒温恒容下自发进行,有关的熵变为( ) A 0,0<∆>∆环境体系S S ; B 0,0>∆<∆环境体系S S C 0,0=∆>∆环境体系S S ; D 0,0>∆>∆环境体系S S11、恒温恒压下,在A 与B 组成的均相体系中,若A 的偏摩尔体积随浓度的改变而增加时,则B 的偏摩尔体积将( )A 增加;B 减小;C 不变;D 不确定12、恒温时,B 溶解于A 中形成溶液。
若纯B 的摩尔体积大于溶液中B 的偏摩尔体积,则增加压力将使B 在A 中的溶解度( )A 增加;B 减小;C 不变;D 不确定13、理想气体与温度为T 的大热源接触作等温膨胀吸热Q ,所作的功是变到相同终态的最大功的50%,则体系的熵变为( )A Q/T ;B 2Q/T ;C 3Q/T ;D 4Q/T二、判断题(每小题2分,共24分):请将判断结果写在括号内(+为正确;-为错误)。
1、通过绝热膨胀可以使理想气体的温度降低( )。
2、通过节流过程可以使理想气体的温度降低( )。
3、恒温过程就是既不吸热又不放热的过程( )。
4、某一体系从始态经一个绝热不可逆过程到达终态,为了计算某些热力学函数的变量,可以设计一个绝热可逆过程,从同一始态出发到同一终态( )。
5、绝热循环过程一定是可逆循环过程( )。
6、不可逆过程的熵永不减少( )。
7、熵值不可能为负值( )。
8、任何等温循环都不能把热转化为功( )。
9、不可逆等温循环一定耗功( )。
10、可逆等温循环既不能把热转化为功,也不能把功转化为热( )。
11、不可逆过程一定是自发的,自发过程一定是不可逆的( )。
12、功可以全部变为热,但热一定不能全部转化为功( )。
三、证明题(每小题5分,共20分) 1、证明Maxwell 关系VS S P V T ⎪⎭⎫⎝⎛∂∂-=⎪⎭⎫ ⎝⎛∂∂。
2、证明p TT V T V p H⎪⎭⎫ ⎝⎛∂∂-=⎪⎪⎭⎫⎝⎛∂∂。
3、比较绝热可逆膨胀与节流过程两种获得低温的方法,哪一种降温效果较好?4、范氏气体经joule 实验后,气体的温度如何变化?计算题(每小题10分,共30分)1、计算下列各过程的熵变(A、B均为双原子分子理想气体)。
(a)n A=1mol n A=2mol n A = 3molT, V T, V T, 2V(b) n A=1mol n B=2mol 绝热n A + n BT A=300K, V T B=400K, V T, 2V2、Zn(l)从419.5℃到907.0℃范围内之热容为113,]1085.466.29[---⋅⋅⨯+=molKJ T C m p ,单原子气体锌的热容为()25,,R g Zn C m p =,正常沸点K T b 1180=,计算773K 时Zn 之蒸气压,假设蒸气为理想气体。
3、汞的正常熔点234.28K 的1367.2-O⋅=∆molkJ H m l s ,设液体汞和过冷液体汞的11,28.28--O ⋅⋅=molKJ C m p ,并认为它是常数,且()11210.6915.223,,--O⋅⋅=K molJ K l Hg S m 。
将1 mol 、223.15 K 、100 kPa 的过冷液体汞,经绝热等压过程相变为234.28 K 的液体汞与固体汞的平衡体系,请计算: (1)1 mol 汞体系由始态到终态的焓变; (2)液体汞变为固体汞的量; (3)体系汞的熵变; (4)体系汞的Gibbs 自由能(5)上述过程是否为不可逆过程?请指明你所用的判据。
Additional problems (10 points)1、J. Gao and J. H. Weiter in their study of the origin of stress on the atomic level in dense polymer systems [Science,266 (1994)748], observe that the tensile force required to maintain the length, l, of a long linear chain of N freely joined links, each of length a, can be interpreted as arising from an entropic spring. For such a chain, S(l) = -3kl2/2Na2 + C, where k is the Boltzmann constant and C is a constant. Using thermodynamic relations show that the tensile force obeys Hook’s law, f = -k f l, if we assume that the energy U is independent of l.2、 Nitric acid hydrates have received much attention as possible catalysts for heterogeneous reactions which bring about the Antarctic ozone hole. Worsnop et al. investigated the thermodynamic stability of these hydrates under conditions typical of polar winter stratophere [Science , 259 (1993)71]. They reported thermodynamic data for the sublimation of mono-, di-, and trihydrates to nitric acid and water vapors, )()()(2323g O nH g HNO s O nH HNO+→⋅,for n = 1, 2, and 3. Given O ∆m r G and O ∆m r H for these reactants at 220K, compute O∆m r G at190K.n 1 2 3O∆m r G (kJ/mol) 46.2 69.4 93.2 O∆m r H(kJ/mol) 127 188 237。
