国际校准品目录(诊断试剂)
体外诊断试剂校准品(物)、质控品(物)研究技术指导原则

体外诊断试剂校准品(物)、质控品(物)研究技术指导原则体外诊断试剂校准品(物)(包括真实度控制品)、质控品(物)(简称校准品、质控品)是实现体外诊断试剂临床检测及监督检验结果准确一致的主要工具,也是保证量值有效传递的计量实物标准。
校准品、质控品研究技术资IFCC)见(不限于):一、范围应明确陈述本标准规范的对象和所涉及的方面,指明使用的界限。
二、规范性引用文件应包括引导语和规范性引用文件的一览表。
一览表中引用文件的排列顺序为:国家标准、行业标准、国际标准及规范性文件等。
例如:下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本应注明校准品赋值及不确定度、质控品的赋值及允许范围,非定值质控品没有指定的参考范围,可以通过在标贴上标示目标浓度(如:低、高、中)表示。
(三)规格应注明规格。
(四)用途应详细注明校准品、质控品的预期用途。
(五)稳定性应提供包括至少一批成品在实际储存条件下保存至有效期后的稳定性、开瓶稳定性研究资料,必要时应当提供加速破坏性试验资料。
该资料可放入产品求。
全性资料。
生物安全性检测应采用国家药品监督管理机构认可的、不低于国家法定用于血源筛查体外诊断试剂灵敏度的检测试剂,对校准品、质控品的HBsA g、HIV抗体、HCV抗体等进行检测。
该资料可放入产品标准的规范性附录中。
(八)校准品、质控品主要原材料、工艺及半成品等质量控制对于按第三类产品申请注册的校准品、质控品,其主要原材料、工艺及半成品等质量控制研究资料应参照《生物制品规程》(2000版)编制。
校准品、质控品生产企业应具备相应的专业技术人员、相适应的仪器设备和生产环境,获得《医疗器械生产许可证》;应当按照《体外诊断试剂生产实施细则(试行)》建立相应的质量管理体系,形成文件和记录,加以实施并保1国生物制品主要原辅材料质控标准》上规定的标准要求,并且要适合于本企业的生产。
《体外诊断试剂分类目录》及《关于实施〈体外诊断试剂分类目录〉有关事项的通告》解读

《体外诊断试剂分类目录》及《关于实施〈体外诊断试剂分类目录〉有关事项的通告》解读文章属性•【公布机关】国家药品监督管理局,国家药品监督管理局,国家药品监督管理局•【公布日期】2024.05.11•【分类】法规、规章解读正文《体外诊断试剂分类目录》及《关于实施〈体外诊断试剂分类目录〉有关事项的通告》解读近日,国家药监局印发《关于发布体外诊断试剂分类目录的公告》(2024年第58号,以下简称《分类目录》)及《关于实施〈体外诊断试剂分类目录〉有关事项的通告》(2024年第17号,以下简称《实施通告》)。
现就《分类目录》修订背景及相关内容说明如下:一、《分类目录》修订背景分类管理是医疗器械监管的重要基础性制度,分类目录是分类管理的重要组成部分。
《6840体外诊断试剂分类子目录(2013版)》(以下简称2013版目录)于2013年发布,后续又发布了《关于过敏原类、流式细胞仪配套用、免疫组化和原位杂交类体外诊断试剂产品属性及类别调整的通告》(国家食品药品监督管理总局通告2017年第226号,以下简称226号通告)和《关于调整〈6840体外诊断试剂分类子目录(2013版)〉部分内容的公告》(国家药品监督管理局公告2020年第112号,以下简称112号公告),对体外诊断试剂产品管理类别予以明确。
上述文件对体外诊断试剂的监管和行业发展起到了积极的推动作用。
近年来,体外诊断技术和产业快速发展,新技术、新方法、新靶标不断涌现,产品数量和种类急剧上升。
2013版目录、226号通告和112号公告不能完全满足监管和产业需求,且部分产品管理类别与2021年10月发布的《体外诊断试剂分类规则》(以下简称《分类规则》)不完全一致。
因此,国家药监局组织开展了《分类目录》修订工作。
二、《分类目录》结构《分类目录》以《分类规则》为依据,根据体外诊断试剂的特点编制而成,《分类目录》结构由"一级序号、一级产品类别、二级序号、二级产品类别、预期用途、管理类别"六个部分组成,其中"一级产品类别"主要依据《分类规则》设立,共25个;"二级产品类别"是在一级产品类别项下的进一步细化,主要根据检测靶标设置,原则上不包括方法或原理,共1852项。
6840体外诊断试剂分类子目录部分内容调整表
用于检测泌乳素,临床上用于泌乳素瘤的治疗监测。
II类
27
206
降钙素检测试剂
用于检测人体样本中的降钙素(CT),临床上主要用于甲状腺髓样癌、小细胞肺癌的辅助诊断。
Ⅲ类
用于检测降钙素,临床上用于甲状腺髓样癌、小细胞肺癌的治疗监测。
II类
28
207
芳香基硫酸酯酶检测试剂
用于检测人体样本中的芳香基硫酸酯酶,临床上主要用于乳腺癌、结直肠癌的辅助诊断。
附件
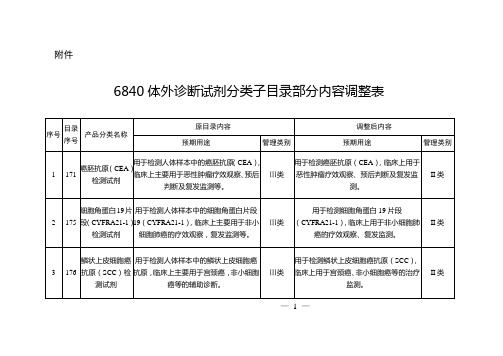
6840体外诊断试剂分类子目录部分内容调整表
序号
目录序号
产品分类名称
原目录内容
调整后内容
预期用途
管理类别
预期用途
管理类别
1
171
癌胚抗原(CEA)检测试剂
用于检测人体样本中的癌胚抗原(CEA),临床上主要用于恶性肿瘤疗效观察、预后判断及复发监测等。
Ⅲ类
用于检测癌胚抗原(CEA),临床上用于恶性肿瘤疗效观察、预后判断及复发监测。
Ⅲ类
用于检测癌抗原15-3(CA15-3),临床上用于乳腺癌治疗疗效及预后观察。
II类
8
181
糖类抗原19-9(CA19-9)检测试剂
用于检测人体样本中的糖类抗原19-9(CA19-9),临床上主要用于胰腺等消化道恶性肿瘤的辅助诊断,疗效监测等。
Ⅲ类
用于检测糖类抗原19-9(CA19-9),临床上用于胰腺等消化道恶性肿瘤的疗效监测。
II类
21
196
胃蛋白酶原(PG)Ⅱ检测试剂
用于检测人体样本中的胃蛋白酶原(PG)Ⅱ。PGⅡ的浓度水平及PGI/Ⅱ的比值可用于胃癌的辅助诊断。
Ⅲ类
用于检测胃蛋白酶原(PG)Ⅱ,临床上用于监测PGII的浓度水平及PGI/Ⅱ的比值可用于胃癌的治疗监测。
特殊物品海关检验检疫名称和商品编号对应名录

附件特殊物品海关检验检疫名称和商品编号对应名录序号检验检疫名称检验检疫编码HS商品名称HS商品编号1人类核酸及其盐2934993010999人类核酸及其盐29349930102其他核酸及其盐(医学或生命科学用途)2934993090101其他核酸及其盐29349930903其他核酸及其盐(《人间传染的病原微生物名录》内一类病原微生物的核酸(两用物项管制遗传物质除外))2934993090401其他核酸及其盐29349930904其他核酸及其盐(《人间传染的病原微生物名录》内二类病原微生物的核酸(两用物项管制遗传物质除外))2934993090402其他核酸及其盐29349930905其他核酸及其盐(《人间传染的病原微生物名录》内三类病原微生物的核酸(两用物项管制遗传物质除外))2934993090403其他核酸及其盐29349930906其他核酸及其盐(《人间传染的病原微生物名录》内四类病原微生物的核酸)2934993090404其他核酸及其盐29349930907其他核酸及其盐(新发传染病或名录外再现传染病病原微生物的核酸)2934993090405其他核酸及其盐29349930908其他多肽激素及衍生物和结构类似物(包括蛋白激素、糖蛋白激素及其衍生物和结构类似物)(医学科研用)2937190099401其他多肽激素及衍生物和结构类似物(包括蛋白激素、糖蛋白激素及其衍生物和结构类似物)29371900999含人类遗传资源的人类腺体、器官及其分泌物的提取物3001200021999含人类遗传资源的人类腺体、器官及其分泌物的提取物300120002110其他人类的腺体、器官及其分泌物的提取物3001200029999其他人类的腺体、器官及其分泌物的提取物300120002911蛇毒制品(供治疗或预防疾病用)3001909010999蛇毒制品(供治疗或预防疾病用)3001909010 12含人类遗传资源的人体制品3001909020999含人类遗传资源的人体制品300190902013人类腺体、器官、组织(含《人间传染的病原微生物名录》内一类病原微生物)3001909092401人类腺体、器官、组织300190909214人类腺体、器官、组织(含《人间传染的病原微生物名录》内二类病原微生物)3001909092402人类腺体、器官、组织300190909215人类腺体、器官、组织(含《人间传染的病原微生物名录》内三类病原微生物)3001909092403人类腺体、器官、组织300190909216人类腺体、器官、组织(含《人间传染的病原微生物名录》内四类病原微生物)3001909092404人类腺体、器官、组织300190909217人类腺体、器官、组织(含《人间传染的病原微生物名录》内含新发传染病或名录外再现传染病病原微生物)3001909092405人类腺体、器官、组织300190909218人类腺体、器官、组织(含寄生虫)3001909092406人类腺体、器官、组织3001909092 19人类腺体、器官、组织(经灭活处理的组织切片)3001909092407人类腺体、器官、组织300190909220人类腺体、器官、组织(其他人类腺体、器官、组织)3001909092408人类腺体、器官、组织300190909221其他未列名的人体或动物制品(供治疗或预防疾病用)(人体制品)3001909099401其他未列名的人体或动物制品(供治疗或预防疾病用)300190909922唾液酸促红素、促红素衍生肽、氨甲酰促红素、达促红素、促红素(EPO)类等促红素(用于人类医学、生命科学相关领域)3002120011401唾液酸促红素、促红素衍生肽、氨甲酰促红素、达促红素、促红素(EPO)类等促红素300212001123胰岛素样生长因子1(IGF-1)及其类似物(用于人类医学、生命科学相关领域)3002120012401胰岛素样生长因子1(IGF-1)及其类似物300212001224机械生长因子类(用于人类医学、生命科学相关领域)3002120013401机械生长因子类300212001325成纤维细胞生长因子类(FGFs)(用于人类医学、生命科学相关领域)3002120014401成纤维细胞生长因子类(FGFs)300212001426肝细胞生长因子(HGF)(用于人类医学、生命科学相关领域)3002120015401肝细胞生长因子(HGF)300212001527血小板衍生生长因子(PDGF)(用于人类医学、生命科学相关领域)3002120016401血小板衍生生长因子(PDGF)300212001628血管内皮生长因子(VEGF)(用于人类医学、生命科学相关领域)3002120017401血管内皮生长因子(VEGF)300212001729转化生长因子-β(TGF-β)抑制剂类(用于人类医学、生命科学相关领域)3002120018401转化生长因子-β(TGF-β)抑制剂类300212001830培尼沙肽、罗特西普(用于人类医学、生命科学相关领域)3002120019401培尼沙肽、罗特西普300212001931缺氧诱导因子(HIF)激活剂类、缺氧诱导因子(HIF)稳定剂类(用于人类医学、生命科学相关领域)3002120021401缺氧诱导因子(HIF)激活剂类、缺氧诱导因子(HIF)稳定剂类300212002132EPO-Fc(IgG4)融合蛋白、EPO-Fc融合蛋白(用于人类医学、生命科学相关领域)3002120022401EPO-Fc(IgG4)融合蛋白、EPO-Fc融合蛋白300212002233含人类遗传资源的抗血清及其他血份(含《人间传染的病原微生物名录》内一类病原微生物)3002120023401含人类遗传资源的抗血清及其他血份300212002334含人类遗传资源的抗血清及其他血份(含《人间传染的病原微生物名录》内二类病原微生物)3002120023402含人类遗传资源的抗血清及其他血份300212002335含人类遗传资源的抗血清及其他血份(含《人间传染的病原微生物名录》内三类病原微生物)3002120023403含人类遗传资源的抗血清及其他血份300212002336含人类遗传资源的抗血清及其他血份(含《人间传染的病原微生物名录》内四类病原微生物)3002120023404含人类遗传资源的抗血清及其他血份300212002337含人类遗传资源的抗血清及其他血份(含《人间传染的病原微生物名录》内新发传染病或名录外再现传染病病原微生物)3002120023405含人类遗传资源的抗血清及其他血份300212002338含人类遗传资源的抗血清及其他血份(含寄生虫)3002120023406含人类遗传资源的抗血清及其他血份3002120023 39含人类遗传资源的抗血清及其他血份(其他抗血清)3002120023407含人类遗传资源的抗血清及其他血份3002120023 40含人类遗传资源的抗血清及其他血份(其他血份)3002120023408含人类遗传资源的抗血清及其他血份300212002341罕见病药品制剂(包括罕见病药品清单第一批、第二批相关商品)(其他人血制品)3002120093401罕见病药品制剂(包括罕见病药品清单第一批、第二批相关商品)300212009342其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(临床采集,含《人间传染的病原微生物名录》内一类病原微生物)3002120099402其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009943其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(临床采集,含《人间传染的病原微生物名录》内二类病原微生物)3002120099403其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009944其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(临床采集,含《人间传染的病原微生物名录》内三类病原微生物)3002120099404其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009945其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(临床采集,含《人间传染的病原微生物名录》内四类病原微生物)3002120099405其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009946其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(临床采集,含新发传染病或名录外再现传染病病原微生物)3002120099406其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009947其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(临床采集,含寄生虫)3002120099407其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009948其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(临床采集,经过血液传播病原体筛查为阴性)3002120099408其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009949其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(商品化含《人间传染的病原微生物名录》内一类病原微生物)3002120099409其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009950其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(商品化含《人间传染的病原微生物名录》内二类病原微生物)3002120099410其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009951其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(商品化含《人间传染的病原微生物名录》内三类病原微生物)3002120099411其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009952其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(商品化含《人间传染的病原微生物名录》内四类病原微生物)3002120099412其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009953其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(商品化经过血液传播病原体筛查为阴性)3002120099413其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009954其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(临床用捐献配型的特殊血型血液的血份)3002120099414其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009955其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(按药品管理的人抗血清)3002120099415其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009956其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(其他人抗血清)3002120099416其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009957其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(其他人血份)3002120099417其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009958其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)(用于人类医学、生命科学相关领域的多克隆抗体)3002120099418其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009959其他抗血清及其他血份(按药品管理人血浆蛋白制品(白蛋白、球蛋白、纤维蛋白原))3002120099419其他抗血清及其他血份(因拆分抗癌药产生的兜底税号)300212009960非混合的免疫制品,未配定剂量或制成零售包装(纯化抗体)3002130000401非混合的免疫制品,未配定剂量或制成零售包装300213000061非混合的免疫制品,未配定剂量或制成零售包装(细胞因子)3002130000402非混合的免疫制品,未配定剂量或制成零售包装300213000062非混合的免疫制品,未配定剂量或制成零售包装(其他医学免疫实验用试剂)3002130000403非混合的免疫制品,未配定剂量或制成零售包装300213000063混合的免疫制品,未配定剂量或制成零售包装(纯化抗体)3002140000401混合的免疫制品,未配定剂量或制成零售包装300214000064混合的免疫制品,未配定剂量或制成零售包装(细胞因子)3002140000402混合的免疫制品,未配定剂量或制成零售包装300214000065混合的免疫制品,未配定剂量或制成零售包装(其他医学免疫实验用试剂)3002140000403混合的免疫制品,未配定剂量或制成零售包装300214000066抗(防)癌药品制剂(不含癌症辅助治疗药品)(生物制品)3002150010401抗(防)癌药品制剂(不含癌症辅助治疗药品)300215001067罕见病药品制剂(包括罕见病药品清单第一批、第二批相关商品)(治疗人类疾病用)3002150030401罕见病药品制剂(包括罕见病药品清单第一批、第二批相关商品)300215003068罕见病药品制剂(包括罕见病药品清单第一批、第二批相关商品)(医学科研用)3002150030402罕见病药品制剂(包括罕见病药品清单第一批、第二批相关商品)300215003069其他免疫制品,已配定剂量或制成零售包装(治疗人类疾病用新型冠状病毒(COVID-19)抗体药)3002150090401其他免疫制品,已配定剂量或制成零售包装300215009070其他免疫制品,已配定剂量或制成零售包装(医学科研用新型冠状病毒(COVID-19)抗体药)3002150090402其他免疫制品,已配定剂量或制成零售包装300215009071其他免疫制品,已配定剂量或制成零售包装(其他治疗人类疾病用)3002150090403其他免疫制品,已配定剂量或制成零售包装300215009072其他免疫制品,已配定剂量或制成零售包装(其他人类医学、生命科学研究用)3002150090404其他免疫制品,已配定剂量或制成零售包装300215009073新型冠状病毒(COVID-19)疫苗,已配定剂量或制成零售包装(预防疾病用)3002410011401新型冠状病毒(COVID-19)疫苗,已配定剂量或制成零售包装300241001174新型冠状病毒(COVID-19)疫苗,已配定剂量或制成零售包装(医学科研用)3002410011402新型冠状病毒(COVID-19)疫苗,已配定剂量或制成零售包装300241001175新型冠状病毒(COVID-19)疫苗,未配定剂量或制成零售包装(预防疾病用)3002410019401新型冠状病毒(COVID-19)疫苗,未配定剂量或制成零售包装300241001976新型冠状病毒(COVID-19)疫苗,未配定剂量或制成零售包装(医学科研用)3002410019402新型冠状病毒(COVID-19)疫苗,未配定剂量或制成零售包装300241001977其他人用疫苗(预防疾病用)3002410090401其他人用疫苗3002410090 78其他人用疫苗(医学科研用)3002410090402其他人用疫苗3002410090 79石房蛤毒素(治疗人类疾病用)3002491000401石房蛤毒素3002491000 80石房蛤毒素(人类医学、生命科学研究用)3002491000402石房蛤毒素3002491000 81石房蛤毒素(其他)3002491000403石房蛤毒素3002491000 82蓖麻毒素(治疗人类疾病用)3002492000401蓖麻毒素3002492000 83蓖麻毒素(人类医学、生命科学研究用)3002492000402蓖麻毒素300249200084两用物项管制细菌及病毒(两用物项管制目录内人及人兽共患病病原体)3002493010401两用物项管制细菌及病毒300249301085苏云金杆菌、枯草芽孢杆菌(环保微生物菌剂)3002493020401苏云金杆菌、枯草芽孢杆菌3002493020 86苏云金杆菌、枯草芽孢杆菌(环保微生物菌剂样品)3002493020402苏云金杆菌、枯草芽孢杆菌300249302087苏云金杆菌、枯草芽孢杆菌(人类医学、生命科学研究用)3002493020403苏云金杆菌、枯草芽孢杆菌300249302088苏云金杆菌、枯草芽孢杆菌(其他)3002493020404苏云金杆菌、枯草芽孢杆菌300249302089其他细菌及病毒(两用物项管制外的《人间传染的病原微生物名录》内第一类病毒)3002493090401其他细菌及病毒300249309090其他细菌及病毒(两用物项管制外的《人间传染的病原微生物名录》内第二类细菌)3002493090402其他细菌及病毒300249309091其他细菌及病毒(两用物项管制外的《人间传染的病原微生物名录》内第二类病毒(含Prion))3002493090403其他细菌及病毒300249309092其他细菌及病毒(两用物项管制外的《人间传染的病原微生物名录》内第三类细菌)3002493090404其他细菌及病毒300249309093其他细菌及病毒(两用物项管制外的《人间传染的病原微生物名录》内第三类病毒(含Prion))3002493090405其他细菌及病毒300249309094其他细菌及病毒(《人间传染的病原微生物名录》内第四类病毒)3002493090406其他细菌及病毒300249309095其他细菌及病毒(新发传染病或名录外再现传染病细菌)3002493090407其他细菌及病毒300249309096其他细菌及病毒(新发传染病或名录外再现传染病病毒)3002493090408其他细菌及病毒300249309097其他细菌及病毒(非菌剂类环保微生物)3002493090409其他细菌及病毒300249309098其他细菌及病毒(经基因编辑的治疗人类疾病用细菌及病毒(环保微生物除外))3002493090410其他细菌及病毒300249309099其他细菌及病毒(经基因编辑的人类医学、生命科学研究用细菌及病毒(环保微生物除外))3002493090411其他细菌及病毒3002493090100其他细菌及病毒(其他医学相关细菌及病毒)3002493090412其他细菌及病毒3002493090 101其他细菌及病毒(环保用微生物菌剂)3002493090413其他细菌及病毒3002493090 102其他细菌及病毒(环保用微生物菌剂样品)3002493090414其他细菌及病毒3002493090103噬菌核霉、淡紫拟青霉、哈茨木霉菌、寡雄腐霉菌3002499010999噬菌核霉、淡紫拟青霉、哈茨木霉菌、寡雄腐霉菌3002499010104其他两用物项管制毒素(人类医学、生命科学研究用)3002499020401其他两用物项管制毒素3002499020105其他毒素、培养微生物(不包括酵母)及类似产品(人类医学、生命科学研究用其他毒素)3002499090401其他毒素、培养微生物(不包括酵母)及类似产品3002499090106其他毒素、培养微生物(不包括酵母)及类似产品(人类医学、生命科学研究用其他类毒素)3002499090402其他毒素、培养微生物(不包括酵母)及类似产品3002499090107其他毒素、培养微生物(不包括酵母)及类似产品(《人间传染的病原微生物名录》内第二类真菌)3002499090403其他毒素、培养微生物(不包括酵母)及类似产品3002499090108其他毒素、培养微生物(不包括酵母)及类似产品(《人间传染的病原微生物名录》内第三类真菌)3002499090404其他毒素、培养微生物(不包括酵母)及类似产品3002499090109其他毒素、培养微生物(不包括酵母)及类似产品(《人间传染的病原微生物名录》内的放线菌)3002499090405其他毒素、培养微生物(不包括酵母)及类似产品3002499090110其他毒素、培养微生物(不包括酵母)及类似产品(《人间传染的病原微生物名录》内的衣原体)3002499090406其他毒素、培养微生物(不包括酵母)及类似产品3002499090111其他毒素、培养微生物(不包括酵母)及类似产品(《人间传染的病原微生物名录》内的支原体)3002499090407其他毒素、培养微生物(不包括酵母)及类似产品3002499090112其他毒素、培养微生物(不包括酵母)及类似产品(两用物项外的《人间传染的病原微生物名录》内的立克次体)3002499090408其他毒素、培养微生物(不包括酵母)及类似产品3002499090113其他毒素、培养微生物(不包括酵母)及类似产品(《人间传染的病原微生物名录》内的螺旋体)3002499090409其他毒素、培养微生物(不包括酵母)及类似产品3002499090114其他毒素、培养微生物(不包括酵母)及类似产品(新发传染病或名录外再现传染病真菌、放线菌、衣原体、支原体、立克次体、螺旋体)3002499090410其他毒素、培养微生物(不包括酵母)及类似产品3002499090115其他毒素、培养微生物(不包括酵母)及类似产品(人类医学、生命科学研究用其他真菌、放线菌、衣原体、支原体、立克次体、螺旋体)3002499090411其他毒素、培养微生物(不包括酵母)及类似产品3002499090116其他毒素、培养微生物(不包括酵母)及类似产品(治疗人类疾病用)3002499090412其他毒素、培养微生物(不包括酵母)及类似产品3002499090117细胞治疗产品(治疗人类疾病用)3002510000401细胞治疗产品3002510000 118细胞治疗产品(人类医学、生命科学研究用)3002510000402细胞治疗产品3002510000 119其他细胞培养物,不论是否修饰(人源血细胞)3002590000401其他细胞培养物,不论是否修饰3002590000120其他细胞培养物,不论是否修饰(临床用捐献配型的骨髓造血干细胞)3002590000402其他细胞培养物,不论是否修饰3002590000121其他细胞培养物,不论是否修饰(临床用捐献配型的外周血造血干细胞)3002590000403其他细胞培养物,不论是否修饰3002590000122其他细胞培养物,不论是否修饰(临床用捐献配型的脐带血造血干细胞)3002590000404其他细胞培养物,不论是否修饰3002590000123其他细胞培养物,不论是否修饰(其他人源干细胞)3002590000405其他细胞培养物,不论是否修饰3002590000124其他细胞培养物,不论是否修饰(国际知名保藏机构的人源细胞株(系))3002590000406其他细胞培养物,不论是否修饰3002590000125其他细胞培养物,不论是否修饰(其他商品化的人源细胞株(系))3002590000407其他细胞培养物,不论是否修饰3002590000126其他细胞培养物,不论是否修饰(经基因编辑的人源细胞(细胞株))3002590000408其他细胞培养物,不论是否修饰3002590000127其他细胞培养物,不论是否修饰(其他培养的人源细胞)3002590000409其他细胞培养物,不论是否修饰3002590000128其他细胞培养物,不论是否修饰(临床采集,含《人间传染的病原微生物名录》内一类病原微生物)3002590000410其他细胞培养物,不论是否修饰3002590000129其他细胞培养物,不论是否修饰(临床采集,含《人间传染的病原微生物名录》内二类病原微生物)3002590000411其他细胞培养物,不论是否修饰3002590000130其他细胞培养物,不论是否修饰(临床采集,含《人间传染的病原微生物名录》内三类病原微生物)3002590000412其他细胞培养物,不论是否修饰3002590000131其他细胞培养物,不论是否修饰(临床采集,含《人间传染的病原微生物名录》内四类病原微生物)3002590000413其他细胞培养物,不论是否修饰3002590000132其他细胞培养物,不论是否修饰(临床采集,含新发传染病或名录外再现传染病病原微生物)3002590000414其他细胞培养物,不论是否修饰3002590000133其他细胞培养物,不论是否修饰(临床采集,含寄生虫)3002590000415其他细胞培养物,不论是否修饰3002590000134其他细胞培养物,不论是否修饰(临床采集,经过血液传播病原体筛查为阴性)3002590000416其他细胞培养物,不论是否修饰3002590000135其他细胞培养物,不论是否修饰(商品化含《人间传染的病原微生物名录》内一类病原微生物)3002590000417其他细胞培养物,不论是否修饰3002590000136其他细胞培养物,不论是否修饰(商品化含《人间传染的病原微生物名录》内二类病原微生物)3002590000418其他细胞培养物,不论是否修饰3002590000137其他细胞培养物,不论是否修饰(商品化含《人间传染的病原微生物名录》内三类病原微生物)3002590000419其他细胞培养物,不论是否修饰3002590000138其他细胞培养物,不论是否修饰(商品化含《人间传染的病原微生物名录》内四类病原微生物)3002590000420其他细胞培养物,不论是否修饰3002590000139其他细胞培养物,不论是否修饰(商品化经过血液传播病原体筛查为阴性)3002590000421其他细胞培养物,不论是否修饰3002590000140人血(临床采集,含《人间传染的病原微生物名录》内一类病原微生物的的人全血)3002909001401人血3002909001141人血(临床采集,含《人间传染的病原微生物名录》内二类病原微生物的人全血)3002909001402人血3002909001142人血(临床采集,含《人间传染的病原微生物名录》内三类病原微生物的人全血)3002909001403人血3002909001143人血(临床采集,含《人间传染的病原微生物名录》内四类病原微生物的人全血)3002909001404人血3002909001144人血(临床采集,含新发传染病或名录外再现传染病病原微生物的人全血)3002909001405人血3002909001145人血(临床采集,含寄生虫的人全血)3002909001406人血3002909001146人血(临床采集,经过血液传播病原体筛查为阴性的人全血)3002909001407人血3002909001147人血(商品化含《人间传染的病原微生物名录》内一类病原微生物的的人全血)3002909001408人血3002909001148人血(商品化含《人间传染的病原微生物名录》内二类病原微生物的人全血)3002909001409人血3002909001149人血(商品化含《人间传染的病原微生物名录》内三类病原微生物的人全血)3002909001410人血3002909001150人血(商品化含《人间传染的病原微生物名录》内四类病原微生物的人全血)3002909001411人血3002909001151人血(商品化经过血液传播病原体筛查为阴性的人全血)3002909001412人血3002909001152人血(临床用捐献配型的特殊血型血液)3002909001413人血3002909001 153人血(其他人血)3002909001414人血3002909001154两用物项管制遗传物质和基因修饰生物体(两用物项管制目录内人及人兽共患病病原体的遗传物质和基因修饰生物体)3002904010401两用物项管制遗传物质和基因修饰生物体(3002904010155X光检查造影剂、诊断试剂(医学诊断用)3006300000401X光检查造影剂、诊断试剂3006300000156安慰剂和盲法(或双盲法)临床试剂盒,用于经许可的临床试验,已配定剂量(含有微生物、人体组织、生物制品、血液及其制品的)3006930000401安慰剂和盲法(或双盲法)临床试剂盒,用于经许可的临床试验,已配定剂量3006930000157白蛋白及白蛋白盐(包括白蛋白衍生物)(用于人类医学、生命科学相关领域,非用于治疗或预防疾病用)3502900000401白蛋白及白蛋白盐(包括白蛋白衍生物)3502900000158其他编号未列名蛋白质及其衍生物(包括蛋白胨的衍生物及皮粉(不论是否加入铬矾))(用于人类医学、生命科学相关领域,非用于治疗或预防疾病用)3504009000401其他编号未列名蛋白质及其衍生物(包括蛋白胨的衍生物及皮粉(不论是否加入铬矾))3504009000159碱性蛋白酶(用于人类医学、生命科学相关领域)3507901000401碱性蛋白酶3507901000 160碱性脂肪酶(用于人类医学、生命科学相关领域)3507902000401碱性脂肪酶3507902000161门冬酰胺酶(用于人类医学、生命科学相关领域,非用于治疗或预防疾病用)3507909010401门冬酰胺酶3507909010162其他酶及酶制品(人类医学、生命科学研究用)3507909090401其他酶及酶制品3507909090163制成的供微生物(包括病毒及类似品)生长或维持用培养基(及制成的供植物、人体或动物细胞生长或维持用的培养基)(含人血及其成分、人体组织、细胞、体液、分泌物、排泄物)3821000000401制成的供微生物(包括病毒及类似品)生长或维持用培养基(及制成的供植物、人体或动物细胞生长或维持用的培养基)3821000000164制成的供微生物(包括病毒及类似品)生长或维持用培养基(及制成的供植物、人体或动物细胞生长或维持用的培养基)(含除人血及其成分、人体组织、细胞、体液、分泌物、排泄物外其他特殊物品成分)3821000000402制成的供微生物(包括病毒及类似品)生长或维持用培养基(及制成的供植物、人体或动物细胞生长或维持用的培养基)3821000000165疟疾诊断试剂盒(诊断人类疾病用)3822110010401疟疾诊断试剂盒3822110010 166疟疾诊断试剂盒(人类医学、生命科学研究用)3822110010402疟疾诊断试剂盒3822110010167其他疟疾用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外(诊断人类疾病用)3822110090401其他疟疾用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外3822110090168其他疟疾用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外(人类医学、生命科学研究用)3822110090402其他疟疾用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外3822110090169寨卡病毒及由伊蚊属蚊子传播的其他疾病用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外(诊断人类疾病用)3822120000401寨卡病毒及由伊蚊属蚊子传播的其他疾病用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外3822120000170寨卡病毒及由伊蚊属蚊子传播的其他疾病用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外(人类医学、生命科学研究用)3822120000402寨卡病毒及由伊蚊属蚊子传播的其他疾病用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外3822120000171血型鉴定用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外(诊断人类疾病用)3822130000401血型鉴定用的附于衬背上的诊断或实验用试剂及不论是否附于衬背上的诊断或实验用配制试剂,不论是否制成试剂盒形式,但税目30.06的货品除外3822130000。
最全的国内外试剂级别划分

国内外试剂级别划分国内试剂级别的划分我国的试剂规格基本上按纯度(杂质含量的多少)划分,共有高纯、光谱纯、基准、分光纯、优级纯、分析纯和化学纯等7种。
国家和主管部门颁布质量指标的主要是优级纯、分级纯和化学纯3种。
除了上述四个级别外,目前市场上尚有:基准试剂(PT:Primary Reagent):专门作为基准物用,可直接配制标准溶液。
光谱纯试剂(SP:Spectrum pure):表示光谱纯净。
但由于有机物在光谱上显示不出,所以有时主成分达不到99.9%以上,使用时必须注意,特别是作基准物时,必须进行标定。
纯度远高于优级纯的试剂叫做高纯试剂(≥ 99.99%)。
瓶签颜色与试剂级别的划分(1)基准试剂(PT,绿标签):作为基准物质,标定标准溶液。
(2)优级纯(GR,绿标签):主成分含量很高、纯度很高,99.8%适用于精确分析和研究工作,有的可作为基准物质。
又称一级品或保证试剂。
(3)分析纯(AR,红标签):主成分含量很高、纯度较高,99.7%,干扰杂质很低,适用于工业分析及化学实验。
又称二级试剂。
(4)化学纯(CP,蓝标签):主成分含量高、纯度较高,≥ 99.5%,存在干扰杂质,适用于化学实验和合成制备。
又称三级试剂。
(5)实验纯(LR,黄标签):主成分含量高,纯度较差,杂质含量不做选择,只适用于一般化学实验和合成制备。
又称四级试剂。
目前,国外试剂厂生产的化学试剂的规格趋向于按用途划分,常见的如下:超高纯试剂:UP-S级(也就是电子纯MOS级):金属杂质含量小于1ppb,适合0.35—0.8微米集成电路加工工艺。
等离子体质谱纯级试剂(ICP-Mass Pure Grade):绝大多数杂质元素含量低于0.1ppb,适合等离子体质谱仪(ICP Mass)日常分析工作。
等离子体发射光谱纯级试剂(ICP Pure Grade):绝大多数杂质元素含量低于1ppb ,适合等离子体发射光谱仪(ICP)日常分析工作。
体外诊断试剂校准品(物)质控品(物)研究技术指导原则

附件5:体外诊断试剂生产及质量控制技术指导原则——体外诊断试剂校准品(物)、质控品(物)研究技术指导原则体外诊断试剂校准品(物)(包括真实度控制品)、质控品(物)(简称校准品、质控品)就是实现体外诊断试剂临床检测及监督检验结果准确一致得主要工具,也就是保证量值有效传递得计量实物标准。
校准品、质控品研究技术资料应包括产品技术要求、试验方法等重要信息,就是指导注册申请人(简称申请人)单独申请注册校准品、质控品得重要技术性文件之一。
本研究技术指导原则基于国家食品药品监督管理局《体外诊断试剂注册管理办法(试行)》、《医疗器械标准管理方法》得相关规定。
参考国际标准化组织(ISO)、美国食品药品监督管理局(FDA)、临床化学国际联合会(IFCC)等有关体外诊断试剂方面得指南,对编写得格式及各项内容得要求进行了详细得说明、其目得就是为体外诊断试剂校准品、质控品单独注册申报进行原则性得指导,同时,也为注册管理部门审核体外诊断试剂校准品、质控品提供参考、由于校准品、质控品种类多、范围广、临床使用重要性强且使用目得差别大,因此,申请人应根据产品特点及临床使用目得编写技术资料,以便于关注者获取准确得信息、申请人应该提供校准品、质控品产品标准与技术资料,技术资料得要求参见《体外诊断试剂注册管理办法(试行)》、产品标准格式与具体内容如下(不限于):一、范围应明确陈述本标准规范得对象与所涉及得方面,指明使用得界限、二、规范性引用文件应包括引导语与规范性引用文件得一览表。
一览表中引用文件得排列顺序为:国家标准、行业标准、国际标准及规范性文件等、例如:下列文件中得条款通过本标准得引用而成为本标准得条款、凡就是注日期得引用文件,其随后所有得修改单(不包括勘误得内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议得各方研究就是否可使用这些文件得最新版本。
凡就是不注日期得引用文件,其最新版本适用于本标准。
GB/T 1、1—2000 标准化工作导则第1部分:标准得结构与编写规则GB/T 191—2000 包装储运图示标志YY 0466—2003 医疗器械用于医疗器械标签、标记与提供信息得符号ISO 17511 体外诊断医疗器械生物源性样品中量得测量校准品与质控物质赋值得计量学溯源性ISO18153 体外诊断医疗器械生物源性样品中量得测量校准品与控制物质中酶催化浓度赋值得计量学溯源性三、分类与组成及其它(一)组成成份应说明主要组成成份及其生物学来源、(二)标示值应注明校准品赋值及不确定度、质控品得赋值及允许范围,非定值质控品没有指定得参考范围,可以通过在标贴上标示目标浓度(如:低、高、中)表示、(三)规格应注明规格、(四)用途应详细注明校准品、质控品得预期用途。
体外诊断试剂校准品(物)、质控品(物)研究技术指导原则57 校准品word版本

体外诊断试剂校准品(物)、质控品(物)研究技术指导原则体外诊断试剂校准品(物)(包括真实度控制品)、质控品(物)(简称校准品、质控品)是实现体外诊断试剂临床检测及监督检验结果准确一致的主要工具,也是保证量值有效传递的计量实物标准。
校准品、质控品研究技术资料应包括产品技术要求、试验方法等重要信息,是指导注册申请人(简称申请人)单独申请注册校准品、质控品的重要技术性文件之一。
本研究技术指导原则基于国家食品药品监督管理局《体外诊断试剂注册管理办法(试行)》、《医疗器械标准管理方法》的相关规定。
参考国际标准化组织(ISO)、美国食品药品监督管理局(FDA)、临床化学国际联合会(IFCC)等有关体外诊断试剂方面的指南,对编写的格式及各项内容的要求进行了详细的说明。
其目的是为体外诊断试剂校准品、质控品单独注册申报进行原则性的指导,同时,也为注册管理部门审核体外诊断试剂校准品、质控品提供参考。
由于校准品、质控品种类多、范围广、临床使用重要性强且使用目的差别大,因此,申请人应根据产品特点及临床使用目的编写技术资料,以便于关注者获取准确的信息。
申请人应该提供校准品、质控品产品标准和技术资料,技术资料的要求参见《体外诊断试剂注册管理办法(试行)》。
产品标准格式和具体内容如下(不限于):一、范围应明确陈述本标准规范的对象和所涉及的方面,指明使用的界限。
二、规范性引用文件应包括引导语和规范性引用文件的一览表。
一览表中引用文件的排列顺序为:国家标准、行业标准、国际标准及规范性文件等。
例如:下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 1.1-2000 标准化工作导则第1部分:标准的结构和编写规则GB/T 191-2000包装储运图示标志YY 0466-2003 医疗器械用于医疗器械标签、标记和提供信息的符号ISO 17511 体外诊断医疗器械生物源性样品中量的测量校准品和质控物质赋值的计量学溯源性ISO 18153 体外诊断医疗器械生物源性样品中量的测量校准品和控制物质中酶催化浓度赋值的计量学溯源性三、分类和组成及其它(一)组成成份应说明主要组成成份及其生物学来源。
6840 体外诊断试剂分类子目录(2013版)

临床上用于福氏志贺菌群分型。 临床上用于宋内志贺菌诊断。 临床上用于志贺志贺菌诊断。 临床上用于外斐(Weil-Felix)反应。 临床上用于外斐(Weil-Felix)反应。 临床上用于外斐(Weil-Felix)反应。 临床上用于肥达(Widal)反应。 临床上用于肥达(Widal)反应。 临床上用于肥达(Widal)反应。 临床上用于肥达(Widal)反应。 临床上用于肥达(Widal)反应。 临床上用于凝集试验诊断肠道致病性大肠埃希菌。 临床上用于诊断O1群霍乱弧菌。 临床上用于鼠疫耶尔森菌诊断。 临床上用于鉴定鼠疫耶尔森菌。 临床上用于鉴定炭疽杆菌。 临床上用于鉴定炭疽杆菌。 用于检测人体样本中的A群β 溶血性链球菌抗原,临床上主要用于呼吸道 感染病原学的辅助诊断和鉴别诊断。
025 026 027 028 029 030 031 032 033 034 035 036 037 038 039 040 041 042 043 044 045
Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂 Ⅲ-1 与致病性病原体抗原、抗体以及核酸等检测 相关的试剂
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
国际校准品目录00/410 MAPREC assay of poliovirus type 1 (Sabin).100% 480-A, 525-C DNA(1st International Reference Preparation)00/416 Low Mutant Virus Reference for MAPREC assay of poliovirus type 1 (Sabin)(1st International Reference Preparation)00/418 MAPREC assay of poliovirus type 1 (Sabin) (1st International Standard)00/422 High Mutant Virus Reference for MAPREC assay of poliovirus type 1 (Sabin)(1st International Reference Preparation)00/440 Influenza Antiserum A/Singapore/1/57 (H2)00/442 Influenza anti B/Yamanashi/166/98 Serum (sheep)00/464 Streptokinase (3rd International Standard 2001)00/500 Botulinum Type A-E Antitoxin, Human Serum00/530 Influenza Virus infectious B/Sichuan/379/9900/542 Influenza anti- A/Chick/Scotland/59 (H5N1) Serum00/544 Influenza Virus infectious B/Victoria/504/0000/546 Influenza Antigen B/Johannesburg/5/9900/552 Influenza Antigen A/Duck/Singapore-Q/F119-3/97 (H5N3)00/556 Influenza anti-B/Johannesburg/5/99/ Serum00/562 Hepatitis A Virus for Nucleic Acid Amplification Techniques(2nd International Standard)00/572 Interferon Beta (Human, rDNA, Glycosylated) (3rd International standard)00/574 Interferon Beta SER17 Mutein (Human, rDNA derived)00/576 Interferon Beta (Human, Fibroblast-derived, Glycosylated)00/614 Influenza virus infectious B/Guangdong/120/2000007SP Human Anti-Pneumococcal capsule Reference Serum (1st International Standard) 01/412 Anti-Meningococcal Immunotype L3,7,9 Monoclonal Antibody01/420 Interleukin-17 (Human rDNA derived)(International Reference Reagent)01/424 Vascular Endothelial Growth Factor, Human rDNA derived01/426 Meningococcal group Y polysaccharide01/428 Meningococcal serogroup W polysaccharide01/450 Influenza anti B/Guangdong/120/2000 Serum01/452 Influenza anti A/Panama/2007/99 (H3N2) HA serum01/506 Botulinum type F antitoxin, equine01/508 Botulinum type C antitoxin, equine01/510 Botulinum Antitoxin Equine Type D01/512 Botulinum type G antitoxin, equine01/514 Anti-Meningococcal Serosubtype P1.7 Monoclonal Antibody01/528 Oral Poliovaccine Sabin Type 1 reference strain [LS-c, 2ab strain] (Panel of 5 ampoules)01/530 Oral Poliovaccine Sabin Type 2 reference strain (Panel of 5 ampoules)01/532 Oral Poliovaccine Sabin Type 3 reference strain (Panel of 5 ampoules)01/538 Anti-Meningococcal Serosubtype P1.16 mAb01/546 Influenza Antigen B/Guangdong/120/200001/572 Anti-D Immunoglobulin(2nd International Standard)01/580 Thrombin, human(2nd International Standard)01/600 Anti-Toxoplasma IgG, Human(International Standard)01/602 Anti-Parvovirus B19, plasma, human(2nd International Standard)01/612 Influenza Virus infectious B/Hawaii/10/0101/614 Influenza Antigen A/New Caledonia/20/9902/102 Influenza anti A/Panama/2007/99 Serum02/144 Anti-Meningococcal Serosubtype P1.15 mAb02/148 Anti-Meningococcal Serosubtype P1.4 mAb02/168 Prekallikrein Activator (PKA), Human(2nd International Standard)02/178 Anti-Meningococcal Serosubtype P1.2 mAb02/180 Anti-Meningococcal Serotype P2.2a mAb02/182 Anti-Japanese Encephalitis Virus Plasma, Human02/184 Anti-Japanese Encephalitis (Anti-JE) Virus Negative Control Plasma, Human02/206 Factor XIII Plasma, Human (1st International Standard)02/210 HIV (antibody), 1st International Reference Panel02/226 IVIG negative control for use with IVIG + anti-D(International Reference Reagent) 02/228 IVIG + anti-D for use with negative control IVIG(International Reference Reagent) 02/230 Biotinylated Brad-5 (Bio-Brad-5)02/232 Tetanus Toxoid (Non-Adsorbed)02/254 Insulin-like Growth Factor-1, recombinant, human, for immunoassay(1st International Standard)02/262 Influenza Virus infectious B/Brisbane/32/200202/264-005 HCV RNA Working Reagent for Nucleic Acid Amplification Techniques02/286 Vascular Endothelial Growth Factor 165 (VEGF165)(recDNA, human sequence)(International Reference Reagent)02/294 Influenza Antiserum A/chick/Italy/1347/99 (H7N1)02/306 Polio Virus Sabin Types 1, 2 and 3(2nd International Reference Reagent)02/308 Anti-Meningococcal Serotype P3.4 mAb02/310 Anti-Meningococcal Serotype P3.15 mAb02/318 Botulinum Antitoxin Equine Type E02/320 Anti-Meningococcal Serosubtype P1.3 mAb02/336 Influenza Antigen A/New Caledonia/20/9902/338 Influenza anti A/Panama/2007/99 Serum02/342 Protein C Plasma, Human(2nd International Standard)03/104-016 HTLV-1 (antibody) Monitor Sample03/110 Influenza anti B/Shangdong/9/97 Serum03/114 Anti-Meningococcal Serosubtype P1.1 mAb03/116 Blood Coagulation Factor V, Plasma Human (1st International Standard)03/124 Thrombopoietin ( Human rDNA derived)03/142 Anti-Meningococcal Serosubtype P1.14 mAb03/148 Keratinocyte growth factor (KGF, FGF-7)(24-163)(1st International Reference Reagent)03/150 Keratinocyte Growth Factor (KGF,FGF-7)(1st International Reference Reagent)03/152 Anti-HPA-1a (International Standard)03/164 Anti-B minimum potency reference preparation(International Standard)03/178 Vitamin B12, Serum Folate and holoTC (International standard)03/182 Anti-Meningococcal Serotype P3.21 mAb03/188 Anti-A minimum potency reference preparation(International Standard)03/190 Anti-HPA-3a(minimum potency)(International Reference Reagent)03/192 Thyroid-Stimulating Hormone, Recombinant, Human, for Bioassay (1st International standard)03/198 Influenza Virus infectious A/Kumamoto/102/0203/200 Interleukin - 18 (Human rDNA derived)(International Reference Reagent)03/210 Anti-Meningiococcal Serosubtype P1.6 mAb03/212 Influenza anti A/Wyoming/03/03 Serum03/220 Influenza Antigen A/Wyoming/03/0303/224 Anti-Meningococcal Serosubtype P1.10 mAb03/226 Anti-Meningococcal Serosubtype P1.5 mAb03/228 Protein S, Plasma, Human(2nd International Standard)03/236 Anti-Meningococcal Serosubtype P1.13 mAb03/242 Influenza anti A/Puerto Rico/8/34 (H1N1) HA Serum03/244 Influenza Antiserum A/chick/Germany/N/4903/258 Influenza Antigen A/New Caledonia/20/99 (IVR-116)03/262 Hepatitis B Surface Antigen subtype adw2, genotype A (International Reference Panel)04/102 Blood Coagulation Factor XI Plasma, Human(1st International Standard)04/122 Anti-Meningococcal Serosubtype P1.12 mAb04/132 IVIG + Anti-D for use with negative control IVIG04/140 IVIG Negative Control for use with IVIG & Anti-D04/150 Tetanus Toxoid For Flocculation Test(2nd International Standard)04/160 Influenza Virus infectious NYMC X-14704/166 TNF-related Apoptosis-Inducing Ligand (trail), Human, rDNA-derived(1st International Reference Reagent)04/170 Influenza Virus infectious A/Wellington/1/200404/172 Influenza Virus infectious IVR-13904/176 Plasmodium falciparum DNA for NAT Assays(1st International Standard)04/198 Anti-Meningococcal Serotype P3.1 mAb04/200 Parathyroid hormone 1-34 ,Recombinant, Human(International Standard)04/202 Influenza Antigen B/ Jiangsu/10/200304/214 Influenza anti A/Vietnam/1194/04 (NIBRG-14) HA Serum (sheep SH440&SH442) 04/224 Factor V Leiden, Human gDNA, 1st International Genetic Reference Panel 200404/228 Influenza anti B/ Neuraminidase Serum04/230 Influenza anti N1 Neuraminidase Serum04/242 Influenza anti B/Jiangsu/10/2003 HA Serum (sheep)04/246 Anti-Meningococcal Serogroup W-135 mAb04/248 Anti-Meningococcal Serosubtype P1.19 mAb04/252 Protein C Concentrate, Human(1st International Standard)04/258 Influenza anti N2 Neuraminidase Serum(prepared from A/Wyoming/3/2003)04/260 Influenza anti A/New Caledonia/20/99 HA Serum (sheep)04/262 Influenza anti A/New York/55/2004 HA Serum (sheep)04/264 Influenza Antigen A/New York/55/2004 (H3N2) (NYMC X-157)05/102 Influenza Virus infectious NYMC BX-705/106 Anti-HPA-1a minimum potency reagent(2nd International Reference reagent)05/110 Influenza Virus infectious A/California/7/200405/112 Low Molecular Weight Heparin for Molecular Weight Calibration (2nd International Standard).05/122 Syphilitic plasma IgG (human)(1st International Standard)05/130 Prothrombin Mutation G20210A, Human gDNA(1st International Genetic Reference Panel 2005)05/132 Syphilitic plasma IgG and IgM (human)(1st International Standard)05/134 Anti-human papillomavirus type 16 serum (1st International Standard)05/138 Influenza Virus infectious B/Shanghai/361/200205/162 Alpha-1-Antitrypsin, plasma derived(1st International standard)05/190 Anti Meningococcal Serosubtype P1.9 Monoclonal Antibody05/192 Anti Meningococcal Serotype P2.2b Monoclonal Antibody05/234 Influenza Antigen A/Hiroshima/52/2005 (H3N2) (IVR-142)05/236 Influenza anti A/Wisconsin/67/2005 Serum (sheep)05/242 IVIG, Anti-D and Negative Control Panel05/252 Influenza anti B Neuraminidase Serum (Sheep SH463)06/108 Influenza Virus infectious IVR-11606/114 Influenza Virus Infectious A/PR/8/3406/124 Monoclonal Antibody for Serotyping Bordela pertussis Fimbrial Antigen 2 (1st International Standard)06/128 Monoclonal Antibody for Serotyping Bordela pertussis Fimbrial Antigen 3 (1st International Standard)06/140 Pertussis Antiserum(human)1st IS-WHO international Standard.06/142 Pertussis Antiserum (Human) 1st WHO Reference Reagent06/164 Influenza Virus infectious 1 VR-14206/166 Antithrombin Concentrate, Human (3rd International Standard)06/170 Influenza Antigen A/New Caledonia/20/9906/192 Influenza anti A/turkey/Turkey/1/05 (NIBRG-23) HA serum(sheepSH465 & SH466) 06/202 Human Papillomavirus (HPV) Type 16 DNA (1st International Standard)06/206 Human Papillomavirus (HPV) Type 18 DNA (1st International Standard)06/242 Influenza Virus Infectious NYMC X-161B (A/Wisconsin/67/2005 HGR)07/102 Influenza Antigen A/Solomon Islands/3/2006 (H1N1)(IVR-145)07/104 Influenza anti A/Solomon Islands/3/2006 (H1N1) (IVR-145) HA Serum (sheep 467,468,469,470)07/112 Influenza Antigen A/turkey/Turkey/1/2005 (H5N1) NIBRG-2307/132 Influenza Virus infectious B/Malaysia/2506/200407/144 Influenza Virus infectious IVR-145,07/146 Influenza anti A/HongKong/1073/99 like (H9) HA Serum (sheep)07/148 Influenza anti A/Vietnam/1194/04 (H5N1) HA Serum07/150 Human Plasma Anti-Influenza H5N1 (1st International Standard)07/164 Anti-hepatitis B surface antigen(Anti-HBs) immunoglobulin (2nd International Standard)07/182 Blood Coagulation Factor IX Concentrate, Human (4th International Standard)07/184 Influenza anti B/Malaysia/2506/2004-HA Serum (sheep)07/202 Recombinant soluble transferrin receptor (rsTfR)(1st WHO Reference Reagent)07/214 Positive Control for use in flow cytometry cross matching (FCXM)07/216 Diphtheria Toxoid (Adsorbed) (4th International Standard)07/222 RhD/SRY Plasma DNA sensitivity standard (1st International Reference Reagent)07/226 Influenza Virus Infectious A/New Caledonia/20/9907/228 Blood Coagulation Factor VIIa, Concentrate, Human, 2nd International Standard”07/246 Influenza Virus Infectious IVR-14707/268 Influenza Virus Infectious B/Brisbane/3/200707/270 BCG Vaccine of Danish 1331 sub-strain (1st WHO Reference Reagent)07/272 BCG Vaccine of Tokyo 172 sub-strain(1st WHO Reference Reagent)07/274 BCG Vaccine of Russian BCG-I sub-strain(1st WHO Reference Reagent)07/278 Influenza anti A/mallard/Netherlands/12/2000 (H7) HA serum (NIBRG-60) (sheep SH474 AND SH475)07/286-012 Hepatitis B Surface Antigen Monitor Sample07/288-012 Hepatitis B Surface Antigen British Working Standard 0.2 IU/ml07/290 Influenza Antigen A/Anhui/1/05 (H5N1) IBCDC-RG-607/294-005 Norovirus GII for Nucleic Acid Amplification Techniques07/296-005 Influenza Virus (A/Christchurch/1/2003, H1N1) for Nucleic Acid Amplification Techniques07/298-004 Influenza Virus (A/Wyoming/3/2003, H3N2) for Nucleic Acid Amplification Techniques07/300-004 Influenza Virus (B/Jiangsu/10/2003) for Nucleic Acid Amplification Techniques07/304 Anti-D for assuring operator and test performance07/306 Anti-A and anti-B in IVIG: Positive control for haemagglutination tests (International Reference Reagent)07/316 Blood Coagulation Factor VIII and Von Willebrand Factor in Plasma (6th I.S.)07/318 Meningococcal Group C Polysaccharide07/326 Blood Coagulation Factors II, IX,and X Concentrate, 6th British Working Standard. 07/328 Unfractionated Heparin (6th I.S.)07/336 Influenza Antigen A/mallard/Netherlands/12/00(H7N3) NIBRG-6007/338 Influenza anti A/Anhui/1/05 (H5)HA serum (IBCDC-RG6) (Sheep SH477)07/348 Influenza Virus infectious NYMC X-171B07/350 Blood Coagulation Factor VIII Concentrate (8th I.S.)07/358 Influenza Virus infectious NIB-5007/362 Influenza Virus infectious IVR-14907/364 Chorionic Gonadotrophin, (5th International Standard)07/B498-16 QCRHBclgMQC1-IgM Anti-HBc Quality Control Serum: Sample108/100 Influenza Antigen A/Brisbane/59/2007 (IVR-148) (H1N1)08/108 Influenza Virus Infectious NIBRG-9108/114-005 Human Adenovirus serotype 2 for Nucleic Acid Amplification Techniques08/118-004 Parainfluenza Virus serotype 3 for Nucleic Acid Amplification Techniques08/120-005 Human Respiratory syncytial virus A2 for Nucleic Acid Amplification Techniques 08/126 Influenza anti A/turkey/Turkey/1/05(N1) NA Serum (NIBRG-74) (Sheep SH485) 08/138 Influenza Virus Infectious B/Florida/4/200608/140 Influenza Antigen B/Florida/4/200608/142 Influenza anti A/Anhui/1/05 (H5) HA serum (IBCDC-RG6) (sheep SH477)08/148 Positive control for Luminex based anti-HLA Class II serology08/150 HIV-2 RNA(1st International Standard)08/154 Influenza Virus Infectious NIBRG-1208/156 Influenza Virus Infectious NIBRG-23 30060 VE308/158 Fragile X Syndrome gDNA (1st International Genetic Reference Panel)08/160 Haemophilia A, Intron-22 inversion, gDNA, (1st International Genetic Reference Panel)08/174-006 Human Coxsackie B4 for Nucleic Acid Amplification Techniques08/176-004 Parainfluenza Virus serotype 1 for Nucleic Acid Amplification Techniques08/178-004 Parainfluenza Virus serotype 2 for Nucleic Acid Amplification Techniques08/180-004 Parainfluenza virus serotype 4 for Nucleic Acid Amplification Techniques08/184 Influenza Antigen B/Malaysia/2506/200408/202 Influenza anti A/chick/Hong Kong/G9/1997/(H9) HA serum (NIBRG-94)(H9N1) 08/204 Thyroid Stimulating Antibody (2nd I.S.)08/208 Influenza Antigen Hong Kong/1073/99 (H9N2)08/210 Influenza anti A/Cambodia/R0405050/2007 (H5) HA serum (NIBRG-86)08/214 Meningococcal Serogroup C polysaccharide (1st International Standard)08/216 Influenza Antigen A/Cambodia/RO405050/2007 (H5N1)08/218 Tetanus Toxoid Adsorbed (4th International Standard)08/224-005 Human Herpes Simplex virus type 1 for Nucleic Acid Amplification Techniques 08/226-005 Human Herpes Simplex virus type 2 for Nucleic Acid Amplification Techniques 08/228 Influenza Antigen A/chick/Hong Kong/G9/1997 (H9N2) NIBRG-9108/230 Streptodornase (2nd International Standard)08/246 Influenza anti A/Brisbane/10/2007- like HA serum08/256 C1- Inhibitor, Concentrate (1st International Standard)08/258 Antithrombin, Plasma (3rd International Standard)08/262 C1 Inhibitor (Plasma)(1st International Standard)08/266 Sex Hormone Binding Globulin.(2nd International Standard)08/268 Influenza Antigen A/mallard/England/727/2006 (H2N3)NIBRG-10708/278 Influenza Antigen A/Brisbane/10/2007-like (Prepared from A/Uruguay/716/2007 (NYMC X-175C))08/282 Follicle-Stimulating Hormone, human, recombinant, for bioassay (2nd International Standard)08/298 Influenza Virus Infectious B/Brisbane/33/2008 30720 E508/300 Influenza Virus Infectious IVR-14808/304 Influenza virus infectious NYMC X-175C08/310-005 Varicella Zoster Virus(Type B) Working Reagent for Nucleic Acid Amplification Testing (NAT)08/314-006 Human Cytomegalovirus for Nucleic Acid Amplification Techniques (AD169)08/316-005 Epstein-Barr Virus for Nucleic Acid Amplification Techniques08/318-005 Human Norovirus GI Working Reagent for Nucleic Acid Amplification Testing08/320-007 Human Metapneumovirus Working Reagent for Nucleic Acid Amplification Testing 08/322-004 Human Parechovirus Working Reagent for Nucleic Acid Amplification Testing08/356 Influenza anti A/Japan/305/57 (H2) HA serum (A/Singapore/1/57-Like) (SheepSH398)08/362 Influenza Antigen A/New York/107/2003 (H7N2)NIBRG-10909/100 Influenza anti A/mallard/England/727/2006 (N3) NA serum (NIBRG-107) (Sheep SH503)09/110 Parvovirus B19 DNA Nucleic Acid Amplification Technology(NAT) based assays Genotype Panel(1st International Standard)09/112 Negative Control for use in flow cytometry cross matching (FCXM) and anti-HLA serology09/130 Influenza Virus Infectious NIBRG-12209/136 Granulocyte Colony Stimulating Factor (Human, rDNA Derived)(2nd International Standard)09/138 Genetic Reference Panel, for the quantitation of BCR-ABL translocation by RQ-PCR (1st I.S.)09/140 Prader Willi & Angelman Syndromes, Human gDNA,(1st International Genetic Reference Panel)09/148 Influenza anti A/New York/107/2003 (H7) HA serum (Sheep SH504 and SH505)09/154 Clostridium sordellii (Gas-gangrene) Antitoxin, Equine,(1st International standard) 09/162 Human Cytomegalovirus (HCMV) for Nucleic Acid Amplification Techniques (1st International Standard)09/170 Anti-Meningococcal factor H binding protein variant 1 (JAR4) monoclonal antibody 09/172 Blood coagulation Factors II, VII, IX, X Plasma (4th International Standard 2010)09/174 Influenza Antigen A/California/7/09 (H1N1)v (NYMCX-179A)(Cell Derived)09/182 VWF Factor Concentrate (2nd International Standard)09/184 Influenza Antigen A/Vietnam/1194/2004 (H5N1) NIBRG-1409/186 Chagas (anti-Trypanosoma cruzi II) antibody in human plasma(1st International Standard)09/188 Chagas (anti-Trypanosoma cruzi I) antibody in Human Plasma (1st International Standard)09/196 Influenza Antigen A/California/7/09 (H1N1)v (NIBRG-121xp) (Egg Derived)09/222 Human anti-Haemophilus influenzae b reference serum09/234 Transforming Growth Factor-BETA 3 (Human, rDNA derived TGF-ß 3) (1st International Standard)09/236 Influenza Virus Infectious IVR-15309/242 Fibrinogen Concentrate (B)(2nd International Standard)09/260 Epstein-Barr Virus for Nucleic Acid Amplification Techniques(1st International Standard)09/264 Fibrinogen Plasma (D)(3rd International Standard)09/266 GLIAL CELL-DERIVED NEUROTROPHIC FACTOR (GDNF), human,rDNA-derived09/268 Influenza Virus Infectious NIBRG-121xp09/272 Placental growth factor Ala 21 - Arg 149, human, rDNA-derived (PlGF, PlGF-1)09/274 Influenza Virus Infectious NYMC X-18509/280 Influenza Virus Infectious NIB-6409/284 Anti-Human Neutrophil Antibody 1a WHO Reference Reagent09/296 Pro-Insulin, human (1st International Standard)09/304 Influenza Virus Infectious IVR-15509/306 Influenza Virus Infectious NIBRG-14709/308 Influenza serology antigen reagent for haemagglutination inhibition assay Pandemic H1N1 2009 (X179A)09/310 Influenza Antigen A/Wisconsin/15/09 (H3N2) (NYMCX-183)09/316 Influenza Anti B Neuraminidase Serum (B/Florida/4/2006)09/B558-06 QCRHIV1RTDQC1- Anti-HIV1 Quality Control Serum: Sample 1 for Rapid Test Devices09/B584-12 QCRTHAVQC1-Total Anti-HAV Quality Control Serum: Sample109/B588-07 QCRTOXOQC1-Anti-Toxoplasma Quality Control Serum: Sample 110/104 Reteplase Reference Material10/120 Influenza Anti A/Brisbane/59/2007 (IVR 148)(H1N1) HA serum (sheep 516 and 517) 10/128 Diphtheria Polyclonal Antibody10/130 Diphtheria Monoclonal Antibody10/132 Tetanus Polyclonal Antibody10/134 Tetanus Monoclonal Antibody10/136-001 HLA-DRB1 Genotyping Reference Panel10/140 Anti-human papillomavirus[HPV] 18 serum (1st International Standard)10/142 Negative control for Luminex based anti-HLA serology10/152 HIV-1 RNA (3rd International standard)10/154-005 Anti-HCV (1 in 8 dilution)(British Working Standard)10/176 Interleukin-29 (Interferon Lamda 1)10/178 Endotoxin (3rd International Standard)10/188 Factor VIII Concentrate (13th British Standard).10/198 Anti-malaria (Plasmodium falciparum) human serum(1st International Reference Reagent)10/202 Influenza antibody (Human) to A/California/7/2009 'like' (H1N1v) virus (2nd International Standard)10/214 Influenza Anti N2 Neuraminidase Serum SH395 & SH39610/218 Influenza Anti A/California/7/2009 (N1) NA Serum (Sheep SH 521)10/226 Influenza Virus Infectious IVR-15810/232 Genomic DNA for blood group genotyping RBC1(AR1R1)(International Reference Reagent)10/234 Genomic DNA for blood group genotyping RBC12 (ODpsi)(International Reference Reagent)10/236 Genomic DNA for blood group genotyping RBC4(OR1R2)(International Reference Reagent)10/238 Genomic DNA for blood group genotyping RBC5(Brr)(International Reference Reagent)10/242 Toxoplasma gondii DNA Nucleic Acid Amplification Techniques(1st International Standard)10/252 Factor VII Concentrate(2nd International Standard)10/258 Influenza Antigen A/California/7/2009-like(NIB-74)10/260 Influenza Virus Infectious NIB-5810/262 Diphtheria Antitoxin Human IgG(1st International Standard)10/264 Hepatitis B Virus for Nucleic Acid Amplification Techniques (3rd WHO International Standard)10/272 BCG vaccine of Moreau-RJ sub-strain(1st International Reference Reagent)10/276 Influenza virus infectious BX-3110/276 Influenza virus infectious BX-3110/280 Anti-HLA Control10/286 Follicle Stimulating Hormone, Luteinizing Hormone human, urinary for bioassay(5th International Standard)10/B592-09 QCRTHBcQC1-Total Anti-HBc Quality Control Serum: Sample 110/B594-06 QCRHCVQC1-Anti-HCV Quality Control Serum: Sample110/B596-09 QCRHSV1QC1-Anti-HSV1 Quality Control Serum: Sample11050 IPV ELISA MAbs Type 1, 2 and 3 (Type 2; No: 1050)11/106 Influenza Virus infectious A/Perth/16/200911/106 Influenza Virus infectious A/Perth/16/200911/108 Influenza Virus infectious NYMC X-18711/108 Influenza Virus infectious NYMC X-18711/126 Factors II and X Concentrate (4th International standard)11/130 Influenza Virus Infectious NIBRG-1411/130 Influenza Virus Infectious NIBRG-1411/134 Influenza Antigen A/California/7/2009 (H1N1) Like (A/Brisbane/10/2010- cell derived)11/170 Erythropoietin, recombinant, for Bioassay (3rd International Standard)11/176 Low Molecular Weight Heparin 2 (3rd International Standard)11/182-001 HBV DNA Working Reagent11/184 High Molecular Weight Urokinase(2nd International Standard)11/206 Influenza anti-A/Perth/16/2009 HA Serum11/208-001 Parvovirus B19 DNA11/210 Anti-human CD4 FITC conjugated 0.5ml11/214 Blood Group Genotyping Reference Panel ((International Reference Reagent)11/216 Chagas Antibody Reference Panel ( 1st International Standard)11/218-001 MLH1/MSH2 Exon Copy Number Reference Panel11/222 Influenza Virus Infectious NIB-7911/226 Influenza Virus Infectious A/Victoria/361/201111/232 Influenza Virus Infectious B/Texas/6/201111/234 Immunoglobulin E(IgE) human serum (3rd International Standard)11/244 Influenza Virus Infectiious NYMC BX-4911/B601-05 QCRHIV1P24QC1-HIV1 p24 Antigen: Quality Control Serum: Sample111/B603-06 QCRHIV2QC2-Anti HIV2:Quality Control Serum: Sample211/B604-002 QCRFLUAH5QC1 Influenza H5 PC111/B606-05 QCRNEGQC1-Negative Quality Control Serum: Sample111/B608-02 QCRHIV1QC1-Anti-HIV1:Quality Control Serum: Sample112/100 Influenza Virus Infectious NYMC X-21712/104 International Standard for IPV 12/104 (3rd International Standard)12/106 Influenza Antigen B/Hubei-Wujiagang/158/2009 (NYMCBX-39)12/110 Influenza Antigen B/Wisconsin/1/2010 (cell derived)12/112 Influenza Antigen A/Victoria/210/2009 (H3N2) (NYMCX-187)12/114 Influenza Antigen A/Victoria/361/2011 (H3N2) (IVR-165)12/116 Influenza anti-A/Victoria/361/2011-like HA serum12/118 Influenza anti-B/Wisconsin/1/2010-like HA serum12/122 Influenza virus infectious A/turkey/Italy/3889/199912/154 Tumour Necrosis Factor alpha (human rDNA derived)(3rd International Standard)12/168 Influenza Antigen A/California/7/09 (H1N1) (NYMCX-181) Egg derived12/172 3rd HCV RNA Genotype Panel for Nucleic acid amplification techniques12/174 Infectious Virus Influenza A/California/7/200912/176 Methylated Human Serum Albumin (mHSA)12/188 Pegylated Granulocyte Colony Stimulating Factor (Human, rDNA derived) (International Standard)12/196-001 Hereditary Haemochromatosis Genotyping Reference Panel12/198 Influenza virus infectious B/Wisconsin/1/2010 34490 E512/200 Influenza virus infectious B/Brisbane/60/2008 34500 E712/202 Influenza virus infectious NYMC BX-3912/204 Influenza Virus infectious IVR-16512/208 Parvovirus B19 (3rd International Standard)12/224 HIV-1 NAT subtypes (Main)(2nd International Reference Panel Preparation)12/226 HBsAg (HBV genotype B4, HBsAg subtypes ayw1/adw2)(3rd International Standard) 12/248-001 JAK2 V617F Genotyping Sensitivity Panel12/252 ADAMTS 13 Plasma (1st International Standard)12/282 Diphtheria Toxin 1Lf/ml12/284 Anti-meningococcal serogroup Y monoclonal antibody12/290 Influenza Virus Infectious B/Brisbane/36/201212/294 Influenza Virus Infectious NYMC BX-51C12/298 Influenza Virus Infectious A/Texas/50/201212/306 Haemophilus Influenzae Polysaccharide Polyribosyl Ribitol Phosphate (PRP)(2nd International Standard)12/B611-02 Anti-VZV Quality control serum: Sample 1 QCRVZV IgM QC112/B612-04 QCRRUBIgMQC1-Anti-Rubella IgM Quality Control Serum: Sample 112/B613-03 QCRRUBQC2-Anti-Rubella: Quality Control Serum: Sample 212/B614-05 QCRHBsQC1- Anti HBs Quality Control Serum: Sample 112/B620-04 QCRHIV1P24QC2-HIV1 p24 Antigen: Quality Control Serum: Sample212/B622-06 QCRSYPHQC1-Anti-Syphilis Quality Control Serum: Sample 112/B623-003 QCRFLUAH1N1QC1-Influenza AH1N1 QC113/100 Activated Blood Coagulation Factor XI (FXIa), Human (1st International Standard) 13/102-001 Hepatitis A Virus RNA Working Reagent13/106 Influenza Antigen B/Massachusetts/02/201213/108 Anti-Meningococcal serogroup B monoclonal antibody13/112 Influenza Antigen A/Texas/50/2012 (NYMC X-223)13/116 Influenza Antigen A/Texas/50/2012 (NYMC X-223A)13/126 Influenza anti-B/Brisbane/60/2008-like HA serum13/132 Anti-Toxoplasma IgM Human. (4th International Standard).13/134 Influenza Antigen B/Massachusetts/02/2012 (Egg derived)13/146 C-Peptide, Human. 1st International Standard.13/152 Influenza Antigen B/Massachusetts/02/2012 (cell derived)13/162 Influenza Antigen A/Texas/50/2012 (NYMC X-223A) (Cell derived)13/164 Influenza Antigen A/California/7/2009 (H1N1pdm)(NYMC X-179A)13/166 Influenza anti-A/Anhui/1/2013 (N9) NA Serum13/168-001 Human Measles Mvi/Moscow Rus/1988 Genotype A Virus for Nucleic Acid Amplification Techniques13/172 Lupus Anticoagulant (1st International Reference Panel)13/176 Influenza Virus Infectious NIBRG-8813/178 Influenza Anti-A/Texas/50/2012-like HA Serum13/180 Influenza A/Anhui/1/2013 (H7) HA Serum13/182 Influenza Anti-B/Massachusetts/02/2012-like HA Serum13/198 Influenza Virus Infectious NYMC X-18113/200 Influenza Virus Infectious NIB-7413/202 Influenza Virus Infectious NIB-74xp13/206 Plasmin (4th International Standard)13/212 Diphtheria Toxoid for use in Flocculation Test (3rd International Standard)13/214 HIV-1 Circulating Recombinant Forms RNA (1st International Reference Panel) 13/216 Anti-meningococcal factor H binding protein variant 1 (JAR5) monoclonal13/218 Polio Anti Sabin type 1 (inactivated) Serum13/220 Polio Anti Sabin type 2 (inactivated) serum13/222 Polio Anti Sabin type 3 (inactivated) serum13/224 Influenza virus Infectious NIB-85. 36210 E513/228 Influenza Virus Infectious. A/Almaty/2958/2013. 35790 E413/234 Influenza antigen B/Brisbane/60/0813/242 FEIBA Concentrate 2nd NIBSC Working Reference Standard13/246 Meningococcal serogroup A polysaccharide. 1st WHO International Standard.13/248 Influenza virus infectious NIBRG-26713/250 Influenza Virus Infectious NIBRG-26813/252 Influenza virus infectious NYMC X-223A13/254 Influenza Anti-B/Brisbane/60/2008-HA serum13/256 Influenza virus infectious. NYMC x-233。
