测量的基本第九章 气体成分测量
气体成分测量

气体成分测量气体检测在工业生产、环境保护、安全检查、航空航天等领域中发挥着重要作用。
近年来频发的煤矿爆炸,有毒气体泄漏事件,使人们深刻认识到气体监测的必要性。
石油、化工、煤矿、汽车等工业的飞速发展致使大气污染日益严重,酸雨、温室效应和臭氧层的破坏引起了全世界的关注。
机场、车站、比赛场馆爆炸物的探测和危险源的定位对人们生命财产保障起到重要作用。
另外,在飞船,潜艇等密闭环境中,气体监测对保证仓内人员安全具有重要意义。
因此,对人类生存和生产环境中的各种有害的危险气体进行准确的识别和浓度测量是非常重要的。
1.MOS 气体传感器1.1 SnO2 传感器工作原理SnO2 气体传感器是一种表面电阻控制型气敏器件,其结构多为多孔制烧结体,即由很多晶粒集合而成。
许多学者的研究表明,晶粒间通过晶界或颈部沟道彼此相连,因晶粒自身体电阻较低,整个器件的电阻取决于晶界部分电阻(或颈部电阻)。
该模型及等效电路可用图表示,图中 a)为烧结体模型,b)为晶粒集合形式,c)为模型等效电路,图中 Rb 表示体电阻, Rn 表示晶界部分电阻或颈部电阻,由于晶界或颈部电子密度很小,电阻率要比晶粒内部大很多,所以 Rn 决定整个器件的气敏电阻。
气敏材料表面特性非常活泼,很容易吸附气体分子"吸附分为物理吸附和化学吸附两种,物理吸附是靠偶极子、四极子和感应偶极子的库仑力形成的,化学吸附是靠交换电子或共有电子形成的。
在常温下一般是物理吸附,高温下发生物理吸附加化学吸附。
例如,在洁净空气中,将 SnO2 气敏材料加热到一定温度,空气中的氧gas O 2就在气敏材料表面发生化学吸附变成-2O ,-O 以及-2O ,氧发生化学吸附存在如下平衡:式中 S 为可被占据的化学吸附位,α的值可为 1/2,1 和 2,分别代表-2O ,-O 以及 -2O ,s O 2 为在吸附位 S 上化学吸附的氧。
由于对氧发生化学吸附,在多晶半导体晶界处会形成空间电荷层即势垒,该势垒能阻碍电子在电场作用下的漂移运动,自由电子浓度下降引起气敏材料电阻升高。
空气成分的测定实验原理

空气成分的测定实验原理一、实验目的本实验旨在通过测定空气中氧气、氮气和二氧化碳的含量,了解空气成分的组成及其浓度变化规律。
二、实验原理1. 空气成分及其浓度空气是一种混合物,主要由氮气、氧气和少量的其他气体组成。
其中,氮气占78%,氧气占21%,其他包括二氧化碳、水蒸汽等占1%。
在大多数情况下,空气中二氧化碳含量较低,通常为0.03%-0.04%。
2. 测定方法(1)测定空气中的二氧化碳含量:利用饱和钙水吸收法。
将经过干燥剂干燥后的样品与饱和钙水反应,反应生成的CaCO3沉淀可以用称重法确定二氧化碳含量。
(2)测定空气中的总压力:利用压力计或差压计。
将压力计或差压计接入样品管道中,在相同条件下比较样品管道与参比管道之间的压力差,即可得到样品管道内的总压力。
(3)测定空气中的氧气含量:利用分光光度法或电化学法。
分光光度法是利用氧气与还原剂反应,生成吸收峰,通过测定吸收峰的强度来确定氧气含量。
电化学法是利用电极在不同氧气浓度下的电位变化来确定氧气含量。
(4)测定空气中的氮气含量:利用差压计或热导仪。
差压计是将样品与参比管道之间的压力差转换为流量信号,通过流量信号和总流量计算出样品管道内的氮气含量。
热导仪是利用热导率与成分相关联的原理进行测定。
三、实验步骤1. 测定空气中二氧化碳含量(1)取一只干燥管,加入适量干燥剂,并将其密封。
(2)将待测空气通入干燥管内,使其与干燥剂接触。
(3)取出干燥管,打开密封盖,加入饱和钙水至标志线处。
(4)摇晃干燥管,使饱和钙水均匀分布。
(5)密封干燥管,摇晃数分钟,使反应充分进行。
(6)取出干燥管,用天平称重,并记录质量。
(7)将干燥管加入适量去离子水中,振荡摇匀,使沉淀溶解。
(8)用滤纸过滤溶液,并将过滤液转移至锥形瓶内。
(9)加入几滴酚酞指示剂,并用0.1mol/L HCl滴定至酚酞变色为止。
(10)计算二氧化碳含量。
2. 测定空气中总压力(1)将压力计或差压计接入样品管道中,并调整好仪器参数和读数范围。
九年级化学空气成分测定知识点

九年级化学空气成分测定知识点空气是我们生活中不可或缺的重要物质,但你知道空气的成分是什么吗?今天我们就来探索一下九年级化学课程中关于空气成分测定的知识点。
首先,我们需要了解空气中常见气体的测定方法。
常见气体主要有氮气、氧气、二氧化碳和氢气。
其中,氮气占据空气的主要成分,约占78%,氧气占21%,二氧化碳和其他气体则只占1%左右。
那么我们如何测定空气中这些气体的含量呢?氮气的测定方法相对简单,一般可以使用气体比色管来进行测定。
这种方法利用了气体分子对特定颜色的吸收和发射特性,将氮气的浓度转化为管内特定颜色的深浅程度,从而测定氮气的含量。
氧气的测定方法则相对复杂一些。
一种常见的方法是使用电解法,通过电解水来制取氢气和氧气。
在这个过程中,气体会在两个电极上产生反应,最终生成氢气和氧气。
通过测量电解水中气体的体积变化,可以得知氧气的含量。
二氧化碳的测定方法也有多种。
最常见的方法是使用酸碱滴定法。
首先,将样品溶液与一种酸反应,生成一种可滴定的物质。
然后,将滴定剂滴入溶液中,当溶液中所有的反应物都反应完毕时,溶液的颜色会发生变化。
通过测定滴定剂的用量,可以计算出二氧化碳的含量。
最后,我们来看看如何测定氢气。
氢气的测定方法常常利用它与氧气的反应生成的水的量来确定。
我们可以使用气体瓶装装置进行实验,首先在气体瓶中装入氢气和氧气,然后通过点燃观察生成的水的量。
根据生成水量的变化,可以计算出氢气的含量。
除了以上提到的气体成分,空气中还含有气溶胶、颗粒物、臭氧等物质。
对于这些物质的测定,常用的方法包括气溶胶采样法、堡集器法、红外吸收法等。
利用这些方法,我们可以测定出这些物质在空气中的含量,并对它们的浓度进行分析。
总结一下,九年级化学课程中关于空气成分测定的知识点主要包括氮气、氧气、二氧化碳和氢气的测定方法,以及其他成分如气溶胶、颗粒物、臭氧的测定方法。
通过学习这些知识点,我们可以更好地了解空气的成分及其含量,进而更好地保护和改善我们的环境。
空气成分测定实验原理

空气成分测定实验原理
空气成分测定实验是一项非常常见的实验,通过该实验可以对空气采样进行分析,了解空气组成和质量。
本文将介绍空气成分测定实验的原理、步骤和注意事项,希望能对读者进行指导和帮助。
一、实验原理
空气主要由氮气、氧气、二氧化碳、少量的氢气、氦气、氖气等气体组成。
空气成分测定实验的原理是根据不同气体的物理和化学性质进行分离和检测。
主要采用分离漏斗、化学吸管、瓶塞式密度计、总量分析仪等仪器设备。
二、实验步骤
1.准备工作:将密闭容器平放在水平桌面上,连接好总量分析仪和瓶塞式密度计。
2.空气采样:用化学吸管采集空气,然后把气体尽量分散到总量分析仪中。
3.密度的测定:在瓶塞式密度计里先注入一定的水,然后钻上导管塞,插入温度计和压力计即可。
4.采样量的测定:打开分离漏斗,让一定量的空气在分离漏斗内分离,利用容积取量器,将气体体积取出。
5.气体分析:通过总量分析仪,分别分析空气样品中的氮气、氧气、二氧化碳等成分的含量。
根据测定结果,计算出每个成分在空气
中的百分比。
三、注意事项
1.实验过程中严格控制温度和压力,以保证采样的可靠性。
2.实验过程中需要注意安全,尽可能避免毒气和可燃气体的泄漏
和聚集。
3.实验前需要进行设备的检查和校准,以保证仪器精度和准确性。
4.实验后需要回收废气和化学废液,以保护环境和工作人员的安全。
以上就是空气成分测定实验的原理、步骤和注意事项,通过该实
验可以了解空气中各组分的含量和质量,为环境监测和治理提供了依
据和参考。
希望本文对读者有所帮助。
9第九章组分浓度测量技术解读

若发射光谱线包含振动带,则TR’和TV’可通过计算得到。分子在基态的转动温度可由吸收 光谱的实验数据获取。吸收光谱线的强度为:
I C Sq abs 2 JJ JJex (p 7h k .3. 2c T )F R J G T 其中:C2为一常数。 由上式对ln(Iabs/C2SJ’j” Vj’J”)和FJ”作图,得斜率-hc/kTR”,可确定转动温度。 若吸收介质的温度及其分子的相关数据已知,则可由吸收光谱数据获取绝对浓度。 谱线的吸收峰可描述为:
ln2 C D
(7.2.3)
这里D和C分别为多普勒加宽碰撞和加宽线型的全宽。 如果火焰的温度已知,则可以对 和N进行最小二乘拟 合和光谱线的匹配计算,即可确定相应组分的浓度。
二、激光吸收法
图7.2.1 激光吸收法测量组分浓度系统示意图图 BS:分束器;PD:光电倍增管
7.2.2 O2、CO、CO2、NO、N2O激光测量系统示意图
IN=(IN-1) (SiN/SiN-1) = N+1N
(7.4.3)
设得到的路径积分测量值的总数目为M。然后利用强度的预测值,根据式 (7.4.1),由路径积分强度的不同测量值得到M的解。预测值的修正如下:
X X ( kii)iM 1jM 1(k1 ii)E (ij/Tj)I(i/Xi)
(7.4.4)
其中吸收系数 被定义为: =S(T)(-o)N
(7.2.2)
其中:S(T)是温度为T时吸收谱线的强度,可通过光谱线的相关参数计算, (-o)为以o为中心波长的谱线的线型, N为吸收气体组分的浓度。
在空气中燃烧的火焰的吸收光谱的线型由于既有多普 勒加宽效应的影响,又有碰撞加宽效应的影响,通常用 福格特(Voigt)线型来描述其谱线的形状,即有
空气成分的测定实验原理

空气成分的测定实验原理引言空气是地球上生命存活的重要基础,了解空气的成分是对环境质量进行监测和评估的基础。
本文将详细介绍与空气成分测定相关的基本原理,包括采样、分析方法以及常见的测定指标。
采样方法空气成分的测定首先需要采集空气样品,以代表空气中的成分。
常用的采样方法包括积分式和即时式两种。
积分式采样法积分式采样法通过收集一段时间内的空气样品,以获取平均成分浓度。
常见的积分式采样方法有气泡罐、活性碳管、气候箱等。
1.气泡罐:利用气泡罐采样时,首先将罐内真空抽乾,并封闭好。
然后将气泡罐接入采样点,打开阀门,让空气进入罐中。
采样结束后,关闭阀门,再次抽真空,以排除外界污染物。
最后,利用气相色谱或质谱仪等仪器分析样品中的成分。
2.活性碳管:活性碳管是一种含有大量微小孔隙的吸附材料,可以吸附空气中的有机物。
采样时,将活性碳管装入采样装置中,通入空气进行吸附。
采样结束后,取出活性碳管,用溶剂润洗,得到吸附在活性碳管上的有机物。
再通过气相色谱等分析方法,对有机物进行定量分析。
3.气候箱:气候箱是一种室内环境模拟装置,可以控制温度、湿度、气流速度等参数。
采样时,将气候箱的条件设置为待测空气的环境参数,然后将空气进入气候箱中,进行湿度、温度、气流等参数的监测和分析。
即时式采样法即时式采样法通过即时采集空气样品,得到短时间内的成分浓度。
常见的即时式采样方法有吸收器、泵吸法等。
1.吸收器:吸收器是一种通过溶液吸收特定成分的装置。
采样时,将吸收液放置在吸收器中,空气经过吸收器时,特定成分会被溶于吸收液中。
采样结束后,取出吸收液,通过化学分析方法进行定量分析。
2.泵吸法:泵吸法是一种通过抽吸空气进样的方法。
采样时,使用抽气泵将空气吸入样品瓶中,然后进行分析。
这种方法适用于气体浓度较高的情况。
分析方法获取样品后,需要利用适当的分析方法来测定空气中各种成分的浓度。
气相色谱法气相色谱法是一种通过气相色谱仪分离和检测空气中有机物的方法。
第九章 气体成分分析1
λF
1000 L
②对于确定的电极体系,浓度和电导之间的关系式 可写为:
m b G=c + K K
其中:K ——电极常数,K=L/F;(在任一浓度附 近,把λ看作常数时) m——常数m=λ/1000;b——与所选的电导值有 关的常数。
(2)测量过程 )测量过程:分仪器:由取样系统、分 析器和测量显示部分组成。 a.被分析碘氧化 炉,将一氧化碳氧化成二氧化碳:
2.特点:不断更新电导液。仪器装备了再生 特点: 特点 装置,用强碱性阴离子交换树脂除去碳酸根, 使电导液再生。 3.适用条件 适用条件 适用于测量含微量的 和CO2组分的气体。 含微量的CO和 含微量的 组分 可以分别测量气体中CO2的量及CO的量,也 可测量气体中CO2与CO的总量。
电导分析仪 电导率变送器
第九章 气体成分分析
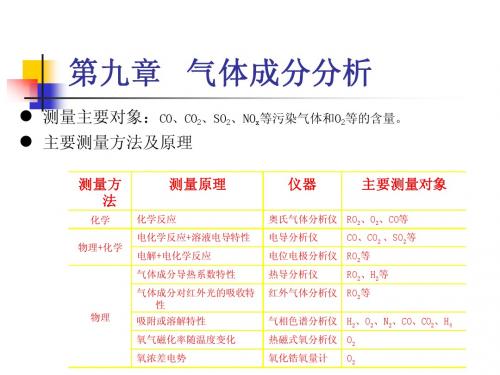
测量主要对象:CO、CO2、SO2、NOx等污染气体和O2等的含量。 主要测量方法及原理
测量方 法
化学 物理+化学
测量原理
化学反应 电化学反应+溶液电导特性 电解+电化学反应 气体成分导热系数特性 气体成分对红外光的吸收特 性
仪器
奥氏气体分析仪 电导分析仪 电位电极分析仪 热导分析仪 红外气体分析仪 气相色谱分析仪 热磁式氧分析仪 氧化锆氧量计
5CO + I 2 O5 → 5CO2 + I 2
用硫胺吸收I2,CO2进入分析器。
b.用氢氧化钠溶液吸收所得的二氧化碳:
2 NaOH + CO2 = Na2CO3 + H 2O
由于OH-的当量电导大于 32-的当量电导, 大于CO 大于 通过测量氢氧化钠溶液吸收CO2前、后的电 导改变,即可确定二氧化碳被吸收的量, 也就是一氧化碳的量,显示电路以CO含量 的形式指示出来。(在一定范围内,氢氧 化钠溶液电导的变化与一氧化碳的量有线 性关系。)溶液的电导是用惠斯登电桥电 溶液的电导是用惠斯登电桥电 路测量的。 路测量的
化学空气的成分测定原理

化学空气的成分测定原理化学空气的成分测定主要是通过各种分析方法,包括物理方法和化学方法来确定空气中各种气体和气体组分的含量。
首先,我们需要了解空气的成分。
空气主要由氮气、氧气、水蒸气、二氧化碳以及其他一些稀有气体和气体微量成分组成。
其中,氮气和氧气是空气的两个主要组分,分别占据约78%和21%的体积。
水蒸气的含量因地理位置和季节而异,一般在0-4%之间,二氧化碳的含量在稀薄大气中约为0.04%,对于封闭环境(如室内)来说,二氧化碳的含量会稍微高一些。
常见的空气成分的测定方法包括但不限于以下几种:1. 气相色谱法:气相色谱法是根据气体成分在固定填料上的分离特性,通过分析样品溶液的色谱图来确定各种气体成分的含量。
这是一种常用的、高效的气体成分分析方法。
2. 气体溶解度测定法:通过将气体与溶液接触,进而测定气体在溶液中的溶解度,从而推断空气成分的含量。
这种方法常用于测定水蒸气和氧气的含量。
3. 紫外-可见吸收光谱法:利用气体分子对特定波长的紫外或可见光的吸收特性,根据吸收光的强度来确定气体成分的含量。
这种方法常用于测定氧气和二氧化碳的含量。
4. 高压电离法:高压电离法是将空气样品置于高压电场中,通过测量空气中正负离子的电流来确定气体成分的含量。
这种方法对于微量气体成分的测定比较有效。
5. 重力法:重力法通过密度差异来测定气体成分的含量,通过从气样中吸收某些成分,然后根据样品质量的变化推算出气体成分的含量。
这种方法常用于测定水蒸气的含量。
这些方法的原理都是基于气体成分在特定条件下的物理和化学特性,从而进行分离和测定。
不同的方法适用于不同的气体成分测定,选择合适的方法取决于所要测定的气体成分的种类和含量范围。
需要注意的是,空气是一个复杂的混合气体,在不同的环境中成分可能会有所不同。
因此,为了准确测定空气成分,需要根据具体的实验条件和要求选择合适的分析方法,并在测定前对样品进行适当的预处理和准备。
综上所述,化学空气的成分测定原理主要涉及各种分析方法,通过物理和化学性质的分析,可以准确测定空气中各种气体和气体组分的含量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
气体成分测量
第九章
气体成分测量
常用气体成分测量仪表
气体成分测量仪表的校正
建筑环境与设备工程气体成分测量的应用
气体成分测量应用实例
9.1概 述
测量主要对象:CO、CO2、SO2、NOx等污染气体和O2等的含量。 主要测量方法及原理
测量方法
化学 物理+化学
测量原理
化学反应 电化学反应+溶液电导特性 电解+电化学反应 气体成分导热系数特性 气体成分对红外光的吸收特性
用来测量锅炉烟气成分的一般采用三管分析仪
氢氧化钾水溶液吸收三原子气体:
CO2 2KOH K2CO3 H 2O
SO2 2KOH K2 SO3 H 2O
焦性没食子酸的碱溶液吸收氧气
C6 H 3 (OH )3 3KOH C6 H 3 (OK )3 3H 2O
4C6 H 3 (OK) 3 O2 2(KO) 3 C6 H 2 2C6 H 2 (OK) 3 2H 2 O
9.2.2 电导分析仪
原理:利用某种特定的溶液选择性地与混合气体中的某些成分
发生反应,溶液电导改变,电导的变化与溶液浓度有关,测定 溶液电导的方法来测定溶液浓度,该浓度由混合气体中参加反 应的气体成分含量决定。
m b Gc K K
结构:电导池:内装特定溶液与被测成分反应,分参比池
和测量池;电极:测量溶液电导,有筒状电极和环状电极。
热导分析仪
结构:热导式气体分析仪的核心部件为
热导室,它是一个圆柱形垂直放置的金属 气室,被测气体进上,室内垂直悬挂一根 铂电阻丝,既是加热元件,又是测量元件, 其阻值与被测混合气体的导热系数存在函 数关系。
Rn R0 (1 at c ) K
2 2 R0 I a
热导室结构
可用于二氧化碳、二氧化硫、氢气、氩气合氦气的成分分析
CuNH 3 2 Cl 2CO CuCO2 Cl 2NH 3 氨性氯化亚铜溶液吸收一氧化碳
单管
三管
四管 奥氏气体分析仪
六管
七管
使用: 用前要气密性检查,用被测气体多次冲洗系统,排出残留的其 它气体;
水准瓶的升降动作要缓慢,防止吸收液或封闭液冲入连通管;
排除量筒中废气时,先抬高水准瓶再开旋塞,关闭旋塞后再放 低水准瓶; 测试读数时,水准瓶与量筒的液面必须在同一水平高度; 仪器使用环境温度应保持相对稳定。
9.2.3 热导分析仪
原理:混合气体中待测组分含量变化,引起混合气体导热系
数变化 。彼此之间无相互作用的多组分混合气体,它的导热 系数可近似地认为是各组分导热系数的算术平均值 。
i ci 1 c1 (1 c1 )2
i 1 n
热导分析仪可把导热系数的变化转换为电阻的变化,然后测量 电阻值,从而得到待测组分含量值。
E E0e
klc
结构
由红外光源、切光器、气室、光检测器及相应的供电、 放大、显示、 记录系统组成。
多要用来测量含有CO、CO2、NH3以及气态烃类,但不能测量单原子分 子和对称结构无极性双原子分子。
9.2.6 氧量分析仪器
(一)热磁式氧分析仪 原理:氧气是一种磁化率远大于其他气体的顺磁性气体,在具有磁场梯
热磁式氧分析仪 氧化锆氧量计
9.2.1 奥氏气体分析仪
原理:使气体混合物与吸收液逐一接触,某一种吸收液只吸收 混合气体中某一种气体,而不吸收其它气体。根据吸收 前后气体体积之差即可计算出被测的某一种气体含量。
结构:量筒用来测量气体体积;水准瓶用来调节烟气流动;吸 收瓶用来吸收某种特定气体成分,有单管、三管、四管、 六管和七管之分。
。 度和温度梯度的环境中,若混合气体中含氧量变化,则其磁化率会随变化, 从而引起热磁对流强度变化,处于磁场中的热电阻温度传感器(铂丝)因 对流换热量变化而温度变化,引起其阻值改变,通过电桥将传感器的阻值 变化以电压的形式反映出来,则该电压读数变化就与混合气体中的含氧量 有关
9.2.4 电位滴定分析仪
原理:在试液中加入适当物质,以一定强度的恒定电流进行电解,
使之在工作电极上电解产生一种试剂(称滴定剂),该试剂与被测 物质在库仑池进行定量反应,反应终点形成的电流与被测成分的含 量有关。
结构:
恒流电源、库仑池、电极、显示部分
电位滴定二氧化硫分析仪工作原理 1—铂丝阳极;2—活性炭参比电极;3—铂网阴极; 4—库仑池;5—放大器
电位滴定分析仪电极源自红外线气体分析器的基本组成 1、2-红外光源;3-切光片;4、5-滤光镜(气室);6-测量室; 7-参比气室;8-使两光路平衡的遮光板;9-薄膜电容微音器; 10-固定金属片;11-金属薄膜
红外CO2气体分析仪
9.2.5 红外气体分析仪
原理:
利用被测气体对红外光的特征吸收来进行定量分析。被测 气体通过受特征波长红外光照射的气室时,被测组分吸收 红外光,透射光强度与入射光强度、吸光组分浓度之间的 关系遵守比尔定律
电导分析仪
电导率变送器
使用:
可用于测量CO、CO2 、SO2等 电导池中吸收液种类应根据测量不同种类的气体成分需要而改变; 使用前用标准被测气体或标准被测气体溶液标定; 使用中并要定期补充吸收液; 为了保证吸收环境相同,可采用以下方法进行温度补偿: (1)使被测溶液恒温; (2)在测量线路中加补偿元件; (3)采用双电导池结构的参比测量法
测量系统构成
取样系统:用于正确地取出被分析介质的样品; 试样预处理系统:对试样进行过滤、稳压、冷却、干燥、定 压、分离等操作; 检测器:利用某种物理或化学原理将被测组分的含量转换成 标准输出信号; 信号处理和显示系统:对发送器输出的信号进行补偿、放大、 运算和显示。
9.2 常用气体成分测量仪表
奥氏气体分析仪 电导分析仪 热导分析仪 电位滴定分析仪 红外气体分析仪 氧量分析仪器
仪器
奥氏气体分析仪 电导分析仪 电位电极分析仪 热导分析仪 红外气体分析仪
主要测量对象
RO2、O2、CO等 CO、CO2 、SO2等 RO2等 RO2、H2等 RO2等
物理
吸附或溶解特性
氧气磁化率随温度变化 氧浓差电势
气相色谱分析仪
热磁式氧分析仪 氧化锆氧量计
H2、O2、N2、CO、CO2、H4
O2 O2
