广东省实验中学2012-2013学年(上)高三级化学考试
广东省实验中学高二数学上学期期中试题 理 北师大版

广东实验中学2012—2013学年(上)高二级模块考试理科数学本试卷分基础检测与能力检测两部分,共4页.满分为150分。
考试用时120分钟.注意事项:1.答卷前,考生务必用黑色字迹钢笔或签字笔将自己的姓名和考生号填写在答卷上,并用2B铅笔填涂学号.2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其它答案标号,不能答在试题卷上.3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后写上新的答案;不准使用铅笔和涂改液.不按以上要求作答的答案无效.第一部分基础检测(共100分)一、选择题:本大题共8小题,每小题5分,共40分,在每小题给出的四个选项中,只有一项是符合题目要求的.1.下列说法错误的是()A.棱柱的两个底面互相平行B.圆台与棱台统称为台体C.棱柱的侧棱垂直于底面D.圆锥的轴截面是一个等腰三角形2.下列几何体各自的三视图中,有且仅有两个视图相同的是( ).A.①② B.①③ C.①④ D.②④3.若m、n为两条不同的直线,α、β为两个不同的平面,则以下命题正确的是( ).A.若m∥α,n∥α,则m∥n B.若m∥n,m⊥α,则n⊥αC.若m∥β,α∥β,则m∥αD.若α∩β=m,m⊥n,则n⊥α4.如图,一个水平放置的平面图形,其斜二测直观图是△OAB,OB=AB=2,则该直观图所表示的平面图形的面积为()A.22 B.42 C.2D.25.已知P为△ABC所在平面外一点,且PA、PB、PC两两垂直,则下列命题:①PA⊥BC;②PB⊥AC;③PC⊥AB;④ AB⊥BC. 其中正确的( )yxOABA .①②③B .①②④C .②③④D .①②③④6.在一个直径为16cm 的圆柱形水桶中放入一个铁球,球全部没入水中后,水面升高了4cm ,则球的半径是( ) A .8cm B .cmC ..7.如图,已知二面角α-l -β为120°,AB ⊂α,CD β⊂AB⊥l 于A ,CD⊥l 于D ,且AB=AD=CD=1,则BC=( )A B C .1D .28.如图,在棱长为a 的正方体1111D C B A ABCD -中,P 为11D A的中点,Q 为11B A 上任意一点,F E 、为CD 上任意两点,且EF 的长为定值,则下面的四个值中不为定值的是( )A .点P 到平面QEF 的距离B .直线PQ 与平面PEF 所成的角C .三棱锥QEF P -的体积D .二面角Q EF P --的大小二、填空题:本大题共5小题,每小题5分,共25分.9.点A(x ,2,3)与点B(-1,y ,z )关于坐标平面yOz 对称,则x =_____,y =______,z =______. 10.点P 和不共线三点A ,B ,C 四点共面,且对于空间任一点O ,都有122OP AB OB OC λ=-+u u u r u u u r u u u r u u u u u r,则λ=_____________.11.已知:直线1l :2x+3y-1=0,2l :Ax-6y+C=0,当A,C 满足条件:__________时,1l //2l .12.已知(1,1,2),(1,1,3)a b ==--r r ,且()ka b +r r//(a b -r r ),则k=______.13.已知直线l 的斜率k ]33,1(-∈,则直线l 的倾斜角的范围是______________. 三、解答题:本大题共3小题,共35分.解答应写出文字说明、证明过程或演算步骤. 14.(本小题满分11分)C 1A C已知直线m 过点(-1,2),且垂直于l : x+2y+2=0 (1)求直线m ;(2)求直线m 和直线l 的交点。
广东省实验中学2012届高三阶段检测试题

广东省实验中学2012届高三阶段检测试题英语本试卷共10页,满分135分。
考试时间120分钟。
注意事项:1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名和学号填写在答题卡和答在密封线内相应的位置上,用2B铅笔将自己的学号填涂在答题卡上。
2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;如需改动,用橡皮擦干诤后,再选涂其他答案:不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔在答卷纸上作答,答案必须写在答卷纸各题目指定区域内的相应位置上,超出指定区域的答案无效:如需改动,先划掉原来的答案,然后再写上新的答案:不准使用铅笔和涂改液。
不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁和平整。
5.信息匹配选项,E项请在答题卡上填涂AB;F项请在答题卡上填涂CD。
I 语言知识及应用(共两节,满分45分)第一节完形填空(共15小题:每小题2分,满分30分)阅读下面短文,掌握其大意,然后从1~15各题所给的A、B、C和D项中,选出最佳选项,并在答题卡上将该项涂黑。
Ben Franklin was right, at least on the healthy part."Early to bed and early to rise"appears to have helped a cross-section of early-bird Australian 1 keep slimmer and more physically active than their night-owl peers, even though both groups got the _2_amount of sleep. A study in the Oct. 1 issue of the journal Sleep___3___the bedtimes and wake times of 2,200 Australian participants, ages 9 to 16, and compared their weights and___4__of free time over four days. Children who went to bed___5___and got up late were 1.5 times more likely to__6__obese than those who went to bed early and got up early.Furthermore,late-nighters were almost twice as likely to be physically__7___and 2.9 times more likely to sit in front of the TV and computer or play video games for more hours than guidelines.__8__. "The children who went to bed late and woke up late, and the children who went to bed early and woke up early got virtually the same amount of sleep__9___," said co-author Carol Maher,PhD,a postdoctoral fellow with the University of South Australia. "Scientists have__10___in recent years that children who get less sleep__11__to do worse on a variety of health outcomes,including the risk of being overweight and obese. Our study suggests that the__12__of sleep is even more important.""It is widely accepted that the sleep patterns of adolescents are___13__different from children and adults, and that it is normal for adolescents to stay up very late and sleep in late in the morning,"Maher said."Our findings show that this sleeping pattern is associated with___14__activity patterns and health outcomes, and that the adolescents who don't__15___this sleep pattern do better."1. A. people B. adults C. youths D.children2. A. different B.great C. little D. same3. A. published B.stated C. wrote D. recorded4. A. possession B. uses C. control D. opinions5. A. late B. early C. more D.less6. A. have B. become C. avoid D. start7. A.healthy B. fat C. inactive D. ill8. A. recommend B. promote C. claim D. encourage9. A.in time B. in total C. all over D. all around10. A. predicted B. studied C. surveyed D. realized11. A. get B. learn C. used D. tend12. A. amount B. timing C. place D. quality13. A. fundamentally B. equally C. potentially D. mainly14. A. beneficial B. unfavorable C. desirable D. changeable15. A. do B. make C. follow D. fall第二节语法填空(共10小题;每小题15分,满分15分)阅读下面短文,按照句子结构的语法性和上下文连贯的要求,在空格处填入一个适当的词或使用括号中词语的正确形式填空,并将答案填写在答题卷标号为16~25的相应位置上。
广东实验中学 2021—2022 学年(上)高二级期中考试化学试卷

广东实验中学2021—2022 学年(上)高二级期中考试化学本试卷分选择题和非选择题两部分,共8 页,满分100 分,考试用时75 分钟。
注意事项:1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考号填写在答题卷上。
2.选择题每小题选出答案后,用2B 铅笔把答题卷上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其它答案;不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卷各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液.不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束后,将答题卷收回。
相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 Al 27 Fe 56 Cu 64 Zn 65第一部分选择题(共44 分)一、(每题2 分,共20 分)1.3.25 g 锌与100 mL 1 mol·L-1 的稀硫酸反应,为了加快反应速率而不改变H2 的产量,可采取的措施是( )A.加入少量锌粒B.滴加几滴硫酸铜溶液C.滴加几滴浓硝酸D.滴加几滴浓盐酸2.1,3-丁二烯(CH2=CH—CH=CH2)与HBr 发生1,2-加成反应分两步进行:第一步H+进攻1,3-丁二烯生成碳正离子();第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。
下列说法正确的是( )A.第一步反应速率大于第二步反应速率B.加入催化剂可以改变该反应的反应热C.该总反应为放热反应D.两步均为吸热反应3.下列事实能用勒夏特列原理解释的是( )A.工业合成氨选择500 ℃B.SO2 氧化成SO3,需要使用催化剂C.光照新制氯水时,溶液的颜色逐渐变浅D.由NO2(g)和N2O4(g)组成的平衡体系,加压后颜色加深4.已知热化学方程式2SO 2 (g)+O 2 (g) 2SO 3 (g) ΔH=-Q kJ/mol(Q>0) ,则下列说法正确 的是( )A .降低温度,平衡正向移动,热化学方程式中的 Q 值增大B .若该反应放热 Q kJ ,则此过程中有 2 mol SO 2(g)被氧化C .将 2 mol SO 3(g)置于一密闭容器中充分反应,需吸收Q kJ 的热量 D .恒温下,增大压强,可增大活化分子百分数,从而加快反应速率5.三氯氢硅(SiHCl 3)是制备硅烷、多晶硅的重要原料,在催化剂作用下可发生反应: 2SiHCl 3(g)SiH 2Cl 2(g)+SiCl 4(g),在 50 ℃和 70 ℃时 SiHCl 3 的转化率随时间变化的结果如图所示。
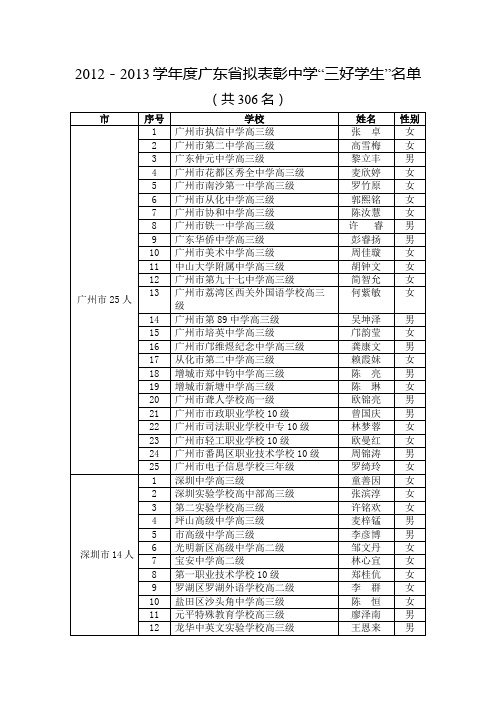
2012-2013学年度拟表彰广东省中学“三好学生”名单
男
3
惠州市华罗庚中学高三级
刘烜奕
男
4
惠州市惠城惠台学校九年级
陈华靖
女
5
惠州市惠城惠港中学高三级
邱耀庆
男
6
惠州市博罗县博罗中学高三级
徐芷君
女
7
惠州市惠东县惠东中学高三级
肖晓婷
女
8
惠州市惠东中学高级中学高三级
张国明
男
9
惠州市龙门县龙门中学高二级
李晓慧
女
10
惠州市惠州大亚湾经济技术开发区第一中学九年级
陈小群
女
7
湛江市麻章区第一中学高三级
黄文武
男
8
湛江市吴川市覃巴中学中学高三级
欧沈健
女
9
湛江市吴川市第一中学高三级
黄俊琳
男
10
湛江市吴川市张炎纪念中学高三级
谭伟健
男
11
湛江市徐闻县实验中学高三级
林子植
男
12
湛江市徐闻中学高三级
肖阳阳
女
13
湛江市雷州市第二中学高三级
吴梅青
女
14
湛江市雷州市第三中学高三级
2012-2013学年度广东省拟表彰中学“三好学生”名单
(共306名)
市
序号
学校
姓名
性别
广州市25人
1
广州市执信中学高三级
张卓
女
2
广州市第二中学高三级
高雪梅
女
3
广东仲元中学高三级
黎立丰
男
4
广州市花都区秀全中学高三级
麦欣婷
女
5
广州市南沙第一中学高三级
广东省实验中学2015届高三第一次阶段考试化学

广东实验中学2015届高三阶段考试(一)化学7.能在水溶液中大量共存的一组离子是A.Al3+、Mg2+、SO-24、CO-23B.NH+4、OH-、Cl-、HCO-3C.K+、SO2-4 、Cu2+、NO-3D.H+、I-、NO-3、SiO2-38.设n A为阿伏加德罗常数的数值,下列说法正确的是A.铁与足量稀硝酸反应,1 mol Fe失去电子数为2n AB.常温常压下,22.4L 乙烯中含极性共价键数目为5n AC.1 L 1 mol·L-1的NH4Cl中有n A个NH4+D.46 g NO2和N2O4混合气体中含有原子数为3N A9.下列有关物质性质的应用正确的是A.液氨汽化时要吸收大量的热,可用作制冷剂B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸C.生石灰能与水反应,可用来干燥氯气D.氯化铝是一种电解质,可用于电解法制铝10.下列有关化学实验的叙述正确的是A.用待测液润洗滴定用的锥形瓶B.配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸C.用稀硝酸洗涤做过银镜反应的试管D.液溴保存时液面覆盖一层水,装在带橡胶塞的试剂瓶中11.下列各项叙述Ⅰ,Ⅱ都正确且二者的原理最相似的是叙述Ⅰ叙述ⅡA FeS难溶于水,却溶于稀硝酸CaCO3难溶于稀硫酸,却溶于醋酸B 浓硝酸要密封保存阴凉处漂白粉要密封保存在阴凉处C 盐酸与铁反应生成氯化亚铁少量氯气与铁反应生成氯化亚铁D 碳酸钠溶液显弱碱性氯化铵溶液显弱酸性12.同主族常见的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性强弱顺序为:HXO4<HYO4<HZO4,下列判断不正确...的是A.Y 单质可以在海水中提取B.单质氧化性: Y>ZC .气态氢化物稳定性:HX<HZD .离子半径: X ->Y -22.下列有关实验操作、现象和解释或结论都正确的是选项实验操作现象 解释或结论A 过量的Fe 粉中加入稀HNO 3,充分反应后,滴入KSCN 溶液溶液呈红色稀HNO 3将Fe 氧化为Fe 3+B AgCl 沉淀中滴入稀KI 溶液 有黄色沉淀出现AgI 比AgCl 更难溶C Al 箔插入稀HNO 3中无现象 Al 箔表面被HNO 3氧化,形成致密的氧化膜D 用玻璃棒蘸取浓氨水点到红色石蕊试纸上试纸变蓝色浓氨水呈碱性23.已知:X 、Y 、Z 、W 为短周期元素,原子半径X :99pm Y: 154pm Z :125pm W: 117pm ,X Y W 位置如右图所示(副族省略),X 、Y 、Z 的最高价氧化物对应的水化物相互能反应,下列说法正确的是A .元素Z 处于周期表的阴影位置B .非金属性:X>WC .X 与W 形成化合物熔点很高,为离子化合物D .Y 、W 的最高价氧化物对应的水化物能反应30.(16分)化合物G 的合成路线如下:(1)D 中含氧官能团的名称为 ,D 的分子式为 ,1 mol D 完全燃烧所需氧气为 mol ; (2)写出A →B 的化学反应方程式 。
广东省广东实验中学2022-2023学年高三上学期第一次阶段考试化学试题(解析版)

6.价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,以物质类别为横坐标的二维平面图像。如图为氯元素的价类二维图。下列叙述不正确的是
A.上述6种物质,属于电解质的有4种
B.将②与SO2按物质的量之比1:1通入水中,再滴加紫色石蕊试液,溶液变红
C.可以用浓氨水检查输送②的管道是否漏气,在此过程中②既作氧化剂又作还原剂
D. 为弱酸,不能拆分,正确的是: ,选项D错误;
答案选C。
4.陈述I和陈述II均正确,且具有因果关系的是
选项
陈述I
陈述II
A
钠金属性比钾强
可用Na和熔融KCl在高温下反应制备K
B
过氧化钠用于制造呼吸面具
过氧化钠与人呼出的H2O、CO2都能发生反应生成O2
C
Al2O学与生活、科学、技术、社会、环境密切相关,下列说法正确的是
A.高温结构陶瓷、醋酸纤维、光导纤维都属于新型无机非金属材料
B.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
C.明矾净水的原理是水解出的氢氧化铝能凝聚水中的悬浮物、吸附色素并杀菌消毒
D.用飞机播撒AgI是实现人工增雨的方法之一
【详解】A.SO2具有还原性,可与Br2发生反应 ,试管内CCl4层溶液褪色,说明Br2具有氧化性,A正确;
D.用H2C2O4、NaClO3和H2SO4三种物质制取③时,还会生成CO2等。生成1mol CO2转移电子的物质的量为1mol
【答案】C
【解析】
【分析】图为氯元素的价类二维图,由图可知,①②③④⑤⑥分别为HCl、Cl2、ClO2、HClO、NaCl、NaClO;
【详解】A.电解质是溶于水或在熔融状态下能够导电的化合物;上述6种物质,属于电解质的有HCl、HClO、NaCl、NaClO共4种,A正确;
广东省实验中学2015-2016学年高二上学期期末考试 化学(文)试题(Word版)

广东实验中学2015—2016学年(上)高二级期末考试文 科 化 学命题:叶其辉 校对:叶其辉本试卷全部为选择题,共6页,满分100分,考试用时60分钟。
注意事项:1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考号填写在答题卡上。
2.选择题每小题选出答案后,用2B 铅笔把答题卷上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其它答案;不能答在试卷上。
3.考生必须保持答题卡的整洁,考试结束后,将答题卡收回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Mg 24 Al 27 Cl 35.5一、单项选择题Ⅰ(本题共30小题,每小题1分,共30分。
在每小题列出的四个选项中,只有一项最符合题意)1.下列名言名句中隐含化学变化的是( )A .冰封三尺B .涂脂抹粉C .沙里淘金D .火上浇油2.下列反应属于化合反应的是( )A .2Mg +O 2=====点燃2MgOB .2Al +Fe 2O 3=====高温Al 2O 3+2Fe C .2HClO=====光照2HCl +O 2 ↑ D .NaOH +Al(OH)3===NaAlO 2+2H 2O3.18 g 水的物质的量是( )A .0.5 molB .1 molC .0.1 molD .6.02×1023 mol4.对NaNO 3分类,不正确的是( )A .属于钠盐B .属于硝酸盐C .属于正盐D .属于酸式盐5.下列关于 816O 的叙述正确的是 ( )A .质量数为8B .质子数为8C .中子数为16D .电子数为16 6.关于FeCl 3溶液和Fe(OH)3胶体描述正确的是( )A .两者都能产生丁达尔现象B .两者都不能产生丁达尔现象C .FeCl 3溶液能产生丁达尔现象,Fe(OH)3胶体不能产生丁达尔现象D .FeCl 3溶液不能产生丁达尔现象,Fe(OH)3胶体能产生丁达尔现象 7.下列物质分类合理的是( )A .氧化物:COB .酸:NaHSO 4C .碱:纯碱D .铵盐:NH 3·H 2O8.下列物质属于电解质的是( )A .铁线B .蔗糖C .氯化钠D .盐酸9.下列化学反应中,H 2SO 4作为氧化剂的是( )A .2NaOH +H 2SO 4===Na 2SO 4+2H 2OB .C +2H 2SO 4(浓)=====△CO 2↑+2SO 2+2H 2O C .BaCl 2+H 2SO 4===BaSO 4↓+2HCl D .CuO +H 2SO 4===CuSO 4+H 2O 10.在2H 2+O 2=====点燃2H 2O 的反应中,能量转化方式为( )A .化学能转化为热能B .化学能转化为电能C .热能转化为化学能D .化学能转化为机械能11.下列选项中,表示ⅥA 族某元素原子结构示意图的是( )A B C D 12.下列说法不正确的是( )A .氢处于第一周期B .氯处于第ⅦA 族C .硅与碳处于同一主族D .第三周期元素全部是金属元素13.下列物质中既有有离子键又有共价键的是( )A .Na 2SB .NaClC .Na 2O 2D .BaCl 214.能用H ++OH -===H 2O 来表示的化学反应是( )A .氢氧化钡溶液与H 2SO 4溶液反应B .氢氧化钡溶液与HNO 3溶液反应C .KOH 溶液和醋酸溶液反应D .氢氧化钠溶液与NaHCO 3溶液反应15.下列元素中非金属性最强的是( )A .MgB .NaC .FD .Cl16.下列反应属于吸热反应的是( )A .碳酸钙受热分解B .氧化钙溶于水C .甲烷燃烧D .铝粉与盐酸反应17.下列微粒只有氧化性的是( )A .Cu 2+B .Fe 2+C .Cl 2D .Cl -18.下列说法正确的是( )A .由H 原子形成1 mol H —H 键要吸收能量B .所有燃烧的反应都是放热反应C.NaOH溶于水是放热反应D.凡经加热而发生的化学反应都是吸热反应19.工业生产硫酸时,其中之一的反应是2SO2+O22SO3,下列说法错误的是() A.增大氧气的浓度可提高反应速率B.升高温度可提高反应速率C.使用催化剂能显著增大反应速率D.达到化学平衡时,正、逆速率相等且等于零20.下列各组元素的性质递变情况错误的是()A.N、O、F原子最外层电子数依次增加B.N、O、F原子半径依次增大C.Na、Mg、Al元素最高正化合价依次升高D.Li、Na、K的金属性依次增强21.下列钠的化合物俗名为小苏打的是()A.Na2SO4·10H2O B.Na2CO3C.NaHCO3D.NaOH22.下列物质敞口放置不会对空气造成污染的是()A.食盐B.苯C.浓盐酸D.浓硝酸23.饱和食盐水露置在空气中一段时间后,有少量固体析出,这是因为()A.氯化钠溶解度减小B.溶液中溶质的质量分数变小C.溶剂的质量减小D.溶液变成不饱和溶液24.根据报道,我国某些城市的酸雨严重,为了改变这一状况,某市正准备推广使用清洁能源,下列不是清洁能源的是()A.太阳能B.煤C.天然气D.酒精25.下列物质不属于天然高分子化合物的是()A.淀粉B.纤维素C.蛋白质D.塑料26.红磷和白磷互为()A.同分异构体B.同素异形体C.同位素D.同系物27.小李为了鉴别新买来的饮料不是牛奶而是豆浆,最好选用()A.溴水B.氯水C.碘酒D.酒精28.下列物质中能使湿润的红色石蕊试纸变蓝的是()A.CO2B.SO2C.NH3D.H229.硼的原子序数是5,硼的最高价氧酸的化学式不可能是()A.HBO2B.H3BO3C.H2BO3D.H4B2O530.1 mol/L MgCl2的含义是()A.1 L水中含有1 mol MgCl2B.1 L溶液中含有1 mol Cl-C.将95 g MgCl2溶于1 000 g水中配成溶液D.1 L溶液中含有95 g MgCl2二、单项选择题Ⅱ(本题共20小题,每小题2分;共40分。
广东实验中学2020-2021学年高一上学期期末考试+化学+PDF版含答案

广东实验中学2020—2021学年(上)高一级期末考试化学命题:林加明左英审定:韩世瑞校对:左英本试卷共6页,满分100分,考试用时75分钟。
注意事项:1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考号填写在答题卷上。
2.选择题每小题选出答案后,用2B铅笔把答题卷上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其它答案;不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卷各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液.不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束后,将答题卷收回。
第一部分选择题(共54分)相对原子质量H=1 C=12 O=16 Na=23 N=14 Fe=56单选题(每题3分,共54分)1.分类是科学研究的重要方法,下列物质分类正确的是()A.碱性氧化物:Na2O、Fe2O3、Na2O2B.同素异形体:石墨、C60、金刚石C.非电解质:乙醇、二氧化碳、氯气D.碱:苛性钠、纯碱、一水合氨2.下列反应的离子方程式中,书写正确的是()A.碳酸钙跟盐酸反应:2H+ + CO2-3===H2O+ CO2↑B.铁粉跟稀盐酸反应制备氢气:2Fe+ 6H+===2Fe3+ + 3H2↑C.向双氧水中加入酸性高锰酸钾溶液:5H2O2+2MnO4-=2Mn2++5O2↑+6OH-+2H2OD.钠和冷水反应:2Na+ 2H2O=2Na+ + 2OH-+ H2↑3.下列能在溶液中大量共存的离子组是()A.Na+、H+、ClO-、Fe2+B.K+、NH4+、NO3-、OH-C.K+、HCO3-、SO42-、OH-D.Al3+、Mg2+、Cl-、SO42-4.一定条件下,卤素互化物碘化砹( AtI )与Zn、NH3发生反应,化学方程式:2AtI+2Zn=ZnI2+ZnAt2、AtI+2NH3 = NH4I+AtNH2。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
广东省实验中学2012-2013学年(上)高三级考试
理综化学
2012.10.6
一、单选题:
7、下列说法正确的是()
A、电解从海水中得的氯化镁溶液可获得金属镁
B、铜具有良好的导电性,可用来制作印刷电路版
C、水晶项链和餐桌上的瓷盘都是硅酸盐制品
D铝合金是一种混合物,它比纯铝的熔点高。
8、用N A表示阿伏加德罗常数,下列说法正确的是()
A、5.6g铁粉在过量的氯气中充分燃烧,失去的电子数为0.2N A
B、1mol/L NH4Cl溶液中,NH4+ 数目等于N A
C、22.4LCO(g)与1molN2(g)所含的电子数目相等
D、在标准状况下,2.24L二氧化硫与氧气混合气体中所含氧原子数为0.2N A
9、下列A—D四组实验中,使用的试剂错误的是()
10、下列A-D四组反应中,Ⅰ和Ⅱ可用同一个离子方程式表示的是()
11、室温下,下列各组离子在指定溶液中能大量共存的是( )
A、饱和氯水中:Cl-、NO3-、Na+、SO32-
B、NaHCO3溶液中:Na+、CO3 2 - 、Al3+、NO3-、
C、加入Al能放出H2的溶液中:Cl-、CO3 2 - 、NO3-、NH4+
D、碱性溶液中:Na+、Ba2+CO3 2 - 、AlO2-
12、一定温下,向饱和NaOH溶液中投入一小块金属钠,充分反应后恢复到原来温度,下列叙述中不合理的是()
A、NaOH溶液浓度增大并放出H2
B、溶液中NaOH的质量分数不变,有H2放出
C、溶液的质量减少,有H2放出
D、钠浮于液面上到处游动,了出“嘶嘶”的响声
二、双题
22、下列离子方程式正确的是()
A、石灰石溶于醋酸溶液中:CaCO3 + 2CH3COOH = 2CH3COO- + Ca2+ + CO2↑+ H2O
B、钠与硫酸铜溶液反应:Cu2+ +2 Na = 2Na+ +Cu
C、过量铁屑溶于稀硝酸:3Fe + 8H+ + 2NO3- = 3Fe2+ +2NO↑+ 4H2O
D、向明矾溶液中加入过量的氢氧化钡溶液:Al3+ + 2SO42- + 2Ba2+ + 3OH-=2BaSO4↓+ Al(OH)3↓
合 金
滤滤渣B
溶液
滤渣D 沉淀
足量盐酸绿 矾
液胆 矾
23、用硫酸铁电化浸出黄铜矿工艺中,精矿在阳极的反应比较复杂,其中有一主要反应:
CuFeS 2 +4Fe 3+ = Cu 2++ 5Fe 2+ + 2S 。
下列说法正确的是( )
A 、反应中硫元素被氧化,所有铁元素均被还原
B 、该反应证明Fe 3+
的氧化性强于S C 、氧化产物是S ,还原产物是Fe 2+和Cu 2+ D 、当转移2mol 电子时,46gCuFeS 2参加反应 三、非选择题
30.(13分)工业上用含有铝、铁、铜的合金工业废料制取纯净的氯化铝溶液,绿矾晶体FeSO 4.7H 2O 和胆矾晶体CuSO 4.5H 2O ,设计了如下方案:请回答相关问题:
(1)、写出合金溶于足量烧碱溶液时相关反应的离子反应方程式: 写出途径Ⅰ中相关反应的离子反应方程式: (2)、由滤液A 得到AlCl 3溶液的途径有Ⅰ和Ⅱ两种,你认为合理的是途径(填“Ⅰ”或“Ⅱ”)理由是
(3)、H 2O 2是一种绿色氧化剂,应用十分广泛,在滤渣D 中加入稀硫酸和H 2O 2来制备胆矾晶体
是一种绿色工艺,写出稀硫酸和H 2O 2溶解滤渣D 的离子反应方程式: (4)、如何在实验室从滤液C 中获得绿矾晶体(写出主要的实验操作名称)
31.(17分)某同学想通过下图装置(夹持装置已略去)实验,探究SO 2与Na 2O 2反应的产物。
C 中的固 体 配成 溶液
加Ba(NO 3)2 溶液
白色沉淀
加足量稀 HNO 3
沉 淀 不 溶
解
Ⅰ、装置B 的作用 装置D 的作用 Ⅱ、如何检验反应中是否有O 2生成 Ⅲ、对C 中固体产物提出如下假设:
假设1:只有Na 2SO 3 假设2:只有Na 2SO 4 假设3: (1)、假设2的反应方程式:
(2)、若Na 2O 2反应完全,为确定C 中固体产物的成分,甲设计如下实验:
得出结论:产物是Na 2SO 4。
该方案是否合理 (填“是”或“否”),理由是 。
(3)、设计实验验证假设3:取少量C 中固体产物于试管中,加入适量的蒸馏水溶解, 则假设3成立。
样品 a g
操作Ⅰ操作Ⅱ
盐酸
水
250.0 ml
25.0 ml 溶
液
①溴水②过量氨水
沉淀
灼烧
红 棕色固 体溶液A
32. (13分)某氯化铁样品含有少量FeCl3杂质。
现要测定其中铁元素的质量分数,实验按以下步骤进行:
请根据上面流程回答以下问题:
(1)、操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须有 ,
(填仪器名称)。
(2)、请写出加入溴水发生反应的离子反应方程式: 。
(3)、检验沉淀是否已经洗涤干净的操作是: 。
(4)、该实验中可以回收利用的物质是 。
(5)、若蒸发皿质量是W 1g ,蒸发皿与加热后固体总质量是W 2g ,则样品中铁元素的质量分数是 (列出算式,不需要化简);若称量准确,最终测量结果偏大,则造误差的原因可能是 。
(6)、为进一步探究样品的性质,他们又利用溶液A 做了如下一些实验,其中现象、结论均正确的是 (填写序号)。
A 、向氢氧化镁悬浊液中滴加A 溶液出现红褐色沉淀,证明Ksp[Fe(OH)3]< Ksp[Mg(OH)2)]
B 、向A 溶液中加入少量铁粉,铁粉溶解,溶液颜色由黄色变成浅绿色。
C 、向沸水中滴加A 的饱和溶液,立即出现红褐色沉淀。
D 、将A 溶液加热蒸干并灼烧,得到Fe 2O 3固体。
金
焦Ti
液
、结晶
33.(15分)钛(Ti )具有高强度和耐酸腐蚀性,是重要的工业原料,以金红石(主要成份为TiO 2,含有少量Fe 2O 3、SiO 2)为原料可制取Ti 。
工业流程如下:
(1)粗TiCl 4中含有少量FeCl 3、SiCl 4等,它们的部分性质如下:
从粗TiCl 4 中精制TiCl 4 的方法是: A .用水溶解后,重结晶 B. 蒸馏 C. 用乙醚萃取后,分液
(2)写出金红石高温反应制取TiCl 4 的化学方程式 (3)写出电解熔融NaCl 的化学方程式 (4)粗钛产品粉碎后用盐酸浸洗。
其主要目的是 , (5)Ti 可以溶解在浓HF 溶液中,请完成下列离子方程式。
Ti + HF = TiF 62-
+ ( ) + H 2↑。
