2007年北京化学竞赛(高一)试题
2007年全国高中化学竞赛模拟试题
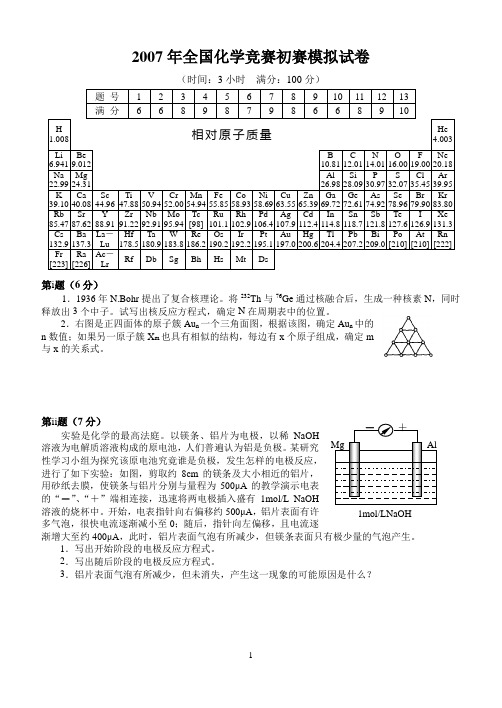
2007年全国化学竞赛初赛模拟试卷(时间:3小时 满分:100分)第i 题(6分)1.1936年N.Bohr 提出了复合核理论。
将232Th 与76Ge 通过核融合后,生成一种核素N ,同时释放出3个中子。
试写出核反应方程式,确定N 在周期表中的位置。
2.右图是正四面体的原子簇Au n 一个三角面图,根据该图,确定Au n 中的n 数值;如果另一原子簇X m 也具有相似的结构,每边有x 个原子组成,确定m 与x 的关系式。
第ii 题(7分)实验是化学的最高法庭。
以镁条、铝片为电极,以稀NaOH溶液为电解质溶液构成的原电池,人们普遍认为铝是负极。
某研究性学习小组为探究该原电池究竟谁是负极,发生怎样的电极反应,进行了如下实验:如图,剪取约8cm 的镁条及大小相近的铝片,用砂纸去膜,使镁条与铝片分别与量程为500μA 的教学演示电表的“-”、“+”端相连接,迅速将两电极插入盛有1mol/L NaOH 溶液的烧杯中。
开始,电表指针向右偏移约500μA ,铝片表面有许多气泡,很快电流逐渐减小至0;随后,指针向左偏移,且电流逐渐增大至约400μA ,此时,铝片表面气泡有所减少,但镁条表面只有极少量的气泡产生。
1.写出开始阶段的电极反应方程式。
2.写出随后阶段的电极反应方程式。
3.铝片表面气泡有所减少,但未消失,产生这一现象的可能原因是什么?1mol/LNaOH第iii题(9分)在我们地球的物质世界里的周期系是根据4个量子数建立的,即n=1,2,3,……;l=0,1,…,(n-1);m l=0,±1,±2…,±l;m s=±1/2。
如果在另一个星球,那里的周期系也是由4个量子数建立的,但它们的关系为n=1,2,3,……;l=0,±1,±2,…,±(n-1);m l=0,1,2,…,l-1;m s=±1/2。
如果在地球上的基本原理在这个星球上也是适用的(但不发生能级交错现象),回答下列问题:(1)这个星球中第一、二、三、四、五、六层各有几个亚层?(2)这个星球中s、p、d、f、g、h亚层各有几个轨道?(3)这个星球中第一、二、三、四、五、…、n层各有几种元素?(4)写出9、33号元素的价电子构型;(5)写出前112号元素电负性最大和最小的元素的原子序数;(6)写出第二周期中可能的杂化轨道。
2007年北京市化学竞赛高二组试题及答案

2007年北京市高中学生化学竞赛试题(高中二年级)·竞赛时间2小时。
迟到超过30分钟者不得进场。
1小时内不得离场。
时间到,把答题纸及试题纸(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在答题纸上,使用黑色或蓝色圆珠笔、签字笔或钢笔答题,使用红色或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸上方指定位置,写在他处者按废卷处理。
·允许使用非编程计算器及直尺等文具。
·答题纸按密封线封装。
第一题单选题(共12分)(每一个答案得1.5分)1.已知H 2CO3的第二级电离比HAlO2的电离容易,则下列推论正确的是(A)。
A.通适量的CO2于含有AlO2-的溶液中,反应后生成Al(OH) 3B.CO32-在水溶液中易使Al(OH) 3溶解变成AlO2-C.HCO3-只能跟Al3+反应,不能与AlO2-反应D.HCO3-只能与AlO2-反应,不能与Al3+反应2.两瓶气体分别为NO2和Br2蒸气,外观相同,某同学设计了多种鉴别法,①用湿润的KI淀粉试纸;②加少量NaCl溶液;③加少量AgNO3溶液;④加少量水后再加适量苯;⑤一定条件下改变温度,则下列选项中正确的是:( C )A.只能采用①②③B.只能采用②③④C.能采用②③④⑤D.都可以3.下列有关实验现象叙述正确的是(A)。
A.Cu跟浓HNO3反应后溶液呈绿色B.Cu溶于热、浓H2SO4后溶液呈蓝色C.NaHCO3溶液可使苯酚的乳浊液变得澄清D.Mg跟盐酸反应放出H2的速率不断减慢4.锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大,电压高的特性。
锂离子电池放电时的电极反应式为:CH OH 负极反应:C 6Li – x e - = C 6Li 1 - x + x Li +(C 6Li 表示锂原子嵌入石墨形成的复合材料)正极反应:Li 1 - x MO 2 + x Li + + x e -= Li MO 2(Li MO 2表示含锂的过渡金属氧化物) 下列说法正确的是( D )。
2007年全国化学竞赛初赛模拟试卷(07)附答案

2007年全国化学竞赛初赛模拟试卷(07)(时间:3小时满分:100分)题号123456789101112满分2857125107991610H 1.008相对原子质量He4.003Li 6.941Be9.012B10.81C12.01N14.01O16.00F19.00Ne20.18Na 22.99Mg24.31Al26.98Si28.09P30.97S32.07Cl35.45Ar39.95K 39.10Ca40.08Sc44.96Ti47.88V50.94Cr52.00Mn54.94Fe55.85Co58.93Ni58.69Cu63.55Zn65.39Ga69.72Ge72.61As74.92Se78.96Br79.90Kr83.80Rb 85.47Sr87.62Y88.91Zr91.22Nb92.91Mo95.94Tc[98]Ru101.1Rh102.9Pd106.4Ag107.9Cd112.4In114.8Sn118.7Sb121.8Te127.6I126.9Xe131.3Cs 132.9Ba137.3La-LuHf178.5Ta180.9W183.8Re186.2Os190.2Ir192.2Pt195.1Au197.0Hg200.6Tl204.4Pb207.2Bi209.0Po[210]At[210]Rn[222]Fr [223]Ra[226]Ac-Lr Rf Db Sg Bh Hs Mt Ds第题(2分)香皂一般呈碱性,长期用香皂洗脸容易造成面部油脂层破坏,皮肤老化;而洗面奶一般呈弱酸性,和皮肤酸碱性相似,有利于皮肤健康。
“曼秀雷登”推出了新型化妆品——天性炭男士第题(8分)正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如右图)。
1.正硼酸晶体属于晶体;2.片层内微粒间的作用力是上面?片层间微粒间的作用力又是什么?3.含1mol H3BO3的晶体中有mol氢键;4.以1个片层为研究对象,画出其二维晶胞(右图上),并指出其所包含的内容。
2007年北京市高中学生化学竞赛试题(高中二年级)

CH OH 2007年北京市高中学生化学竞赛试题(高中二年级)2007年4月14日上午8:30-10:30 北 京第一题 单选题(共12分)(每一个答案得1.5分)1. 已知H 2CO 3的第二级电离比HAlO 2的电离容易,则下列推论正确的是( )。
A . 通适量的CO 2于含有AlO 2-的溶液中,反应后生成Al(OH) 3B . CO 32-在水溶液中易使Al(OH) 3溶解变成AlO 2-C . HCO 3-只能跟Al 3+反应,不能与AlO 2-反应D . HCO 3-只能与AlO 2-反应,不能与Al 3+反应2. 两瓶气体分别为NO 2和Br 2蒸气,外观相同,某同学设计了多种鉴别法,①用湿润的KI 淀粉试纸;②加少量NaCl 溶液;③加少量AgNO 3溶液;④加少量水后再加适量苯;⑤一定条件下改变温度,则下列选项中正确的是:( ) A . 只能采用①②③ B . 只能采用②③④ C . 能采用②③④⑤ D . 都可以3.下列有关实验现象叙述正确的是( )。
A . Cu 跟浓HNO 3反应后溶液呈绿色 B . Cu 溶于热、浓H 2SO 4后溶液呈蓝色C . NaHCO 3溶液可使苯酚的乳浊液变得澄清D . Mg 跟盐酸反应放出H 2的速率不断减慢4. 锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大,电压高的特性。
锂离子电池放电时的电极反应式为:负极反应:C 6Li – x e - = C 6Li 1 - x + x Li +(C 6Li 表示锂原子嵌入石墨形成的复合材料)正极反应:Li 1 - x MO 2 + x Li + + x e -= Li MO 2(Li MO 2表示含锂的过渡金属氧化物) 下列说法正确的是( )。
A . 锂离子电池充电时电极反应为C 6Li + Li 1 - x MO 2 == Li MO 2 + C 6Li 1 - xB . 电池反应中,锂、锌、银、铅各失去1mol 电子,金属锌所消耗的质量最小C . 锂离子电池放电时电池内部锂离子向负极移动D . 锂离子电池充电时阴极反应为C 6Li 1 - x + x Li ++ x e -= C 6Li5. 某烃的组成为C 15H 24,分子结构非常对称。
第七套2007年化学岛岛题

● 竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
● 试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
● 姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
● 允许使用非编程计算器以及直尺等文具。
1.008Zr Nb Mo T c Ru Rh Pd Ag CdIn Sn Sb T e I Hf T a W Re Os Ir Pt Au Hg T l Pb Bi Po At Ac-Lr HLiBeB C N O F Na MgAl Si P Cl S K Ca Sc T i V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Rb Cs Fr Sr BaRaY LaLu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210][210]126.979.9035.454.00320.1839.9583.80131.3[222]He Ne Ar KrXe Rn 相对原子质量Rf Db Sg Bh Hs Mt第1题(1) 填满下表,要使NO,N 2O,NO +,NH 3+OH 和NO 3-等分子与表中最后一栏所列的对应N-O 键长相匹配。
2007年全国高中学生化学竞赛(省级赛区)模拟试题

第1题近年来正在开发一种新型绿色化学介质—离子液体。
通常离子化合物的熔点较高,而离子液体是室温下表现为液体的离子化合物。
最早发现的离子液体硝酸乙基胺的熔点只有12℃。
离子液体由有机阳离子和无机阴离子组成。
制备方法非常简单,如卤盐和金属卤化物直接化合,酸碱中和,复分解反应等。
写出下列离子液体的制备反应方程式。
1.硝酸乙基胺2.由甲基咪唑NH NH 3C —制氯化1—丁基—3—甲基咪唑,再与三氯化铝作用。
3.由甲基咪唑制碘化1—乙基—3—甲基咪唑,再在甲醇中与四氟硼酸银作用。
第2题3.07 g 的化合物D 溶解解在过量NaOH 水溶液中。
由硝酸中和到pH=7,并加入过量硝酸钙,获得的溶液过滤了白色沉淀后, 烘干并称量,沉淀的质量是3,1 g.。
剩余的溶液中,加入过量硝酸银溶液得到8,61 g 另外的白色沉淀。
1.确定物质D 写出所有提及到的反应的方程式。
2. D 与氨反可能形成什么物质?第3题1874年德国化学家Piter Austen 合成出F 。
由于物质F 的有趣性质,它在工业上开始生产。
物质F 按照如下表合成:1.008Zr Nb Mo Tc Ru Rh Pd Ag CdIn Sn Sb Te I Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Ac-Lr HLi BeB C N O F Na MgAl Si P Cl S K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Rb Cs Fr Sr BaRaY La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210][210]126.979.9035.454.00320.1839.9583.80131.3[222]He Ne Ar KrXe Rn 相对原子质量Rf Db Sg Bh Hs MtF的1H-NMR谱只有两个信号,加入D2O后其中一个信号消失。
2007年全国化学竞赛初赛模拟试卷(20)

2007年全国化学竞赛初赛模拟试卷(20)(时间:3小时满分:100分)第一题(3分)最新研究的纳米型电池是世界上最小的V olta电池,该电池是用扫描隧道显微镜将彼此进挨着的很小的金属点沉积在一个表面上,制备出的有四个电极的电池,其中两个铜电极两个银电极。
将电池浸在稀的硫酸铜溶液中,既有电子流产生20mV,1×10-18A的微小电流。
写出第二题(7分)根据条件写出下列反应式2+3222626NO是已知最简单的热稳定的单电子分子,具有高度的化学活性。
1.奇电子化合物具有强烈的聚合倾向,试写出NO的聚合反应并画出聚合体的结构;2.NO与O2在一定的化学计量关系下进行反应时生成一种氧化物,该化合物在低温下是淡蓝色固体,该化合物也由NO与NO2在低温下作用形成,写出生成该氧化物的反应方程式;3.NO有一定的还原性,在Cl2的作用下生成化合物A,A研究表明与王水的强腐蚀性有一定的联系。
A与NaN3在无水的条件下生成一种极不常见的氧化物B。
写出A、B化学式及各步反应方程,并画出B的所有共振式,假定各共振式贡献相同,求N-O的键级(注:相邻原子带相同电荷的共振式极不稳定,可不予考虑)4.NO也具有一定的氧化性,且一般还原产物为N2,已知NO与P4在无氧条件下反应生成的氧化物中仅存在σ键,写出该反应方程式并画出该氧化物的结构;5.NO比CO多一个电子,在一些配位反应中,NO可看作是3e的给体,而在另一些反应中,NO又可以看作是1e的给体,试从前面的信息中解释NO形成此配位现象的原因;6.已知在NO的作用下,O2可以部分转变为O3,假定NO在反应中充当催化剂,试写出NO催化O2生成O3的反应机理。
第四题(4分)有机物的显色一般是由于大的共轭体系所造成,酸碱指示剂亦是如此,已知酚酞的结构式如右图,在碱性作用下,酚酞由无色转变为红色,在浓碱的作用下红色又消失,写出上述变化的方程式。
在20世纪50年代,kealy 等想以环戊二稀基溴化镁为原料,以FeCl 3作催化剂制备化合物A 却意外地得到一种稳定的橙色化合物B ,已知A 的化学式为C 10H 8。
2007年北京市高中学生化学竞赛试卷(高二)答案

2007北京市高中化学竞赛高二答案第一题(共12分)1. A2. C3. A4. D 5. C 6. C 7. C 8. B第二题(共8分)(1)Fe 3+ + 3SCN - = Fe (SCN) 3(方程式中SCN -系数3-6均可,只要配平合理即可。
要看出明显颜色系数需3以上。
)(2)2Fe (SCN) 3 + SO 2 + 2H 2O = 2Fe 2+ + SO 42- + 4H + + 6SCN -(方程式中只要能显示出Fe 被还原,S 被氧化,硫酸根写成H 2SO 4也可得分。
) (3)MnO 4- + 5Fe 2+ + 8H + = Mn 2+ + 5Fe 3++ 4H 2O(4)Fe 3+ + [Fe(CN) 6] 4- + K + = KFe [Fe(CN)6]↓第三题(共10分)Ag + + 2CN [Ag(CN)2] 平衡浓度(mol ·dm -3) x 2x 0.1-x 0.1 xx (2x )2= 1.25 1021得 x = 2.7×10-8 c Ag + = 2.7 × 10-8 mol ·dm -3Q = c Ag +•c Cl - = 2.7×10-8 ×0.10 = 2.7×10-9因为Q > K sp (AgCl ),因而会有AgCl 沉淀从溶液中析出。
(写不出浓度商但如有计算数据2.7×10-9 > K sp (AgCl ),可判断出AgCl 沉淀也可得满分。
)第四题(共9分)2SO 2 + 2HS - = 3S + SO 32- + H 2O * (2分)S + Na 2SO 3 = Na 2S 2O 3 ** (2分)S 2O 32- + 2H + = S + H 2SO 3 (2分)1:2 (1.5分)1:2 (1.5分) (*在pH > 7时生成S ,所以不宜写成H 2SO 3 + 2H 2S = 3S + H 2O ,若写成此式建议扣0.5分。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2007年北京市高中学生化学竞赛试卷(高中一年级) 第1页 (共7 页)
2007年北京市高中学生化学竞赛试卷
(高中一年级)
2007年4月14日上午8:30-10:30 北 京
题
号
1 2 3 4 5 6 7 8 9 10
总分
满
分
24 8 12 8 10 6 6 6 12 8 100
得分
评卷人
·竞赛时间2小时。迟到超过30分钟者不得进场。1小时内不得离场。时间
到,把答题纸及试题纸(背面向上)放在桌面上,立即离场。
·竞赛答案全部写在答题纸上,使用黑色或蓝色圆珠笔、签字笔或钢笔答题,
使用红色或铅笔答题者,试卷作废无效。
·姓名、准考证号和所属区、县、学校必须填写在答题纸上方指定位置,写
在他处者按废卷处理。
·允许使用非编程计算器及直尺等文具。
·答题纸按密封线封装。
题中可能用到的元素相对原子质量如下:
H C N O Na P S Fe Cu
1.008 12.01 14.01 16.00 22.99 31 32.07 55.85 63.55
第一题 单选题(共24分,选对一个答案得3分,选一个错误答案扣3分)
1.科学家正拟合成一种“二重构造”的球形分子,即把足球型的C60分子熔
进Si80的分子中,外围的硅原子与里面的碳原子以共价键结合。关于这种分子
的下列说法正确的是( )。
A.它是两种单质组成的混合物 B.它是一种硅酸盐 C.它是一种新型化合物
D.它是一种高聚物
2.下列说法中正确的是( )。(NA为阿伏加德罗常数)
A.1 mol Na2O2晶体中阴离子的个数为2NA
B.1 mol Na2O2与足量水反应,转移的电子数为2NA
C.常温常压下,1mol任何气体单质都含有2NA个原子
D.31 g白磷含有1.5 NA的共用电子对
2007年北京市高中学生化学竞赛试卷(高中一年级) 第2页 (共7 页)
3.氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的初步生成物是
( )。
A.HI和HClO B.HCl和HIO C.HClO3和HIO
D.HClO和HIO
4. 下列离子方程式书写正确的是( )。
A.Cl 2溶于水:Cl 2 + H 2O == 2H+ + Cl- + ClO-
B.向Na2CO3溶液中通入少量的SO2气体:
2CO32-+ H 2O + SO2 == 2HCO3- + SO32-
C.用氨水吸收少量的SO2:NH3·H 2O + SO2 == NH4+ + HSO3-
D.向NaHSO4溶液中滴加Ba(OH)2溶液至恰好为中性:
Ba2+ + OH-+ H+ + SO 42- == BaSO4↓+ H 2O
5.Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H 2O,
当NO2和NO的物质的量之比为1:1时,实际参加反应的Cu2S与HNO3的物
质的量之比为( )。
A.1:7 B.1:9 C.1:5
D.2:9
6.有一种混合气体,它可能由CO、CO2、SO2、HCl中的一种或多种气体组
成。该混合气体依次通过下列物质的现象如下:先通入澄清石灰水无白色沉
淀析出;通过品红溶液,溶液红色褪去;再通过炽热的氧化铜,固体变成红
色;最后通过澄清石灰水,出现白色沉淀。该混合气体组成的各种说法中正
确的是( )。
A.肯定不含有CO2
B.只含有SO2和CO
C.含有SO2、CO、和CO2,可能含HCl
D.含有HCl、SO2和CO,可能含CO
2
7.已知1~18号元素的离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,
下列关系正确的是( )。
A.质子数 c > b B.离子的还原性Y2- > Z- C.氢化物的稳定性 H 2Y < HZ
D.原子半径 X < W
8.使5.6 L CO2气体迅速通过Na2O2固体后得到4.48 L(标准状况下)气体,
这4.48 L气体的质量为( )。
A.8.8 g B.6.4 g C.8.2 g
D.6.2 g
2007年北京市高中学生化学竞赛试卷(高中一年级) 第3页 (共7 页)
第二题(共8分)运用原子和分子结构的知识解释B、N、P所形成的下列化
合物的性质:
(1) BF3、BCl3为非极性分子,而NH3、NCl3、PH3却都是极性分子。为什
么?
(2) 对比NH3和PH3谁的极性大?对比NH3和NCl3谁的极性大?理由何
在?
第三题(共12分)试确定下题中B、C、D、E各为何物质?写出下述①、②、
③、④各步反应的离子方程式。硫代硫酸钠(Na2S2O3)A溶于水后,①加入
稀盐酸,有刺激性气体 B 产生,同时有黄色沉淀 C 析出,
反应为: 。
②气体B能使高锰酸钾溶液褪色,
反应为: 。
③若通足量Cl2于A的溶液中,Cl2消失并得到溶液 D ,
反应为: 。
④D与钡盐作用,产生不溶于稀硝酸的白色沉淀 E ,
反应为; 。
2007年北京市高中学生化学竞赛试卷(高中一年级) 第4页 (共7 页)
第四题(共8分)回答关于卤素F、Cl、Br、I的下列问题
(1)单质的活泼性次序为: ;原因是:
。
(2)在常温常压下,它们的物理状态是: ;
原因是:
。
(3)HX水溶液的酸强度次序为: ;
原因是:
。
第五题(共10分)X、Y、Z属于周期表前面4个周期的元素。X、Y、属于
同一主族,Z属于过渡金属元素。Y的原子序数是X的2倍,Z的原子序数比
Y大13。X与Y可形成YX2和YX3型化合物;X与Z可形成Z2X和ZX型化
合物。Z与Y形成的ZY化合物为不溶于水的黑色固体。
(1) 试写出X、Y、Z三种元素的元素符号;
(2) 它们的原子基态电子构型(表示各原子的原子轨道占据方式);
(3) 化合物YX3、Z2X、ZX、ZY的化学式。
第六题(共6分)金属钠的晶胞呈
立方体(如右图所示),有两个钠
原子,立方体的体对角线上的钠原
子是相切的,设钠原子的半径为r,
求晶胞的边长a。
2007年北京市高中学生化学竞赛试卷(高中一年级) 第5页 (共7 页)
a
c
b
第七题(共6分)液态SO2是一种非水溶剂,可发生电离:二氧化硫分子SO
2
+ 和SO32-
。把带有标记硫原子的Na2*SO3、*SOCl2分别加到液态SO2中。不
久,在加Na2*SO3的溶液中发现有带标记硫原子的*SO2,而加*SOCl2的溶液
中没有*SO2,可能原因是什么?(注:元素符号前*表示该原子是使用放射性
同位素标记的)
第八题(共6分)区域熔融可把硅的纯度提高
到99.9999%以上。右为硅的区域加热示意图。
把要提纯的硅制成条状,实验时可移动加热装
置C,使局部硅熔融,当它慢速(~0.25cm/min)
右移时,前进方向一端固态硅熔融,而另一端熔态硅转化为固态。除杂质原
理和凝固点下降——稀溶液开始析出固态溶剂的温度低于纯溶剂——相同。
请问,当加热装置C从a移动到b时,原先硅中的杂质将主要集中在a端还
是b端?,简述理由。
第九题(共12分)因 (CN)2、CN-、N3-的某些性质分别与X2、X-相似,故
被称为拟卤素(pseudo halogen)、拟卤离子。
(1)(CN)2和NaOH溶液的反应方程式为:
(2)足量HN3和Na2CO3溶液的反应方程式为:
(3)把N2O通入熔融的NaNH2(190º~194ºC)能制得NaN3,反应方程式为
(注:NaNH2能与N2O反应):
(4)I2溶于液态HN3中形成具有导电性的红色溶液,反应式为:
2007年北京市高中学生化学竞赛试卷(高中一年级) 第6页 (共7 页)
第十题(共8分)将m 克铜屑、铁屑的混合物溶解在过量稀硝酸中,得到
NO气体(标准状况下)的体积v L;向上述溶液中加入过量的1 mol/L的NaOH
溶液,得到沉淀。请分别写出铜和铁与稀硝酸反应的化学方程式,并给出得
到沉淀的质量(请简述得到沉淀质量的表达式的推导过程)
2007年北京市高中学生化学竞赛试卷(高中一年级) 第7页 (共7 页)
草 稿 纸
