氯气碘量法原始记录表
环境空气和废气 氯气 固定污染物排气中氯气的测定 碘量法 HJ547-2017

编号:XXXXXX有限公司方法验证报告固定污染源氯气的测定碘量法HJ547-2017方法验证人员:方法验证日期:一、实验室基本情况1.1人员情况公司安排分析人员XXX和XXX进行了《固定污染源氯气的测定碘量法》(HJ 547-2017)分析方法的验证。
验证人员通过培训学习熟悉了该标准方法原理及分析流程,能够熟练操作仪器,独立完成整个分析过程,并通过了公司自认定考核。
分析人员见表1。
表1 分析人员一览表1.2仪器设备及试剂、标准物质该标准主要使用的仪器设备由XXX有限公司进行检定和校准,具体内容见表2。
表2仪器设备(包括仪器、前处理装置)标准除非另有说明,分析时均使用符合国家标准的分析纯化学试剂;实验用水为新制备的蒸馏水或去离子水。
本次方法验证使用试剂见表3。
表3试剂1.3实验室环境条件标准方法对测试环境无特殊要求,符合实验室日常环境控制即可。
目前实验室环境监控设备配置有温湿度表。
实验室配有通风橱,实验人员配备防毒面具。
二、方法简介2.1样品2.1.1样品采集2.1.1.1采样点位布设及采样方法应符合GB/T16157的规定。
2.1.1.2串联两个内装40ml氢氧化钠吸收液的多孔玻板吸收瓶,将其连接到采样系统中,以0.5L/min~1L/min流量恒流采样20min~30min。
若排气中含有固体颗粒物时,应将滤膜置于滤膜夹内,接装在采样管前端,采样系统见图1。
当废气温度高于环境温度或含湿量较大时,需要加热滤膜夹内的滤膜及采样管,保持采样管保温夹套温度在120℃,防止水分凝结。
记录采样流量、时间、温度、气压等,采样完毕后,用连接管密封吸收瓶出口,避光运回实验室。
注:当氯气浓度高、含湿量大(烟气含湿量在25%以上)时,须进行等速采样。
2.1.2样品保存样品采集后应尽快分析,若不能当天测定,应于4℃以下冷藏,48h内完成测定。
2.1.3样品制备2.1.3.1样品将第一级吸收瓶的吸收液转移至100ml的容量瓶中,用第二级吸收瓶中的吸收液洗涤第一瓶后转入容量瓶,再用少量水洗涤两个吸收瓶和吸收管,洗涤液一并转入容量瓶中,加水至标线,混匀。
五步碘量法

连续运行检测记录表格A.五步碘量法A.1 一般规定A.1.1 本标准所用试剂和水,在没有注明其它要求时,均指分析纯试剂和GB/T 6682-1992中规定的三级水。
A.1.2 试验中所用标准滴定溶液,杂质标准溶液,制剂及制品,在没有注明其它要求时,均按HG/T 3696.1的规定制备。
A.2 范围本方法适合于测定0.1mg/L ~100.0mg/L范围的二氧化氯,高浓度溶液可稀释后测定;含量低的样品可适当增加取样量,或将标准溶液稀释后测定。
A.3原理该法是利用不同pH值条件下ClO2、 Cl2、 ClO2-、ClO3-与 I-的反应来测定各物质含量的方法。
如方程式所示:Cl2+2I-=I2+2Cl-(pH≤7 )2 ClO2+ 2 I-= I2+ 2 ClO2-(pH =7 )2 ClO2+10 I-+8H+=5 I2+2Cl-+4H2O (pH≤2 )ClO2-+4 I-+4 H+=2 I2+ Cl-+2 H2O (pH≤2 )ClO3-+6 I-+6 H+=3 I2+Cl-+3 H2O (pH≤0.1)然后用硫代硫酸钠作滴定剂,以淀粉溶液作指示剂,分步滴定游离出的碘,算出各种氧化性物质的含量。
A.4 试剂和材料1 碘化钾;2 盐酸;3 盐酸溶液:1+1;4 溴化钾溶液:50g/L,贮存于棕色瓶中。
5 磷酸氢二钠饱和溶液;6磷酸盐缓冲溶液:pH=7,称取25.4g无水磷酸二氢钾和86.0g十二水磷酸氢二钠,溶于800mL水中,用水稀释至1000mL。
7 硫代硫酸钠标准滴定溶液:c(Na2S2O3)约为0.05mol/L;用水准确稀释按HG/T3696.1配制标定的0.1mol/L硫代硫酸钠标准滴定溶液。
8 淀粉指示液:10g/L。
A.5仪器、设备A.5.1 高纯氮气钢瓶。
A.6 采样A.6.1 应用清洁干燥的棕色玻璃瓶采集样品。
采样时,将发生器采样口的管子直接插到瓶底,打开采样口阀门,直至样品溶液溢出达采样瓶体积的一倍时,关闭阀门,立即盖上瓶盖。
氯离子原始记录
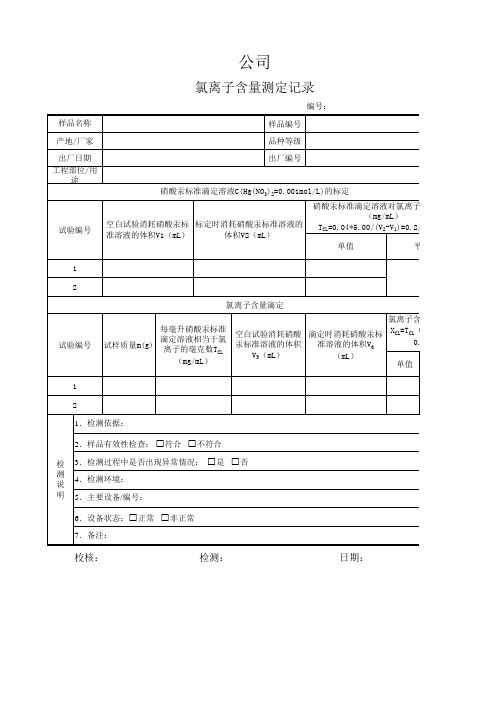
氯离子含量测定记录
编号: 样品名称 产地/厂家 出厂日期 工程部位/用途 硝酸汞标准滴定溶液C(Hg(NO3)2=0.001mol/L)的标定 硝酸汞标准滴定溶液对氯离子的滴定度 (mg/mL) TCL=0.04*5.00/(V2-V1)=0.2/(V2-V1) 单值 1 2 氯离子含量滴定 每毫升硝酸汞标准 滴定溶液相当于氯 试样质量m(g) 离子的毫克数TCL (mg/mL) 氯离子含量XCL(%) 空白试验Байду номын сангаас耗硝酸 滴定时消耗硝酸汞标 XCL=TCL(V6-V5)× 0.1/m 汞标准溶液的体积 准溶液的体积V6 V5(mL) (mL) 单值 平均值 样品编号 品种等级 出厂编号
检测: 日期:
校核:
溶液对氯离子的滴定度 (mg/mL) /(V2-V1)=0.2/(V2-V1) 平均值
氯离子含量XCL(%) XCL=TCL(V6-V5)× 0.1/m 平均值
试验编号
空白试验消耗硝酸汞标 标定时消耗硝酸汞标准溶液的 准溶液的体积V1(mL) 体积V2(mL)
试验编号
1 2 1.检测依据:
检 测 说 明
□符合 □不符合 3.检测过程中是否出现异常情况: □是 □否
2.样品有效性检查: 4.检测环境: 5.主要设备/编号: 6.设备状态: 7.备注:
□正常 □非正常
第七组原始记录表
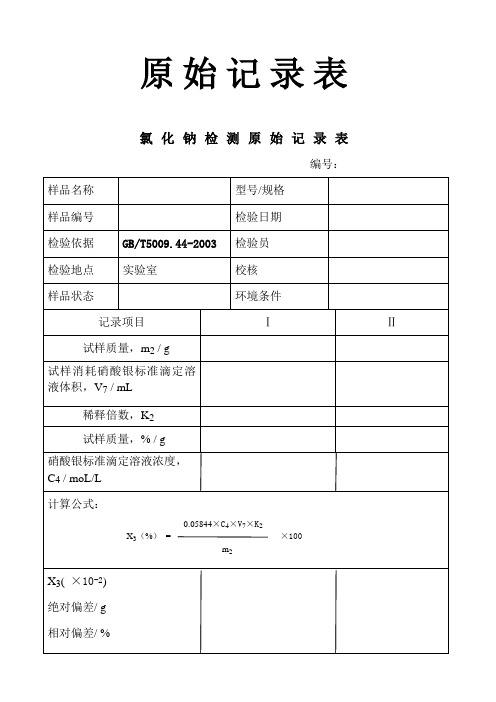
氯 化 钠 检 测 原 始 记 录 表
编号: 样品名称 样品编号 检验依据 检验地点 样品状态 记录项目 试样质量,m2 / g 试样消耗硝酸银标准滴定溶 液体积,V7 / mL 稀释倍数,K2 试样质量,% / g 硝酸银标准滴定溶液浓度, C4 / moL/L 计算公式:
0.05844×C4×V7×K2 X3(%) = m2 ×100
方法摘要:称取一定量的样品于一固定的温度下干燥,除去其中的水分,根据 失去的质量计算出其中水分的含量。 记录项目 (皿+试样)质量,m1/g 皿质量,m3/g 试样质量,(m1-m3)/g 烘后(皿+试样)质量,m2/g 计算公式:
m1-m2 w (H2O) = m1-m3 ×100%-2) 绝对偏差/ g 相对偏差/ %
食品中亚硝酸盐含量的测定原始记录表 检测项目 1.数据记录: 管号 A538
X A 100 m V / 250 1000
检验方法
检验依据
0
1
2
3
4
样液
2.结果计算:
X — 样品中亚硝酸盐的含量, mg/kg; A—测定用滤液中亚硝酸盐的质量,µg; m — 样品质量,g; v— 测定用样液体积,ml; 250 — 试样处理液总体积,ml;
型号/规格 检验日期 GB/T5009.44-2003 实验室 检验员 校核 环境条件 Ⅰ Ⅱ
X3( ×10-2) 绝对偏差/ g 相对偏差/ %
水 分 检 测 原 始 记 录 表
编号:
样品名称 样品编号 检验依据 检验地点 样品状态 直接干燥法: GB/T 5009.3-2010 实验室
型号/规格 检验日期 检验员 校核 环境条件
GB/T 5009.33
测定 二氧化氯 原始记录
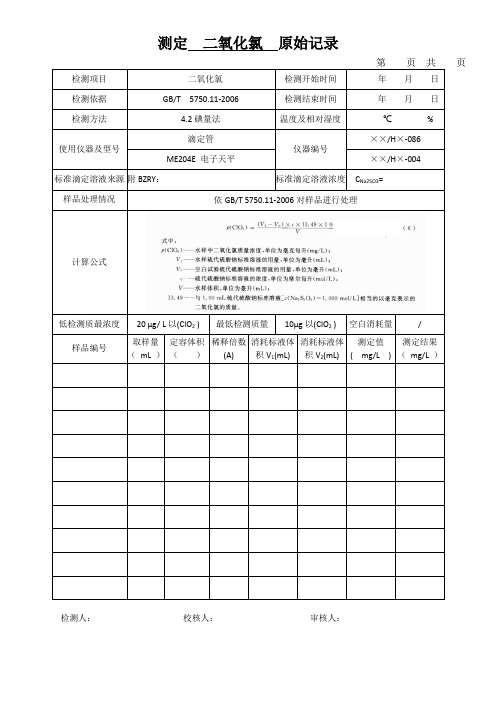
第 页 共 页
检测项目
二氧化氯
检测开始时间
年月日
检测依据
GB/T 5750.11-2006
检测结束时间
年月日
检测方法ቤተ መጻሕፍቲ ባይዱ
4.2碘量法
温度及相对湿度
℃%
使用仪器及型号
滴定管
仪器编号
××/H×-086
ME204E电子天平
××/H×-004
标准滴定溶液来源
附BZRY:
标准滴定溶液浓度
CNa2SO3=
容量法测定原始记录(续表)
第 页 共 页
样品编号
取样量
(mL)
定容体积
()
稀释倍数
(A)
消耗标液体积V1(mL)
消耗标液体积V2(mL)
测定值( mg/L )
测定结果
(mg/L)
检测人: 校核人: 审核人:
样品处理情况
依GB/T 5750.11-2006对样品进行处理
计算公式
低检测质最浓度
20 µg/ L以(ClO2)
最低检测质量
10μg以(ClO2)
空白消耗量
/
样品编号
取样量
(mL)
定容体积
()
稀释倍数
(A)
消耗标液体积V1(mL)
消耗标液体积V2(mL)
测定值( mg/L )
测定结果
(mg/L)
检测人: 校核人: 审核人:
容量法测定 氯离子 原始记录
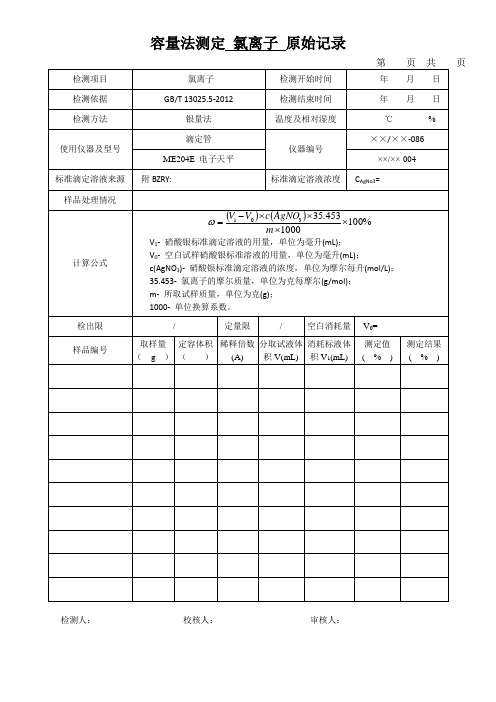
计算公式
V1-硝酸银标准滴定溶液的用量,单位为毫升(mL);
V0-空白试样硝酸银标准溶液的用量,单位为毫升(mL);
c(AgNO3)-硝酸银标准滴定溶液的浓度,单位为摩尔每升(mol/L);
35.453-氯离子的摩尔质量,单位为克每摩尔(g/mol);
m-所取试样质量,单位为克(g);
1000-单位换算系数。
消耗标液体积V1(mL)
测定值( % )
测定结果
( % )
检测人: 校核人: 审核人:
容量法测定氯离子原始记录
第 页 共 页
检测项目
氯离子
检测开始时间
年月日
检测依据
GB/T 13025.5-2012
检测结束时间
年月日
检测方法
银量法
温度及相对湿度
℃%
使用仪器及型号
滴定管
仪器编号
××/××-086
ME204E电子天平
××/××-004
标准滴定溶液来源
附BZRY:
标准滴定溶液浓度
CAgNo3=检出限/定量限/空白消耗量
V0=
样品编号
取样量
(g)
定容体积
()
稀释倍数
(A)
分取试液体积V(mL)
消耗标液体积V1(mL)
测定值( % )
测定结果
( % )
检测人: 校核人: 审核人:
容量法测定氯离子原始记录(续表)
第 页 共 页
样品编号
取样量
(g)
定容体积
()
稀释倍数
(A)
分取试液体积V(mL)
化学原始记录

复核:计算:试验:
RD20003D-2013化学分析原始记录表(三)
样品编号
样品名称
试验日期
试验项目
设备型号
设备编号
试样量(g)
温度(℃)
稀释倍数
标液浓度
标液名称
氧化钾
第一次测定的读数
含量1
(mg)
第二次测定的读数
含量2
(mg)
平均值(%)
氧化钠
第一次测定的读数
含量1
(mg)
第二次测定的读数
含量2
三氧化硫
二氧化硅
三氧化二铁
三氧化二铝
氧化钙
氧化镁
氯离子
样品质量(第一次测量)
样品质量(第二次测定)
样品质量(平均值)
备注
项目
坩埚质量
初始质量
终点质量
质量分数
第一次称量
第二次称量
第一次称量
第二次称量
第一次称量
第二次称量
第一次
第二次
平均值
烧失量
温度(℃)
时间
年月日点分至年月日点分
备注
项目
第一次试验
第二次试验
(mg)
平均值(%)
备注
复核:计算:试验:
波长(nm)
试样量
(ml)
温度(℃)
湿度
标液浓度(μg/ ml)
序号
取样量(mL)
定容体积(mL)
吸光度(A)
参比吸光度(A0)
含量(mg)
质量分数(%)
1
2
质量分数平均值(%)
计算公式:
含量==(m1*V1/m0*V0)*100%
m1——从工作曲线上查得的量,g;V1——分取试液的体积,ml;
消毒剂中有效氯容量分析原始记录

空白标准溶液加入量(ml)
标准溶液浓度( )
浓度均值( )
重铬酸钾
硫代硫酸钠
样品编号
碘量瓶号
氯消毒剂用量(g)
稀释倍数
(硫代硫酸钠)标准溶液消耗量(ml)
含氯消毒剂中有效氯含量w
(%)
平均值
()
相对偏差/回收率
计算公式:
w(CL2)
w(CL2)-含氯消毒剂中有效氯含量,%;
V-硫代硫酸钠碘量瓶号
氯消毒剂用量(g)
稀释倍数
(硫代硫酸钠)标准溶液消耗量(ml)
含氯消毒剂中有效氯含量w
(%)
平均值
()
相对偏差/回收率
计算公式:
w(CL2)
w(CL2)-含氯消毒剂中有效氯含量,%;
V-硫代硫酸钠标准溶液用量(mL);
C-硫代硫酸钠标准溶液浓度,(mol/L);
0.03545-与1.00mL硫代硫酸钠溶液(1.000mol/L)相当的以克表示的有效氯的质量;
氯消毒剂中有效氯原始记录
第页共页
项目编号:分析项目:消毒剂中有效氯样品性质:收样日期:分析日期:检出限:/.
分析方法:生活饮用水标准检验方法消毒剂指标GB/T 5750.11-2006仪器型号规格:仪器管理编号:检测地点:理化室环境温度:℃相对湿度:%RH
基准试剂名称
基准试剂加入量(g)
标准溶液名称
m-氯消毒剂的用量(g)
始读
终读
消耗
备注:
/
分析/日期:校核/日期:复核/日期:
C-硫代硫酸钠标准溶液浓度,(mol/L);
0.03545-与1.00mL硫代硫酸钠溶液(1.000mol/L)相当的以克表示的有效氯的质量;
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氯气碘量法原始记录表
摘要:
一、氯气碘量法简介
1.氯气碘量法的定义
2.氯气碘量法的基本原理
二、氯气碘量法原始记录表的填写
1.实验基本信息
a.实验名称
b.实验目的
c.实验日期
d.实验人员
2.实验仪器与试剂
a.仪器设备
b.试剂材料
3.实验步骤与结果
a.实验步骤
b.实验结果
4.实验数据处理与分析
a.数据处理方法
b.数据分析结论
正文:
氯气碘量法是一种常用的分析化学方法,主要用于测定样品中氯离子的含量。
该方法基于氯离子与碘单质反应生成碘化氯的化学反应,通过测定反应前后碘的量差来计算氯离子的含量。
氯气碘量法具有操作简便、结果准确等优点,在工业、环保等领域具有广泛的应用。
在实际操作过程中,需要详细记录实验的相关信息,以便对实验过程进行回顾和分析。
氯气碘量法原始记录表就是用于记录这些信息的表格。
原始记录表主要包括实验基本信息、实验仪器与试剂、实验步骤与结果、实验数据处理与分析等内容。
1.实验基本信息
实验基本信息包括实验名称、实验目的、实验日期和实验人员。
实验名称应简洁明了,能够反映实验的主要内容;实验目的明确实验要解决的问题;实验日期记录实验进行的日期,以便对实验过程进行时间追溯;实验人员记录参与实验的人员,以便对实验过程进行责任追溯。
2.实验仪器与试剂
实验仪器与试剂包括实验中使用的仪器设备以及试剂材料。
仪器设备应记录型号、数量等信息;试剂材料应记录名称、规格、数量等信息。
这些信息的记录有助于对实验过程进行重现和复验。
3.实验步骤与结果
实验步骤应详细记录实验的操作过程,以便对实验过程进行回顾和分析。
实验结果应记录实验所得数据,包括各指标的测定值、计算值等。
实验结果的记录应准确、完整。
4.实验数据处理与分析
实验数据处理与分析应记录数据处理的方法、分析的结论等。
数据处理方法应根据实验目的和要求选择合适的方法;分析结论应明确实验要解决的问题是否得到解决以及解决的程度。
总之,氯气碘量法原始记录表是对实验过程的详细记录,对于保证实验质量、分析实验结果具有重要作用。
