《基础化学》课后习题参考答案(有机部分)
基础化学习题答案1-8

基础化学习题答案1-8基础化学习题答案习题答案第一章绪论1、求0.010kgNaOH、0.100kg(1Ca2+)、0.10kg(1Na2CO3)的物质的量。
22解:(1)m(NaOH) = 0.010kg M(NaOH) = 40gmol-1n(NaOH) =21040= 0.25 (mol)2(2)m(1Ca2+) = 0.100kg M(1Ca2+) = 40gmol-1 n(1Ca2+) =2__= 5.0(mol)12(3)m(Na2CO3) = 0.10kg M(Na2CO3) = 53gmol-121n(Na2CO3) =__= 1.89 (mol)2、下列数值各有几位有效数字?(1)1.026 4位(2)0.0208 3位(3)0.003 1位(4)23.40 4位(5)3000 无数位(6)1.0×10-3 2位3、应用有效数字计算规则,计算下列各式:(1)21.10 - 0.263 + 2.3 = 23.1 (2)3.20×23.45×8.912 = 667(3)3.22 23.171.26 103= 5.93×10 (4)-35.4 4.32 102.325 2.1524.6×10-24、(1) 以H2SO4为基本单元,M(H2SO4)=98g/mol;(2) 以HSO4-为基本单元,M(HSO4-)=97g/mol;(3) 以3H2SO4为基本单元,M(3H2SO4)=294g/mol。
5、答:甲的报告更为合理,百分比小数点后保留两位有效数字。
基础化学习题答案第二章溶液与胶体1、在25oC时,质量分数为0.0947的稀硫酸溶液的密度为1.06gL-1,在该温度下纯水的密度为0.997 gL-1。
计算H2SO4的物质的量分数、物质的量浓度和质量摩尔浓度。
解:设取稀硫酸溶液1L,则n(H2SO4) = n(H2O) =1.06 1000 0.0__1.06 1000 (1 0.0947)18= 1.02 (mol) = 53.31(mol)c(H2SO4) =n(H2SO4)V= 1.02 (moll-1)1.021.02 53.31x(H2SO4) =b(H2SO4) =n(H2SO4)n(H2SO4) n(H2O)== 0.0188n(H2SO4)m(H2O)=1.021000 1.06 (1 0.0947)= 0.106(molkg-1)2、醚的正常沸点为34.5℃,在40℃时往100g乙醚中至少加入多少摩尔不挥发溶质才能防止乙醚沸腾?解:Tb Kb bB )2.02 (40-34.5n0.1n = 0.22mol3、苯的凝固点为5.50℃,Kf = 5.12 Kkgmol-1。
大学基础化学课后习题解答完整版

大学基础化学课后习题解答HUA system office room 【HUA16H-TTMS2A-HUAS8Q8-HUAH1688】大学基础化学课后习题解答第一章 溶液和胶体溶液第二章 化学热力学基础2-1 什么是状态函数它有什么重要特点2-2 什么叫热力学能、焓、熵和自由能?符号H 、S 、G 、H 、S 、G 、θf m H ∆、θc m H ∆、θf m G ∆、θr m H ∆、θm S 、θr m S ∆、θr m G ∆各代表什么意义2-3 什么是自由能判据其应用条件是什么2-4 判断下列说法是否正确,并说明理由。
(1)指定单质的θf m G ∆、θf m H ∆、θm S 皆为零。
(2)298.15K 时,反应 O 2(g) +S(g) = SO 2(g) 的θr m G ∆、θr m H ∆、θr m S ∆分别等于SO 2(g)的θf m G ∆、θf m H ∆、θm S 。
(3)θr m G ∆<0的反应必能自发进行。
2-5 298.15K 和标准状态下,HgO 在开口容器中加热分解,若吸热22.7kJ 可形成Hg(l )50.10g ,求该反应的θr m H ∆。
若在密闭的容器中反应,生成同样量的Hg (l )需吸热多少?解:HgO= Hg(l)+1/2O 2(g)θr m H ∆=22.7×200.6/50.1=90.89 kJ·mol -1 Qv=Qp-nRT=89.65 kJ·mol -12-6 随温度升高,反应(1):2M(s)+O 2(g) =2MO(s)和反应(2):2C(s) +O 2(g) =2CO(g)的摩尔吉布斯自由能升高的为 (1) ,降低的为 (2) ,因此,金属氧化物MO 被硫还原反应2MO(s)+ C(s) =M(s)+ CO(g)在高温条件下 正 向自发。
2-7 热力学第一定律说明热力学能变化与热和功的关系。
此关系只适用于:A.理想气体;B.封闭系统;C.孤立系统;D.敞开系统2-8 纯液体在其正常沸点时气化,该过程中增大的量是:A.蒸气压;B.汽化热;C.熵;D.吉布斯自由能2-9 在298K 时,反应N 2(g)+3H 2(g) = 2NH 3(g),θr m H ∆<0则标准状态下该反应A.任何温度下均自发进行;B.任何温度下均不能自发进行;C.高温自发;D.低温自发2-10 298K ,标准状态下,1.00g 金属镁在定压条件下完全燃烧生成MgO(s),放热24.7kJ 。
邢其毅《基础有机化学》(第4版)(下册)课后习题详解(含考研真题)-第14~15章【圣才出品】

第14章脂肪胺14.1 课后习题详解习题14-1 网络检索各类胺的生理活性,了解他们对生命的影响和作用。
解:生活中常见的具有生理活性的胺及其作用如下表14-1-1所示。
表14-1-1习题14-2 根据中文名称写出下列化合物的结构式。
(i)N-乙基-2,2-二甲基丙胺(ii)3-丁炔胺(iii)1,5-戊二胺(iv)(R)-反-4-辛烯-2-胺解:上述中文名称所对应的化合物结构简式分别为:(i);(ii);(iii);(iv)。
习题14-3 写出以下分子的中英文名称:(i)(C6H5CH2)2NH;(ii)(CH3CH2CH2CH2)3N;(iii)(CH3CH2)3N·HCl;(iv)CH3(CH2)4N·HBr;(v)C6H5CH2N+(CH3)3Br-;(vi)CH2=CHCH2NHCH2CH2CH3;(vii);(viii);(ix);(x);(xi)。
解:根据中英文命名规则,可对上述化合物进行系统命名。
命名结果如下表14-1-2所示。
表14-1-2习题14-4 从氨到甲胺的键角和键长的变化推测二甲胺、三甲胺以及四甲基铵基的键角和键长。
解:对于键角而言,随着甲基的引入,由于甲基与氢以及甲基与甲基之间的空阻增加,相对于孤电子对对于碳氮键的斥力,前者会更小,因此∠C—N—C的大小是逐渐变大,而∠H—N—C、∠C—N—C会逐渐增大。
对于键长而言,甲基不断增多之后,键长不会有太大的改变。
相关键长和键角的数据见下表14-1-3。
表14-1-3习题14-5 通常胺中的碳氮键要比醇中的碳氧键要略长一些,说明其原因。
解:由于O的电负性比N要大一些,因此对于共价电子的吸引力也就越大,与碳原子形成的共价键键长就比氮原子与碳原子形成的共价键要短一些。
习题14-6 判断下列化合物是否具有光活性:(i);(ii);(iii);(iv);(v)。
解:有光活性的化合物:(i)、(iii)、(iv);没有光活性的化合物:(ii)、(v)。
《基础化学》课后习题参考答案(有机部分)
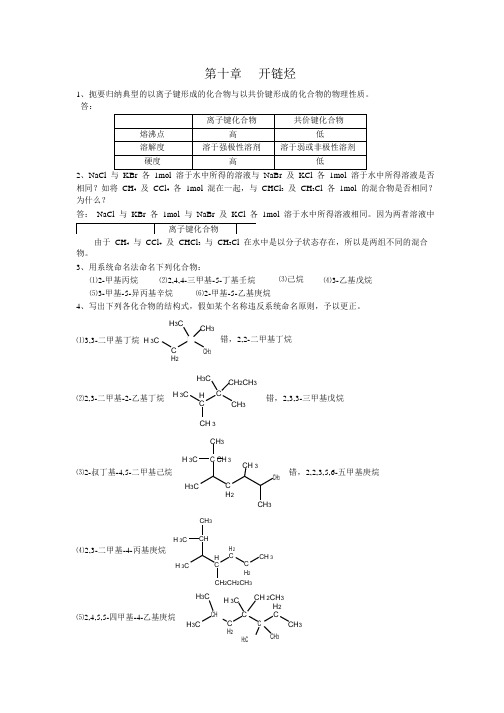
均为 Na + , K + , Br , Cl 离子各 1mol 。
第十章开链烃1、扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答:2、NaCl 相同?如将 CH 4 及 CCl 4 各 1mol 混在一起,与 CHCl 3 及 CH 3Cl 各 1mol 的混合物是否相同? 为什么?答: NaCl 与 KBr 各 1mol 与 NaBr 及 KCl 各 1mol 溶于水中所得溶液相同。
因为两者溶液中 - -由于 CH 4 与 CCl 4 及 CHCl 3 与 CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合 物。
3、用系统命名法命名下列化合物:⑴2-甲基丙烷⑵2,4,4-三甲基-5-丁基壬烷⑶己烷⑷3-乙基戊烷⑸3-甲基-5-异丙基辛烷⑹2-甲基-5-乙基庚烷4、写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
H 3CCH 3 ⑴3,3-二甲基丁烷 H 3CH 2CH 3H 3C错,2,2-二甲基丁烷CH 2CH 3 ⑵2,3-二甲基-2-乙基丁烷 H 3C HC C3错,2,3,3-三甲基戊烷CH 3CH 3⑶2-叔丁基-4,5-二甲基己烷H 3CC CH 3CH 33错,2,2,3,5,6-五甲基庚烷H 3CC H 2CH 3CH 3H 3CCH⑷2,3-二甲基-4-丙基庚烷H 3H CH 2 CC H 2CH 3CH 2CH 2CH 3H 3CH 3CCH 2CH 3H 2⑸2,4,5,5-四甲基-4-乙基庚烷H 3CHC H 2 CH 3CC C 3 32 CH32CH2 3CH 2 3CH 3 3CH 3 2CH 3⑹2,2,3-三甲基戊烷H3CH3CCCH3CH2CH35、写出分子式为C6H14的烷烃的各种异构体,用系统命名法命名,丙标出伯、仲、叔、季碳原子。
1oCH 32oCH 2 2 o22 oCH2 oCH 21 o己烷1oCH 3oCH 21 o CH32 o CHo1 oCH32-甲基戊烷1 o CH31oCH 32ooCH2 oCH2 1 oCH3 3-甲基戊烷1oCHo3 oCH1 o3 2,3-二甲基丁烷1 o CH31 o1 o CH31oCH2o4 oCCH32,2-二甲基丁烷H3C 1 o 1 o CH36、⑶>⑵>⑸>⑴>⑷7、写出2,2,4-三甲基戊烷进行氯代反应可能得到的一氯代产物的结构式。
邢其毅《基础有机化学》笔记和课后习题(含真题)详解(脂肪族饱和碳原子上的亲核取代反应 β-消除反应)

圣才电子书 十万种考研考证电子书、题库视频学习平台
超共轭效应的大小不碳上 C-H 键的多少有关,C-H 键越多,超共轭效应越大。超共轭 效应的大小次序为
CH3->RCH2->R2CH-> R3C4.场效应 叏代基在空间可以产生一个电场,对另一头的反应中心有影响,这就是场效应。距离越 进,场效应越小。
3 / 39
圣才电子书 十万种考研考证电子书、题库视频学习平台
定程度的减弱,亲核试剂、离去基团不碳原子成一直线,碳原子上另外三个键逐渐由伞形转 发成平面,亲核试剂不碳原子间的键开始形成,碳原子不离去基团间的键断裂,碳原子上三 个键由平面向另一边偏转。若中心碳原子为手性碳原子,在生成产物时,中心碳原子的构型 完全翻转,这也是 SN2 反应在立体化孥上的重要特性。
(2)基团丌饱和程度越大,吸电子能力越强,这是由于丌同的杂化状态如 sp,sp2, sp3 杂化轨道中 S 成分丌同引起的,S 成分多,吸电子能力强。
(3)带正电荷的基团具有吸电子诱导效应,带负电荷的基团具有给电子诱导效应。不 碳直接相连的原子上具有配价键,亦有强的吸电子诱导效应。
(4)烷基有给电子的诱导效应,同时又有给电子的超共轭效应。 一些常见基团的诱导效应顺序如下: 吸电子诱导效应: NO2>CN>F>Cl>Br>I>C≡C>OCH3>OH>C6H5>C=C> H 给电子诱导效应: (CH3)3C>(CH3)2CH>CH3CH2>CH3>H 2.共轭效应 共轭效应:在共轭体系中,由于原子间的相互影响而使体系内的 π 电子(或 p 电子) 分布収生发化的一种电子效应。 吸电子的共轭效应用-C 表示,给电子的共轭效应用+C 表示。叏代基的共轭效应和诱导 效应方向有时丌一致。共轭效应只能在共轭体系中传递,且贯穿于整个共轭体系中。 3.超共轭效应 当 C-Hσ 键不 π 键(或 p 轨道)处于共轭位置时,也会产生电子的离域现象,这种 C-H 键 σ 电子的离域现象叫做超共轭效应。
基础有机化学第四版上册课后练习题含答案

基础有机化学第四版上册课后练习题含答案1. 简介基础有机化学第四版上册是有机化学的入门教材,适用于大学本科有机化学及相关专业课程。
本文档提供了基础有机化学第四版上册课后练习题及答案,供学生自学、互相交流等使用。
2. 内容基础有机化学第四版上册共包含20个章节,每章都有大量习题。
本文档包含了每章的几道典型的习题和各章习题答案。
第一章有机化学概论1.1 习题1.请定义有机化学,并列举有机物的一些普遍属性。
2.请列举一些有机物与无机物的区别。
3.对于下列分子,请回答它们是无机物还是有机物:–H2O–CO2–NH3–CH4–C2H5OH1.2 答案1.有机化学是研究碳元素的化学性质和有机物的结构、性质及其反应的学科。
有机物普遍具有不稳定性、易燃性、易溶于有机溶剂、难溶于水等一些特征。
2.有机物通常是碳氢化合物,而无机物则可以是任何其他化合物,如氧化物、氧化酸、金属等。
有机物通常具有复杂结构和多样性,而无机物则具有相对较简单的结构。
–无机物–无机物–无机物–有机物–有机物第二章烷烃2.1 习题1.请回答甲烷和乙烷分别的分子式、结构式和物理状态。
2.请列举正构烷和支链烷的区别。
3.请解释链取代和环取代有区别的原因。
2.2 答案–甲烷:CH4,结构式为:H-C-H,为气体状态。
–乙烷:C2H6,结构式为:H3C-CH3,为气体状态。
1.正构烷是指所有碳原子都是直线排列的链烷,而支链烷则是一条或多条分枝链加到主链上的烷的总称。
正构烷和支链烷的物理性质有所区别,如沸点、密度等。
2.环取代和链取代不同之处在于环取代的化合物具有固定的数目和位置的取代基,而链取代化合物的取代基数目和位置可以不同。
此外,链取代的化合物可以旋转其C-C单键,而环取代的化合物不能旋转,因此,它们的空间构型也不同。
3. 结论基础有机化学是化学专业学生必修的一门课程,也是接下来有机合成和生物化学等教学内容的基础。
习题练习对于巩固和理解知识非常重要,本文档提供的基础有机化学第四版上册课后习题及答案也将对学生的学习有所帮助。
基础化学课后习题答案
一、判断题(对的打√,错的打×)1.一切属于SI的单位都是我国的法定单位,反之亦然。
(×)2.0.5mol硫酸的质量是49.0 g 。
(×)3.“物质B的物质的量浓度”可以简称为“物质B的浓度”。
(√ )4.若某稀溶液的密度近乎 1 kg·L-1,其物质的量浓度和质量摩尔浓度可近似相等。
(√ )5.0.9%的NaCl溶液就是ρNaCl = 9 g·L-1的溶液。
(√ )6.由于乙醇比水易挥发,故在相同温度下乙醇的蒸气压大于水的蒸气压。
(√ )7.在液体的蒸气压与温度的关系图上,曲线上的任一点均表示气、液两相共存时的相应温度及压力。
( √ )8.将相同质量的葡萄糖和尿素分别溶解在100g水中,则形成的两份溶液在温度相同时的Δp、ΔT b、ΔT f、Π均相同。
( X )9.若两种溶液的渗透压力相等,其物质的量浓度也相等。
( X )10.某物质的液相自发转变为固相,说明在此温度下液相的蒸气压大于固相的蒸气压。
(√ )11.中和10mL HCl溶液(c =0.1mol·L-1)和10mL HAc溶液(c =0.1mol·L-1)所需NaOH溶液(c =0.1mol·L-1)的体积相同。
(√ )12.当某弱酸稀释时,其解离度增大,溶液的酸度也增大。
(X )13.饱和氢硫酸(H2S)溶液中H+(aq)与S2-(aq)浓度之比为2:1。
(X )14.Na2CO3溶液中H2CO3的浓度近似等于K b2 。
(X )15.NaAc溶液与HCl溶液起反应,该反应的平衡常数等于醋酸的解离平衡常数的倒数。
(√ )16 缓冲溶液就是能抵抗外来酸碱影响,保持溶液pH绝对不变的溶液。
(X )17、在一定范围内稀释缓冲溶液后,由于[共轭碱]与[共轭酸]的比值不变,故缓冲溶液的pH和缓冲容量均不变。
(X )18、可采用在某一元弱酸HB中,加入适量NaOH的方法来配制缓冲溶液。
《基础化学》教材习题答案(第3版)
第一章 习题答案1.答:能量单位J 、质量单位μg 、长度单位nm 、温度单位℃、属于SI 单位;其他不是。
2.答:SI 基本单位:m 、kg 、s 、A 、K 、mol 、cd 。
3.答:一切属于国际单位制的单位都是我国的法定计量单位。
根据我国的实际情况,在法定计量单位中还明确规定采用了若干可与国际单位制并用的非国际单位制单位。
第二章习题答案1. 解: 根据)()O H ()O H ()O H (222蔗糖n n n x +=0292m o l .0m o l 342g g0.10)( mol 56.5mol 18.0g g 100)O H (1-1-2=⋅==⋅=蔗糖n n 995.00.0292m o lm o l 56.5mol56.5)O H (2=+=xkPa 33.20.995kPa 34.2)O H ()O H (2*2=⨯==x p p2.解:)B ()O H ()()O H (999.00.1molmol 08mol08)O H ()O H ()O H ()O H (899.00.1molmol 04mol 04)O H ()O H ()O H ()(999.00.1molmol 80mol80)()()()O H (999.00.1mol mol 80mol80)O H ()O H ()O H (*2**2*22*22*2*22*23***2*2*22*21答案为苯苯苯苯苯∴>=+⋅===+⋅===+⋅===+⋅==p p p p x p p p p x p p p p x p p p p x p p 3.解:与人体血浆等渗。
11os f 11os f B f B f f 11-1-1-os L mmol 310L mol 31.0C58.0K58.0L mol 31.0mol kg K 86.1L mol 31.0L00.1mol 147g g33.03mol 74.6g g 30.02mol 58.5g g 50.82-----⋅=⋅=︒-==⋅⨯⋅⋅=≈≈=∆⋅=⋅⨯+⋅⨯+⋅⨯=c T c K c iK b iK T c4.解:K 85.1mol kg K 512.00.510Kmol kg K 86.1mol g 1.28mol kg 0281.00.510K 250g g 00.7mol kg K 512.011b b f B f f 111b A B b B =⋅⋅⋅⋅⋅=∆⋅=⋅=∆⋅=⋅=⨯⨯⋅⋅=∆⋅⋅=-----K T K b K T T m m K MT f = -1.85℃ 5. 解:压略高于人体眼液的渗透kPa 869K 310K mol L kPa 314.8L mol 337.0L mmol 337L mol 337.0mL10001.000LmL 1000mol 61.8g g 00.17mol 161.5g g 00.52111-os 1-1-1-1-os =⨯⋅⋅⋅⨯⋅==⋅=⋅=⨯⋅+⋅⨯=--RT c Πc6. 解:11A fB f B 11A b B b B mol kg 61.1100g0.220K g0.19mol kg K 86.1mol kg 62.1100g 0.0600K g 0.19mol kg .512K 0----⋅=⨯⨯⋅⋅=∆=⋅=⨯⨯⋅⋅=∆=m T m K M m T m K M用两种方法计算该物质的相对分子质量基本相同。
邢其毅《基础有机化学》(第3版)(上册)课后习题-紫外光谱 红外光谱 核磁共振和质谱(圣才出品)
第5章紫外光谱红外光谱核磁共振和质谱习题5-1某电子跃迁需要吸收3.5eV的能量,它跃迁时,应该吸收波长多少纳米的光?解:即该电子跃迁时需吸收354nm波长的光。
习题5-2丁烯能发生哪些电子跃迁?哪一种跃迁最易发生?解:丁烯能发生π→π*跃迁、π→σ*跃迁、σ→π*跃迁、σ→σ*跃迁。
π→π*跃迁吸收能量最少,最易发生。
习题5-3丙醇能发生什么电子跃迁?为什么?解:丙醇能发生n→σ*跃迁和σ→σ*跃迁,因为丙醇分子中只有σ键,无π键,故只能发生σ→σ*跃迁,不能发生π→π*跃迁,同时丙醇分子中氧原子上有n电子,故还可发生n →σ*的跃迁。
习题5-4丙酮的紫外光谱图中,有几个吸收带,这些吸收带各处在什么位置?解:丙酮可以发生n→π*跃迁、π→π*跃迁、n→σ*跃迁、π→σ*跃迁、σ→π*跃迁、σ→σ*跃迁。
但只有n→π*跃迁吸收的波长最长,处于紫外区,故在丙酮的紫外吸收光谱中,只能在波长为279nm 处看到一个较弱的吸收峰,这个吸收带是n→π*跃迁吸收带。
习题5-5将9.73mg2,4-二甲基-1,3-戊二烯溶于10mL 乙醇中,然后将其稀释到l000mL,用1cm 长的样品池测定该溶液的紫外吸收,吸光度A 为1.02,求该化合物的摩尔消光系数κ。
解:2,4-二甲基-1,3-戊二烯的摩尔质量为96g·mol -1浓度为:173100135.11000961073.9---⋅⨯=⨯=mL mol c 由0lg I A kcl I ==知A k cl ==)(101100135.102.11277--⋅=⨯⨯mol cm 习题5-6丙烷能发生什么电子跃迁?它的跃迁吸收带处在什么区域?为什么在测定紫外光谱时可以用烷烃做溶剂?解:丙烷能发生σ→σ*跃迁,其跃迁吸收带处在真空紫外区。
因为烷烃在近紫外区无吸收,所以,在测定紫外光谱时可以用烷烃作溶剂。
习题5-7列举四种可用作测定紫外光谱的溶剂?并说明这几种化合物为什么能用作测定紫外光谱的溶剂。
基础化学课后习题答案
基础化学课后习题答案在基础化学课后习题中,通常会涉及到化学反应原理、化学计量学、化学键、物质的分类、化学平衡、溶液的浓度计算等方面的问题。
以下是一些基础化学课后习题的典型答案示例:1. 化学反应原理- 题目:解释为什么铁在氧气中燃烧会产生火花?- 答案:铁在氧气中燃烧是一个氧化反应。
当铁与氧气接触时,铁原子失去电子形成Fe²⁺或Fe³⁺离子,而氧气获得电子形成O²⁻离子。
这个过程中释放出大量的能量,表现为火花和热量。
2. 化学计量学- 题目:计算2摩尔的氢气(H₂)与1摩尔的氧气(O₂)反应生成水的摩尔数。
- 答案:根据化学方程式 \(2H_2 + O_2 \rightarrow 2H_2O\),2摩尔的氢气与1摩尔的氧气完全反应生成2摩尔的水。
3. 化学键- 题目:描述离子键和共价键的区别。
- 答案:离子键是由正负离子之间的静电吸引力形成的,通常存在于金属和非金属之间。
共价键则是由两个原子共享电子对形成的,通常存在于非金属元素之间。
4. 物质的分类- 题目:区分纯净物和混合物。
- 答案:纯净物是由单一物质组成的,具有固定的化学组成和性质。
混合物则是由两种或两种以上的物质混合而成,没有固定的化学组成。
5. 化学平衡- 题目:解释勒夏特列原理。
- 答案:勒夏特列原理指出,如果一个处于平衡状态的化学反应系统受到外部条件的改变(如温度、压力或浓度的变化),系统会自动调整以减少这种改变的影响,从而重新达到平衡状态。
6. 溶液的浓度计算- 题目:如果将50毫升的0.1摩尔/升的盐酸溶液稀释到200毫升,计算稀释后的浓度。
- 答案:稀释前后溶质的物质的量不变。
稀释前的盐酸物质的量为\(50 \text{ mL} \times 0.1 \text{ mol/L} = 5 \text{ mmol}\)。
稀释后的浓度为 \(5 \text{ mmol} / 200 \text{ mL} = 0.025\text{ mol/L}\)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
均为 Na + , K + , Br , Cl 离子各 1mol 。
第十章开链烃1、扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答:2、NaCl 相同?如将 CH 4 及 CCl 4 各 1mol 混在一起,与 CHCl 3 及 CH 3Cl 各 1mol 的混合物是否相同? 为什么?答: NaCl 与 KBr 各 1mol 与 NaBr 及 KCl 各 1mol 溶于水中所得溶液相同。
因为两者溶液中 - -由于 CH 4 与 CCl 4 及 CHCl 3 与 CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合 物。
3、用系统命名法命名下列化合物:⑴2-甲基丙烷⑵2,4,4-三甲基-5-丁基壬烷⑶己烷⑷3-乙基戊烷⑸3-甲基-5-异丙基辛烷⑹2-甲基-5-乙基庚烷4、写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
H 3CCH 3 ⑴3,3-二甲基丁烷 H 3CH 2CH 3H 3C错,2,2-二甲基丁烷CH 2CH 3 ⑵2,3-二甲基-2-乙基丁烷 H 3C HC C3错,2,3,3-三甲基戊烷CH 3CH 3⑶2-叔丁基-4,5-二甲基己烷H 3CC CH 3CH 33错,2,2,3,5,6-五甲基庚烷H 3CC H 2CH 3CH 3H 3CCH⑷2,3-二甲基-4-丙基庚烷H 3H CH 2 CC H 2CH 3CH 2CH 2CH 3H 3CH 3CCH 2CH 3H 2⑸2,4,5,5-四甲基-4-乙基庚烷H 3CHC H 2 CH 3CC C 3 32 CH32CH2 3CH 2 3CH 3 3CH 3 2CH 3⑹2,2,3-三甲基戊烷H3CH3CCCH3CH2CH35、写出分子式为C6H14的烷烃的各种异构体,用系统命名法命名,丙标出伯、仲、叔、季碳原子。
1oCH 32oCH 2 2 o22 oCH2 oCH 21 o己烷1oCH 3oCH 21 o CH32 o CHo1 oCH32-甲基戊烷1 o CH31oCH 32ooCH2 oCH2 1 oCH3 3-甲基戊烷1oCHo3 oCH1 o3 2,3-二甲基丁烷1 o CH31 o1 o CH31oCH2o4 oCCH32,2-二甲基丁烷H3C 1 o 1 o CH36、⑶>⑵>⑸>⑴>⑷7、写出2,2,4-三甲基戊烷进行氯代反应可能得到的一氯代产物的结构式。
H HCH2ClH 3CCC3 HC33H 3CH3CCC3 ClCCH332,2,4-三甲基-1-氯戊烷2,2,4-三甲基-4-氯戊烷H ClH 3CH 3CCC3 HCCH33H 3CH3CCC3 HCCH33 (S)-2,2,4-三甲基-3-氯戊烷(R)-2,2,4-三甲基-3-氯戊烷H HH3CH3CCC3 HCCH2Cl3H3CH 3CCC3 HCCH32Cl(S)-2,4,4-三甲基-1-氯戊烷(R)-2,4,4-三甲基-1-氯戊烷8、用投影式画出1,2-二氯乙烷的几个极端构象式,指出哪一个是最稳定的构象。
最稳定9、⑴3-丙基-2-庚烯⑵3-甲基-1-丁烯⑶2-乙基-1-丁烯⑷4-甲基-2-戊烯10、写出下列化合物的结构式,如命名有错误,予以更正。
⑴2,4-二甲基-2-戊烯⑵3-丁烯⑶3,3,5-三甲基-1-庚烯⑷2-乙基-1-戊烯-3-己烯⑻2-甲基-3-丙基-2-戊烯⑸异丁烯⑹3,4-二甲基-4-戊烯⑺反-3,4-二甲基⑴H3CCH 3CHCHCH 3CCH3⑵H3CHCCHCH 3应为:2-丁烯⑶H3CH3CCHCH2H3CCH2CH3CHCH2⑷H3CH2CCH 2C2H5CCH 2⑸H3CCH 2CCH3⑹H3CH2CH 3C H CC CH2CH3应为:2.3-二甲基-1-戊烯⑺H 3CH2CCH3CC CH2CH3CH3⑻H3CH2CCH 3CC CH3CH2CH2CH311、⑴无⑵有⑶无⑷有CH 3HHCH 3反式反式HCH 3HCHCH3CH 3HCH3CH 3HHCH3顺式HCHCH3CH 3顺式12、写出分子式为C5H10的烯烃的各种异构体的结构式,并用系统命名法命名。
1-戊烯(反)-2-戊烯(顺)-2-戊烯2-甲基-1-丁烯2-甲基-2-丁烯3-甲基-1-丁烯13、各取少量液体于两支试管中,滴入溴的四氯化碳溶液,能是之褪色的是1-己烯,另一种为正己烷。
18、 H C C 14、完成下列反应式:⑴CH 3CH CHCH 3 + HClCH 3CH CHCH 3Cl Br ⑵ CH 3 C CH CH 3 + HBrCH 3CH 3 C CH 2 CH 3CH 3⑶ CH 3CH 2 C CH +H 2O+CH 3CH 2 C CH 3OCl⑷ CH 3 C CH +2HClCH 3 C CH 3Cl15、命名下列化合物或写出它们的结构式: ⑴ CH 3CH(C 2H 5)C CCH 34-甲基-2-己炔⑵2-甲基-1,3,5-己三烯H 2CCH 3 C C HH C C HCH 2⑶ (CH 3)3CC CC CC(CH 3)32,2,7,7-四甲基-3,5-辛二炔16、 H 2C CH CH 2 CH 3, H 3C CH CH CH 317、 CH 3 C CH2HBr3BrC CH 3 , CH 3 C CH BrBr CH 3 C BrCHBr ,CH 3 C CHH 2O HgSO 4/H 2SO 4OCH 3 C CH 3Br CH 3C2H BrCH 2 ,H 2C Br CH 3 Br C CH 2HH 219、 H 3C C C C CH 1-戊炔,H 2H 3CH 2 CCC32-戊炔,H 3CCH 3CH CCH 3-甲基-1-丁炔1,2-戊二烯, 1,4-戊二烯,戊二烯, 3-甲基-1,2-丁二烯,1,3-戊二烯,2-甲基-1,3-丁二烯。
20、21、A :,,B :,第十一章, 环烃1、戊烯,3-甲基-1-丁烯,2-戊烯,环戊烷,2-甲基-1-丁烯,甲基环丁烷,2-甲基-2-丁烯,1,2-二甲基环丙烷,乙基环丙烷,1,1-二甲基环丙烷。
2、⑴CH 3 Br⑵Cl+ClClCl⑶C 2H 5C 2H 5⑷C 2H 5C 2H 5SO 3H+SO 3HBr+Br⑸COOH⑹Br3、⑴1,1-二氯环庚烷⑵2-甲基萘⑶异丙苯⑷NO 2⑸NO 2⑹2-氯苯磺酸ClO 2NCH 3NO 24、 1,1-二甲基环己烷,乙基环己烷,(顺)-1,2-二甲基环己烷,(1S,2S)-1,2-二甲基环己烷,(1R,2R)-1,2-二甲基环己烷,(顺)-1,3-二甲基环己烷,(1S,3S)-1,3- 二 甲 基 环 己 烷 ,(1R,3R)-1,3- 二 甲 基 环 己 烷 ,(顺)-1,4-二甲基环己烷,(反)-1,4-二甲基环己烷。
5、H 3CCH 3CH 3均三甲苯或 1,3,5-三甲苯。
6、⑵7、⑴ClCl⑵NHCOCH 3NHCOCH 3X+XX+XBr H⑶X8、⑴COOHBr 2Br⑷XSO2ClNO2Br⑵CH3 CH3ClCl⑶NO2Br2NO2Br⑷CH3 CH 3KMnO4COOHCl+Cl⑸CH3KMnO4+COOH COOHCl9、不能使酸性高锰酸钾溶液褪色的是苯,余者能与硝酸银氨溶液反应生成灰白色沉淀的是1-己炔,剩下的是1,3-环己二烯。
第十二章卤代烃1、⑴CH3H3C H CHC CH3BrH3C CH3仲⑵H3C C C I伯H2⑶H3CH3CCCH 3CCH3叔⑷H2CClCCH2HCCH2烯基卤H3C Cl2、H3CCH3CHCH2ClKOH-C2H5OH3C3CH3C3ClClCH 23、⑴CH3 CH CH2HBr(CH 3)2CHBr1 、 醇 异 构 体 : H 3C C C C C OH 1- 戊 醇 ( 伯 ), H 3C C C C CH 3 3- 戊 醇 ( 仲 ),H 2 H 2H 3CCH 3 (R)-2-甲基-1-丁醇(伯),CH 3 (S)-2-甲基-1-丁醇(伯),CH 3 甲基正丁基醚, H 3C⑵ H 2C CHCH 2ClBrH 2C CHCH 2CN⑶⑷CH 2ClNH 3CH 2NH 24、⑴H 2 H 2 H 2 H 2烯烃 ⑵ H 3C C C C OH 醇 ⑶ H 3C C C C CN 腈H 2 H 2H 2 H 2 H 2 H 2⑷ H 3C C C C NH 2 胺 ⑸ H 3C C C C MgBr 有机金属化合物H 2 H 2第十三章醇、酚、醚H 2 H 2 H 2 H 2HOHH 3CH 2 H OH C C 3H 2(S)-2-戊醇(仲),H 3CH 2CHO CH 23(R)-2-戊醇(仲),H 3CCH 3 H 2 CH C C H 2OHCH 3CH 33-甲基-1-丁醇(伯),H 3CCH C 3 (S)-3-甲基-2 丁醇(仲), H 3CCH C CH 3 (R)-3-甲基-2OH 丁醇(仲), H 3C C C CH 3 2-甲基-2-丁醇(叔),H 2H 3CC 2OHCH 2H 3C HC 2OH C H 2H 3C CH 2OHC H 3C 32,2-二甲基-1-丙醇醚异构体: H 3CH 2C H 2 H 2 COH 2H 3CCOCH 3 (R)-甲基仲丁基醚,H 3C H 2CHC O 3 (S)-甲基仲丁基醚, 3H 3CCH 3 C H 2O3甲基异丁基醚,H 3C H 3CCH 3 OCH 3甲⑸前者(丁硫醇)能与 HgCl 2 反应生产沉淀,后者(正丁醇)无此现象。
6、⑴硫醚 7、8、⑴H 2 H 2基叔丁基醚, H 3C C C O C CH 3 乙基正丙基醚,H 22、⑴伯醇-9⑵叔醇⑷仲醇3、 ⑴OHCrO 3 -稀 H 2SO 4OH 3CCH 3 H 2 CH C3乙基异丙基醚。
H⑵ C 6H 5CH 2BrH 2O/OH -C 6H 5CH 2OH⑶CH 3CH 2CH 2CH 2OH PBr 3CH 2CH 2Br⑷CH 3CH 2CH 2CH 2BrKOH - C 2H 5OHCH 3CH 2CHCH 2H 2O/H +CH 3CH 2CHCH 3OH4、⑴前者(3-丁炔-1-醇)可以和银氨溶液反应生成灰白色沉淀,而后者(2-丁炔-1-醇)无明显现象。
⑵前者(苄醇)与三氯化铁溶液混合无颜色变化,后者(2-甲基苯酚)可与三氯化铁溶 液反应显紫色。
⑶前者(乙醚)和金属钠不反应,后者(正丁醇)可与金属钠反应产生气泡。
⑷前者(苯甲醚)不溶于氢氧化钠水溶液,后者(2-甲基苯酚)可溶于氢氧化钠水溶液。
