化学选修5 第三章复习总结
高中化学选修五-第三章第四节-有机合成
③2mol-OH或2mol-COOH与活泼金属反应放出1molH2。
④1mol-COOH与碳酸氢钠溶液反应放出1molCO2
⑤1mol一元醇与足量乙酸反应生成1mol酯时,其相对分子 质量将增加42,1mol二元醇与足量乙酸反应生成酯时,其相 对分子质量将增加84。
解析:由题意可知,C不是甲酸,E为酮(分子中含碳原子数≥3),
故A可能为
或
。
• 答案:B
25
解有机物综合推断类试题的常用方法 (1)逆推法。由产物推断未知反应物或中间产物时叫逆推法。 (2)根据反应条件推断。在有机合成中,可以根据一些特定反应的 条件,推出未知有机物的结构简式。如“N―aO― △H→/醇”是卤代烃消去的条 件;“ N―aO△―H→/水 ”是卤代烃水解的条件,“ 浓― 17―硫0 →℃酸 ”是乙醇消去的条 件,“浓硫酸,△”是羧酸和醇发生酯化反应的条件。
(1).碳骨架构建:构建方法会以信息形式给出。 包括碳链增长和缩短 、成环和开环等。
(2.官能团的引入和转化: (1)官能团的引入:
思考与交流
1、引入碳碳双键的三种方法: 卤代烃的消去;醇的消去;炔烃的不完全加成。
2、引入卤原子的三种方法:
醇(或酚)的取代;烯烃(或炔烃)的加成;
烷烃(或苯及苯的同系物)的取代。
•2020/2/14 ⑩遇浓硝酸变黄的有机物为: 蛋白质
1717
寻找题眼.确定范围---【有机物·条件】
①当反应条件为NaOH醇溶液并加热时,必定为 卤代烃的消去反应。 ②当反应条件为NaOH水溶液并加热时,通常为 卤代烃或酯的水解反应。
③当反应条件为浓H2SO4并加热时,通常为
高中化学选修5_有机化学总复习

高中化学选修5_有机化学总复习高中化学选修 5——有机化学总复习在高中化学的学习中,选修 5 的有机化学是一个重要且富有挑战性的部分。
为了帮助同学们更好地掌握这部分知识,进行一次全面的总复习是非常必要的。
首先,让我们来回顾一下有机化学的基本概念。
有机化合物是指含碳的化合物,但一些简单的含碳化合物,如一氧化碳、二氧化碳、碳酸盐等,由于它们的性质与无机物相似,通常不被视为有机化合物。
碳原子的独特结构使得它能够形成多种多样的化学键,从而构建出复杂而丰富的有机分子。
碳原子可以通过单键、双键和三键与其他原子相连,形成链状、环状等不同的结构。
这就为有机化合物的多样性奠定了基础。
有机化合物的分类是我们学习的重要内容之一。
按照官能团的不同,有机化合物可以分为烃类(包括烷烃、烯烃、炔烃和芳香烃)、卤代烃、醇、酚、醚、醛、酮、羧酸、酯等。
烷烃是最简单的一类烃,其通式为 CₙH₂ₙ₊₂。
它们的化学性质相对稳定,通常在光照条件下能与卤素单质发生取代反应。
烯烃含有碳碳双键,通式为 CₙH₂ₙ。
双键的存在使得烯烃具有较强的反应活性,能与卤素单质、氢气、水等发生加成反应。
炔烃则含有碳碳三键,通式为 CₙH₂ₙ₋₂。
它们的化学性质与烯烃类似,但反应活性可能更强。
芳香烃,如苯,具有特殊的环状结构和独特的化学性质。
苯环上的氢原子可以在一定条件下被取代,而苯环本身在特定条件下也能发生加成反应。
卤代烃是烃分子中的氢原子被卤素原子取代后的产物。
它们在有机合成中起着重要的桥梁作用,可以通过水解反应转化为醇,也可以通过消去反应生成烯烃。
醇类化合物,官能团为羟基(—OH)。
根据羟基所连接的碳原子类型,醇可以分为伯醇、仲醇和叔醇。
醇能发生氧化反应、消去反应等。
酚类的官能团也是羟基,但羟基直接连接在苯环上。
酚具有一定的酸性,能与氢氧化钠等碱反应。
醚的官能团是醚键(—O—),结构相对较为稳定。
醛和酮的官能团分别为醛基(—CHO)和羰基()。
醛能被氧化为羧酸,也能与氢气发生加成反应生成醇。
人教版选修5化学第三章第二节醛练习知识点

人教版选修5化学第三章第二节醛练习知识点第二节醛知识点一醛类1.醛的结构(1)概念:由烃基或氢原子与醛基相连而构成的化合物。
(2)官能团:醛基(—CHO或)。
2.醛的分类3.甲醛和乙醛物质甲醛(蚁醛)乙醛分子式CH2O C2H4O 结构简式HCHO CH3CHO物理性质颜色无色无色气味有刺激性气味有刺激性气味状态气态液态溶解性易溶于水,35%~40%的甲醛水溶液又称福尔马林能跟水、乙醇等互溶(1)概念:羰基与两个烃基相连的化合物。
(4)代表物:丙酮,其结构简式为CCH3OCH3,不能被银氨溶液、新制的Cu(OH)2等弱氧化剂氧化,能与H2发生加成反应。
1.下列物质中不属于醛类的是()解析:选B。
①属于醛,②属于酯类,③属于醛,④中含有氯元素,不属于醛。
2.下列关于醛的说法中正确的是()A.所有的醛都有醛基和烃基B.一元醛的通式为C n H2n OC.醛的官能团为—COHD.所有的醛都能发生银镜反应解析:选D。
A项,甲醛(HCHO)中没有烃基,B项为饱和一元醛的通式,C项醛的官能团为—CHO。
醛和酮的区别与联系类别醛酮区别官能团官能团位置碳链末端碳链中间简写形式类别醛酮联系通式饱和一元醛:C n H2nO饱和一元酮:C n H2n O 同分异构现象相同碳原子数的饱和一元醛和饱和一元酮互为同分异构体下列物质分子结构中含有醛基,但是不属于醛的是()[解析]醛的结构为R—CHO,其中R为H或烃基,A项物质不含—CHO,B、C、D项中含—CHO,但B项物质—CHO连接的不是H或烃基,B为甲酸乙酯,不属于醛类。
[答案]B能发生银镜反应的有机物是不是都属于醛类答案:有机物只要含有醛基就可以发生银镜反应,能发生银镜反应的不一定都是醛,可能是其他含有醛基的有机物。
例如:甲酸,甲酸某酯,另外,还有将要学习的葡萄糖等。
醛的概念及性质1.下列有关说法正确的是()A.含有醛基的物质一定是醛B.含醛基的物质能发生银镜反应,但不能使KMnO4酸性溶液褪色C.醛类物质常温、常压下都为液体或固体D.醛与H2发生的加成反应也是还原反应解析:选D。
鲁科版高中化学选修五第3章章末系统总结.docx

高中化学学习材料唐玲出品章末系统总结一、重点知识梳理二、实验专项探究——有机物的分离和提纯1.分离与提纯的区别。
分离是把混合物中的各物质逐一分开,得到各种纯净物,分开后的物质应该尽量减少损失,各组分要尽量纯净。
提纯是将物质中的杂质除掉而得到纯净物质,除掉的杂质可以不进行恢复。
2.分离提纯的原则。
(1)不增:不增加新的杂质。
(2)不减:不减少被提纯的物质。
(3)易分离:被提纯物质与杂质易分离。
(4)易复原:被提纯物质转变成其他物质后,易恢复到原来的状态。
3.分离提纯的几种思路。
(1)杂转纯:如除去Na2CO3中的NaHCO3,将混合物加热使NaHCO3全部转化为Na2CO3。
(2)杂变沉:如除去NaCl溶液中的BaCl2,先加过量Na2CO3使BaCl2转化为BaCO3沉淀,过滤后再在滤液中加盐酸。
(3)杂转气:如除去NaCl溶液中的Na2CO3,加盐酸使Na2CO3转化为CO2。
(4)萃取分:如用CCl4将碘水中的碘萃取出来并分液。
4.有机物分离提纯的常用方法。
(1)物理方法。
易错提醒在分离和提纯物质时,应依据被提纯物质的性质,选择适当的物理方法和化学方法,同时还应注意以下几个方面:(1)除杂试剂需过量。
(2)过量试剂需除尽。
(3)除去多种杂质时要考虑加入试剂的顺序。
(4)选择最佳的除杂路径。
即时训练乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。
实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:物质相对分子质量密度/(g·cm-3)沸点℃水中溶解性异戊醇88 0.812 3 131 微溶乙酸60 1.049 2 118 溶乙酸异戊酯130 0.867 0 142 难溶在A中加入4.4 g异戊醇、6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片。
开始缓慢加热A,回流50 min。
反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
2019-2020学年高中化学选修五人教版:第三章章末系统总结Word版含解析

章末系统总结、重点知识梳理通式:R—0H・泡和一兀醇通式:C n H2…—10H 官能团:一OH(①中性•不电离出0H-或H +空与活泼金等)反应放出③可被氧化成醛代表物:CH3CH2OH^④分子间脱水生成乙讎•分子内脱水生成乙烯区可与竣酸酯化生成酯、⑥与HX发生取代反应生成卤代泾催化剂I ①CH —CH,-H. 0 ~<H.CH^OHCH;CH:O H的制聪°°_加热、加压」_丨②淀粉发酵制C2H=OH『官能团:一OH「①易被氧化变色/—江②与Be发生取代反应酣米代表物:< 、一OH < _朋大“、一/③遇FeCl3溶液显紫色弱酸性(不能使指示剂变邑)的制取:《—:一-一" 0H■通式:R-CHO H 饱和一元醛分子式为CHO 或C H H :…O 官能团t —CHO卄辽虽化反宣:银攪反宜.与新制CuCOH'h 悬浊液反应.能便强水用MnQ 陵性擂液褪色醛类”代a^rCH.CHO 总初或反宜:牺缶竝还原成匚H .CH 2OHC LL 或 AgCH^CHO :2CH.CH ;OH-O.—— 2CH L CHO-2H ?O通式:K —COOH.t&和一元幾酸的通式齿C^Hi.-xCOOH 或匚“比“住官能团「一 COOH①具有史的澄性(醋釀盐几乎全涪于水) 芒与酣发主昌址豆应生成幽CH :COOH 制脱:乙醇■.乙盤氧化注igjtiRCOOR'.R 和应可以栢同’也寸以不同CH :COOC :H=的制 ^:CH ;COOH-C ?H :OH^—^*€H.CQOC,H=亠比 O台迸任4礎骨架的搐律和官能团的引人、转化、诺变 有机合成£有机合成路线——連合成分析法有削合成的应用二、实验专项探究一一有机物的检验和鉴别的方法1根据溶解性:通常是向有机物中加水,观察其是否溶于水, 如鉴别羧酸与四氯化碳(或烃、酯、油脂等),醇与四氯化碳(或烃、酯、 油脂等)。
选修5 第三章 第一节 乙醇 醇类
CH2=CH-CH2OH
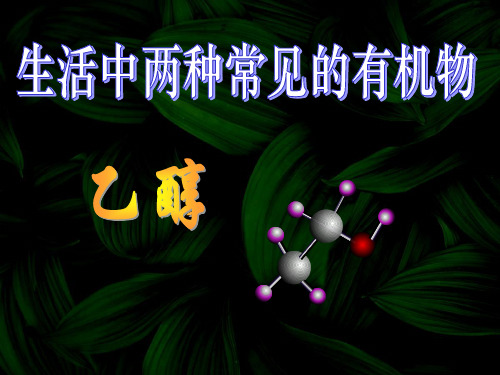
可以发生的化学反应有( C )
⑴加成 ⑵氧化 ⑶燃烧 ⑷加聚 ⑸取代
A ⑴⑵⑶ C ⑴⑵⑶⑷⑸ B ⑴⑵⑵⑷ D ⑴⑶⑷
四Байду номын сангаас 乙醇的工业制法
1. 乙烯水化法 CH2=CH2 + H2O
催化剂
加热 加压
CH3CH2OH
2. 发酵法
糖类(淀粉、纤维素)→葡萄糖→乙醇 C6H12O6
酒曲酶
30℃
2CH3CH2OH+2CO2 ↑
一、定义 分子中含有跟链烃基或苯环侧链上的 碳结合的羟基的化合物 羟基与苯环直接相连的化合物是酚 分子结构特点 含有—OH (羟基) 醇的官能团是—OH(羟基)。
⑶乙醇的催化氧化 Cu或Ag 2CH3CH2OH + O2 加热 2CH3CHO +2H2O 反应机理的探究 H H H H H C H H H C H H O H
H C C O H
O
CH3CH CH CHO 3 H C C O 与-OH相连C上有H才可以发生 醇的催化氧化, 生成C=O 书75、教辅86
一、乙醇的分子结构
化学式 结构式 H H
自主探究
结构简式
CH3CH2OH C2H6O H-C-C-O-H 或C H OH 2 5 H H 请 1. 乙醇式量 46 ,官能团 -OH 。 回 答 2. 乙醇是 极 性分子,属于 非电 解质
二、乙醇的物理性质 乙醇俗称 酒精 ,它是 无色、透明 而
具有 特殊醇香味 的液体,密度比水 小 ,
20。C时的密度是0.7893g/cm3,沸点是 78℃。乙醇 易挥发 ,能溶解多种无机 物和有机物,能跟水以 任意比互溶 。 结构相似相溶 乙醇(或氨)的水溶液的物质的量分数 越大,密度越小
高中化学选修五第三章 3.2 醛

CnH2n+2O
CnH2n O
CnH2nO2
⑴、某学生用1mol/LCuSO4溶液2mL和 0.5mol/LNaOH溶液4mL混合后加入40%的甲醛溶 液0.5mL,加热到沸腾未见红色沉淀生成。主 要原因是( ) A.甲醛的量太少 B. CuSO4的量太少
2HCHO + NaOH(浓) →
HCOONa + CH3OH 属康尼查罗反应,下列说法正确的是 (A)
A 此反应是氧化还原反应
B 甲醛只被氧化成甲酸
C 甲醛只被还原成甲醇
D 甲醛既被氧化成甲醇又被还原为甲酸
加热至沸腾。
乙醛和新制的氢氧化铜反应
CH3CHO + 2Cu(OH)2 +NaOH Cu O CH3COONa+ 2↓ +3H2O
砖红色
碱必须过量
常用的氧化剂:
银氨溶液、新制的Cu(OH)2、O2、酸 性KMnO4溶液
(3)乙醛的用途 乙醛是有机合成工业中的重要 原料,主要用来生产乙酸、丁醇、 乙酸乙酯等。如:
四、醛基的检验
1、哪些有机物中含有—CHO? 醛、HCOOH、HCOOR、
葡萄糖、麦芽糖 2、怎样检验醛基的存在?
银镜反应、新制的Cu(OH)2
【巩固练习】
常见的醛
甲醛
CHO CHO 乙二醛 丙烯醛 苯甲醛
CH2
乙醛
CH CHO CHO
科学视野
五、酮: 羰基(>C=O)与两个烃 基相连的化合物。
银镜反应
CH3CHO+ 2Ag(NH3)2OH CH3COONH4 (银氨溶液) +2Ag↓+3NH3+H2O
和新制的Cu(OH)2反应
高中化学选修五第三章第二节醛

【练习2】
某有机物加氢反响的复原产物
是:CH3CHCH2OH,原有机物是(D ) | CH3
A.乙醇的同系物 B.丙醇的同分异构体 C.丙醛的同分异构体 D.乙醛的同系物
【练习3】
判断以下哪些不能使酸性KMnO4溶液褪色?
【构造特点】甲醛中:醛基, 有2个活泼氢可被氧化 分子为平面形极性分子。
一、甲醛与酸性KMnO4溶液的反响
实验现象:酸性KMnO4溶液褪色 实验结论:甲醛具有复原性
(1) 甲醛与酸性高锰酸钾溶液反响 现象:是酸性高锰酸钾溶液退色。 HCHO KMnO4 HCOOH
二、甲醛与新制氢氧化铜的反响
实验现象:生成砖红色沉淀 实验结论:氢氧化铜是氧化剂,甲醛是复原剂
④乙醛用量不可太多; (5〕实验后,银镜用HNO3浸泡,再用水洗
〔3〕银镜反响
现象:试管内壁有光亮的银生成。
△
HCHO+2[Ag(NH3)2]OH→ HCOONH4+2Ag↓+3NH3+H2O
△
HCHO+4[Ag(NH3)2]OH→ CO2+4Ag↓+8NH3+3H2O
四、与氢气的加成反响
O
H—C—H +H2
Cu
2CH3CH2OH+O2 △
2CH3CHO+2H2O
氧化反响: 有机物分子中参加 氧原子或 失去氢原子的反响
〔2〕乙醛的氧化反响
a. 催化氧化 工业上就是利用这个反响制取乙酸。 2CH3CHO+O2 催化剂 2CH3COOH
【完全燃烧】在点燃的条件下,乙醛能在空气或 氧气中燃烧。乙醛完全燃烧的化学方程式为:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
课标版 · 化学 · 选修⑤
第4页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
2 () 掌握2个碳原子的烃及烃的衍生物的相互转化
第5页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
3 () 掌握含苯环的烃及其衍生物的相互转化
第6页
第三章
本章整合
与名师对话· 系列丛书
第三章 本章整合
第24页
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
解析:SO2使溴水褪色是溴水将SO2氧化,乙烯使高锰酸 钾褪色是高锰酸钾将乙烯氧化,原理相同,所以A正确;除 去乙酸乙酯中的乙酸用饱和碳酸钠溶液,用氢氧化钠溶液会 促进乙酸乙酯水解,B项 错 误 ; 水 与 电 石 反 应 剧 烈 , 所 以 用 饱和食盐水代替水,C项正确;硝酸银与氯化钾反应生成白 色沉淀氯化银,硝酸银与碘 化 钾 反 应 生 成 黄 色 沉 淀 碘 化 银 , D项 正 确 。
课标版 · 化学 · 选修⑤
第7页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
二、有机推断 1.有机推断题的特点 1 () 一般是要求推导有机物的结构简式,书写限定条件的 同分异构体、化学方程式、反应类型及判断物质的性质等。 2 () 提供的条件一般有两类:一类是有机物的性质及相互 关系,一类是定量关系或相关数据。 3 () 提供一些新信息,让同学们现场学习再迁移应用,即 所谓的信息迁移题。
2 () ③的反应类型为___ _ _ _ _
3 () 化合物A可由环戊烷经三步反应合成:
反应1的试剂与条件为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ ;反应3可用的试剂为_ _ _ _ _ _ _ _
;反应2的化学方程式为 。
第29页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
第1页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
第2页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
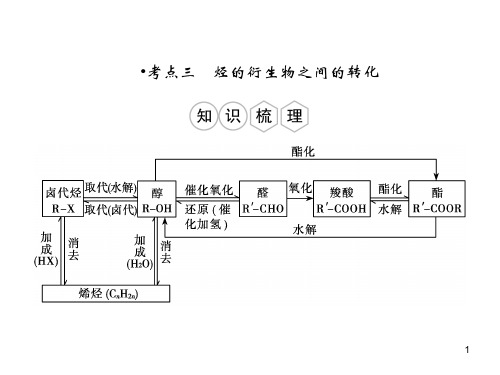
2.重要的有机物之间的相互转化关系 1 ( ) 烃的衍生物的相互转化关系
第3页
第三章
本章整合
与名师对话· 系列丛书
。
第三章 本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
【解析】 本题依托有机化合物的推断,考查官能团的 重要性质、化学方程式的书写、同分异构体等知识,属中档 题。1 ( ) 分子中含有—Br、—C O O H 应、—C O O H 官 能 团 , —Br发生水解反
发生中和反应。2 ( ) 联系①②两个反应知反应⑤ ;
第17页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
第18页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
3 ( C )H H O C H
H O (H C )H 3C )H O 3C
H O 2C
、CH3CH2C H O (H C )H O
、
H C (H 2C
能及高稳定性等特点,因此合成立方烷及其衍生物成为化学 界关注的热点。下面是立方烷衍生物Ⅰ的一种合成路线:
第28页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
回答下列问题: 1 ( C ) 的结构简式为_ _ _ _ _ _ _ _ ,E的结构简式为_ _ _ _ _ _ ,⑤的反应类型为_ _ _ _ _ __。 __。
5 () 乙醇、乙酸均能与Na反应放出H2,二者分子中官能团 相同(
第20页
)
第三章 本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
6 ( ) 乙酸与丙二酸互为同系物( 7 ( )
) 互为同系物( ) )
8 ( ) 乙酸和乙酸乙酯可用Na2CO3溶液加以区别( 9 ( ) 乙醇可由乙烯通过加成反应制取( )
课标版 · 化学 · 选修⑤
2.下列叙述错误的是(
)
4溶液褪色的原理相
A.SO2使溴水褪色与乙烯使K M n O 同 B.制备乙酸乙酯时可用热的N a O H 其中的乙酸
溶液收集产物以除去
C.用饱和食盐水替代水跟电石反应,可以减缓乙炔的 产生速率 D.用A g N O C l 3溶液可以鉴别K 和KI
第9页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
3.有机推断题的解题突破口 有机化学中一些重要物质的组成结构特点、状态、颜 色、燃烧规律、典型反应的数量变化关系、特殊现象等,往 往是推断题的突破口。 1 () 从有机物的物理特性突破。有机物中各类代表物的颜 色、状态、气味、溶解性、密度、熔点、沸点等往往各有特 点,平时学会归纳,解题时才能由此找到突破口。
第8页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
2.有机推断题的解题思路 解答有机推断题,首 先 必 须 全 面 掌 握 有 机 物 的 性 质 及 其 相互转化关系,审清题意,准确获取信息;然后抓住问题突 破口,再从突破口上发散,通过顺推法、逆推法、假设法、 知识迁移法等得出结论;最后进行全面的检查,验证结论是 否符合题意。
第19页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
1.判断正误,正确的画“√”, 错 误 的 画 1 () 医用酒精的浓度通常为9 5 % ( )
“×”。
2 ()
3 () 乙醇与乙醛互为同分异构体( 4 () 用食醋可除去热水壶内壁的水垢(
4 ( ) 在Ⅰ的合成路线中,互为同分异构体的化合物是 _ _ _ _ _ _ _ _ ( 填化合物代号)。 5 ( ) Ⅰ与碱石灰共热可转化为立方烷。立方烷的核磁共振 氢谱中有_ _ _ _ _ _ _ _ 个峰。
6 ( ) 立方烷经硝化可得到六硝基立方烷,其可能的结构有 _ _ _ _ _ _ _ _ 种。
___ _ _ _ _ _ _ _
。
的 同 分 异 构 体 有 多 种 。 写 出 其 中 既 能 发 生 银 镜 反 应 ,
又 能 发 生 酯 化 反 应 且 结 构 中 只 有 一 个 甲 基 的 所 有 可 能 的 物 质 的 结 构 简 式
第16页
_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _
回 答 下 列 问 题 :
1 () 为_ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ 2 ( D ) 3 ( B ) 与 足 量 乙 醇 反 应 生 成
与 足 量 N a O H 。
溶 液 反 应 的 化 学 方 程 式
E的 化 学 方 程 式 为
第10页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
2 ( ) 有机反应往往各有特定的条件,因此反应的特定条件 也可能是突破口。例如“浓硫酸,1 7 0 ℃”的条件可能是乙醇 发生消去反应制取乙稀;“烃 与 溴 水 反 应 饱和烃。 ”,则该烃应为不
第11页
第三章
本章整合
与名师对话· 系列丛书
第12页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
第13页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
5 () 从特征现象突破。例如,与F e C 3 l
溶液发生显色反
应,该有机物中有酚羟基;能与银氨溶液反应生成银镜,则 该有机物为含醛基的化合物。特征现象可以从产生气体、沉 淀颜色、溶液颜色的变化等方面考虑。 6 () 从特定的量变突破。例如,相对分子质量增加了16, 可能是加入了氧原子(如C H 3 C H O ―→C H 3 C O O H ) 。平日复
课标版 · 化学 · 选修⑤
3 () 从特定的转化关系突破。例如,某有机物能被连续氧 氧化 氧化 化,该有机物是烯烃或醇。因为烯烃――→醛――→羧酸;醇 氧化 氧化 ――→醛――→羧酸。这是两个重要的氧化系列。若某有机物 还原 氧化 既能被氧化又能被还原:B ――→ A ――→ C,则该物质A可能 是醛,醛是既能被氧化(转化成羧酸)又能被还原(转化成醇)的 物质。可见,熟悉有机物间的转化关系非常重要。
, 所 以 反 应
⑤
第32页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
3 () 解 决 本 小 题 可 采 用 逆 合 成 分 析 法 , ―→ ―→
―→
,故反应1的试剂是Cl2, 条 件 是 光 照 ; 反 +N a O H 。 H2O ――→ △ +N a C l ;反
应2的化学方程式是 应3可用的试剂是O2C /u
答案:B
第25页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
第26页
第三章
本章整合
与名师对话· 系列丛书
课标版 · 化学 · 选修⑤
解析:苹果酸中有羟基和羧基,都能发生酯化反应,A 正确;分子中含有两个—C O O H 1 , m o l N a O H 苹 果 酸 能 与 2 m o l
第三章 本章整合
