试验四溴丁烷的制备4学时
4-6正溴丁烷的制

四、实验装置
回流装置
气体吸收装置
蒸馏装置
分液装置
五、实验步骤
1、投料
25g溴化钠 25g溴化钠 19ml正丁醇 19ml正丁醇
在圆底烧瓶中加入20ml水 在圆底烧瓶中加入20ml水,再慢 20ml 慢加入30ml浓硫酸, 30ml浓硫酸 慢加入30ml浓硫酸,混合均匀并冷 至室温后,再依次加入19ml 19ml正丁醇 至室温后,再依次加入19ml正丁醇 25g溴化钠 溴化钠, 和25g溴化钠,充分振荡后加入几 沸石。( 。(硫酸在反应中与溴化钠 粒沸石。(硫酸在反应中与溴化钠 作用生成溴化氢, 作用生成溴化氢,溴化氢与正丁醇 作用发生取代反应生成正溴丁烷。 作用发生取代反应生成正溴丁烷。 硫酸用量和浓度过大, 硫酸用量和浓度过大,会加大副反 应进行;若硫酸用量和浓度过小, 应进行;若硫酸用量和浓度过小, 不利于主反应的发生, 不利于主反应的发生,即氢溴酸和 正溴丁烷的生成) 正溴丁烷的生成)
4.分液漏斗的处理:用完后须立即洗净,烘干或沥干, 4.分液漏斗的处理:用完后须立即洗净,烘干或沥干,再在塞 分液漏斗的处理 子和口子之间垫一小纸片,以免粘结。 子和口子之间垫一小纸片,以免粘结。
6、收集产物
将干燥好的产物移 至小蒸馏瓶中, 至小蒸馏瓶中,在 石棉网上加热蒸馏, 石棉网上加热蒸馏, 收集96 103℃ 收集96—103℃的馏 96 103℃的馏 分。
30ml浓 30ml浓H2SO4 20ml水 20ml水
2、加热回流
以电热套为热源, 以电热套为热源,安装回流装 含气体吸收部分)。( )。(注 置(含气体吸收部分)。(注 意圆底烧瓶底部与电热套间的 距离和防止碱液被倒吸) 距离和防止碱液被倒吸) 调整圆底烧瓶底部与电热套的 距离, 距离,以保持沸腾而又平稳回 流,并不时摇动烧瓶促使反应 完成。反应约30 40min。 完成。反应约30—40min。 30 40min (注意调整距离和摇动烧瓶的 操作) 操作)
1-溴丁烷的合成实验报告

1-溴丁烷的合成实验报告实验一1-溴丁烷的制备计划学时:5学时一、实验目的:1、学习以溴化钠、浓硫酸和正丁醇制备正溴丁烷的原理与方法;2、练习带有吸收有害气体装置的回流加热操作。
二、实验原理:本实验中正溴丁烷是由正丁醇与溴化钠、浓硫酸共热而制得:【反应式】主反应:NaBr + H2SO4n-C4H9OH + HBr可能的副反应:HBr + NaHSO4n-C4H9Br + H2OCH3CH2CH2CH2OH2CH3CH2CH2CH2OH2HBr + H2SO4CH2CH2CH=CH2 + H2O(CH3CH2CH2CH2)2O + H2O 2 + SO2 + 2H2O三、主要原料、产品和副产物的物理常数【试剂】7.5ml(0.08mol)正丁醇,10g(0.10mol)溴化钠,浓硫酸,饱和碳酸氢钠溶液,无水氯化钙四、实验装置:图1五、实验步骤:1、投料在圆底烧瓶中加入10ml水,再慢慢加入12ml浓硫酸,混合均匀并冷至室温后,再依次加入7.5ml正丁醇和10g溴化钠,充分振荡后加入几粒沸石。
(硫酸在反应中与溴化钠作用生成氢溴酸,氢溴酸与正丁醇作用发生取代反应生成正溴丁烷。
硫酸用量和浓度过大,会加大副反应进行;若硫酸用量和浓度过小,不利于主反应的发生,即氢溴酸和正溴丁烷的生成)2、以电热套为热源,按图1安装回流装置(含气体吸收部分)。
(注意防止碱液被倒吸)3、加热回流在石棉网上加热至沸,调整加热速度,以保持沸腾而又平稳回流,并不时摇动烧瓶促使反应完成。
反应约30—40min。
4、分离粗产物待反应液冷却后,改回流装置为蒸馏装置(用直形冷凝管冷凝),蒸出粗产物。
(注意判断粗产物是否蒸完)。
见【注释】(2)5、洗涤粗产物将馏出液移至分液漏斗中,加入10ml的水洗涤(产物在下层),静置分层后,将产物转入另一干燥的分液漏斗中,用5ml的浓硫酸洗涤(除去粗产物中的少量未反应的正丁醇及副产物正丁醚、1—丁烯、2—丁烯。
有机化学实验报告--1-溴丁烷的制备
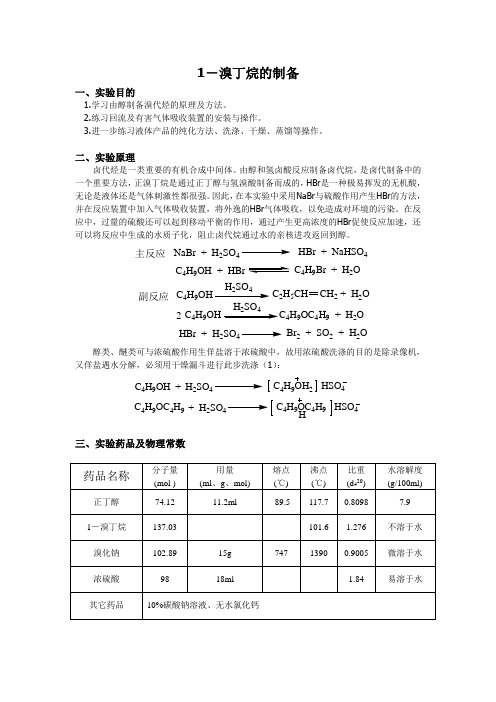
1-溴丁烷的制备一、实验目的1.学习由醇制备溴代烃的原理及方法。
2.练习回流及有害气体吸收装置的安装与操作。
3.进一步练习液体产品的纯化方法、洗涤、干燥、蒸馏等操作。
二、实验原理卤代烃是一类重要的有机合成中间体。
由醇和氢卤酸反应制备卤代烷,是卤代制备中的一个重要方法,正溴丁烷是通过正丁醇与氢溴酸制备而成的,HBr 是一种极易挥发的无机酸,无论是液体还是气体刺激性都很强。
因此,在本实验中采用NaBr 与硫酸作用产生HBr 的方法,并在反应装置中加入气体吸收装置,将外逸的HBr 气体吸收,以免造成对环境的污染。
在反应中,过量的硫酸还可以起到移动平衡的作用,通过产生更高浓度的HBr 促使反应加速,还可以将反应中生成的水质子化,阻止卤代烷通过水的亲核进攻返回到醇。
NaBr + H 2SO 4HBr + NaHSO 4C 4H 9OH + HBrC 4H 9Br + H 2O 主反应副反应C 4H 9OHC 2H 5CHCH 2+ H 2OC 4H 9OH+ H 2O 24H 9OC 4H 9HBr + H 2SO Br 2 + SO 2 + H 2O 2424醇类、醚类可与浓硫酸作用生佯盐溶于浓硫酸中,故用浓硫酸洗涤的目的是除录像机,又佯盐遇水分解,必须用干燥漏斗进行此步洗涤(1):+ H 2SO 4C 4H 9OH +C 4H 9OC 4H 9H 2SO 4C 4H 9OH 2HSO 4C 4H 9OC 4H 9H HSO 4三、实验药品及物理常数四、实验装置图回流冷凝装置蒸馏装置五、实验步骤(1)在100ml圆底烧瓶中加入15ml水,然后加入18ml浓硫酸(分3-4次加),摇匀后,冷却至室温,再加入11.2ml正丁醇,混合后加入15g溴化钠(小心加入,节不可在磨口处留有固体),充分振荡,加入几粒沸石,在烧瓶上装上球形冷凝管回流(因为球型冷凝管冷凝面积大,各处截面积不同,冷凝物易回流下来),在冷凝管的上口用软管连接一个漏斗,置于盛水的烧杯中。
有机化学实验 1溴丁烷制备实验报告模板

实验六1-溴丁烷的制备1、实验目的(1)学习由醇制备溴代烃的原理及方法;(2)练习回流及有害气体吸收装置的安装与操作。
2、实验原理卤代烃是一类重要的有机合成中间体。
由醇和氢卤酸反应制备卤代烷,是卤代制备中的一个重要方法,正溴丁烷是通过正丁醇与氢溴酸制备而成的,HBr 是一种极易挥发的无机酸,无论是液体还是气体刺激性都很强。
因此,在本实验中采用NaBr与硫酸作用产生HBr的方法,并在反应装置中加入气体吸收装置,将外逸的HBr气体吸收,以免造成对环境的污染。
在反应中,过量的硫酸还可以起到移动平衡的作用,通过产生更高浓度的HBr促使反应加速,还可以将反应中生成的水质子化,阻止卤代烷通过水的亲核进攻返回到醇。
3、仪器:球形冷凝管、直形冷凝管、圆底烧瓶、分液漏斗、加热套、烧杯、玻璃漏斗。
4、试剂:溴化钠、正丁醇、浓硫酸。
5、装置图6、操作步骤及注意事项(1)回流反应。
在50 mL圆底烧瓶中加入8.3 g研细的溴化钠【加溴化钠时不要粘到烧瓶磨口,可先加固体再加液体,或者把称量纸卷一下】、6.2 mL正丁醇、沸石,烧瓶上装球型冷凝管。
小锥形瓶加10 mL水,冷水浴中【用一个大烧杯里加水,小锥形瓶放里冷却】边摇边慢慢滴加10 mL浓硫酸。
将稀释的硫酸分4次从冷凝管上端加入烧瓶,边加边摇。
加完后,冷凝管上端用胶皮管连接尾气吸收装置【吸收液5%碳酸钠溶液,自己用自来水配】。
加热回流30 min【第一滴回流液滴下开始计时】。
(2)第一次蒸馏。
反应完成后,冷却,烧瓶不动,补加沸石,组装不带温度计的蒸馏装置蒸馏【控制好温度,如果爆沸喷出,倒回重蒸】,直到无油滴蒸出为止【馏出液表面有水相出现】。
蒸馏结束后把圆底烧瓶洗干净放烘箱,第二次蒸馏烧瓶需要干燥。
(3)分液洗涤。
将上一步馏出液倒入分液漏斗中,将油层【体积A】从下面放入干燥的锥形瓶中,用3 mL浓硫酸分2次加入瓶内。
将混合物倒入分液漏斗,放出下层浓硫酸。
油层依次用10 mL水、5 mL 10% 碳酸钠溶液、10 mL水洗涤。
1-溴丁烷的制备实验流程

1-溴丁烷的制备实验流程下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!1-溴丁烷的制备实验流程1. 实验目的2. 实验原理3. 实验步骤3.1 原料准备3.2 制备1-溴丁烷4. 实验注意事项5. 实验结果及分析6. 实验结论1. 实验目的本实验旨在通过一系列化学反应制备1-溴丁烷,并通过一些物理和化学性质的测试来确定其纯度。
溴丁烷的制备

溴丁烷的制备-溴丁烷的制备————————————————————————————————作者:————————————————————————————————⽇期:1-溴丁烷的制备⼀、实验⽬的1. 学习⽤溴化钠,浓硫酸和正丁醇制备1-溴丁烷的原理和⽅法2.练习带有吸收有害⽓体装置的回流加热操作。
3.进⼀步掌握分液漏⽃的使⽤和熟悉液体产品的纯化⽅法 --------洗涤、⼲燥、蒸馏等操作。
⼆、实验原理1、卤代烃是⼀类重要的有机合成中间体。
由醇和氢卤酸反应制备卤代烷,是卤代制备中的⼀个重要⽅法。
正溴丁烷是通过正丁醇与氢溴酸制备⽽成的。
主反应:NaBr + H2SO4HBr + NaHSO4??→49492n-C H OH + HBrn-C H Br+ H O可能的副反应:492C H OH C2H5CH=CH2+ H O →24浓H SO 49494922C H OH C H OC H + H O →24浓H SO242222HBr +H SO Br + SO + H O ??→本反应是可逆反应。
HB r是⼀种极易挥发的⽆机酸,⽆论是液体还是⽓体刺激性都很强。
因此,实验中采⽤NaBr 与硫酸作⽤产⽣HBr 的⽅法,使H Br 边⽣成边参与反应,这样可提⾼H Br 的利⽤率。
但是由于HBr 有毒害且HB r⽓体难以冷凝,所以在反应装置中加⼊⽓体吸收装置,将外逸的HBr ⽓体吸收,以免造成对环境的污染。
在反应中,过量的硫酸起到移动平衡的作⽤的同时还起到催化脱⽔作⽤,并通过产⽣更⾼浓度的HBr促使反应加速,还可以将反应中⽣成的⽔质⼦化,阻⽌卤代烷通过⽔的亲核进攻返回到醇。
为防⽌反应物正丁醇及产物1-溴丁烷逸出反应体系,反应采⽤了回流装置(此反应较慢,需要在较⾼的温度下、长时间反应,⽽玻璃反应装置可达到的最⾼反应温度是回流温度,所以采⽤回流反应装置)。
回流后再进⾏粗蒸馏,⼀⽅⾯使⽣成的产品1-溴丁烷分离出来,便于后⾯的分离提纯操作;另⼀⽅⾯,粗蒸过程可进⼀步使醇与HBr 的反应趋于完全。
-溴丁烷的制备

1 -溴丁烷的制备一.实验目的 (略)二.反应式三.实验试剂 (略)正丁醇 M =74.12 b.p.=117.25℃正丁醚 M =130 b.p.=142.4℃1-溴丁烷 M =136.02 b.p.=101.6℃四.实验步骤1、配制62%硫酸,水浴冷却至室温;安装反应装置,加料,硫酸分批缓加,充分冷却。
2、回流反应,控制好反应温度,注意尾气吸收;微沸30min ,冷却5min3、蒸馏(补加沸石) 下层有机层6ml 浓H SO洗涤一次 上层有机层 注: 若显棕红色,少量NaHSO 3/H 2O 洗涤(除H 2SO 4 ,HBr)20ml 水洗涤一次下层有机层无水CaCl 2干燥蒸馏,收集99-102℃馏分产品(称重上交) 分液时加水促进分层,并降低水相密度,保证1-溴丁烷比重大于水相而在下层五.实验注意事项 1.配硫酸正确操作 2.注意加料顺序;加硫酸,分批缓慢加入,并充分振荡3.控制反应温度,不能太高,溴易被硫酸氧化;微沸,尾气吸收。
4.改为蒸馏装置时,要充分冷却,再加1~2粒沸石,防止暴沸;n-C 4H 9OH HBr +主反应:副反应: CH 3CH 2CH 2CH 2OH C 4H 8 H 2O 24+NaBr H 2SO 4HBr NaHSO 4++ n-C 4H 9Br H 2O+2 CH 3CH 2CH 2CH 2OH( CH 3CH 2CH 2CH 2 )2 O H 2O +H 2SO 4 , 135 ℃+HBr H 2SO 4Br 2 SO 2 H2O ++正确判断蒸馏终点5.在后处理洗涤过程中,要清楚有机层和水层及各步洗涤的目的浓硫酸洗涤除正丁醇时,硫酸分批加入,充分振荡,冷却后再加6.用无水CaCl2干燥时,所用锥形瓶要干燥无水讲解部分:1.实验反应的关键是控制反应温度(强调火焰的调节,反应瓶底离石棉网0.5-1cm的距离,避免温度太高)2.配料时,先加NaBr,正丁醇;从冷凝管上口加入已充分稀释、冷却的硫酸,每加一次都要充分振荡,混合均匀,同时用冷水浴冷却。
溴丁烷的制备操作规程及流程
【实验目的】1、掌握以溴化钠、浓硫酸和正丁醇制备1-溴丁烷的原理和方法。
2、掌握带有吸收有害气体装置的回流等基本操作。
【实验原理】卤代烷制备的一个重要方法是由醇与氢卤酸发生亲核取代反应来制备。
在实验室制备正溴丁烷是用正丁醇与氢溴酸反应得到。
氢溴酸是一种极易挥发的无机酸,因此在制备时采取用溴化钠与硫酸作用产生氢溴酸直接参与反应。
在反应中,过量的硫酸可以起到移动平衡的作用,通过产生更高浓度的氢溴酸促使反应加速,还可以将反应中生成的水质子化,阻止卤代烷通过水的亲核进攻而返回到醇。
但硫酸的存在易使醇生成烯和醚等副产品,因而要控制硫酸的用量。
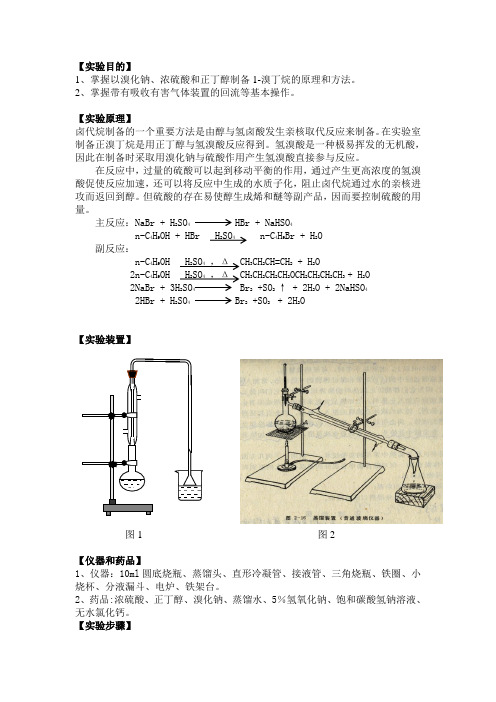
主反应:NaBr + H2SO4HBr + NaHSO4n-C4H9OH + HBr H2SO4n-C4H9Br + H2O副反应:n-C4H9OH H2SO4,Δ CH3CH2CH=CH2+ H2O2n-C4H9OH H2SO4,Δ CH3CH2CH2CH2OCH2CH2CH2CH3+ H2O2NaBr + 3H2SO4Br2+SO2↑ + 2H2O + 2NaHSO42HBr + H2SO4Br2+SO2+ 2H2O【实验装置】图1 图2【仪器和药品】1、仪器:10ml圆底烧瓶、蒸馏头、直形冷凝管、接液管、三角烧瓶、铁圈、小烧杯、分液漏斗、电炉、铁架台。
2、药品:浓硫酸、正丁醇、溴化钠、蒸馏水、5%氢氧化钠、饱和碳酸氢钠溶液、无水氯化钙。
【实验步骤】2mL水、2.8mL浓硫酸装入10ml圆底烧瓶中,装置如图1。
回流30min。
1.84mL正丁醇稍冷,改为蒸馏装置如图2。
2.6g溴化钠磁子粗产品分液漏斗分上层:无色(水)3-5ml水层下层:乳白色(产品)粗产品分液漏斗分上层:淡棕黄色(产品)2-3ml浓硫酸层下层:无色(硫酸层)粗产品分液漏斗分上层:无色(水)3-5ml水层下层:乳白色(产品)粗产品分液漏斗分上层:无色(水)3-5ml饱和碳酸氢钠层下层:乳白色(产品)粗产品倒入三角瓶,加无水氯化钙产品。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验四
1-溴丁烷的制备(4学时)
主讲教师:王婷婷
有机化学实验
Chem is try !
有机化学实验
Chem is try !
一、实 验 目 的:
学习从醇制备卤代烃的原理与方法;
练习带有有害气体吸收装置的回流加热操作; 掌握蒸馏、萃取、洗涤、液体干燥等基本操作。
有机化学实验
Chem is try !
(1)吸收反应中生成的H2O使HBr保持较高浓度,做吸水剂; (2)提供质子,使醇质子化,作催化剂; (3)使生成的水质子化,减少逆反应的发生。
副反应:
三、相关物质的物理常数:
水中 溶 解 度 (g/100mL) 915 0.0616
名 称
分子量
性 状
密度
熔点(℃) 沸点(℃) 折光率
正丁醇 1-溴丁烷
2013-9-17
有机化学实验
Chem is try !
4、洗涤粗产物
将馏出液移至分液漏斗中,加入5ml水洗涤,静置分层 后,将产物转入分液漏斗中,用3ml浓硫酸洗涤,分去硫 酸层。有机相依次用10ml水、5ml 10%Na2CO3溶液和 10ml水洗涤后,转入干燥的锥形瓶中。
振摇后要及时放气!
2013-9-17
C4H9Br、C4H9OH、 馏出液 (C H ) O、H O、HBr 4 9 2 2 残留液
稍冷、改为蒸馏装置
补加2~3粒沸石
加热回流30min
加5mL水 洗涤 上层
弃去
弃去
H2O 、 HBr、 C4H9OH
下层 C4H9Br、C4H9OH、(C4H9)2O 加10mL水 洗涤
+
上层 C4H9Br、(少)H2SO4
有机化学实验
Chem is try !
5、产物的干燥
在上述装有产物的锥形瓶中加入1-2g的无水CaCl2 干燥,间歇摇动锥形瓶,直到液体清亮为止。
将待干燥的液体倒 入干燥的锥形瓶
CaCl2 + H2 O
加入大小适中块 状的无水CaCl2
少量多次加入
盖好玻璃塞 放置一段时间
间歇摇动
CaCl2 . 6 H2O
受热放出水
干燥后,应除去干燥剂,再蒸馏
有机化学实验
Chem is try !
干燥剂的选择 1)与被干燥有机物不发生化学反应或催化作用;
如酸性物质不能用碱性干燥剂,强碱性干燥剂氢氧化钠能 催化某些醛类或酮类发生缩合,氯化钙易与醇、酯、胺类形成 络合物。 2)不能溶解于该有机物中; 3)吸水量大、干燥速度快、价格低廉; 干燥剂的用量——观察法 观察被干燥的液体:溶液变为澄清透明。
+
加3mL浓H2SO4 2次洗涤 加5mL10%Na2CO3 洗涤 倒入废液桶内
下层 H2SO4 、 C4H9OH2、C4H9-O-C4H9 H 无水CaCl2 蒸馏 加10mL水 洗涤 干燥
收集99~102℃馏分
有机化学实验
Chem is try !
具体操作步骤:
1、投料
(1) 先配制稀硫酸:在烧杯中加入 10ml水,再缓慢加入10ml浓硫酸,混 合均匀,并冷至室温后备用。 (2)在100mL圆底烧瓶中依次加入 8.3g溴化钠和6.2ml正丁醇,充分振荡 后加入2-3粒沸石。 (3)安装回流冷凝管,从上方分4-5次 加入稀硫酸。
观察干燥剂在液体中的外观:加入干燥剂后,变黏,粘在壁上,
摇动不易旋转,表明干燥剂用量不够,应补加。直到新的干燥剂 不结块,不粘壁。干燥剂棱角分明,摇动时旋转,表明所加干燥 剂用量合适。
有机化学实验
Chem is try !
6、蒸馏收集产物
用塞有棉花的小漏斗滤掉干
燥剂后,移至小蒸馏瓶中,加热 蒸馏,收集99-102℃的馏分(注 意勿使氯化钙掉入蒸馏烧瓶中)。 产品回收!
有机化学实验
Chem is try !
四、实 验 装 置 图:
回流装置
气体吸收装置
蒸馏装置
分液装置
五、实 验 流 程:
100mL圆底烧瓶
8.3g 无水NaBr,6.2mL n-C4H9OH 2~3粒沸石 安装气体吸收装置 安装回流冷凝管
分4次从冷凝管上端加入
(10mL水 + 10mL浓H2SO4 )
二、实 验 原 理:
• 将结构对应的醇通过亲核取代反应转变为卤代物,常用的 试剂有氢卤酸、三卤化磷和氯化亚砜。 • 醇与氢卤酸的反应是制备卤代烷最方便的方法。根据醇的 结构不同,反应存在着两种不同的机理,叔醇按SN1机理, 伯醇则主要按SN2机理进行。
1-溴丁烷的制备:
主反应:
问题: 浓硫酸的作用是什么?
(注意:投料时不要让固体沾到磨口以及 液面以上的烧瓶壁上。
投料后,一定要混合均匀)。
2013-9-17
有机化学实验
Chem is try !
2、加热回流
在冷凝管上端接一吸收溴化氢气 体的装置,用5%的氢氧化钠做吸收 剂。(注意倒扣的漏斗口与碱液间 的距离,防止碱液被倒吸)。 电热套小火加热到沸腾,回流 30min。并不时摇动烧瓶促使反应完 成。(注意摇动烧瓶的操作,并控 制回流速度)
• 问题:
5%NaOH水 溶 液
• 如果产生的是碱性气体(如:氨气),用什么物质做吸收液?
2013-9-17
有机化学实验
Chem i装置(用75度 弯管和直形冷凝管冷凝),再补加2粒沸石,蒸出粗产物。 判断产物是否蒸完,可依据以下几点: (a) 反应瓶内上层油层消失; (b)蒸出液是否由混浊变为澄清; (c)用内盛水的烧杯收集馏液, 观察有无油珠物质的存在。
产率计算 因其它试剂过量,理论产量按正丁醇计算。
2013-9-17
有机化学实验
Chem is try !
操作重点及注意事项
投料顺序应严格按教材上进行,浓硫酸要分批加入,混合均匀。 正确安装和使用气体吸收装置。
蒸馏前必须加止暴剂(沸石)。
蒸馏1-溴丁烷粗产物时,注意判断蒸馏终点。 洗涤粗产物时,注意正确判断哪一层是有机层。 洗后产物呈红色,可用少量的饱和亚硫酸氢钠水溶液洗涤, 以除去由于浓硫酸的氧化作用生成的游离溴。 干燥剂不可在空气中暴露太久,否则会吸水。干燥剂用量应 合理。 精制蒸馏时一整套仪器均需干燥。
74.12 137.03
液 体 液 体 无色油 状液体
0.810 1.275
-89.8 -112.4
117.4 101.6 340 (分解)
1.3971 1.4390
浓硫酸 正丁醚
98.08 130.22
1.84 0.773
10.35 -97.9
- 1.3992
∞ <0.05
液 体
142.4
数据来源:Combined Chemical Dictionary
