浓差极化
反渗透膜 浓差极化

反渗透膜浓差极化
反渗透膜是一种特殊的薄膜,它具有高度选择性的分离功能,可以有效地过滤掉溶液中的溶质和杂质分子。
当水或其他溶液通过反渗透膜时,溶剂分子可以自由通过膜孔,而较大的溶质分子(如盐离子、有机物等)则被阻隔在膜表面。
通过调节反渗透膜的孔径和膜材料的选择,可以实现对不同大小和种类的溶质的有效分离。
浓差极化是指在渗透过程中,溶剂(通常为水)在膜表面聚集形成浓度较高的层,从而形成溶液浓度的梯度。
当溶剂通过膜时,浓度较高的层会阻碍后续溶剂的渗透,导致渗透速率降低。
这种现象称为浓差极化。
浓差极化会导致反渗透膜系统的效率下降和通量降低。
为了减轻浓差极化的影响,可以采取以下措施:
1. 水流的搅动:通过搅拌或强制对溶液进行剧烈搅动,可以有效地减轻浓差极化现象。
2. 渗透液的交替使用:可以交替使用不同的渗透液,在一定程度上减缓浓差极化的发生。
3. 渗透膜的清洗和维护:定期清洗和维护反渗透膜,以去除膜表面的污染物和沉积物,有助于减轻浓差极化的影响。
电池极化分析及工艺改进

电池极化分析及工艺改进电池极化是指电池在使用过程中,电极表面形成的物理、化学过程导致电能转化效率下降的现象。
电池极化主要分为浓差极化、活性极化和阻抗极化。
为了提高电池的性能,需要进行工艺改进,减少极化现象的发生。
首先,浓差极化是由于溶液的浓度差异导致的。
在电池工作过程中,溶液中的活性物质被电极表面吸附,形成物质浓度的不均匀分布,导致电位下降。
要减少浓差极化,可以改进电解质中的浓度分布。
一种方法是通过循环使用溶液,使其均匀分布,减少浓度差异。
另一种方法是通过改变电解质的浓度,控制物质的扩散速率,减少浓差极化。
其次,活性极化是由于电极表面的活性物质与电解质之间存在的电化学反应导致的。
电池工作过程中,活性物质不断与电解质接触,发生氧化还原反应,形成物质的氧化物或还原物。
在电池的极化过程中,活性物质的生成速率与扩散速率之间存在差异,导致电位下降。
要减少活性极化,可以改进电极表面的活性物质分布。
一种方法是通过改变电极材料的结构或成分,提高活性物质的扩散速率。
另一种方法是控制电极表面的形貌,增加活性物质的触点数,提高反应速率。
最后,阻抗极化是由于电池内部的电阻导致的。
电池工作过程中,电解质中的离子在导电材料中传输时会遇到阻力,导致电压降低。
要减少阻抗极化,可以改进电池内部的电阻分布。
一种方法是通过调整电池的几何形状,减小电极间的距离,减少电阻。
另一种方法是优化电池的导电材料,提高离子的传输速率,减少电阻。
总的来说,要改进电池的性能,减少极化现象的发生,可以从浓差极化、活性极化和阻抗极化三个方面进行工艺优化。
通过调整溶液浓度分布、改进电极表面的活性物质分布,以及优化电池内部的电阻分布,可以提高电池的电能转化效率。
此外,合理设计电池结构,选择合适的电解质和电极材料也是重要的工艺改进措施。
通过不断的研究和改进,电池的性能将得到进一步提升,为各个领域的应用提供更可靠的电源。
第四章液相传质过程与浓差极化

4.1.1 极化的原因
此时,由于电极表面的电化学过程为快 步骤,仍可认为其处于平衡状态。所以,依 旧可以用能斯特方程来解释浓差极化产生的 本质。
“浓差过电位η浓差”是电极浓差极化程度
的度量。
4.1.1 极化的原因
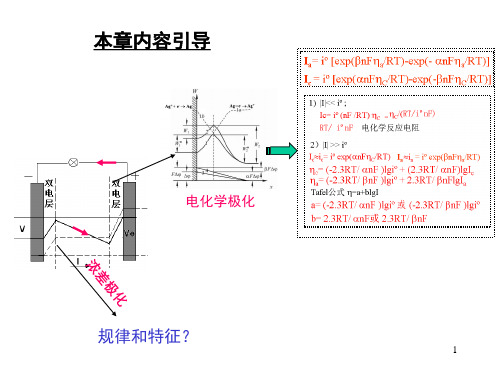
(2)活化极化(电化学极化)
在有限电流通过电极时,由于电化学反应进行的迟缓
而造成电极上带电程度与可逆状态下不同,从而导致电极 电位偏离平衡电位的现象,叫做“活化极化”。
经典恒电流法原理
采用直流电源V、限流电阻R、直流电流表A与电解池串联, 构成测量回路,r为电解池内阻。
I V V Rr R
(R>>r)
经典恒电流方法原理图
4.1.2 极化曲线的测量
c) 恒电流法与恒电位法的区别 当极化曲线上,电流与电位为一一对应关系时,两种方
法没有区别,采用两种方法测得的极化曲线是相同的。 当一个电流值下对应有多个电位时,就不能采用恒电流
ci:为i离子的浓度,单位(mol·m-3); Jc,i:粒子i在单位时间、垂直于运动方向的单
位截面积上流过的量,单位(mol·m-2·s-1)
4.2.1 液相传质的三种方式
(2) 电迁移
在电场力的作用下,引起的带电粒子迁移。电迁移作用引起的传 质速度为Je,i。
“+” 表示阳离子 “-” 表示阴离子 Je,i:i离子的电迁移量(mol·cm-2·s-1); ci: i离子的浓度(mol·cm-3); i: i离子的电迁移速度(cm·s-1); ui: i离子的淌度(cm2·s-1·V-1),单位电场强度下离子运动速度; E: 电场强度(V·cm-1);
(3)传质发生的区域 电极表面附近
的液层可以分 为双电层区、 扩散层区、对 流区。
浓差极化

浓差极化:1.在膜分离过程中,料液中的溶剂在压力驱动下透过膜,溶质被截留,于是在膜与本体溶液界面区域浓度越来越高;2.在浓度梯度作用下,溶质由膜面向本体液液扩散,形成边界层,使流体阻力与局部渗透压增加,从而导致溶剂通量下降;3.当溶剂向膜面流动时,引起溶质向膜面流动速度与浓度梯度使溶质向本体溶液扩散速度达到平衡时,在膜面附近存在着一个稳定的浓度梯度区域、浓度极化边界层浓度极化不可干预、可逆转,膜污染不可逆膜污染:在膜过滤过程中,由于浓度差极化、大颗粒溶质的吸附和吸附层的聚合三种情况下,所导致的膜的通透流量与分离特性发生不可逆现象膜污染特点:膜通透量减少,透过膜的压力和膜两侧压力差减小,分离物的截留率减小浓差极化:是指在超滤过程中,由于水透过膜,因而在膜表面的溶质浓度增高形成梯度,在梯度作用下,溶质与水以相反方向扩散,在达到平衡状态时,膜表面形成一溶质浓度分布的边界层,它对水的透过起阻碍作用浓度极化的危害:1.使膜表面溶质浓度增大,渗透压增加,减小传质驱动力;当膜表面溶质浓度达到其饱和浓度时,便会在膜表面形成沉淀或凝胶层,增加透过阻力膜的分类按孔径大小:除菌,微滤膜;蛋白质,超滤膜;离子,纳滤膜、反渗透膜改善膜污染的方法:预防和控制膜污染1.预处理法,预先去除使膜性能发生变化的因素;2.采取错流操作并增加流器2.控制溶液温度、流速、流动状态、压力等 4.膜组件的清洗膜操作方式:死端操作,错流操作膜分离技术:在分子水平上,不同粒径的混合物在通过分离膜时实现选择性分离的技术,其实质是物质透过或被截留于膜的过程,类似于筛分过程,即依据膜孔径大小而达到物质分离的目的特点:物质在膜分离过程中不发生相变;具有浓缩和纯化双重功效,选择性较高;常温下进行,由压力驱动,特别适合热敏物质;分离装置简单,操作容易中性盐盐析法:蛋白质溶液加入中性盐后会压缩双电层,降低电位,即中性盐既会使蛋白质脱水,又会中和蛋白质所带的负电荷,使颗粒间的相互排斥力失去,而在布朗运动的互相碰撞下,蛋白质分子结合成凝聚物而沉淀析出β分级盐析法:在一定的离子强度下,改变溶液的pH值及温度,达到沉淀的目的Ks分级盐析法:在一定的 pH 值及温度条件下,改变盐的浓度(即离子强度)达到沉淀的目的盐析原理:1.蛋白质本身的稳定性;2.当中性盐达到一定浓度时,会破坏蛋白质的水化层和双电层,使变性失去排斥力,聚集而沉淀细胞破碎的方法:化学破碎、物理破碎、机械破碎、酶解破碎固体剪切方法、液体剪切法、超声波法、其他;非机械法(酶法溶胞、化学法、物理法、其他)低速离心,一般用离心速度,转速5000r/min高速离心(超速离心),以相对离心力表示g=颗粒所受离心力/地心引力悬浮法预处理的方法:加热法、调节悬浮液的pH值、凝聚和絮凝、加入反应剂凝聚:指在投加的化学物质作用下,胶体脱稳并使粒子相互聚集成1mm大小块状凝聚体的过程。
液流电池极化作用

液流电池极化作用引言:液流电池是一种常见的电化学能量转换装置,具有很高的能量密度和较长的使用寿命。
然而,随着使用时间的增加,液流电池的性能可能会下降,这主要是由于极化作用的影响。
本文将探讨液流电池极化作用的原理、影响因素以及可能的解决方案。
一、极化作用的原理极化是指在液流电池正常工作期间,电极表面出现的一种电化学现象。
它是由于电极与电解液之间的反应导致的,主要包括两种类型的极化:活化极化和浓差极化。
1. 活化极化:活化极化是由于电极表面发生的电化学反应速率较慢而导致的。
在液流电池中,电极表面的活性物质与电解液中的离子发生反应,产生电流。
然而,由于反应速率较慢,电流的传输速度受到限制,从而导致电池性能下降。
2. 浓差极化:浓差极化是由于电解液中离子浓度不均匀而导致的。
在液流电池中,离子会在电解液中自由移动,但随着时间的推移,电解液中的离子浓度会逐渐降低。
这会导致电解液中的离子在电极表面聚集,形成浓差差异,从而使电流传输受到限制。
二、影响因素液流电池极化作用的程度受到多种因素的影响,包括但不限于以下几个方面:1. 温度:温度是影响液流电池极化作用的重要因素之一。
在较低的温度下,电化学反应速率较慢,活化极化的程度较高。
因此,适当提高温度可以减轻极化效应。
2. 电流密度:电流密度是指单位面积上通过的电流量。
较高的电流密度会导致活化极化和浓差极化的程度增加,从而加剧极化作用。
因此,在设计液流电池时需要考虑合适的电流密度。
3. 电解液浓度:电解液中的离子浓度对液流电池的性能有重要影响。
较高的电解液浓度可以减轻浓差极化,从而改善电池的性能。
4. 电极材料:不同的电极材料对液流电池极化作用的影响也不同。
选择合适的电极材料可以降低极化效应。
三、解决方案为了减轻液流电池的极化作用,可以采取以下几种解决方案:1. 增加电极表面积:增加电极表面积可以提高电流传输速度,减轻活化极化的程度。
2. 优化电解液组成:调整电解液中的离子浓度和组成,以提高电解液的导电性能,减轻浓差极化。
电化学chapter4_液相传质与浓差极化

正离子在电极上氧化、负离子在电极上还原,电迁作用相反;
26
惰性电解质的作用:
假设溶液中除MA外,存在大量惰性电解质M’A,则稳态下应有:
-DM(dcM/dx)+Exu0McM= - υMI/nF -DM’(dcM’/dx)+Exu0M’ cM’= 0 -DA(dcA/dx)-Exu0AcA= 0 根据cM+cM’=cA, cM’ » cM, DM≈DM’≈DA, u0M≈u0M’≈u0A
12
理想情况下的稳态过程
13
◆扩散流量:
x,扩=-D(dC/ dx)
◆稳态扩散电流密度: I=-nF x,扩= nFD(dC/ dx)X=0 =nFD( C0-CS)/ ◆完全浓差极化: CS 0
极限扩散电流密度:
Id=nFDC0/
14
实际情况下的稳态扩散传质过程
实际情况下的稳态扩散为“对流扩散”;
因此,整个圆盘电极表面各点的扩散层厚度相同,扩散电流密度均一。
17
f
-vy
稳态下,三个坐标方向对流效应总和等于扩散 流失效应的总和。据此,可以得到扩散层有效厚 度表达式:
vf
vr
r
0
δi = 1.61 Di1/3ω-1/2υ1/6 I = 0.62 nF Di2/3 ω1/2 υ-1/6 (Ci0-CiS) Id = 0.62 nF Di2/3 ω1/2 υ-1/6 Ci0
0 C0 C0s
I d nFD0
0 C0
0 C0s C0 (1
0
I ) Id
(2)
(2)代入(1)中:
RT I RT I 0 0’ RT 0 In[C0 (1 )] 平 InC0 In 1 nF Id nF nF Id 0’ RT 0 当I 0时,平 平 InC0 nF RT I 平 In 1 nF I d
浓差极化与膜污染

② 膜材料的选择(考虑膜的亲疏水性、荷电性。亲 水性膜及膜材料电荷与溶质电荷相同的膜较耐污 染;对膜表面进行改性)
③ 膜孔径或截留分子量的选择(通过实验选择最佳 孔径的膜)
④ 膜结构选择(不对称结构膜较耐污染) ⑤ 组件结构选择
增加湍流,减小边界层厚度以减小浓差极化
膜浓缩加大,浓差极化加大
膜通量加大,浓差极化加大
溶质扩散系数增大,浓差极化减少
湍 流 强 化 器
Flow dynamics around the spacer netting often used to promote turbulence in a membrane module and reduce
对膜材料的改性
物理改性 – 增加膜表面粗糙度以强化膜表面附近流体湍流程度 的方法 – 亲水性溶剂处理膜表面,减小膜面对溶质的吸附
化学改性 – 有机物接枝膜改性 – 等离子聚合法 – 有机物嵌段共聚膜改性 – 离子移变凝胶膜 – 共混复合改性 – 溶剂化
7. 膜的清洗与再生
在任何膜分离技术应用中,尽管选择了较合适的 膜和适宜的操作条件,在长期运行中,膜的透水 量随运行时间增长而下降现象,即膜污染问题必 然产生。因此,必须采取一定的清洗方法,使膜面 或膜孔内污染物去除,达到透水量恢复,延长膜 寿命的目的。
2. 当膜表面溶质浓度达到其饱和浓度时,便会在膜 表面形成沉或凝胶层,增加透过阻力;
3. 膜表面沉积层或凝胶层的形成会改变膜的分离特 性;
4. 当有机溶质在膜表面达到一定浓度有可能对膜发 生溶胀或恶化膜的性能;
5. 严重的浓差极化导致结晶析出,阻塞流道,运行 恶化。
电化学chapter4_液相传质与浓差极化讲解
扩散传质步骤控制时的稳态极化曲线形式 唯一净反应: 扩散传质步骤是唯一的慢步骤,且溶液中存在大量惰性电解质
—标准平衡电势
20
分三种情况分析:O ne R
1)反应开始时R不存在,反应后生成的R可溶 (Fe3 e Fe2 )
C
0 R
0
平0’
RT nF
In
C0s CRs
I ≈nFDM(1+1/2 cM/ cM’) dcM/dx 若cM’ ≥50cM, 则第二项最多占1%,那么:
I ≈nFDMdcM/dx 表明:加入大量惰性电解质可忽略电迁作用
27
静止液体中平面电极上的非稳态扩散过程
静止液体—表面液层中对流可以忽略的场合
瞬间扩散电流:I (t) = nFDi (dCi/ dx)X=0,t
处理非稳态扩散传质,一般从Fick第二定律出发:
( Ci t
)扩
Di
(
2Ci x2
)
解二阶偏微分方程,需要确定初始条件和两个边界条件:
1、初始条件:ci(x,0) = ci0 2、边界条件: (1)、 ci(∞,t) = ci0
(2)、x=0处的具体极化条件
28
A、恒电势极化时的非稳态扩散过程(电势阶跃法)
26
惰性电解质的作用:
假设溶液中除MA外,存在大量惰性电解质M’A,则稳态下应有:
-DM(dcM/dx)+Exu0McM= - υMI/nF -DM’(dcM’/dx)+Exu0M’ cM’= 0
-DA(dcA/dx)-Exu0AcA= 0
根据cM+cM’=cA, cM’ »cM, DM≈DM’≈DA, u0M≈u0M’≈u0A
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.4. 球状电极的非稳态扩散
4.5 滴汞电极的扩散电流
4.5.1 滴汞电极的特征
4.5.2 依科维奇公式
4.5.3 极谱波
4.5.4 电容电流
4.5.5 极谱极大
4.6 浓差极化对不可逆电极反应动力学的影响
4.6.1 稳态下电极电位与电流密度的关系
4.6.2 恒电位下电流密度与时间的关系
第四章 浓差极化
§4.1 §4.2 §4.3 4.4 §4.5 §4.6
通电时电极附近的浓度变化 稳态扩散过程 浓差极化的动力学公式及极化曲线 非稳态扩散过程 滴汞电极上的扩散电流 混合步骤控制的电极过程动力学
4.1 通电时电极附近的浓度变化
4.1.1 液相传质的三种方式
4.1.2 稳态扩散和非稳态扩散
4.6.3 恒电流下电极电位与时间的关系
4.7 表面转化步骤不可逆条件下的扩散电 流
4.7.1 动力电流
4.7.2 催化电流
4.2 稳态扩散过程
4.2.1 理想状态下的稳态扩散
4.2.2 对流扩散
4.2.3 旋转圆盘电极
4.2.4 电迁传质的影响
4.3 浓差极化公式和极化曲线
4.4 非稳态扩散过程
4.4.1 平面电极的非稳态扩散 1) 完全浓度极化
2) 恒电位极化
3) 恒电流极化
