所有剂型流程图
药剂科流程图(全)

目录目录 (1)四查十对操作流程 (2)调剂差错管理流程 (2)药品召回程序流程图 (3)门诊处方调剂流程图 (4)中心药房工作流程图 (4)模糊医嘱的澄清流程 (5)住院药房(门诊药房)药品效期管理流程 (6)药库工作流程图 (7)药库药品效期管理流程 (8)假、劣药品,调剂药品导致人身伤害处置流程图 (8)突发事件药事管理应急预案流程 (8)突发事件药品供应应急预案流程图 (9)特殊使用抗菌药物使用流程 (9)药品采购流程图 (10)备用药品管理流程图 (11)麻、精、高危药品管理流程 (13)科室急救备用药品领用、补充工作流程 (13)输液反应处置流程 (15)细菌耐药监测和预警管理流程 (16)四查十对操作流程调剂差错管理流程发药人员对药名、规格、剂量、用法和处方内容是否相查药品对姓名、年龄,并交待用法及注意事项对药品有无变质、是否超过有效期对和处方内容是否相符 查标签(药袋)查药品查姓名、年龄调剂人员对科别、姓名、年龄查处方对临床诊断对药品性状、 用法用量对药名、剂型、规格、数量 查药品 查配伍禁忌 查用药合理性 报告部门负责人报药剂科主任报医务办严 重 事 件填写报告事件处理核对相关处方和药品查找患者发现差错药品召回程序流程图(一级24h 内)(二级7d 内)NOYESYes)药剂科各部门负责接收退回的药品,通知各科室停止销售和使用, 填写《药品召回登记表》,报告质量管理人员当使用被召回药品不会对治疗或患者的健康造成不良影响时,应采用二级召回当继续使用被召回药品将对治疗或患者的健康造成不良影响时,应采用一级召回反馈到投诉人或医院药品质量管理领导小组收到存在安全隐患可能的信息药品安全隐患的调查召回决定/确定召回等级制定召回计划/通告发放启动召回是否存在药品安全隐患的评估质量安全和管理小组组织召回 质量控制小组调查评估报告和召回计划上报汇总药品召回登记表,召回实施情况定期上报医院药品质量领导小组,召回总结报告召回产品的处理如需销毁,报医院药品质量安全领导小组,由药监部门监督销毁质量控制小组总结报告,上报医院药品质量领导小组验收/取样待处理药库负责接收各药房撤架和患者退回的药品,按《药剂科退药制度》的规定办理手续并记录,统一、专人妥善保管。
药剂科流程图(全).docx

目录目录 (1)四查十对操作流程 (2)调剂差错管理流程 (3)药品召回程序流程图 (4)门诊处方调剂流程图 (5)中心药房工作流程图 (6)模糊医嘱的澄清流程 (7)住院药房(门诊药房)药品效期管理流程 (8)药库工作流程图 (9)药库药品效期管理流程 (10)假、劣药品,调剂药品导致人身伤害处置流程图 (11)突发事件药事管理应急预案流程 (12)突发事件药品供应应急预案流程图 (13)特殊使用抗菌药物应用流程 (14)药品采购流程图 (14)备用药品管理流程图 (15)麻、精、高危药品管理流程 (17)科室急救备用药品领用、补充工作流程 (18)输液反应处置流程 (19)细菌耐药监测与预警管理流程 (20)四查十对操作流程调剂人员查处方查药品查配伍禁忌查用药合理性对科别、姓名、对药名、剂型、对药品性状、对临床诊断年龄规格、数量用法用量发药人员查药品查标签(药袋)查药品对药名、规格、对与处方内容对药品有无变质、剂量、用法与处是否相符是否超过有效期方内容是否相查姓名、年龄对姓名、年龄,并交待用法及注意事项调剂差错管理流程核对相关发现差错处方和药查找患者事件处理填写报告品报告部门报药剂科报医务办主任负责人严重事件质量安全与管理小组组织召回(一级 24h 内)(二级 7d 内)药剂科各部门负责接收退回的YES药品,通知各科室停止销售和使用,填写《药品召回登记表》,报告质量管理人员质量控制小组调查评估报告和召回计划上报药品召回程序流程图收到存在安全隐患可能的信息药品安全隐患的调查NO是否存在药品安全隐患的评估召回决定 /确定召回等级Yes精品文档反馈到投诉人或医院药品质量管理领导小组当继续使用被召回药品将对治疗或患者的健康造成不良影响时,应采用一级召回当使用被召回药品不会对治疗或患者的健康造成不良影响时,应采用二级召回)汇总药品召回登记表,召回实施情况定期上报医院药品质量领导小组,如需销毁,报医院药品质量安全领导小组,由药监部门监督销毁制定召回计划/通告发放启动召回召回产品的处理召回总结报告药库负责接收各药房撤架和患者退回的药品,按《药剂科退药制度》的规定办理手续并记录,统一、专人妥善保管。
药品生产典型工艺流程框图汇编

药品生产典型工艺流
程框图
常见药品生产典型工艺流程框图
药品生产对环境的洁净等级要求与药品的品种、剂型和生产特点有关。
常见药品生产的典型工艺流程及环境区域划分如图1-1至图1-9。
图1-1 非无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-2 无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-3 片剂生产工艺流程框图及环境区域划分
图1-4 硬胶囊剂生产工艺流程框图及环境区域划分
图1-5 压制法软胶囊剂生产工艺流程框图及环境区域划分
图1-6 可灭菌小容量注射剂生产工艺流程框图及环境区域划分
图1-7 可灭菌大容量注射剂生产工艺流程框图及环境区域划分
图1-8 注射用无菌分装产品生产工艺流程框图及环境区域划分
图1-9 注射用冷冻干燥制品生产工艺流程框图及环境区域划分。
5各剂型主要产品的配方生产工艺和质量标准,工艺流程图
各剂型主要产品的配方、生产工艺和质量标准、工艺流程图西安量维生物纳米科技股份有限公司是一家专门从事纳米保健食品的高新技术产业,公司所有保健食品剂型均为片剂,主要生产天赐源大豆异黄酮片。
1、配方原辅料称量配料配比:以每批10万片计2、生产工艺原辅料领料:称量岗位操作工依据《生产指令》,经小组负责人审核批准后从库房领取原辅料。
清洁脱去外包装,放置缓冲间,紫外灯照射30分钟以上,移至物料暂存间。
称量开工准备:1)复查工作场所:确认无前次生产遗留物,卫生清洁,温度、湿度等环境符合要求。
2)电子台秤:反应灵敏,回零、计量准确。
3)复核原辅料:品名无误、批号(编号)与检验报告单一致,质量合格。
操作:1)按电子台秤操规程,准确秤取各物料。
每批10万片,分一个批次配料,每次按10万片用量分别称量各原辅料。
2)每种物料称配后,应由第二人独立复核、签名。
品质监督员应现场监督或抽查称量记录。
3)秤配好的物料应袋入双层塑料袋中,扎紧后转入周转桶内,挂物料卡,转制粒工序。
结束:1)所有物料秤配结束后,应将剩余物料退回。
2)清理作业场所。
3)按规定及时填写生产记录及清场记录。
过程控制:制粒、干燥、总混过程:开工准备:1)复查作业场所:确认无前次生产遗留物,卫生清洁,温度18--25℃、湿度40-65%等环境符合要求。
2)设备:状态标志完好,清洁合格。
3)复核物料:名称、数量无误。
预混合:将原粉、糊精二者按处方比例加入槽型混合机,按混合机操作规程混合10-15分钟,将上述辅料混合均匀。
制粒:待辅料混合均匀后,加入90-95%乙醇适量混合制软材,以手握成团,轻触即散为度,用12目尼龙筛网依摆式颗粒机操作规程制湿颗粒。
干燥:将制得的湿颗粒平铺于不锈钢托盘上,成厚约1Cm的薄层,从上往下一层层放置热风循环烘箱,50-60℃干燥3--4小时后,用快速水分测定仪检颗粒水分在%以下后,将颗粒从下往上一层层收装入料斗转入总混。
整粒、总混:1)将III号树脂用95%的乙醇溶解成5%的溶液,取约1000ml撒入料斗中,略翻,到入锥型混合机;2)按锥型混合机操作规程进行混合,约5分钟,放料。
制剂工艺流程图
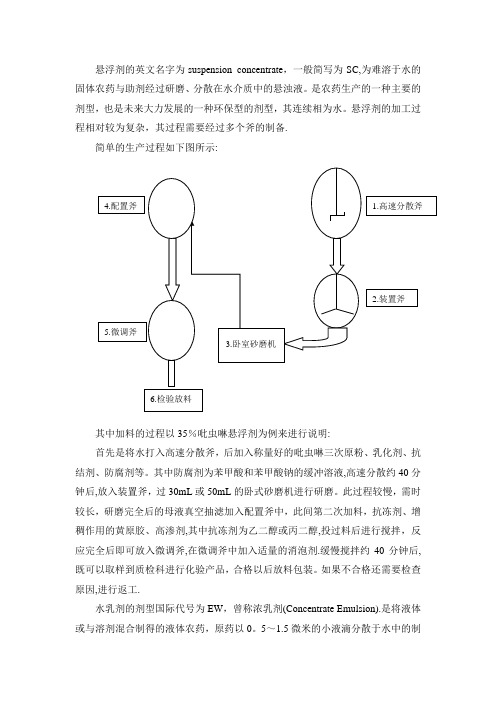
悬浮剂的英文名字为suspension concentrate ,一般简写为SC,为难溶于水的固体农药与助剂经过研磨、分散在水介质中的悬浊液。
是农药生产的一种主要的剂型,也是未来大力发展的一种环保型的剂型,其连续相为水。
悬浮剂的加工过程相对较为复杂,其过程需要经过多个斧的制备.简单的生产过程如下图所示:其中加料的过程以35%吡虫啉悬浮剂为例来进行说明:首先是将水打入高速分散斧,后加入称量好的吡虫啉三次原粉、乳化剂、抗结剂、防腐剂等。
其中防腐剂为苯甲酸和苯甲酸钠的缓冲溶液,高速分散约40分钟后,放入装置斧,过30mL 或50mL 的卧式砂磨机进行研磨。
此过程较慢,需时较长,研磨完全后的母液真空抽滤加入配置斧中,此间第二次加料,抗冻剂、增稠作用的黄原胶、高渗剂,其中抗冻剂为乙二醇或丙二醇,投过料后进行搅拌,反应完全后即可放入微调斧,在微调斧中加入适量的消泡剂.缓慢搅拌约40分钟后,既可以取样到质检科进行化验产品,合格以后放料包装。
如果不合格还需要检查原因,进行返工.水乳剂的剂型国际代号为EW ,曾称浓乳剂(Concentrate Emulsion).是将液体或与溶剂混合制得的液体农药,原药以0。
5~1.5微米的小液滴分散于水中的制剂,外观为乳白色牛奶状液体。
水乳制剂有:25%咪鲜胺EW(m/v)、5%功夫EW(m/v)、30%毒死蜱EW(m/v)等。
水乳剂的生产过程,主要包括了水相斧、油相斧、微调剪切斧、容器等部分,其过程相对悬浮剂来说相对简单。
其主要的生产过程如下图所示:微胶囊剪切斧已经装备完毕,而生产上还没有具体应用,近几年来,微囊技术被广泛应用于微生物、动植物细胞、酶和其他多种生物活性物质和化学药物的固定化方面.具体的应用有待进一步的研究。
乳油的加工过程相对来说比较简单,主要是按照一定的配比将原料计算好了之后,用真空泵将其打入加工混合斧中,搅拌约1小时后,用输送泵打到沉降区的沉降槽中,检验产品合格后放料。
药品生产典型工艺流程框图

常见药品生产典型工艺流程框图
药品生产对环境的洁净等级要求与药品的品种、剂型和生产特点有关。
常见药品生产的典型工艺流程及环境区域划分如图1-1至图1-9。
图1-1 非无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-2 无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-3 片剂生产工艺流程框图及环境区域划分
图1-4 硬胶囊剂生产工艺流程框图及环境区域划分
图1-5 压制法软胶囊剂生产工艺流程框图及环境区域划分
图1-6 可灭菌小容量注射剂生产工艺流程框图及环境区域划分
图1-7 可灭菌大容量注射剂生产工艺流程框图及环境区域划分
图1-8 注射用无菌分装产品生产工艺流程框图及环境区域划分
图1-9 注射用冷冻干燥制品生产工艺流程框图及环境区域划分。
药品生产典型工艺流程框图
常见药品生产典型工艺流程框图
药品生产对环境的洁净等级要求与药品的品种、剂型和生产特点有关。
常见药品生产的典型工艺流程及环境区域划分如图1-1至图1-9。
图1-1 非无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-2 无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-3 片剂生产工艺流程框图及环境区域划分
图1-4 硬胶囊剂生产工艺流程框图及环境区域划分
图1-5 压制法软胶囊剂生产工艺流程框图及环境区域划分
图1-6 可灭菌小容量注射剂生产工艺流程框图及环境区域划分
图1-7 可灭菌大容量注射剂生产工艺流程框图及环境区域划分
图1-8 注射用无菌分装产品生产工艺流程框图及环境区域划分
图1-9 注射用冷冻干燥制品生产工艺流程框图及环境区域划分。
药厂固体车间工艺流程
四、各种类型散剂的配制
• 1、普通固体药物散剂 • 2、含小剂量药物的散剂 • 3、含浸膏的散剂 • 4、含共熔成分的散剂 • 5、中药散剂
痱子粉的制备
• 痱子粉
[处方] 麝香草酚0.6g
0.6ml
薄荷脑0.6g
薄荷油
樟脑0.6g 4g
水杨酸1.4g 升华硫
麝香草酚硼酸8.5g
10g 薄荷脑
研磨
混合方式
• 实验室的混合方式:搅拌、研磨、过筛 。
• 大批量生产时的混合方式: 搅拌和容器旋转方式。
(三)分剂量
• 分剂量是将混合均匀的物料,按 剂量要求分装的过程。
• 常用的方法:目测法、重量法、 容量法。
(四)包装贮存
散剂包装与储存的重点在于防潮,散剂的吸湿特 性及防止吸湿措施成为控制散剂质量的重要内容
晶型,制成固体分散物等)
粉碎技术、药物的固体分散技术、药物的包合技术 等可以有效地提高药物的溶解度或溶出表面积。
口服制剂吸收的快慢顺序:
溶液剂 > 混悬剂 > 散剂 > 颗粒剂 > 胶囊剂 > 片剂 > 丸剂
散剂
• 一、概述
• 散剂(Powders)系指一种或数种药物均匀混 合而制成的粉末状制剂,可外用也可内服。
冲击
20~200 4~325
软性粉体 大部分医药品
胶体磨
磨碎
20~200 软性纤维状
气流粉碎机 撞击、研磨
1~30
中硬度物质
筛分
• 筛分法(sieving method)是借助筛网孔径 大小将物料进行分离的方法。
筛分的目的是为了获得较均匀的粒子群
冲眼筛
药筛
工 业
几种典型制药实用工艺流程图
常见药品生产典型工艺流程框图
药品生产对环境的洁净等级要求与药品的品种、剂型和生产特点有关。
常见药品生产的典型工艺流程及环境区域划分如图1-1至图1-9。
图1-1 非无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-2 无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-3 片剂生产工艺流程框图及环境区域划分
图1-4 硬胶囊剂生产工艺流程框图及环境区域划分
图1-5 压制法软胶囊剂生产工艺流程框图及环境区域划分
图1-6 可灭菌小容量注射剂生产工艺流程框图及环境区域划分
图1-7 可灭菌大容量注射剂生产工艺流程框图及环境区域划分
图1-8 注射用无菌分装产品生产工艺流程框图及环境区域划分
图1-9 注射用冷冻干燥制品生产工艺流程框图及环境区域划分。
固体剂型的制备工艺流程图
口服用片剂
(3) 泡腾片(Effervescent tablets)
泡腾片是含有泡腾崩解剂的片剂。泡腾 崩解剂是指碳酸氢钠与枸橼酸等有机酸 成对构成的混合物,遇水时二者反应产 生大量二氧化碳气体,从而使片剂迅速 崩解。应用时将片剂放入水杯中迅速崩 解后饮用。 非常适用于儿童、老人及吞服药片有困 难的病人。
1)均匀度 取供试品适量置光滑纸上 平铺约5cm2,将其表面压平,在 亮处观察,应呈现均匀色泽,无 花纹、色斑。 2)水分 取供试品照水分测定法测定, 除另有规定外,不得超过9.0%。 3)装量差异 单剂量、一日剂量包装 的散剂,装量差异限度应符合规 定。 此外,还应按《中国药典》附 录中的“微生物限度检查法”作 卫生学检查,并应符合有关规定。
如雷尼替丁分散片、阿司匹林分散片。
口服用片剂
(6) 缓释片(Sustained release tablets) 或控释片(Controlled release tablets)
(二)粉碎
粉碎操作的意义: 有利于提高难溶性药物的溶出速度以及 生物利用度; 有利于各成分的混合均匀; 有利于提高固体药物在液体、半固体、 气体中的分散度; 有助于从天然药物中提取有效成分等。
粉碎机
( 1 ) 研钵 一般用瓷、玻璃、玛瑙、铁或 铜制成, ( 2 ) 球磨机 在不锈钢(或陶瓷)制成的 圆筒内,装有直径不同的钢球(或瓷 球),当电机转动时,这些钢球(或瓷 球)正好能从最高位置落下,使药物手 受到强烈的撞击和研磨从而被粉碎,故 而将这种粉碎机械称为球磨机。
颗粒剂的质量检查
④溶化性:取供试颗粒剂10g,加热水 200ml,搅拌5分钟,可溶性颗粒应全部 溶化或可允许有轻微混浊,但不得有焦 屑等异物。混悬型颗粒剂应能混悬均匀, 泡腾性颗粒剂应立即产生二氧化碳气体, 并呈泡腾状。
