压力管道探伤口数量计算说明
钢管x光射线探伤张数计算

钢管x光射线探伤张数计算
钢管x光探伤的张数计算与管子的直径、壁厚、探伤速度有关。
通常,管子直径越大、壁厚越薄、探伤速度越快,所需的张数就越少。
假设有一根直径为10cm,壁厚为1cm的钢管需要进行x光探伤,探伤速度为10m/min,则每张探伤片的长度为10m。
根据管子周长计算,每张探伤片可覆盖的管长为:
管长= π × 直径 = 3.14 × 10cm = 31.4cm
将管长转换为米,得到:
管长 = 0.314m
因此,每张探伤片的覆盖面积为:
覆盖面积 = 长度 ×宽度 = 10m × 0.314m = 3.14平方米
假设需要覆盖的钢管长为100m,则需要的张数为:
张数 = 总管长 ÷单张覆盖管长 = 100m ÷ 0.314m = 318.5张
因此,我们需要约319张探伤片完成对这根钢管的x光探伤。
需要注意的是,实际的探伤情况可能因为管子表面情况、探伤机器性能等因素而有所不同,因此以上计算结果仅供参考。
其它管道的探伤比例及要求

其它管道的探伤比例及要求:-----《工业金属管道工程施工及验收规范》中的第七章《管道检验、检查和试验》中第四条中的有关部分:1 射线照相检验和超声波检验2 管道焊缝的内部质量,应按设计文件的规定进行射线照相检验或超声波检验。
射线照相检验和超声波检验的方法和质量分级标准应符合现行国家标准《现场设备、工业管道焊接工程施工及验收规范》的规定。
3 管道焊缝的射线照相检验或超声波检验应及时进行。
当抽样检验时,应对每一焊工所焊焊缝按规定的比例进行抽查,检验位置应由施工单位和建设单位的质检人员共同确定。
4 管道焊缝的射线照相检验数量应符合下列规定:5 下列管道焊缝应进行100%射线照相检验,其质量不得低于Ⅱ级:(1)输送剧毒流体的管道;(2)输送设计压力大于等于10MPa或设计压力大于等于4MPa且设计温度大于等于400℃的可燃流体、有毒流体的管道;(3)输送设计压力大于等于10MPa且设计温度大于等于400℃的非可燃流体、无毒流体的管道;(4)设计温度小于-29℃的低温管道。
(5)设计文件要求进行100%射线照相检验的其他管道。
6 输送设计压力小于等于1MPa且设计温度小于400℃的非可燃流体管道、无毒流体管道的焊缝,可不进行射线照相检验。
7 其他管道应进行抽样射线照相检验,抽检比例不得低于5%,其质量不得低于Ⅲ级。
抽检比例和质量等级应符合设计文件的要求。
8 经建设单位同意,管道焊缝的检验可采用超声波检验代替射线照相检验,其检验数量应与射线照相检验相同。
9 对不要求进行内部质量检验的焊缝,质检人员应按本章第7.2节的规定全部进行外观检验。
10 当检验发现焊缝缺陷超出设计文件和本规范规定时,必须进行返修,焊缝返修后应按原规定方法进行检验。
11 当抽样检验未发现需要返修的焊缝缺陷时,则该次抽样所代表的一批焊缝应认为全部合格;当抽样检验发现需要返修的焊缝缺陷时,除返修该焊缝外,还应采用原规定方法按下列全国注册建筑师、建造师考试备考资料历年真题考试心得模拟试题管道的探伤比例2规定进一步检验:12 每出现一道不合格焊缝应再检验两道该焊工所焊的同一批焊缝。
管道焊口无损探伤

管道焊口无损探伤一、管道焊缝应按照设计要求的检验方法和数量进行无损探险伤二、管口焊接含量取定可参考下表:序号项目10米直管焊口含量(个)10米管件焊口含量(个)单根管取定长度(m)碳钢、不锈钢、铬钼钢、有缝低温钢管、≤DN2501.27 20.6 6碳钢、不锈钢、铬钼钢、有缝低温钢管、≥DN3001 20.6 8碳钢板卷管、DN200~600 1.56 20.6 6.4碳钢板卷管、DN700~900 1.96 20.6 6.4碳钢板卷管、DN1000~1400 2.48 20.6 4.8碳钢板卷管、DN1600~3000 2.38 20.6 4.8螺旋卷管0.67 20.6 12三、无损探伤的拍片张数按设计规定计算的探伤焊缝总长度除以定额取定的胶片有效长度计算。
定额取定的胶片有效长度为250mm,设若计无明确规定,可参照下表计算,结算时按现场实际拍片张数计算。
管道焊口透视拍片张数表序号管外径底片规格张数序号管外径底片规格张数1 ≤89 1502 12 ≤1020 300 132 ≤133 1504 13 ≤1220 300 153 ≤159 2404 14 ≤1420 300 184 ≤273 300 4 15 ≤1620 300 205 ≤377 300 5 16 ≤1820 300 236 ≤478 300 6 17 ≤2020 300 257 ≤529 300 7 18 ≤2220 300 288 ≤630 300 8 19 ≤2420 300 309 ≤720 300 9 20 ≤2620 300 3310 ≤820 300 10 21 ≤2820 300 3511 ≤920 300 12 22 ≤3020 300 38四:管道探伤计算方法:每10米管道含有1.27个焊缝,X射线张数=1.27×延长米数×一圈管道所需的张数×0.2。
管道焊接拍片数量确定
管道焊接对焊接方式和焊接质量,应按设计规定套用相应定额。
如设计无规定时,可参考以下规定套用相应定额项目。
1.Ⅰ、Ⅱ级焊缝以及管内壁清洁度要求严格,且焊后不易清理的管道(如透平机入口管、锅炉给水管、机组的循环油、控制油、密封油管道等)单面焊缝、宜采用氩电联焊。
合金钢管焊缝采用氩弧焊打底时,焊缝内侧宜充氩气保护。
2.奥氏体不锈钢管单面焊的焊缝,宜采用手工钨极氩弧焊打底,手工电弧焊填充盖面(氩电联焊)。
公称直径在50毫米以下的采用氩弧焊。
3.Ⅲ级以下焊缝碳钢管,公称直径在50毫米以下的(壁厚在3.5毫米以下)采用氧炔焊。
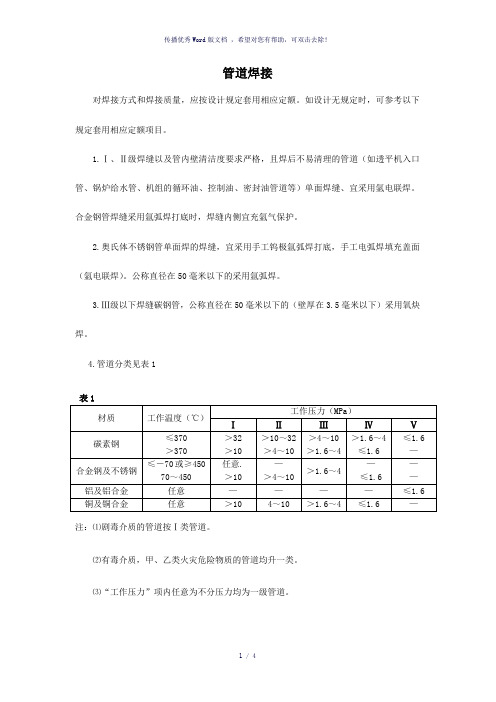
4.管道分类见表1注:⑴剧毒介质的管道按Ⅰ类管道。
⑵有毒介质,甲、乙类火灾危险物质的管道均升一类。
⑶“工作压力”项内任意为不分压力均为一级管道。
5.管口焊前预热和焊后热处理要求见表2。
表2注:⑴当焊接环境温度低于零度时,除规定壁厚必须作预热要求的金属外,其余金属壁厚也均应作适当的预热,使被焊接母材有手温感。
规定必须作预热要求的金属,定额项目内的预热消耗已考虑了温度变化因素,故不再增加预热。
⑵有应力腐蚀的碳素钢、合金钢,不论其壁厚条件,均应进行焊后热处理。
6.管口焊缝无损探伤计算规定数据:(1)管口焊接含量取定见表3。
(2)每个管口焊缝X光拍片张数,如无规定者可按表4计算。
注:⑴公称直径80毫米以下的管道焊缝X光透视检查拍片,一个焊口要求至少拍两张片。
定额中采用的胶片为85×300毫米的,实际上可用85×150毫米的胶片,执行定额时,人工和机械使用费不变,材料费乘0.5系数。
⑵片子有效长度按片长减去搭接每边25毫米计算。
⑶管道焊口透视拍片的张数=管道等级规定的探伤百分比×焊口数量×张数(见表4)(3)管道各级焊缝射线探伤数量,应按设计规定计算。
如设计无规定时,按表5规定计算。
表5注:每条管线上最低探伤不得少于一个焊口。
-----精心整理,希望对您有所帮助!。
管道焊缝无损探伤拍片数量的确定
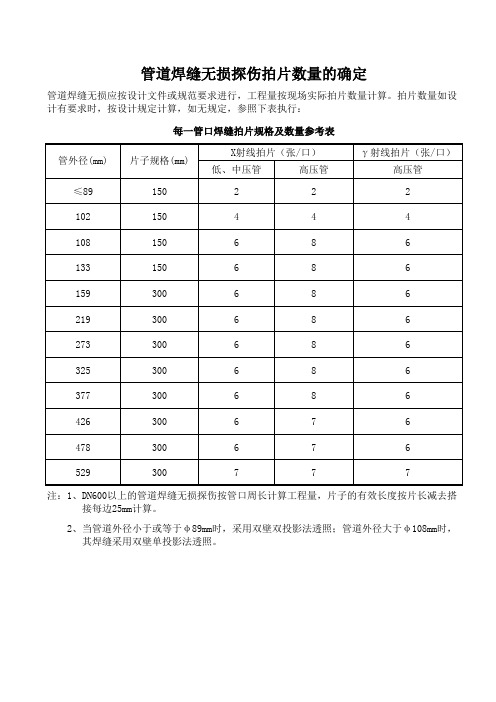
管道焊缝无损应按设计文件或规范要求进行,工程量按现场实际拍片数量计算。拍片数量如设 计有要求时,按设计规定计算,如无规定,参照下表执行:
每一管口焊缝拍片规格及数量参考表
管外径(mm)
片子规格(mm)
X射线拍片(张/口)
低、中压管
高压管
γ 射线拍片(张/口) 高压管
≤89
150
2
2ቤተ መጻሕፍቲ ባይዱ
2
102
150
4
4
4
108
150
6
8
6
133
150
6
8
6
159
300
6
8
6
219
300
6
8
6
273
300
6
8
6
325
300
6
8
6
377
300
6
8
6
426
300
6
7
6
478
300
6
7
6
529
300
7
7
7
注:1、DN600以上的管道焊缝无损探伤按管口周长计算工程量,片子的有效长度按片长减去搭 接每边25mm计算。
2、当管道外径小于或等于φ 89mm时,采用双壁双投影法透照;管道外径大于φ 108mm时, 其焊缝采用双壁单投影法透照。
片数量如设
压力管道需要探伤的标准

压力管道需要探伤的标准
压力管道需要探伤的标准包括以下几种情况:
1. 毒性程度为极度危害的流体管道。
2. 设计压力大于或等于10MPa的可燃流体、有毒流体的管道。
3. 设计压力大于或等于4MPa、小于10MPa,且设计温度大于等于400℃的可燃流体、有毒流体的管道。
4. 设计压力大于或等于10MPa,且设计温度大于或等于400℃的非可燃流体、无毒流体的管道。
5. 设计文件注明为剧烈循环工况的管道。
6. 设计温度低于-20℃的所有流体管道。
7. 夹套管的内管。
8. 按本规范第条规定做替代性试验的管道。
9. 设计文件要求进行焊缝100%无损检测的其他管道。
请注意,这些标准可能会根据具体的管道设计、用途和工作环境有所不同,建议在实际操作中参考相关标准和规范,并咨询专业人士进行指导。
管道工程量的计算规则
管道工程量的计算规则管道工程量计算规则1、工程量计算顺序:工艺管线工程量计算尽量以以下顺序计算:管道安装管件安装阀门安装法兰安装管道压力试验无损探伤及焊口热处理管道支架制作安装管口充氩保护、套管制作安装设备安装(泵、电机等)2、管道安装2.1 压力等级:低压0<p≤1.6mpa,< font=""></p≤1.6mpa,<>中压1.6<p≤10mpa,< font=""></p≤10mpa,<>高压10<p≤42mpa< font="">。
</p≤42mpa<>2.2 连接方式:电弧焊、氩弧焊、氩电联焊、螺栓连接、埋弧自动焊、氧乙炔焊、热风焊、承插粘接等2.3 工程量计算:工艺管线以施工图纸标明的延长米计算,不扣除管件、阀门、法兰长度,主材消耗量是扣除管件、阀门、法兰长度后加损耗的量。
方型补偿器不单独提取工程量,工程量包含在管道工程量及管件工程量中。
3、管件安装3.1 管件种类:弯头、三通、异径管、管帽(盲板)、管接头、挖孔制三通;3.2 各种管件连接均按压力等级、材质、连接方式以10个(个也行)为单位计算工程量,主管上挖眼制三通应以管件安装计算工程量,如:挖眼制三通DN500*35020 个2.5MPa,不另计主材费,挖眼制三通支线管径小于主管径1/2时,不计算管件工程量,若支管线较短相当于管接头及凸台时,应按配件管径计算工程量(相当于管件);3.3 对于仪表而言,管道开孔不计算工程量,以预留考虑,但压力表表弯制作,凸台制作安装、温度计扩大管制作安装应分别计算工程量,均以个为单位,应注明管径大小;3.4 焊接盲板工程量以“个”为单位,执行管件连接乘以系数0.6(造价用)。
4、阀门安装4.1 应注明压力等级、规格型号、安装方式(法兰连接、焊接、螺纹连接等),以个为单位;4.2 各种法兰及阀门安装的配套法兰安装应分别计算工程量,螺栓、透镜垫的安装费已包括在定额内,本身材料费应另行计算,在阀门安装或法兰安装工程量后提供其数量(主材费不计的可以不予考虑);4.3 直接安装在管道上的仪表流量计应归入阀门安装中,以个为单位,执行阀门安装乘以系数0.7(造价用)。
管道焊缝射线探伤数量和合格年级别
SY4056<<石油天然气钢制管道对接焊缝射线照相及质量分级>>
SY4065<<石油天然气钢制管道对接焊缝超
声波探伤及质量分级>>
焊缝的射线探伤可用超声波代替,合格级别与射线探伤相同,超声波探伤数量不少于射线探伤数量。
当选用超声波探伤时,应对超声波探伤部位作射线复验,复验数量为规定探伤数量5%,且不得少于一条焊缝。
设计压力大于1.6Mpa 的管道环焊缝宜选用射线探伤。
注汽管道的焊缝的无损探伤除符合上述规定外,合格级别为Ⅱ级的焊缝不得有未焊透缺陷,当选用超生探伤时,应对超生探伤的部位作20%的射线复验。
油田集输管道类别和等级划分方法
管道焊缝射线探伤数量和合格级别
焊接层数及焊条直径
焊道焊接应采用多层焊,焊道熔渣应清除干净,并进行外观检查,合格后可进行下道焊接。
低氢焊条在常温下4h应重新烘干,重复烘干次数不得超过两次。
压力管道探伤口数量计算说明
压力管道焊缝无损检测数量计算说明
1、不同管段编号的管段焊缝无损检测数量基数单独计算;
2、同一管段编号的管段中有不同规格的无损检测数量基数分别统计,分别计算无损检测数量;
3、同一管段编号的管段中有不同材质的无损检测数量基数分别统计,分别计算无损检测数量;
4、同一管段编号中,对接焊缝无损检测数量应以转动焊口和固定焊口的焊缝数量分别计算。
当设计中无损检测比例≤40%时,转动焊口的无损检测数量按设计中无损检测比例计算,固定焊口的无损检测数量按固定焊口的40%计算;当设计中无损检测比例>40%时,固定焊口和转动焊口的无损检测数量均按设计中无损检测比例计算。
转动口和固定口无损检测数量计算例1:
管段编号:PL0101,设计中无损检测比例:10%,该管段焊缝数量共40个,其中转动口30个,固定口10个,该管段探伤口数量计算如下:
转动口30×10%=3个;
固定口10×40%=4个;
则该管段探伤口为7个,其中3个为转动口,4个为固定口。
例2:
管段编号:PL0102,设计中无损检测比例:100%,该管段焊缝数量共40个,其中转动口30个,固定口10个,该管段探伤口数量计算如下:
转动口30×100%=30个;
固定口10×100%=10个;
则该管段探伤口为40个,其中30个为转动口,10个为固定口。
管道焊接拍片数量确定
管道焊接对焊接方式和焊接质量,应按设计规定套用相应定额.如设计无规定时,可参考以下规定套用相应定额项目。
1。
Ⅰ、Ⅱ级焊缝以及管内壁清洁度要求严格,且焊后不易清理的管道(如透平机入口管、锅炉给水管、机组的循环油、控制油、密封油管道等)单面焊缝、宜采用氩电联焊。
合金钢管焊缝采用氩弧焊打底时,焊缝内侧宜充氩气保护.2。
奥氏体不锈钢管单面焊的焊缝,宜采用手工钨极氩弧焊打底,手工电弧焊填充盖面(氩电联焊)。
公称直径在50毫米以下的采用氩弧焊。
3.Ⅲ级以下焊缝碳钢管,公称直径在50毫米以下的(壁厚在3.5毫米以下)采用氧炔焊。
4。
管道分类见表1表1注:⑴剧毒介质的管道按Ⅰ类管道.⑵有毒介质,甲、乙类火灾危险物质的管道均升一类。
⑶“工作压力”项内任意为不分压力均为一级管道。
5.管口焊前预热和焊后热处理要求见表2.表2注:⑴当焊接环境温度低于零度时,除规定壁厚必须作预热要求的金属外,其余金属壁厚也均应作适当的预热,使被焊接母材有手温感.规定必须作预热要求的金属,定额项目内的预热消耗已考虑了温度变化因素,故不再增加预热。
⑵有应力腐蚀的碳素钢、合金钢,不论其壁厚条件,均应进行焊后热处理.6.管口焊缝无损探伤计算规定数据:(1)管口焊接含量取定见表3。
(2)每个管口焊缝X光拍片张数,如无规定者可按表4计算。
表4注:⑴公称直径80毫米以下的管道焊缝X光透视检查拍片,一个焊口要求至少拍两张片。
定额中采用的胶片为85×300毫米的,实际上可用85×150毫米的胶片,执行定额时,人工和机械使用费不变,材料费乘0。
5系数.⑵片子有效长度按片长减去搭接每边25毫米计算。
⑶管道焊口透视拍片的张数=管道等级规定的探伤百分比×焊口数量×张数(见表4)(3)管道各级焊缝射线探伤数量,应按设计规定计算。
如设计无规定时,按表5规定计算。
表5注:每条管线上最低探伤不得少于一个焊口。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
压力管道探伤口数量计
算说明
Company Document number:WTUT-WT88Y-W8BBGB-BWYTT-19998
压力管道焊缝无损检测数量计算说明
1、不同管段编号的管段焊缝无损检测数量基数单独计算;
2、同一管段编号的管段中有不同规格的无损检测数量基数分别统计,分别计算无损检测数量;
3、同一管段编号的管段中有不同材质的无损检测数量基数分别统计,分别计算无损检测数量;
4、同一管段编号中,对接焊缝无损检测数量应以转动焊口和固定焊口的焊缝数量分别计算。
当设计中无损检测比例≤40%时,转动焊口的无损检测数量按设计中无损检测比例计算,固定焊口的无损检测数量按固定焊口的40%计算;当设计中无损检测比例>40%时,固定焊口和转动焊口的无损检测数量均按设计中无损检测比例计算。
转动口和固定口无损检测数量计算例1:
管段编号:PL0101,设计中无损检测比例:10%,该管段焊缝数量共40个,其中转动口30个,固定口10个,该管段探伤口数量计算如下:
转动口30×10%=3个;
固定口10×40%=4个;
则该管段探伤口为7个,其中3个为转动口,4个为固定口。
例2:
管段编号:PL0102,设计中无损检测比例:100%,该管段焊缝数量共40个,其中转动口30个,固定口10个,该管段探伤口数量计算如下:
转动口30×100%=30个;
固定口10×100%=10个;
则该管段探伤口为40个,其中30个为转动口,10个为固定口。
