化学平衡常数练习题
化学平衡常数 专题

化学平衡常数题组1、N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g) 4NO2(g)+O2(g) ΔH>0T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:时间/s 0 500 1000 1500c(N2O5)/mol·L-1 5.00 3.52 2.50 2.50下列说法中不正确的是( )A.T1温度下,500 s时O2的浓度为0.74 mol·L-1B.平衡后其他条件不变,将容器的体积压缩到原来的1/2,则再平衡时c(N2O5)>5.00 mol·L-1 C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2D.T1温度下的平衡常数K1=125,平衡时N2O5的转化率为0.52、在一定温度下,固定体积为 2 L的密闭容器中,发生反应:2SO2(g)+O2(g) 2SO3(g)ΔH<0,n(SO2)随时间的变化如下表:时间/min 0 1 2 3 4 5n(SO2)/mol 0.20 0.16 0.13 0.11 0.08 0.08 则下列说法正确的是( )A.当v(SO2)=v(SO3)时,说明该反应已达到平衡状态B.用O2表示0~4 min内该反应的平均速率为0.005 mol/(L·min)C.若升高温度,则SO2的反应速率会变大,平衡常数K值会增大D.平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大3、已知反应:2D+E3F+2G,用传感器测得该反应在不同pH条件下,物质D的浓度(用每升溶液所含溶质的质量表示,单位为mg/L)变化如图所示,下列有关说法正确的是( )A.pH=6.8时,D的浓度(mg/L)一定最大B.调节pH到8.8,可使该反应正、逆反应速率都为0C.在pH相同的条件下,增大压强,D的浓度(mg/L)增大D.温度相同时,不同pH条件下,该反应的平衡常数相同4、用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g) CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。
2.2.1 化学平衡状态 化学平衡常数(练习)(解析版)

2.2.1 化学平衡状态化学平衡常数练习(解析版)1.在一个恒容密闭容器中发生反应:2SO2(g)+O2(g)⇌2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为1.0mo1•L﹣1、1.0mo1•L﹣1、0.5mo1•L﹣1,当反应达到最大限度时,可能出现的数据是()A.c(SO3)═1.5mo1•L﹣1B.c(O2)=c(SO3)═0.75mo1•L﹣1 C.c(O2)═1.25mo1•L﹣1D.c(SO2)+c(SO3)═1.5mo1•L﹣1【答案】D【解析】A.为可逆反应,不能完全转化,则c(SO3)<1.5mo1•L﹣1,故A错误;B.某一时刻测得SO2、O2、SO3的浓度分别为1.0mo1•L﹣1、1.0mo1•L﹣1、0.5mo1•L﹣1,SO3的浓度增大0.25mol/L变为0.75mo1•L﹣1,此时转化的氧气为0.125mol/L,此时c(O2)=1.0mol/L﹣0.125mol/L=0.875mol/KL,故B错误;C.为可逆反应,不能完全转化,结合上述分析可知,c(O2)<1.25mo1•L﹣1,故C错误;D.由S原子守恒可知,c(SO2)+c(SO3)═1.5mo1•L﹣1,故D正确;故选:D。
2.观察图:对合成氨反应中,下列叙述错误的是()A.开始反应时,正反应速率最大,逆反应速率为零B.随着反应的进行,正反应速率逐渐减小,逆反应速率逐渐增大C.反应到达t1时,正反应速率与逆反应速率相等,反应停止D.反应在t1之后,正反应速率与逆反应速率相等,反应达到化学平衡状态【答案】C【解析】A、反应开始时,反应物的浓度最大,正反应速率最大,生成物的浓度为零,逆反应速率为零,故A正确;B、随着反应的进行,反应物的浓度降低,则正反应速率逐渐减小,生成物的浓度增大,则逆反应速率逐渐增大,故B正确;C、反应到达t1时,正反应速率与逆反应速率相等,但都不为零,反应没有停止,故C错误;D、反应在t1之后,正反应速率与逆反应速率相等,但都不为零,达到化学平衡状态,故D正确;故选:C。
化学平衡常数及计算练习(附答案)

化学平衡常数练习一、单选题1.在一密闭容器中,反应aX(g)+bY(g)cZ(g)达到平衡时平衡常数为K1;在温度不变的条件下向容器中通入一定量的X和Y气体,达到新的平衡后Z的浓度为原来的1.2倍,平衡常数为K2,则K1与K2的大小关系是()A.K1<K2B.K1=K2C.K1>K2D.无法确定2.在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)⇌Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:温度/℃25 80 230平衡常数5×104 2 1.9×10-5下列说法不正确的是( )A.上述生成Ni(CO)4(g)的反应为放热反应B.在25 ℃时,反应Ni(CO)4(g)⇌Ni(s)+4CO(g)的平衡常数为2×10-5C.在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v正>v逆D.在80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-13.在一定温度下,改变反应物中n(SO2),对反应2SO2(g)+O2(g)⇌2SO3(g)ΔH<0的影响如图所示,下列说法正确的是( )A .反应b 、c 点均为平衡点,a 点未达到平衡且向正反应方向进行B .a 、b 、c 三点的平衡常数K b >K c >K aC .上述图象可以得出SO 2的含量越高得到的混合气体中SO 3的体积分数越高D .a 、b 、c 三点中,a 点时SO 2的转化率最高 4.下列关于化学平衡常数的说法中,正确的是( ) A .可以用化学平衡常数来定量描述化学反应的限度B .在平衡常数表达式中,反应物浓度用起始浓度表示,生产物浓度用平衡浓度表示C .平衡常数的大小与浓度、压强、催化剂有关D .化学平衡发生移动,平衡常数必定发生变化5.在一定温度下,向2L 体积固定的密闭容器中加入1molHI ,发生反应:2HI(g)⇌H 2(g)+I 2(g) ∆H>0,测得2H 的物质的量随时间变化如表,下列说法正确的是( )t /min123()2n H /mol0.060.10.1A .2 min 内的HI 的分解速度为0.0511mol L min --⋅⋅B .该温度下,平衡时HI 的转化率为10%C .该温度下的平衡常数为1K ,温度升高10℃后平衡常数为2K ,则K 1>K 2D .达平衡后其他条件不变,压缩容器体积,平衡不移动,()c HI 不变6.关于 C(s)+H 2O(g)CO(g)+H 2(g)的平衡常数(K)书写形式,正确的是( )A .K=22c(C)c()c(CO)c O (H H )B .K=22c(CO)c()c(C)c(H H O)C .K=22c(CO)c()c(H H O)D .K=22c()c(C O O)c(H H )7.吸热反应N 2(g )+O 2(g )2NO (g ),在2000℃时,K =6.2×10-4。
化学平衡常数习题

训练6化学平衡常数[基础过关]-、化学平衡常数的含义1 •关于化学平衡常数的叙述正确的是( )A. 温度一定,一个化学反应的平衡常数不是一个常数B. 两种物质反应,不管怎样书写化学方程式,平衡常数不变C. 温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数D. 浓度商Q<K 时,v 正<v 逆2 •化学平衡常数可以用 K 来表示,下列关于化学平衡常数的说法中正确的是( )A. K 越大,反应物的转化率越小B. K 与反应物的浓度有关C. K 与生成物的浓度有关D. K 与温度有关3.某温度下,可逆反应mA(g)+ nB(g)一pC(g)的平衡常数为 K,下列对K 的说法正确的是()A. 5%B. 17% 三、化学平衡常数的综合应用A . K 值越大,表明该反应越有利于 C 的生成, 反应物的转化率越大B .若缩小反应器的容积,能使平衡正向移动,则 K 增大C .温度越高,K 一定越大D .如果 m + n = p ,贝U K = 1 4 .当把晶体N 2O 4放入密闭容器中气化,并建立了N 2O 4(g) ■:—2NO 2(g)平衡后,保持温度不C 2(NO 2) C (N 2O 4)变,再通入若干N 2O 4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其 A .变大 B.不变 C .变小 D.无法确定 二、化学平衡常数的计算 5 .将 4 mol SQ 与 2 mol O 2放入4 L 的密闭容器中,在一定条件下反应达到平衡: 2SO 2 +O2—2SQ ,测得平衡时 SQ 的浓度为 mol I 1。
则此条件下的平衡常数 K 为( A . 4 B.C.D .HX(g)的平衡常数为10。
若将mol 的HX(g 通入体积为L 的密闭容器中,在该温度时 HX(g)的最大分解率接近于 C. 25% D . 33%D .对于反应③,恒温恒容下,增大压强,H 2浓度一定减小7 .在淀粉-KI 溶液中存在下列平衡:l 2(aq) +1 (aq) •—b (aq)。
化学平衡常数习题

(也叫(也叫 )值越大,表示反应进行得 ,反应物转化率,反应物转化率 ;值越小,表示反应进行得 ,反应物转化率,反应物转化率 。
mA(g)+ nB(g)pC(g)+ qD(g),反应向,反应向进行进行 ,反应向,反应向进行进行 若升高温度,K值增大,则正反应为若升高温度,K值增大,则正反应为 反应1、化学平衡常数只与1、化学平衡常数只与 (g)(g)NH 1/2N 的关系式:的关系式: 。
的关系式:的关系式:。
的关系式:的关系式:O(g)CO )平衡常数的大小反映了化学反应进行的 反应若升高温度,K值减小,则正反应为若升高温度,K值减小,则正反应为 有关,与反应物或生成物的浓度无关。
有关,与反应物或生成物的浓度无关。
Fe(s)+CO 。
t ℃ 700 800 830 1000 1200 K 0.6 0.9 1.0 1.7 D 、c(CO) = c(CO 2) E、化学平衡常数K 不变不变F 、单位时间内生成CO 的分子数与生成H 2O 的分子数相等的分子数相等 ⑷某温度下,各物质的平衡浓度符合下式:c(CO 2)×)×c(H c(H 2)=c(CO)×)=c(CO)×c(H c(H 2O),试判此时的温度为 。
试推导在下列浓度下反应进行的方向试推导在下列浓度下反应进行的方向 序号 CO(mol/L ) H 2O (mol/L )CO 2 (mol/L )H 2 (mol/L )Q C 与K 关系及反应进行方向 1 0.3 0.5 0.4 0.4 2 1.0 0.3 0.5 0.6 3 0.8 1.6 0.7 1.7 7对于反应2SO 2(g)+ O 2(g) == 2SO 3(g) ,若在一定温度下,若在一定温度下,将0.1mol 的SO 2(g)和0.06mol O 2(g)注入一体积为2L 的密闭容器中,当达到平衡状态时,测得容器中有0.088mol 的SO 3(g) 试求在该温度下试求在该温度下(1)此反应的平衡常数。
化学平衡化学平衡常数(习题)()

第七章化学反应速率和化学平衡7.2 化学平衡化学平衡常数考点一可逆反应与化学平衡状态1.在一密闭容器中进行反应:2SO2(g)+O2(g)2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为mol·L1、mol·L1、mol·L1,当反应达到平衡时,可能存在的数据是()为mol·L1,O2为mol·L12为mol·L12为mol·L13、SO3均为mol·L121.B[解析] 由题中数据及该反应为可逆反应,则平衡时0<c(SO2) mol·L1、0<c(SO3) mol·L1,则A、C错误,B正确;反应物、生成物的浓度不可能同时减小,一个浓度减小,另一个浓度一定增大,D错误。
2.一定温度下,将2 mol SO2和1 mol O2充入2 L密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)2SO3(g),正反应放热。
下列说法中正确的是()A.达到反应限度时,SO2和SO3的分子数一定相等B.任意时刻,SO2和SO3物质的量之和一定为2 mol的消耗速率等于O2的生成速率时,达到反应限度2D.达到反应限度后,升高温度,正反应速率加快,逆反应速率减慢2.B[解析] 达到反应限度时,反应物和生成物的量与方程式的化学计量数无关,SO2和SO3的分子数不一定相等,故A错误;反应中SO2与SO3的化学计量数相等,二氧化硫的消耗量与三氧化硫的生成量相等,故SO2和SO3物质的量之和一定为2 mol,故B正确;SO2的消耗速率等于O2的生成速率时,正逆反应速率不相等,反应未达到平衡状态,故C错误;达到反应限度后,升高温度,正、逆反应速率均增大,故D错误。
3.在1 L恒温恒容的密闭容器中充入一定量N2O5,发生如下反应:O2(g)反应1:N2O5(g)N2O4(g)+12ΔH kJ·mol1反应2:N2O4(g)2NO2(g)ΔH kJ·mol1现有下列情况:①混合气体的密度保持不变;②气体压强保持不变;③气体的平均摩尔质保持不变;⑤O2的物质的量保持不变;⑥v正(N2O4)∶v逆(NO2)=1∶2。
化学平衡常数及计算练习(附答案)

化学平衡常数练习一、单选题1.在一密闭容器中,反应aX(g)+bY(g)cZ(g)达到平衡时平衡常数为K1;在温度不变得条件下向容器中通入一定量得X与Y气体,达到新得平衡后Z得浓度为原来得1、2倍,平衡常数为K2,则K1与K2得大小关系就是( )A.K1<K2ﻩB.K1=K2ﻩC.K1〉K2D。
无法确定2.在300 mL得密闭容器中,放入镍粉并充入一定量得CO气体,一定条件下发生反应:Ni(s)+4CO(g)⇌Ni(CO)4(g),已知该反应平衡常数与温度得关系如下表:下列说法不正确得就是( )A.上述生成Ni(CO)4(g)得反应为放热反应B。
在25 ℃时,反应Ni(CO)4(g)⇌Ni(s)+4CO(g)得平衡常数为2×10-5C.在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均为0、5 mol·L-1,则此时v正>v逆D.在80 ℃达到平衡时,测得n(CO)=0、3 mol,则Ni(CO)4得平衡浓度为2 mol·L-13.在一定温度下,改变反应物中n(SO2),对反应2SO2(g)+O2(g)⇌2SO3(g) ΔH<0得影响如图所示,下列说法正确得就是()A。
反应b、c点均为平衡点,a点未达到平衡且向正反应方向进行B.a、b、c三点得平衡常数Kb>K c〉K aC.上述图象可以得出SO2得含量越高得到得混合气体中SO3得体积分数越高D.a、b、c三点中,a点时SO2得转化率最高4。
下列关于化学平衡常数得说法中,正确得就是()A。
可以用化学平衡常数来定量描述化学反应得限度B.在平衡常数表达式中,反应物浓度用起始浓度表示,生产物浓度用平衡浓度表示C.平衡常数得大小与浓度、压强、催化剂有关D.化学平衡发生移动,平衡常数必定发生变化5.在一定温度下,向2L体积固定得密闭容器中加入1molHI,发生反应:2HI(g)⇌H2(g)+I2(g) ∆H>0,测得得物质得量随时间变化如表,下列说法正确得就是()1 2 3A。
化学平衡常数专题训练
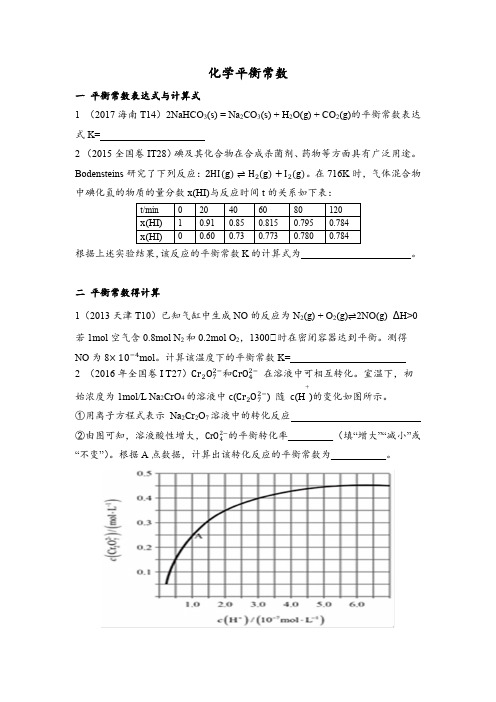
化学平衡常数一平衡常数表达式与计算式1 (2017海南T14)2NaHCO3(s) = Na2CO3(s) + H2O(g) + CO2(g)的平衡常数表达式K=2 (2015全国卷IT28)碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。
Bodensteins研究了下列反应:2HI(g)⇌H2(g)+I2(g)。
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:根据上述实验结果,该反应的平衡常数K的计算式为。
二平衡常数得计算1(2013天津T10)已知气缸中生成NO的反应为N2(g) + O2(g)⇌2NO(g) ∆H>0若1mol空气含0.8mol N2和0.2mol O2,1300℃时在密闭容器达到平衡。
测得NO为8×10−4mol。
计算该温度下的平衡常数K=2 (2016年全国卷I T27)Cr2O72−和CrO42−在溶液中可相互转化。
室温下,初始浓度为1mol/L Na2CrO4的溶液中c(Cr2O72−) 随c(H +)的变化如图所示。
①用离子方程式表示Na2Cr2O7溶液中的转化反应②由图可知,溶液酸性增大,CrO42−的平衡转化率_________(填“增大”“减小”或“不变”)。
根据A点数据,计算出该转化反应的平衡常数为___________。
3 (2017全国卷I T28)H2S与CO2在高温下发生反应:H2S(g)+CO2(g)⇌COS(g)+H2O(g)。
在610K时,将0.10mol CO2与0.40mol H2S充入2.5L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
H2S的平衡转化率α1=%,反应平衡常数K= 。
I固体,t ℃时发生如下4(2019天津T7)在1 L真空密闭容器中加入a mol PH4反应①PH4I(s)⇌PH3(g)+HI(g)②4PH3(g)⇌P4(g)+6H2(g)③2HI(g)⇌H2(g)+I2(g)达平衡时,体系中n(HI)=b mol,n(I2)=c mol ,n(H2)=d mol ,则t℃时反应①的平衡常数值为(用字母表示)5(2017年4月浙江T30)在常压、Ru/TiO2催化下,CO2和H2混合气体(体积比1:4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化得CO2中生成CH4或CO的百分比)反应I CO2(g) + 4H2(g) ⇌CH4(g) + 2H2O(g) ∆H1反应II CO2(g) + H2(g) ⇌CO(g) + H2O(g) ∆H2350℃时,反应I在t1时刻达到平衡,平衡时容器体积为VL该温度下反应I的平衡常数为(用a、V表示)三压强平衡常数1(2014年全国卷IT28)气相直接水合法C2H4(g)+H2O(g)=C2H5OH(g)中乙烯的平。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学平衡常数
1.关于化学平衡常数的叙述正确的是
A.温度一定,一个化学反应的平衡常数不是一个常数
B.两种物质反应,不管怎样书写化学方程式,平衡常数不变
C.温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数D.浓度商Qc<K时,v正<v逆
2 化学平衡常数可以用K来表示,下列关于化学平衡常数的说法中正确的是A.K越大,反应物的转化率越小B.K与反应物的浓度有关
C.K与生成物的浓度有关D.K与温度有关
3 某温度下,可逆反应mA(g)+nB(g)pC(g)的平衡常数为K,下列对K的说法正确的是
A.K值越大,表明该反应越有利于C的生成,反应物的转化率越大
C.温度越高,K一定越大D.如果m+n=p,则K=1
4 将4mol SO2与2mol O2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2+O22SO3,测得平衡时SO3的浓度为0.5mol·L-1。
则此条件下的平衡常数K为()
A.4B.0.25C.0.4D.0.2
5 CO(g)+2H2(g)CH3OH(g)该反应的平衡常数表达式K=__________;
6 下列有关化学平衡常数K的说法中,正确的是()
A.K的大小与起始浓度有关B.温度越高,K值越大
C.K值越大,平衡体系中生成物所占比例越大
D.K值越大,正向反应进行的程度越小
8在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误
..的是:
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z,其平衡常数为1600(mol/l)-2
D.改变温度可以改变此反应的平衡常数
9在10 L 容器中,加入2 mol SO2(g)和2 mol NO2(g),保持温度恒定,发生反应:SO2(g)+ NO2(g) SO3(g)+ NO(g),当达到平衡状态时,测得容器中
SO2(g)的转化率为50%,该温度下的该反应的平衡常数= (算出数值)
10在一定条件下,向密闭容器中充入30 mL CO和20 mL水蒸气,使其反应,当反应CO(g)+H2O(g)CO2(g)+H2(g)达到平衡时,水蒸气的体积分数与H2的体积分数相等,则下列叙述错误的是()
A.平衡后CO的体积分数为40% B.平衡后CO的转化率为25%
C.平衡后水的转化率为50% D.平衡后混合气体的平均相对分子质量为24
11已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.
(1)写出上述反应的化学方程式________
(2)该反应的正反应是__________反应(填“放热”或者“吸热”),
12在80 ℃时,将0.40 mol 的N2O4气体充入2 L 已经抽空的固定容积的密闭容器中,发生如下反应:N2O4(g)2NO2(g)ΔH >0,隔一段时间对该容器内的物质进行分析,
时间/s
(1)计算20~40 s 内用N2O4表示的平均反应速率为__________ mol·L-1·s-1。
(2)计算在80 ℃时该反应的平衡常数K=____ __。
13一定温度下,将3 mol A气体和1 mol B气体通人一密闭容器中,发生如下反应:3A(g)+B(g) xC(g)。
请填写下列空白:
(1)
.......为2 L,反应2min时测得剩余0.6 mol B,C的浓度为0.4 ...若容器体积固定
mol/L。
①2min内,A的平均反应速率为_______________;x=_________________;
②若反应经4min达到平衡,平衡时C的浓度_______________0. 8 mol/L (填“大于”、“等于” 或“小于”);
③平衡混合物中c的体积分数为22%,则B的转化率是__________________;
A
B
P /MPa
0.50 0.10
0.80
0.85
α 14 二氧化硫和氮的氧化物是常用
的化工原料,但也是大气的主要污染物。
综合治理 其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO 2催化氧化生成SO 3:
2SO 2(g)+O 2(g)
2SO 3(g)
某温度下,SO 2的平衡转化率(a)与体系总压强(p)
的关系如右图所示。
根据图示回答下列问题:
①将2.0mol SO 2和1.0mol O 2置于5L 密闭容器中,反应达平衡后,体系总压强为0.10MPa 。
该反应的平衡常数等于_____ 。
②平衡状态由A 变到B
时.平衡常数K(A)_______K(B)(填>、<或=)
15 氮化硅(Si 3N 4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中通过以下反应制得:
(1)配平上述反应的化学方程式(将化学计量数填在方框内); (2)该反应中的氧化剂是________,其还原产物是________; (3)该反应的平衡常数表达式为K =________;。
