有机化合物的紫外-可见吸收光谱
合集下载
第三章 紫外-可见吸收光谱分析

2.不饱和脂肪烃 .
在不饱和烃类分子中,除含有σ键外,还含有π 键,它们可以产生 σ→σ*和π→π* 两种跃迁。 如果存在共轭体系,则随共轭系统的延长, 吸收带将明显向长波方 向移动,吸收强度也随之增强 在共轭体系中, π→π*跃迁产生的吸收带又称为K(Konjugation) 带。其特点是:强度大,εmax›104;位置一般在217~280nm λmax和εmax的大小与共轭链的长短及取代基的位置有关 根据K带是否出现,可判断分子中共轭体系的存在的情况。在紫外光 根据 带是否出现,可判断分子中共轭体系的存在的情况 带是否出现 谱分析中有重要应用。
紫外- §3-3 紫外-可见分光光度法的应用 一、 定性分析 二、纯度检查 三、结构推测 四、定量分析 单组分样品的定量分析 多组分样品的定量分析
一、 定性分析
1、依据:吸收光谱的特征——形状、波长、峰数目、强度、 吸光系数。 、依据:吸收光谱的特征 形状、 形状 波长、峰数目、强度、 吸光系数。 2、方法:对比法 、方法: (1) 对比吸收光谱特征数据 (2) 对比吸光度或吸光系数的比值
3.芳香烃 .
苯有三个吸收带 E1带180∼184nm ε=47000 E 2带200∼204 nm ε=7000 苯环上三个共扼双键的 π → π*跃迁特征吸收带 B带 230-270 nm
ε=200
π → π*与苯环振动引起; 含取代基时, B带简化,红移 当苯环上有取代基时,苯的三个特征谱带都会发生显著的变化, 其中影响较大的是E2带和B谱带。
化合物 H2O CH3OH CH3CL CH3I CH3NH2
λmax(nm) 167 184 173 258 215
εmax 1480 150 200 365 600
有机化合物的紫外吸收光谱

直链共轭二烯基本值
217
非骈环共轭双烯
217
烷基或环残余取代
5
环外双键
5
卤素取代
17
CH3 CH2=C-C=CH2
CH3
基本值 烷基取代 计算值
测量值
217nm 2× 5nm
227nm 226nm
H3C
1
3
4
C
CH3
2
CH3
基本值 烷基取代 环外双键
计算值 测量值
217 4× 5nm
5nm 242nm 243nm
溶剂 修正值 溶剂 修正值
溶 剂
水 -8nm 乙醚 +7nm
修 正
甲醇
0 正己烷 +11nm
值
氯仿 +1nm 环己烷 +11nm
二氧六环 +5nm
(CH3)2C=CHCOCH3
计算值 甲醇中的测定值 己烷中的测定值
239nm 237nm 230nm (230+11=241nm)
B、α、β不饱和羧酸及酯吸收波长的计算方法
R2 -C6H4 -COR
R1为烷基时的基本值 R1为H时的基本值 R1为OH时的基本值 R2为下列基团时
烷基
-OH -OR
-O-
-Cl
-Br
-NH2 -NHAc
-NR2
K吸收带波长λ/nm
246 250
230 邻位 间位 对位
3
3 10
7
7
25
11
20 78
0
0
10
2
2
15
13 13 58
20 20 45 20 20 85
2、α、β不饱和羰基化合物π→π*跃迁的吸收波长计算办法
(完整版)图吸收光谱曲线

(8) B带
➢ 由芳香族化合物的π →π*跃迁而产生的精 细结构吸收带。
例如: 苯的B带: 摩尔吸光系数:200 L ·mol-1 ·cm-1 吸收峰的位置:230~270nm之间
(9) E带
➢ 芳香族化合物的π →π*跃迁所产生的吸收带, 也是芳香族的特征吸收峰。
苯的紫外吸收光谱
4、影响紫外-可见吸收光谱的因素
(2) 助色团
➢ 助色团是指本身不产生吸收峰,但与生色团 相连时,能使生色团的吸收峰向长波方向移动, 并使其吸收强度增强的基团。
例如:
—NH2 、—OH 、—OR 、—SH 、—SR 、—Cl 、—Br等
(3) 红移和蓝移
➢ 在有机化合物中,常常因取代基的变更或溶 剂的改变,使其吸收带的最大吸收波长max发生 移动。
例如:含有杂原子的不饱和基团:
(4) 电荷转移跃迁:
➢ 某些分子同时具有电子给予体和电子接受体, 它们在外来辐射照射下会强烈吸收紫外光或可 见光,使电子从给予体轨道向接受体轨道跃迁, 这种跃迁称为电荷转移跃迁,其相应的吸收光 谱称为电荷转移吸收光谱。
➢ 电荷转移跃迁实质上是一个内氧化还原过程。
例如:某些取代芳烃可产生这种分子内电荷转移 跃迁的吸收带。
➢ n → σ* 跃迁的摩尔吸光系数ε较小
(2) π→ π*跃迁:
➢ 吸收峰处于近紫外光区,在200nm左右,摩
ε 尔吸收系数 max > 104 L ·mol-1 ·cm-1 ,为强吸收带。
例如:含有π电子的基团:
(3) n → π*跃迁:
➢ 近紫外-可见光区,ε<100 L ·mol-1 ·cm-1
3、常用术语 (1) 生色团
➢ 生色团是指分子中能吸收紫外或可见光的 基团,它实际上是一些具有不饱和键和含有 孤对电子的基团。
紫外可见吸收光谱基本原理
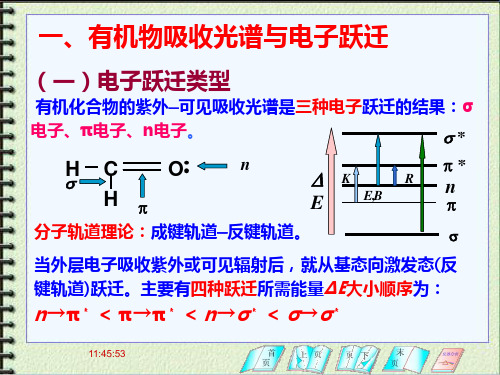
n→π* < π→π* < n→σ* < σ→σ*
11:51:47
2
σ→σ*跃迁
所需能量最大;σ电子只有吸收远紫外光的能量
才能发生跃迁;
饱和烷烃的分子吸收光谱出现在远紫外区; 吸收波长λ <200 nm; 例:甲烷的λ max为125nm , 乙烷λ max为135nm 。 只能被真空紫外分光光度计检测到; 作为溶剂使用;
max(甲醇) max(水) max(氯仿)
n → p*跃迁:蓝移; ;
max(正己烷)
p → p* n → p*
230 329
11:51:47
238 315
237 309
243 305
溶剂的影响
苯 酰 丙 酮 1 1:乙醚 2:水
2
250
300
极性溶剂使精细结构 消失;
11:51:47
11:51:47
11:51:47
精品课件!
11:51:47
精品课件!
11:51:47
(三) 金属离子影响下的配位体内π→π*跃迁 金属离子的微扰,将引起配位体吸收波长和 强度的变化。变化与成键性质有关,若共价 键和配位键结合,则变化非常明显。 茜素磺酸钠: 弱酸性介质:黄色(λ max=420nm) 弱碱性介质:紫红色(λ max=560nm )
一、有机物吸收光谱与电子跃迁
(一)电子跃迁类型
有机化合物的紫外—可见吸收光谱是三种电子跃迁的结果: σ电子、π电子、n电子。 s*
E p 分子轨道理论:成键轨道—反键轨道。
s
H
C H
OnKR Nhomakorabeap*
E,B
n
p
s
当外层电子吸收紫外或可见辐射后,就从基态向激发态(反 键轨道)跃迁。主要有四种跃迁所需能量ΔΕ大小顺序为:
有机化合物的紫外吸收光谱

摩尔吸光系数一般都较大(10 左右), 摩尔吸光系数一般都较大 4左右 ,适宜于微量金 属的检出和测定
08:51:49
配位场的跃迁
以金属配合物的电子吸收光谱为例, 以金属配合物的电子吸收光谱为例,产生机理有 三种类型: 三种类型: 配位体微扰的金属离子d-d电子跃迁和f-f电子 跃迁摩尔吸收系数ε很小,对定量分析意义不大。 很小,对定量分析意义不大。 金属离子微扰的配位体内电子跃迁 金属离子的微扰, 金属离子的微扰,将引起配位体吸收波长和 强度的变化。变化与成键性质有关, 强度的变化。变化与成键性质有关,若静电引力 结合,变化一般很小。若共价键和配位键结合, 结合,变化一般很小。若共价键和配位键结合, 则变化非常明显。 则变化非常明显。 电荷转移吸收光谱 辐射下,分子中原定域在金属M轨道上的电 辐射下,分子中原定域在金属 轨道上的电 荷转移到配位体L的轨道 或按相反方向转移, 的轨道, 荷转移到配位体 的轨道,或按相反方向转移, 所产生的吸收光谱
08:51:49
溶剂对紫外吸收光谱的影响
(一) 溶剂极性对紫外吸收光谱的影响 1、n→π *跃迁所产生的吸收峰随溶剂极性的 增加而向短波方向移动。 增加而向短波方向移动。
例如,异丙叉丙酮CH 例如,异丙叉丙酮CH3COCH=C(CH3)2发生 n→π *跃迁吸收 的光波波长在正己烷中为329nm 在氯仿中为315nm 329nm, 315nm, 的光波波长在正己烷中为329nm,在氯仿中为315nm,在 甲醇中为309nm 在极性最大水中则为305nm 309nm, 305nm。 甲醇中为309nm,在极性最大水中则为305nm。
08:51:49
第二章 紫外吸收光谱 分析法
一、 有机化合物的紫外吸收光谱
有机化合物结构中价电子类型: 有机化合物结构中价电子类型: 按分子轨道理论,分子中外层价电子有三种:σ 按分子轨道理论,分子中外层价电子有三种: 电子、 电子。 电子、π电子和n电子。 一般对应于4种类型的跃迁: 一般对应于4种类型的跃迁: (1) N-V跃迁:基态轨道→反键轨道,σ→σ* 跃迁:基态轨道→反键轨道, π→π* 跃迁:未成键n电子→反键轨道, (2) N-Q跃迁:未成键n电子→反键轨道, n→σ* n →π* 跃迁: 电子→高能级→ (3) N-R跃迁: σ电子→高能级→分子离子 电荷迁移跃迁:电荷从化合物的一部分→ (4) 电荷迁移跃迁:电荷从化合物的一部分→另一 部分
08:51:49
配位场的跃迁
以金属配合物的电子吸收光谱为例, 以金属配合物的电子吸收光谱为例,产生机理有 三种类型: 三种类型: 配位体微扰的金属离子d-d电子跃迁和f-f电子 跃迁摩尔吸收系数ε很小,对定量分析意义不大。 很小,对定量分析意义不大。 金属离子微扰的配位体内电子跃迁 金属离子的微扰, 金属离子的微扰,将引起配位体吸收波长和 强度的变化。变化与成键性质有关, 强度的变化。变化与成键性质有关,若静电引力 结合,变化一般很小。若共价键和配位键结合, 结合,变化一般很小。若共价键和配位键结合, 则变化非常明显。 则变化非常明显。 电荷转移吸收光谱 辐射下,分子中原定域在金属M轨道上的电 辐射下,分子中原定域在金属 轨道上的电 荷转移到配位体L的轨道 或按相反方向转移, 的轨道, 荷转移到配位体 的轨道,或按相反方向转移, 所产生的吸收光谱
08:51:49
溶剂对紫外吸收光谱的影响
(一) 溶剂极性对紫外吸收光谱的影响 1、n→π *跃迁所产生的吸收峰随溶剂极性的 增加而向短波方向移动。 增加而向短波方向移动。
例如,异丙叉丙酮CH 例如,异丙叉丙酮CH3COCH=C(CH3)2发生 n→π *跃迁吸收 的光波波长在正己烷中为329nm 在氯仿中为315nm 329nm, 315nm, 的光波波长在正己烷中为329nm,在氯仿中为315nm,在 甲醇中为309nm 在极性最大水中则为305nm 309nm, 305nm。 甲醇中为309nm,在极性最大水中则为305nm。
08:51:49
第二章 紫外吸收光谱 分析法
一、 有机化合物的紫外吸收光谱
有机化合物结构中价电子类型: 有机化合物结构中价电子类型: 按分子轨道理论,分子中外层价电子有三种:σ 按分子轨道理论,分子中外层价电子有三种: 电子、 电子。 电子、π电子和n电子。 一般对应于4种类型的跃迁: 一般对应于4种类型的跃迁: (1) N-V跃迁:基态轨道→反键轨道,σ→σ* 跃迁:基态轨道→反键轨道, π→π* 跃迁:未成键n电子→反键轨道, (2) N-Q跃迁:未成键n电子→反键轨道, n→σ* n →π* 跃迁: 电子→高能级→ (3) N-R跃迁: σ电子→高能级→分子离子 电荷迁移跃迁:电荷从化合物的一部分→ (4) 电荷迁移跃迁:电荷从化合物的一部分→另一 部分
紫外可见吸收光谱吸收带类型与溶剂效应

13:01:32
4、π→π*跃迁(最重要的、研究最多的吸收带)
所需能量较小,吸收波长处于远紫外区的近紫外端或近 紫外区,εmax一般在104L·mol-1·cm-1以上,大多属于强吸收。 包含有:
K吸收带:共轭非封闭体系中的π→π*跃迁吸收带,一般 为强吸收(ε在104以上)。应用最多。极性溶剂使K带发生红 移。
摩尔吸光系数ε增大或减小
的现象分别称为增色效应或 减色效应,如图所示。
13:01:32
三、溶剂对紫外-可见吸收光谱的影响
1、常用溶剂 溶剂选用的原则: A、溶剂不影响溶质的测量; B、溶剂对溶质具有良好的溶解性; C、溶剂与溶质不相互作用。 一般情况下,极性物质选用极性溶剂;非极
性物质选用非极性溶剂。
这类光谱一般位于可见光区,摩尔吸收系数εmax很小,
对定量分析意义不大,一般用于研究配合物结构及无机配合 物键合理论等方面。
13:01:32
苯的紫外吸收光谱(溶剂:异辛烷)
13:01:32
二、常用术语
发色团:最有用的紫外—可见光谱是由π→π*和n→π*跃迁产 生的。这两种跃迁均要求有机物分子中含有不饱和基团。这 类含有π键的不饱和基团称为发色团,也叫生色团。简单的发 色团(生色团)由双键或叁键体系组成,如乙烯基、羰基、 亚硝基、偶氮基—N=N—、乙炔基、腈基—C≡N等。单一 双键在远紫外区,共轭双键在近紫外区。 助色团:有一些含有n电子的基团(如—OH、—OR、—NH2 、—NHR、—X等),它们本身没有生色功能(不能吸收 λ>200nm的光),但当它们与生色团相连时,就会发生n→π共 轭作用,增强生色团的生色能力(吸收波长向长波方向移动, 且吸收强度增加),这样的基团称为助色团。
第五章 紫外-可见吸
4、π→π*跃迁(最重要的、研究最多的吸收带)
所需能量较小,吸收波长处于远紫外区的近紫外端或近 紫外区,εmax一般在104L·mol-1·cm-1以上,大多属于强吸收。 包含有:
K吸收带:共轭非封闭体系中的π→π*跃迁吸收带,一般 为强吸收(ε在104以上)。应用最多。极性溶剂使K带发生红 移。
摩尔吸光系数ε增大或减小
的现象分别称为增色效应或 减色效应,如图所示。
13:01:32
三、溶剂对紫外-可见吸收光谱的影响
1、常用溶剂 溶剂选用的原则: A、溶剂不影响溶质的测量; B、溶剂对溶质具有良好的溶解性; C、溶剂与溶质不相互作用。 一般情况下,极性物质选用极性溶剂;非极
性物质选用非极性溶剂。
这类光谱一般位于可见光区,摩尔吸收系数εmax很小,
对定量分析意义不大,一般用于研究配合物结构及无机配合 物键合理论等方面。
13:01:32
苯的紫外吸收光谱(溶剂:异辛烷)
13:01:32
二、常用术语
发色团:最有用的紫外—可见光谱是由π→π*和n→π*跃迁产 生的。这两种跃迁均要求有机物分子中含有不饱和基团。这 类含有π键的不饱和基团称为发色团,也叫生色团。简单的发 色团(生色团)由双键或叁键体系组成,如乙烯基、羰基、 亚硝基、偶氮基—N=N—、乙炔基、腈基—C≡N等。单一 双键在远紫外区,共轭双键在近紫外区。 助色团:有一些含有n电子的基团(如—OH、—OR、—NH2 、—NHR、—X等),它们本身没有生色功能(不能吸收 λ>200nm的光),但当它们与生色团相连时,就会发生n→π共 轭作用,增强生色团的生色能力(吸收波长向长波方向移动, 且吸收强度增加),这样的基团称为助色团。
第五章 紫外-可见吸
第五章 紫外-可见吸收光谱法
甲醇 n→σ*跃迁: λmax 183nm
π→π*跃迁:
所需能量较小,λ一般>200nm,εmax > 104。 不饱和基团(乙烯基、乙炔基) 不饱和烃、共轭烯烃和芳香烃类可发生此类跃迁。 乙烯 π→π*跃迁: λmax 165nm
丁二烯 π→π*跃迁: λmax 217nm
n→π*跃迁:
所需能量最小, λ >200nm, -C=N-
色——蓝色。
我们通常见到的有色物质,都是由于他们吸收了可见光的 部分光,呈现出吸收光颜色的互补色。
二、分子吸收光谱的产生
分子吸收光谱的形成是由于电子在能级之间的跃迁所引
起的。
分子内部具有电子能级、振动能级和转动能级。所以分
子的能量 E分子=E电+E振+E转 。
这些能量是量子化的,只有光辐射的能量恰好等于两能 级之间的能量差时,才能被吸收。
苯环本身分子振动、转动能级跃迁而产生的吸 收带,转动能级消失,谱带较宽。 • 芳香物的主要特征吸收带 • Λ= 230~270 nm, 具有精细结构 • ε~200
• 极性溶剂中,或苯环连有取代基
时,其精细结构消失
三、紫外-可见光谱中的常见吸收带
4、E带: (乙烯型ethylenic band) 由苯环环形封闭共轭体系的π→ π*跃迁产生 • 芳香族化合物的特征吸收带
三、紫外-可见光谱中的常见吸收带
2、K带:(共轭作用konjugation))) 由共轭双键的π→ π*跃迁产生 (—CH=CH—)n, —CH=C—CO— 特点:λmax>200nm,强ε>104 共轭体系增长, ε↑, λ↑(红移)
三、紫外-可见光谱中的常见吸收带
3、B带:(苯benzenoid)
紫外-可见吸收光谱

二、影响紫外-可见吸收光谱的因素
物质的吸收光谱与测定条件有密切的关系。测定条 件(温度、溶剂极性、pH等)不同,吸收光谱的形 状、吸收峰的位置、吸收强度等都可能发生变化。
1.溶剂极性增大,导致: *跃迁,能量减少, 所以,吸收带红移, n*跃迁,能量增大, 所以,吸收带蓝移 。 精细结构逐渐消失,合并 为一条宽而低的吸收带。
(a)Lamber-Beer定律的适用条件(前提)
入射光为单色光,均匀非散射的稀溶液 该定律适用于均匀非散射固体、液体和气体样品 在同一波长下,各组分吸光度具有加和性
A=A1+A2++An
4.2定量分析的方法
(1)标准曲线法:预先配 制一系列不同浓度的标 准溶液,以不含待测组 分的空白溶液作参比。 测定标准溶液的吸光度, 描绘出吸光度-浓度的标 准曲线。根据在同等条 件下测定的样品的吸光 度,即可从标准曲线上 求得未知样品的浓度。
浅色位移:由于基团取代或溶剂效应,最大吸收波 长变短。浅色位移亦称为蓝移。
增色效应:使吸收强度增加的效应。 减色效应:使吸收强度减小的效应。 摩尔吸收系数():物质在浓度为1mol/L、液层
厚度为1cm时溶液的吸光度。
5. 无机化合物的紫外-可见吸收光谱
1. f电子跃迁吸收光谱
镧系和锕系元素的离子对紫外和可见光的吸收是基 于内层f电子的跃迁而产生的。其紫外可见光谱为 一些狭长的特征吸收峰,这些峰几乎不受金属离子 的配位环境的影响。
3. 有机化合物的结构推测
化合物的紫外吸收光谱基本上是分子中发色基团和助色基 团的特性,而不是整个分子的特性,所以单独从紫外吸收光 谱不能完全确定化合物的分子结构,必须与IR、NMR、MS及 其它方法配合,才能得出可靠的结论。紫外光谱在研究化合 物的结构中的主要作用是推测官能团、结构中的共轭体系以 及共轭体系中的取代基的位置、种类和数目等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C=S,-N
O O
(共轭双键)
一些含有n电子的基团,本身没有生色功能,但当 它们与生色团相连时,就会发生n—π共轭作用,增 强生色团的生色能力,这样的基团称为助色团。
: : :
助色团:-NH2,-OH,-X (孤对电子)等
2
:
红移和蓝移
3
有机化合物的紫外光谱解析
了解共轭程度、空间效应、氢键等;可对饱和与不饱 和化合物、异构体及构象进行判别。 ⑴ 在200~750nm波长范围内若无吸收峰,则可能是 直链烷烃、环烷烃、饱和脂肪族化合物或仅含一个双 键的烯烃等。若有低强度吸收峰(ε=10~100 L·mol1·cm-1),(n→π跃迁),则可能含有一个简单非共轭且 含有n电子的生色团,如羰基。 ⑵ 若在250~300 nm波长范围内有中等强度的吸收峰 则可能含苯环。
滴定剂与待 测物均吸收
产物吸收
Vsp
Vsp
24
8.5.4 络合物组成的测定
1. 摩尔比法: 固定cM ,改变cR
A
1:1 1.0 2.0
3:1 3,0 c(R)/c(M)
25
2. 等摩尔连续变化法:
M:R=1:1
cM + cR = c(常数)
M:R=1:2
0.5 cM/c cM/c
0 0.2 0.4 0.6 0.8 1 0 0.2 0.4
6
电荷转移吸收光谱
分子中金属离子轨道上的电荷吸收光能后转移到 配体的轨道上,或按反方向转移,这种跃迁称为电 荷转移跃迁,所产生的吸收光谱称为荷移光谱。 本质上属于分子内氧化还原反应 ε一般都较大(104左右),适于微量金属的检测 例:Fe3+与SCN-形成血红色配合物,在490 nm处 有强吸收峰。其实质是发生了如下反应: [Fe3+-SCN-]2+ +hν= [Fe2+-SCN]2+
13
[FeR3 ] lg [Fe′]
pH3~8为适宜 的酸度范围
14
3. 显色温度及显色时间 (c(M)、 c(R) 、 pH一定)
A 50℃
25℃
另外,还有介 质条件、有机 溶剂、表面活 性剂等.
t /min
15
8.4.3 测定中的干扰以及消除方法
1.化学法
测Co2+ :(掩蔽法) Co2+, Fe3+ (2)Sn2+ ⑴NaF Co2+ SCN- Co(SCN)2 (蓝) 3FeF6 SCN- Co(SCN)2
磷钼黄(ε小) Sn2+ 磷钼(V)蓝(ε大)
20
3. 蛋白质测定—溴甲酚绿、考马司亮蓝等 4. 氨基酸测定—茚三酮(紫色化合物) 5. 水质检测: NH4+、NO2-、Mn2+、Fe2+、 SO42-、Hg2+---6. 药物含量测定—比吸光系数定量;荷移 光谱法测定. 7. 紫外吸收(UV): NO2-、NO3-、SO42-、 SO32-、CO32-、SCN-、酪氨酸、色氨 酸、苯丙氨酸、蛋白质等。
8.4.1 显色剂与显色反应
无机显色剂: SCN- ,(NH4)2MoO4 有机显色剂: (p386 附录II.5)
邻二 氮菲
N N OH N OH
PAR
N
N
NH NH N
S N
双硫腙
9
显色反应的选择
灵敏度高,一般ε>10 4; 选择性好; 显色剂在测定波长处无明显吸收, 对照性好, ∆λmax> 60 nm; 反应生成的有色化合物组成恒定,稳定; 显色条件易于控制,重现性好.
5 4 3 2 1
由每份溶液的一 对pH、A,可求 得一个Ka, 取平 均值即可.
Ab (L) 550 600
28
350
Aa 400 450 500
λ/nm
习 题
8.5 (不要求计算桑德尔灵敏度) 8.8 8.11
29
4
(3)若在210~250 nm波长范围内有强吸收峰, 则可能含有2个共轭双键;若在260~300 nm波长 范围内有强吸收峰,则说明该有机物含有3个或3个 以上共轭双键。 (4)若该有机物的吸收峰延伸至可见光区,则该 有机物可能是长链共轭或稠环化合物。
5
2.金属配合物的紫外-可见吸收光谱
金属配合物的生色机理主要有三种类型: ⑴ 配体微扰的金属离子d-d电子跃迁和f-f电子跃 迁: ε很小,对定量分析意义不大 ⑵ 金属离子微扰的配体内电子跃迁 与成键性质有关,若静电引力结合,变化一般很 小。若共价键和配位键结合,则变化非常明显。 ⑶电荷转移吸收光谱 在分光光度法中具有重要意义
10
8.4.2 显色条件的确定
1. 显色剂用量(c(M)、pH一定)
c(R)
Mo(SCN)32+ 浅红 Mo(SCN)5 橙红 Mo(SCN)6- 浅红
c(R)
c(R)
Fe(SCN)n3-n
11
2. 显色反应酸度(c(M)、 c(R)一定)
pH pH1<pH<pH2
12
邻二氮菲-亚铁反应完全度与pH的关系 Fe2++3R
0.33
0.6 0.8 1
M + nR
MR n
26
8.5.5 一元弱酸离解常数的测定;][L]/[HL]
高酸度下,几乎全部以HL存在,可测得AHL=εHL·c(HL); 低酸度下,几乎全部以L存在,可测得AL =εL·c(HL). 代入整理:
配制一系列c相同,pH不同的溶液,测A. ε HL ⋅[H+]⋅ c(HL) ε L ⋅ K a ⋅ c(HL) A=ε HL [HL]+ε L [L] = + + K a +[H ] K a +[H+]
Co2+ Fe2+,Sn4+
16
测Co2+ :(生成络合物性质不同) Co2+, Zn2+, Ni2+, Fe2+ 测Fe3+:(控制pH) Fe3+, Cu2+
pH= 2.5 钴试剂R
CoR,ZnR NiR,FeR
H+
CoR, Zn2+ , Ni2+ , Fe2+
SSal
FeSSal(紫红) Cu2+
如不能通过控制酸度和掩蔽的办法消除干 扰,则需采取分离法。
17
2. 物理法—选择适当的测定波长
钍-偶氮砷III A 试剂 络合物 络合物 试剂 A 钴-亚硝基红盐
515
655
415
500
λ/nm
λ/nm
18
选择适当的参比溶液
1. 仅络合物有吸收,溶剂作参比。 如 phen—Fe2+ 标准曲线 2.显色剂或其他试剂有吸收,试剂空白作参比。 例:邻二氮菲光度法测Li2CO3中的 Fe, 参比溶液为不含Li2CO3样品的所有试剂。 3.待测液有吸收,试样空白作参比。 如测汽水中的 Fe 4.干扰组分与显色剂有反应,又无法掩蔽消除时:
AH
+
β3
H+
OH-
FeR3
β3=1021.3
c(R)≈[R´]=10-4mol·L-1
[FeR 3 ] β3 β 3′ = = 3 [Fe ′][R ′] α Fe(A) ⋅ α 3 R(H)
[FeR 3 ] lg = lg β 3 − lg α Fe(A) − 3lg α R(H) + 3lg[R′] [Fe′]
[L]
K
a
=
AH L - A
A- A
或 pK a = pH + lg A - A HL [H + ]
27
A- A L
L
[HL]
MO吸收曲线
曲线 1 2 3 4 5 6 pH 1.10, 1.38 2.65 3.06 3.48 3.98 5.53,6.80
A
1 2 3 4 5 6
Aa(HL)
Ab 6
1)掩蔽被测组分,再加入显色剂,作参比. 2)加入等量干扰组分到空白溶液中,作参比.
19
8.5 吸光光度法的应用
8.5.1 单一组分的测定
1. 金属离子: Fe-phen, Ni-丁二酮肟, Co-钴试剂 2. 磷的测定: DNA中含P~9.2%, RNA中含P~9.5%, 可得核酸量.
H3PO4+12(NH4)2MoO4+21HNO3 =(NH4)3PO4·12MoO3+12NH4NO3+12H2O
1.有机化合物的紫外-可见吸收光谱 σ电子、π电子、n电子。
当外层电子吸收紫外或可见辐射后,就从基态向激 发态(反键轨道)跃迁。主要有四种跃迁,所需能量 ΔΕ大小顺序为: n→π* < π→π* < n→σ* < σ→σ*
1
有机物分子具有紫外-可见光吸收性质的必 要条件:分子中含有不饱和基团。 含有π键的不饱和基团称为生色团, 生色团:-N=N-,-N=O,
7
朗伯-比尔定律
ε =A/bc (L·mol-1·cm-1)
A= ε b c
吸收物质在一定波长和溶剂条件下的特征 常数; 不随浓度c和光程长度b的改变而改变。在 温度和波长等条件一定时,ε仅与吸收物质 本身的性质有关。 反映了光度法测定该物质可能达到的最大 灵敏度。
8
8.4 显色反应与分析条件的选择
22
8.5.3 光度滴定
NaOH滴定 对硝基酚 pKa=7.15 间硝基酚 pKa=8.39 ∆ pKa=1.24
间硝基酚
酸形均 无色. 碱形均 黄色
对硝基酚
V1 V2 V(NaOH)/mL
23
典型的光度滴定曲线
依据滴定过程中溶液吸光度变化来确定终点的滴定分析方法。
滴定剂吸收
O O
(共轭双键)
一些含有n电子的基团,本身没有生色功能,但当 它们与生色团相连时,就会发生n—π共轭作用,增 强生色团的生色能力,这样的基团称为助色团。
: : :
助色团:-NH2,-OH,-X (孤对电子)等
2
:
红移和蓝移
3
有机化合物的紫外光谱解析
了解共轭程度、空间效应、氢键等;可对饱和与不饱 和化合物、异构体及构象进行判别。 ⑴ 在200~750nm波长范围内若无吸收峰,则可能是 直链烷烃、环烷烃、饱和脂肪族化合物或仅含一个双 键的烯烃等。若有低强度吸收峰(ε=10~100 L·mol1·cm-1),(n→π跃迁),则可能含有一个简单非共轭且 含有n电子的生色团,如羰基。 ⑵ 若在250~300 nm波长范围内有中等强度的吸收峰 则可能含苯环。
滴定剂与待 测物均吸收
产物吸收
Vsp
Vsp
24
8.5.4 络合物组成的测定
1. 摩尔比法: 固定cM ,改变cR
A
1:1 1.0 2.0
3:1 3,0 c(R)/c(M)
25
2. 等摩尔连续变化法:
M:R=1:1
cM + cR = c(常数)
M:R=1:2
0.5 cM/c cM/c
0 0.2 0.4 0.6 0.8 1 0 0.2 0.4
6
电荷转移吸收光谱
分子中金属离子轨道上的电荷吸收光能后转移到 配体的轨道上,或按反方向转移,这种跃迁称为电 荷转移跃迁,所产生的吸收光谱称为荷移光谱。 本质上属于分子内氧化还原反应 ε一般都较大(104左右),适于微量金属的检测 例:Fe3+与SCN-形成血红色配合物,在490 nm处 有强吸收峰。其实质是发生了如下反应: [Fe3+-SCN-]2+ +hν= [Fe2+-SCN]2+
13
[FeR3 ] lg [Fe′]
pH3~8为适宜 的酸度范围
14
3. 显色温度及显色时间 (c(M)、 c(R) 、 pH一定)
A 50℃
25℃
另外,还有介 质条件、有机 溶剂、表面活 性剂等.
t /min
15
8.4.3 测定中的干扰以及消除方法
1.化学法
测Co2+ :(掩蔽法) Co2+, Fe3+ (2)Sn2+ ⑴NaF Co2+ SCN- Co(SCN)2 (蓝) 3FeF6 SCN- Co(SCN)2
磷钼黄(ε小) Sn2+ 磷钼(V)蓝(ε大)
20
3. 蛋白质测定—溴甲酚绿、考马司亮蓝等 4. 氨基酸测定—茚三酮(紫色化合物) 5. 水质检测: NH4+、NO2-、Mn2+、Fe2+、 SO42-、Hg2+---6. 药物含量测定—比吸光系数定量;荷移 光谱法测定. 7. 紫外吸收(UV): NO2-、NO3-、SO42-、 SO32-、CO32-、SCN-、酪氨酸、色氨 酸、苯丙氨酸、蛋白质等。
8.4.1 显色剂与显色反应
无机显色剂: SCN- ,(NH4)2MoO4 有机显色剂: (p386 附录II.5)
邻二 氮菲
N N OH N OH
PAR
N
N
NH NH N
S N
双硫腙
9
显色反应的选择
灵敏度高,一般ε>10 4; 选择性好; 显色剂在测定波长处无明显吸收, 对照性好, ∆λmax> 60 nm; 反应生成的有色化合物组成恒定,稳定; 显色条件易于控制,重现性好.
5 4 3 2 1
由每份溶液的一 对pH、A,可求 得一个Ka, 取平 均值即可.
Ab (L) 550 600
28
350
Aa 400 450 500
λ/nm
习 题
8.5 (不要求计算桑德尔灵敏度) 8.8 8.11
29
4
(3)若在210~250 nm波长范围内有强吸收峰, 则可能含有2个共轭双键;若在260~300 nm波长 范围内有强吸收峰,则说明该有机物含有3个或3个 以上共轭双键。 (4)若该有机物的吸收峰延伸至可见光区,则该 有机物可能是长链共轭或稠环化合物。
5
2.金属配合物的紫外-可见吸收光谱
金属配合物的生色机理主要有三种类型: ⑴ 配体微扰的金属离子d-d电子跃迁和f-f电子跃 迁: ε很小,对定量分析意义不大 ⑵ 金属离子微扰的配体内电子跃迁 与成键性质有关,若静电引力结合,变化一般很 小。若共价键和配位键结合,则变化非常明显。 ⑶电荷转移吸收光谱 在分光光度法中具有重要意义
10
8.4.2 显色条件的确定
1. 显色剂用量(c(M)、pH一定)
c(R)
Mo(SCN)32+ 浅红 Mo(SCN)5 橙红 Mo(SCN)6- 浅红
c(R)
c(R)
Fe(SCN)n3-n
11
2. 显色反应酸度(c(M)、 c(R)一定)
pH pH1<pH<pH2
12
邻二氮菲-亚铁反应完全度与pH的关系 Fe2++3R
0.33
0.6 0.8 1
M + nR
MR n
26
8.5.5 一元弱酸离解常数的测定;][L]/[HL]
高酸度下,几乎全部以HL存在,可测得AHL=εHL·c(HL); 低酸度下,几乎全部以L存在,可测得AL =εL·c(HL). 代入整理:
配制一系列c相同,pH不同的溶液,测A. ε HL ⋅[H+]⋅ c(HL) ε L ⋅ K a ⋅ c(HL) A=ε HL [HL]+ε L [L] = + + K a +[H ] K a +[H+]
Co2+ Fe2+,Sn4+
16
测Co2+ :(生成络合物性质不同) Co2+, Zn2+, Ni2+, Fe2+ 测Fe3+:(控制pH) Fe3+, Cu2+
pH= 2.5 钴试剂R
CoR,ZnR NiR,FeR
H+
CoR, Zn2+ , Ni2+ , Fe2+
SSal
FeSSal(紫红) Cu2+
如不能通过控制酸度和掩蔽的办法消除干 扰,则需采取分离法。
17
2. 物理法—选择适当的测定波长
钍-偶氮砷III A 试剂 络合物 络合物 试剂 A 钴-亚硝基红盐
515
655
415
500
λ/nm
λ/nm
18
选择适当的参比溶液
1. 仅络合物有吸收,溶剂作参比。 如 phen—Fe2+ 标准曲线 2.显色剂或其他试剂有吸收,试剂空白作参比。 例:邻二氮菲光度法测Li2CO3中的 Fe, 参比溶液为不含Li2CO3样品的所有试剂。 3.待测液有吸收,试样空白作参比。 如测汽水中的 Fe 4.干扰组分与显色剂有反应,又无法掩蔽消除时:
AH
+
β3
H+
OH-
FeR3
β3=1021.3
c(R)≈[R´]=10-4mol·L-1
[FeR 3 ] β3 β 3′ = = 3 [Fe ′][R ′] α Fe(A) ⋅ α 3 R(H)
[FeR 3 ] lg = lg β 3 − lg α Fe(A) − 3lg α R(H) + 3lg[R′] [Fe′]
[L]
K
a
=
AH L - A
A- A
或 pK a = pH + lg A - A HL [H + ]
27
A- A L
L
[HL]
MO吸收曲线
曲线 1 2 3 4 5 6 pH 1.10, 1.38 2.65 3.06 3.48 3.98 5.53,6.80
A
1 2 3 4 5 6
Aa(HL)
Ab 6
1)掩蔽被测组分,再加入显色剂,作参比. 2)加入等量干扰组分到空白溶液中,作参比.
19
8.5 吸光光度法的应用
8.5.1 单一组分的测定
1. 金属离子: Fe-phen, Ni-丁二酮肟, Co-钴试剂 2. 磷的测定: DNA中含P~9.2%, RNA中含P~9.5%, 可得核酸量.
H3PO4+12(NH4)2MoO4+21HNO3 =(NH4)3PO4·12MoO3+12NH4NO3+12H2O
1.有机化合物的紫外-可见吸收光谱 σ电子、π电子、n电子。
当外层电子吸收紫外或可见辐射后,就从基态向激 发态(反键轨道)跃迁。主要有四种跃迁,所需能量 ΔΕ大小顺序为: n→π* < π→π* < n→σ* < σ→σ*
1
有机物分子具有紫外-可见光吸收性质的必 要条件:分子中含有不饱和基团。 含有π键的不饱和基团称为生色团, 生色团:-N=N-,-N=O,
7
朗伯-比尔定律
ε =A/bc (L·mol-1·cm-1)
A= ε b c
吸收物质在一定波长和溶剂条件下的特征 常数; 不随浓度c和光程长度b的改变而改变。在 温度和波长等条件一定时,ε仅与吸收物质 本身的性质有关。 反映了光度法测定该物质可能达到的最大 灵敏度。
8
8.4 显色反应与分析条件的选择
22
8.5.3 光度滴定
NaOH滴定 对硝基酚 pKa=7.15 间硝基酚 pKa=8.39 ∆ pKa=1.24
间硝基酚
酸形均 无色. 碱形均 黄色
对硝基酚
V1 V2 V(NaOH)/mL
23
典型的光度滴定曲线
依据滴定过程中溶液吸光度变化来确定终点的滴定分析方法。
滴定剂吸收
