微生物菌剂质检报告单
微生物限度检查记录表格

乳糖胆盐发酵培养基(18~
24h)
EMB培养基(18~24h)
(批号:)
乳糖发酵培养基(24~
48h)
供
试
品
10-
(批号:)
(批号:)
1-
10
2-
10
3
阴性对照
阳性对照
结果
个/g(规定:<个/
微生物限度检查(根据需要在表头补充产品名称、批号,日期等)
供试液制备
取供试品g,加入pH7.0无菌氯化钠-蛋白胨缓冲液至ml,混匀。
供试液制备
取供试品g,加入pH7.0无菌氯化钠-蛋白胨缓冲液至ml,混匀。
□研钵法□振摇法
细菌、霉菌和酵母菌计数□
平皿
号
细菌数(30~35℃3天)
营养琼脂培养基(批号:)
霉菌和酵母菌数(23~28℃5天)
玫瑰红钠琼脂培养基(3
10-4
阴性对照
10-1
10-2
阴性对照
1
2
□研钵法□振摇法
细菌、霉菌和酵母菌计数□
平皿
号
细菌数(30~35℃3天)
营养琼脂培养基(批号:)
霉菌和酵母菌数(23~28℃5天)
玫瑰红钠琼脂培养基(批号:)
10-1
10-2
10-3
10-4
阴性对照
10-1
10-2
阴性对照
1
2
平均
结果
cfu/g(规定:≤cfu/g)
cfu/g(规定:≤cfu/g)
大肠埃希菌检查□培养条件:30~35℃18~24h
平均
结果
cfu/g(规定:≤cfu/g)
cfu/g(规定:≤cfu/g)
如何正确解读微生物报告单

3. 培养阳性报告单中出现以下大些英文缩写具体代 表什末?有何临床意义? MRS:耐甲氧西林葡萄球菌。其中MRSA是耐甲 氧西林金黄色葡萄球菌;MRSE是耐甲氧西林表皮葡 萄球菌;MRCNS是耐甲氧西林凝固酶阴性葡萄球菌。 提示所有β-内酰胺类抗生素均呈耐药,同时对红霉素、 四环素类、磺胺类、庆大霉素和链霉素等氨基糖甙类 及氟喹诺酮类同时耐药,建议使用糖肽类抗生素如万 古霉素、替考拉宁等或垩唑烷类如利奈唑胺进行治疗。
7.大便培养阴性报告怎麽理解? 大便培养阴性我们一般报告“无沙门、无志 贺、无金黄色葡萄球菌、无真菌生长”,因为我 们的大便培养一般只作上述四类细菌的分离鉴定, 所以培养阴性结果只能排除上述四类致病菌。如 需培养其他致病菌需在培养前与实验室联系。大 便厌氧培养阴性我们一般报告“无厌氧梭状芽孢 杆菌生长”,因为大便里面本来就含有大量厌氧 菌,多为一些无芽孢的正常菌群如乳酸杆菌、双 歧杆菌等,我们会在接种之前经过加热破坏掉无 芽孢的细菌,主要培养可引起肠道感染的厌氧梭 状芽孢杆菌。现在咱们实验室无条件开展厌氧菌 培养。
如何正确解读微生物报告单
为了临床工作者能正确解读微生物报告单,我 对我科微生物报告单作简单介绍:
1、微生物报告分几种类型? 我们的微生物报告主要分三种: 培养阳性报告、培养阴性报告及涂片报告。 2、培养阳性报告主要类型? 为什麽培养阳性有的有药敏结果,有的没有药敏结果?
培养阳性报告主要分有药敏结果和 无药敏结果的报告。有药敏结果的报告 时认为该菌为明确致病菌、不排除为致 病菌、院内感染重要病原菌、数量达到 致病菌判读标准、有明确药敏判读标准。
13.为何药敏试验结果有时出现判断结果修改现象? 有时会出现某药物K-B法按正常判读标准应该为 “S”或“R”,但报告结果与之不符,这种现象一般 有两种原因:一是我们在检测过程中发现了某种耐药 机制而修改;二是我们观察到某种药物检测结果可能 不可靠,并通过多种方法验证后作出修改。
微生物限度检验记录表
霉菌、酵母菌数
(玫瑰红钠琼脂培养基
23~28℃培养72小时)
备注
原液
10-1
10-2
10-3
10-4
原液
10-1
10-2
10-3
1
2
3
平均值
菌落数
(个/ml)
二、控制菌检查
阴性对照液:稀释液
阳性对照液:供试液+阳性菌落
大肠埃希菌检查
1 2 3 4 5
BL.增菌MUG-靛基质试液曙红亚甲蓝或Macc平板染色镜检IMVic
文件编号
使用编号
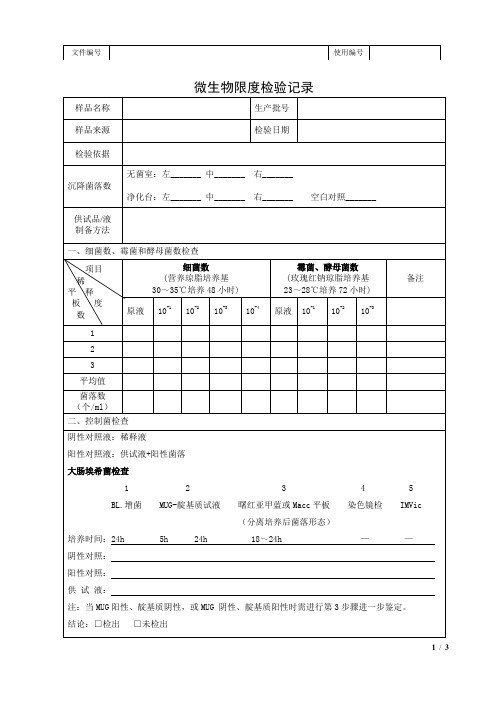
微生物限度检验记录
样品名称
生产批号
样品来源
检验日期
检验依据
沉降菌落数
无菌室:左_______中_______右_______
净化台:左_______中_______右_______空白对照_______
供试品/液
制备方法
一、细菌数、霉菌和酵母菌数检查
项目
基
结论:□检出□未检出
结果分析
结论
□(均)符合规定□(均)不符合规定
检验:审核:复核:日期:
阴性对照:
阳性对照:
供试品:
注:当第2步发现有菌落生长且形态与金黄色葡萄球菌疑似时需挑选2~3个菌落,分别接种于营养琼脂培养基斜面上,培养18~24小时,再进行第3步骤进一步鉴定。
结论:□检出□未检出
铜绿假单胞菌检查
1 2 3 4 5
BL增菌溴化十六烷基三甲铵平板革兰氏染色镜检氧化酶试验绿脓菌素试验
培养时间:24h24h———
阴性对照:
阳性对照:
供试品:
注:当第2步发现有菌落生长且形态与铜绿假单胞菌疑似时需挑选2~3个菌落,分别接种于营养琼脂培养基斜面上,培养18~24小时,再进行第3步骤进一步鉴定。
丁酸梭菌水环境修复剂质检报告

丁酸梭菌水环境修复剂质检报告
本报告对丁酸梭菌水环境修复剂进行质量检测,以评估其性能和安全性。
一、产品描述
丁酸梭菌水环境修复剂是一种微生物制剂,主要成分是丁酸梭菌。
该产品主要用于修复水体中的污染物质,提高水质。
二、质量检测项目
1.外观:产品应为深棕色液体,无沉淀和杂质。
2.活性成分:丁酸梭菌含量应符合产品标签上的规定。
3.微生物含量:产品应无致病菌和寄生虫。
4.重金属含量:产品中重金属含量应符合相关标准。
5.稳定性:产品应在标签上标注的储存条件下保持稳定。
三、检测结果
1.外观:产品为深棕色液体,无沉淀和杂质。
2.活性成分:丁酸梭菌含量为9.5×10^8 CFU/mL,符合标签上的规定。
3.微生物含量:产品中未检测到致病菌和寄生虫。
4.重金属含量:产品中重金属含量符合相关标准。
5.稳定性:产品在标签上标注的储存条件下保持稳定。
四、结论
根据检测结果,该丁酸梭菌水环境修复剂符合质量标准,可以安全使用于水环境修复。
微生物分析检测报告模板

广东省微生物分析检测报告CUANNGONG DETECTION CENITE OF MICROBIOLOGY分析检测报告REPORT FOR ANAL YSIS样品名称Name of Sample委托单位Customer委托登记号Sample Receipt NO.检测地点Place for Analysis地址:Address:邮政编码:Postcode :电话及传真号码:Tel&Fax:广东省微生物分析检测报告CUANNGONG DETECTION CENITE OF MICROBIOLOGY分析检测报告REPORT FOR ANAL YSIS样品名称接样方式及数量Name of Sample Way and Quantity of Reception 样品规格及批号样品状态和特性Specification and Group Number of Sample State and Charactcristic委托单位接样日期Customer Date for Sample Supplyine检测项目检测日期Item of Analysis Date for Analysis委托登记号签发日期Sample Receipt NO. Date for Repoeting检验依据和分析方法Standard and Methods分析检测结果编审:批准:盖章:Checker Technique Controller Official Seal职务:高级工程师职务:工程师Business:Senior engineer Business:Engineer。
微生物检测报告

微生物检测报告微生物检测报告一、检测目的与方法本次检测目的是为了评估环境中微生物的种类和数量,并综合判断是否存在潜在的健康风险。
采用了标准的培养基方法进行微生物的定性和定量检测。
二、检测结果经过检测,我们发现环境中存在多种微生物,包括细菌、真菌和酵母菌等。
其中,细菌是数量最多的微生物,共有5个菌落形成单位(cfu)/mL。
主要的细菌种类包括大肠杆菌、金黄色葡萄球菌和假单胞菌等。
真菌和酵母菌的数量相对较少,分别为2个cfu/mL和1个cfu/mL。
三、结果分析1. 细菌:大肠杆菌是一种潜在的病原菌,通常在人和动物的肠道中存在,过多的大肠杆菌可能导致肠道感染和食物中毒等。
金黄色葡萄球菌是一种属于常微生物的细菌,它通常存在于皮肤和黏膜上,过多的金黄色葡萄球菌可能引发感染并导致皮肤疾病等。
假单胞菌是一种常见的土壤和水中微生物,一般情况下对人体无害,但过多的假单胞菌会增加感染的风险。
2. 真菌和酵母菌:真菌和酵母菌通常在自然环境中广泛存在,但过多的真菌和酵母菌可能导致室内空气质量下降和可能的感染风险。
综上所述,根据本次检测结果,目前环境中的微生物数量在安全范围内,不会造成明显的健康风险。
但仍建议定期对环境进行检测,采取相应的卫生保健措施,确保环境的卫生状况。
四、建议措施1. 加强清洁措施:定期对环境进行清洁,包括地面、墙壁、家具和设备等。
选择合适的清洁剂,确保有效杀灭微生物。
2. 保持通风良好:保持室内空气流通,有助于减少微生物的滋生和传播。
在天气条件允许的情况下,可以打开窗户或安装通风设备。
3. 健康饮食习惯:加强个人卫生,避免食品交叉污染和食品中毒的风险。
定期清洁和消毒厨房设备和工具。
4. 定期检测:定期对环境进行微生物检测,及时发现和解决潜在的卫生问题。
五、结论本次检测结果显示环境中存在一定数量的微生物,但未发现明显的健康风险。
通过加强清洁措施、保持通风良好和健康饮食习惯等措施,可以有效控制微生物的滋生和传播,确保环境的卫生状况。
微生物检验检测报告(六).
SMAC:
DFI:
显色培养基:
镜检:
氧化酶:
TSI:TSA:
色素:
VITEK:
API 20E:
菌种号:
VRBGA:SMAC:
DFI:TSA:镜检:
氧化酶:TSI:色素:
VITEK:
API 20E:
未检出100g
检出100g
检验员:复核:年月日
XLD:HE:BS:
显色平板:镜检:
氧化酶:TSI:URE:
VITEK:
API 20E:
血清学检验:
未检出25g
检出25g
单增李斯特氏菌
□GB 89.30-2010
□SN/T 0184.1-2005
培养箱:
取样量:g
LB1:LB2:
FB1: FB2:
PAL:
OXA:
显色培养基:
镜检:
触酶:
溶血:
EMB:
CT-SMAC:
显色培养基:
镜检:
氧化酶:TSI:
VITEK:
API:
血清学检验:
菌种号:
麦康凯:镜检:氧化酶:
VITEK:
API:
血清学检验:
未检出
检出
阪崎肠杆菌
□GB 4789.40-2010
□SN/T 1632.1-2005
培养箱:
取样量:g
45℃蒸馏水:
肠道菌增菌液:
44℃BPW:
mLST-Vm:
乳制品微生物检验记录表(六)
报验编号:样品名称:检验日期:年月日
培养箱
⑴200244Bf0020-1;⑵200244Bf0020-2;⑶200244Bf0041-1;⑷200244Bf0041-2;⑸200244Bf0019-1;⑹200244Bf0019-2;⑺199944BfW004;⑻199644Bf5019;⑼200844Cf0186;⑽200044Bf0020。
2017年3月微生物报告单
采样日期报告日期
1胃镜室<1cfu/c㎡ 未检出 未检出 未检出2胃镜室<1cfu/c㎡ 未检出 未检出 未检出3胃镜室<1cfu/c㎡ 未检出 未检出 未检出4胃镜室<1cfu/c㎡ 未检出 未检出 未检出5胃镜室<1cfu/c㎡ 未检出 未检出 未检出6胃镜室<1cfu/c㎡ 未检出
未检出 未检出
7口腔科10cfu/c㎡ 未检出 未检出 未检出8供应室<1cfu/c㎡ 未检出 未检出 未检出9供应室<1cfu/c㎡ 未检出 未检出 未检出10妇产科
<1cfu/c㎡ 未检出 未检出 未检出11妇产科<1cfu/c㎡ 未检出 未检出 未检出12妇产科<1cfu/c㎡ 未检出
未检出 未检出
13妇产科<1cfu/c㎡ 未检出 未检出 未检出14妇产科<1cfu/c㎡ 未检出 未检出 未检出15手术室<1cfu/c㎡ 未检出 未检出 未检出16手术室3cfu/c㎡
未检出
未检出 未检出17手术室86cfu/c㎡ 未检出
未检出 未检出
18
手术室
<1cfu/c㎡ 未检出 未检出 未检出
报告者:董梅
采样者:沈君华
医生刘东翠手护士吉勾尔良手万级间器械台百级间手术床无菌物品置物架马晶晶外科洗手
李七一手俄木尔里手无菌物品下送车隔离产房接生床隔离产房辐射接生台1产房无影灯初洗槽次洗槽干燥台末洗槽内窥镜储镜柜检测项目:染菌量、金黄色葡萄球菌、溶血性链球菌、大肠杆菌、沙门氏菌方法依据:消毒技术规范(2012)美姑县人民医院检验报告(复查)
样品名称:物表、手、消毒液、无菌物品2017年3月21日检毕日期:
2017年3月21日
2017年3月24日。
微生物检测表
签收确认
广州华侬化妆品有限公司 员工手部、灌装间机器及工作台面微生物检测报告 版本:A/0
温度℃: 采样时间及日期: 员工姓名 工作内容
湿度%: 采样地点
细菌总数 (CFU/只手)
检验日期:
霉菌 (CFU/只手)
结果判定
企业: 员工手部细菌检测标准≤300cfu/只手, 霉菌不得检出。 机器设备内表面细菌 ≤10 cfu/100 cm2,霉菌不得检出。 工作台及机器表面细菌菌落数应≤20 cfu/ cm2,霉菌不得检出。 附则说明:采样方法、检验方法参照GB15979-2002《一次性使用卫生用品卫生标准》。 检测人员: 检测报告日期: 生产副总 技术部 审核: 生产主管 审核日期: 灌装班长 灌装QC
玉米应用微生物菌剂试验报告
微生物菌剂肥效验证试验报告(玉米)摘要:为了验证微生物菌剂,在我省不同地区对玉米的增产效果进行试验。
通过试验证明能促进玉米增产,穗大,籽粒饱满。
试验结果方差分析表明:玉米应用该微生物菌剂增产效果明显,处理1比处理4(对照)小区增3.7千克,增产率 8.2 %,差异极显著;处理2(灭活)比处理4(对照)小区增产0.2千克,增产率0.45 %,差异不显著;处理3(细沙)与处理4(对照)产量一致差异不显著。
关键词:微生物菌剂玉米施肥产量1.试验目的为验证微生物菌剂在我地区对玉米的增产效果,为大面积推广应用提供依据,特此试验。
2.材料与方法2.1供试材料微生物菌剂、玉米专用肥、尿素、玉米品种:福园2号2.2试验布置2.2.1试验地点:2.2.2试验时间:2012年3月—11月2.2.3试验执行人:2.2.4试验设计采用小区试验方法,4个处理,三次重复,每小区采用6行区,行长10米,面积42平方米,各小区随机排列。
2.2.4.1试验处理处理1:常规施肥(亩施20公斤玉米专用肥底肥,10公斤尿素于6-8叶期做追肥。
)+微生物菌剂0.5kg/亩。
处理2:常规施肥(亩施20公斤玉米专用肥底肥,10公斤尿素于6-8叶期做追肥。
)+微生物菌剂(灭活)0.5kg/亩。
处理3:常规施肥(亩施20公斤玉米专用肥底肥,10公斤尿素于6-8叶期做追肥。
)+与处理1同期等量喷施清水。
处理4(对照):常规施肥(亩施20公斤玉米专用肥底肥,10公斤尿素于6-8叶期做追肥。
)小区排列图2.2.5试验地基本情况试验地基本情况及土壤农化性状见下表。
试验地基本情况地形土壤类型质地前茬作物PH值有机质(%)碱解氮(ppm)有效磷(ppm)速效钾(ppm)平地黑土中壤玉米 6.2 3.86 262.1 42.5 137.93.结果与分析3.1微生物菌剂对玉米生育进程的影响田间调查表明,各处理间的生育期没有差异,见下表。
生育期调查表单位:月日播种期出苗期拔节期抽雄期成熟期处理1 5.6 5.19 6.28 8.18 9.23处理2 5.6 5.19 6.28 8.18 9.23处理3 5.6 5.19 6.28 8.18 9.23处理4 5.6 5.19 6.28 8.18 9.233.2微生物菌剂对玉米产量的影响3.2.1秋后考种,详见下表:处理重复株高cm株数/平方米穗数/平方米粒数/穗百粒重g籽粒重/穗g小区产量千克增产千克增产%1 1 248 5.1 5.1 620.2 36.2 224.5 48.12 245 5.1 5.1 634.6 36.2 229.7 49.23 251 5.1 5.1 622.6 36.2 225.3 48.3平均248 5.1 5.1 625.8 36.2 226.5 48.5 3.7 8.22 1 248 5.1 5.1 580.1 36.1 209.4 44.82 252 5.1 5.1 580.2 36.1 209.5 44.93 244 5.1 5.1 584.8 36.1 211.1 45.2平均248 5.1 5.1 581.7 36.1 210.0 45.0 0.2 0.453 1 251 5.1 5.1 572.6 36.1 206.7 44.32 248 5.1 5.1 584.7 36.1 211.1 45.23 245 5.1 5.1 583.6 36.1 210.7 45.1平均248 5.1 5.1 580.3 36.1 209.5 44.8 0 04 1 241 5.1 5.1 570.6 36.1 206 44.12 248 5.1 5.1 582.6 36.1 210.3 45.03 255 5.1 5.1 587.4 36.1 212.1 45.4 平均248 5.1 5.1 580.2 36.1 209.4 44.83.2.2进行方差分析微生物菌剂不同处理小区产量汇总单位:千克1 2 3 4 总数处理重复Ⅰ48.1 44.8 44.3 44.1 181.3Ⅱ49.2 44.9 45.2 45.0 184.3Ⅲ48.3 45.2 45.1 45.4 184.0总数145.6 134.9 134.6 134.5 549.6 微生物菌剂试验不同处理间方差分析处理观测数求和平均方差1 3 145.6 48.53333 0.3433332 3 134.9 44.96667 0.0433333 3 134.6 44.86667 0.2433334 3 134.5 44.83333 0.443333方差分析差异源SS df MS F P-value F crit组间29.91333 3 9.971111 37.15942 4.81E-05 4.066181 组内 2.146667 8 0.268333总计32.06 113.2.3列表对各处理的平均产量进行多重比较处理平均产量差值差异显著性α=0.05 α=0.011 48.5 3.7 a A2 45 0.2 b B3 44.8 0 b B4 44.8 b B查表知t0.05=2.306,t0.01=3.355,计算出LSD0.05=0.973,LSD0.01=1.416,而3.7>1.416,0.2<0.973。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2.5蛔虫卵死亡率不符合技术指标;
2.6砷、镉、铅、铬、汞中任一含量不符合技术指标;
2.7有机物料腐熟剂产品中所测酶活不符合技术指标;
2.8在外观、水分、细度、pH值等检测项目中,有2项(含)以上不符合要求。
检验结论
农用微生物菌剂质量检验报告单
样品名称
批号
检验依据
GB 20287-2006
重量
采样日期
报告日期
检验报告
检测项目
国家标准
企业标准
实测值
是否合格
剂型
液体
粉剂
颗粒
有效活菌数(cfu)a,亿/g(mL)
≥
2.0
2.0
1.0
霉菌杂菌数,个/g(mL)
≤
3.0×106
3.0×106
3.0×106
杂菌率,%
≤
10.0
B判定规则
1具下列任何一条款者,均为合格产品
1.1检验结果各项技术指标均符合标准要求的产品;
1.2在产品的外观、水分、细度、pH值等检测项目中,有1项不符合要求,而其它各项技术指标符合要求的产品。
2具下列任何一条款者ห้องสมุดไป่ตู้均为不合格产品
2.1有效活菌数不符合技术指标;
2.2霉菌杂菌数不符合技术指标;
2.3杂菌率不符合技术指标;
20.0
30.0
水分,%
≤
-
35.0
20.0
细度,%
≥
-
80
80
pH值
5.0~8.0
5.5~8.5
5.5~8.5
保质期b,月
≥
3
6
6
粪大肠菌群数,个/g(mL)
≤
100
蛔虫卵死亡率,%
≥
95
砷及其化合物(以As计),mg/kg
≤
75
镉及其化合物(以Cd计),mg/kg
≤
10
铅及其化合物(以Pb计),mg/kg
≤
100
铬及其化合物(以Cr计),mg/kg
≤
150
汞及其化合物(以Hg计),mg/kg
≤
5
注:
A注解
a复合菌剂,每一种有效菌的数量不得少于0.01亿/g(mL);以单一的胶质芽胞杆菌(Bacillus mucilaginosus)制成的粉剂产品中有效活菌数不少于1.2亿/g。
b此项仅在监督部门或仲裁双方认为有必要时检测。
