08化学第四章
第四章原子吸收光谱分析3
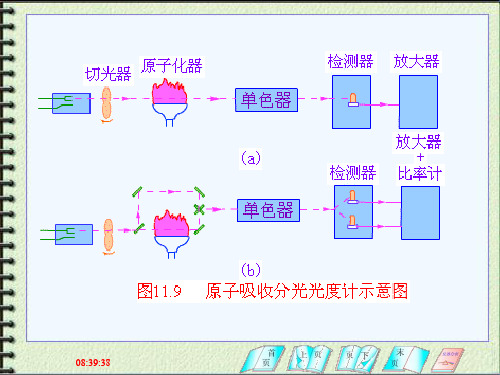
景吸收的总吸光度AT,在分析线邻近选一条非共振线, 非共振线不会产生共振吸收,此时测出的吸收为背景吸 收AB 。两次测量吸光度相减,所得吸光度值即为扣除背 景后的原子吸收吸光度值A。
AT = A + AB
A = AT - AB = k c
08:39:38
4.4.1 光谱干扰
光散射 ➢ 光散射是待测元素的吸收度增大,光散射出现在各个方
向,效果是入射光减弱,似乎被组分吸收了,因而使T 减小、A增大。 ➢ 消除:一般可用“调零”的方法消除。
08:39:38
背景干扰校正方法
背景干扰可采用仪器校正背景方法,有邻近非共振线、 连续光源、Zeeman效应等校正方法。
➢ 对于曲线斜率太小的测定,易引进较大的误差。
08:39:38
定量分析方法
(2)标准加入法
标准加入法有时只用单标准加入,即取两分相同量的被测
试液,其中一分加入一定量的标准溶液,稀释到相同体积后
测定吸光度。根据吸收定律,可得:
Ax = k Cx As = k(Cx + Cs )
Cx
Ax A0 Ax
本法适用于分析线附近背景吸收变化不大的情况, 否则准确度较差。
08:39:38
背景干扰校正方法
① 邻近非共振线校正法 参比谱线选择: ➢ 参比线与测量线很近(保证二者经过的背景一致) ➢ 待测物基态原子不吸收参比线。 ➢ 参比线是测量原子的非共振线或元素灯内惰性气体元素
的谱线。
08:39:38
1
原子
光电池 光电倍增管 光敏晶体管 (2)放大器:将光电倍增管输出的较弱信号,经 电子线路进一步放大。 (3)对数变换器:光强度与吸光度之间的转换。 (4)显示、记录:新仪器配置:原子吸收计算机 工作站
《第四章第三节化学键》作业设计方案-高中化学人教版19必修第一册

《化学键》作业设计方案(第一课时)一、作业目标本作业设计旨在通过《化学键》第一课时的学习,使学生能够:1. 掌握化学键的基本概念及其分类;2. 理解离子键和共价键的形成原理及特点;3. 学会运用化学键知识分析简单物质的结构。
二、作业内容本课时的作业内容主要包括以下几个方面:1. 基础知识巩固:要求学生复习化学键的定义、分类及基本特点,并完成相关选择题和填空题,以检验学生对基础知识的掌握情况。
2. 理论应用实践:布置实验报告或小组讨论的形式,让学生分析常见物质(如水、氯化钠等)的化学键类型及结构特点,并绘制出相应的结构示意图。
3. 拓展延伸:布置一些拓展性题目,如让学生探讨化学键与物质性质的关系,分析不同类型化学键对物质物理性质的影响等。
三、作业要求为保证作业的完成质量和效果,特提出以下要求:1. 按时完成:学生需在规定时间内完成作业,并保证作业的完整性。
2. 独立思考:学生在完成作业过程中应独立思考,不抄袭他人答案。
3. 规范书写:作业书写应规范、整洁,符合化学学科的要求。
4. 实验报告或小组讨论需有明确的分工和合作,确保每位同学都参与其中。
四、作业评价本课时的作业评价将根据以下几个方面进行:1. 基础知识的掌握情况;2. 实践应用的能力;3. 拓展性题目的思考深度;4. 作业的规范性和完整性。
评价方式包括教师批改、小组互评和自我反思等多种形式,以确保全面、客观地评价学生的作业完成情况。
五、作业反馈作业反馈是本作业设计的重要环节,具体包括:1. 教师批改后,将学生的作业情况进行总结,并在课堂上进行点评,指出学生的优点和不足。
2. 对于共性问题,教师需在课堂上进行集中讲解,帮助学生解决疑惑。
3. 对于个别学生的问题,教师可通过个别辅导或课后答疑的方式,帮助学生解决作业中的困难。
4. 学生需根据教师的反馈意见,对自身的作业进行反思和总结,以便在今后的学习中不断提高。
通过以上作业设计旨在通过系统性的作业内容,让学生在掌握化学键基本概念的同时,能够运用所学知识分析实际问题,提高学生的实践能力和拓展性思维。
化学各单元知识点总结第四章复习课

毒性有毒 强还原性:
2SO2+O2
2SO3
漂白性:能使品红溶液褪色(加热后又恢复原色)
酸雨的形成途径
根据硫酸的性质,回答下列问题
(1)一瓶浓盐酸和一瓶浓硫酸长期敞口放置,质量如何变 化?浓度如何变化 ?
(2)如何鉴别浓硫酸和稀硫酸? (3)下列气体能否用浓硫酸干燥:HCl、HBr、NH3、CO、
H2、SO2? (4)把浓硫酸滴在蓝色石蕊试纸上会产生什么现象?
根据硫酸的性质,回答下列问题
(5)硫酸在下列用途或反应中各表现的性质是: A.强酸性 B.难挥发性 C.吸水性 D.脱水性 E.强氧化性 F.高沸点性
①干燥H2、SO2等气体____C____; ②用铝槽车装运浓硫酸___E_____; ③清洗镀件表面氧化物___A_____; ④浓硫酸使湿润石蕊试纸变红, 后来又变黑_A__、__D___; ⑤胆矾中加入浓硫酸,久置变为白色粉末____C____; ⑥蔗糖中加入浓硫酸,形成“黑色发糕”__D__、__E__。
液氯
新制氯水
久置氯水Biblioteka 成分Cl2 Cl2 HClO HCl
HCl
有无漂白性 无
有
无
物理性质
化学性质
颜色无色
与水反应 SO2+H2O H2SO3
状态气体
酸性氧化 与碱反应 物的性质
SO2+2NaOH===Na2SO3+H2O SO2+Ca(OH)2===CaSO3↓+H2O
与碱性氧化物 SO2+CaO===CaSO3
二氧化硅是一种酸性氧化物,能否直接与水反应 制得它所对应的酸——硅酸?如不行,该如何操作? 写出化学方程式。
SiO2+2NaOH===Na2SiO3+H2O Na2SiO3+2HCl===2NaCl+H2SiO3↓或 Na2SiO3+CO2+H2O===Na2CO3+H2SiO3↓
08天然产物化学

核磁共振波谱法
原理
利用原子核在外磁场中的自旋能级跃迁产生的共振信号来推断分子 结构的方法,主要包括氢谱、碳谱等。
应用范围
适用于各种天然产物的结构鉴定,尤其对于复杂分子的立体结构和 构象分析具有重要意义。
优缺点
能够提供详细的分子结构和构象信息,但仪器价格昂贵,操作复杂, 需要专业人员操作。
质谱法
原理
如含有红曲霉素、植物甾醇等成分的 产品。
抗氧化保健食品
如富含维生素C、维生素E、硒等成 分的产品。
其他特定功能的保健食品
如针对老年人骨质疏松的保健食品、 改善记忆力的保健食品等。
其他应用
在饮料中的应用
如天然果汁、茶饮料等,提供天 然风味和营养。
在烘焙食品中的应用
如使用天然酵母、果干等制作的 面包、蛋糕等,增加口感和营养 价值。
天然产物定义
天然产物是指动物、植物、昆虫、海洋生物和微生物体内的组成成分或其代谢产物以及人和动物体内许许多多内 源性的化学成分统称作天然产物。
天然产物分类
天然产物可分为植物类、动物类、海洋类和微生物类等。其中,植物类天然产物包括萜类、黄酮类、生物碱类等; 动物类天然产物包括蛋白质、酶、多糖等;海洋类天然产物包括海藻多糖、鱼油、珊瑚等;微生物类天然产物包 括抗生素、维生素、氨基酸等。
黄酮类化合物
定义与结构
黄酮类化合物是一类具有苯并γ吡喃酮结构的化合物,广泛存在 于植物界中。它们通常以游离态 或与糖结合成苷的形式存在。
分类
根据结构的不同,黄酮类化合物 可分为黄酮、黄酮醇、异黄酮、 查尔酮等。
生物活性
黄酮类化合物具有多种生物活性, 如抗氧化、抗肿瘤、抗心血管疾 病等。例如,槲皮素是一种黄酮 类化合物,具有显著的抗氧化和 抗炎作用。
第四章原子结构简介

18
【例如】n=3, l=0,1,2 l 可以有三个取值。也就是说,第三电子层有
三个亚层,分别是:3s、3p、3d。 同一层中(n相同),l 越大,则轨道的能量越高。
E3s E3p E3d
另外,l 不同的原子轨道,形状不一样。
08:28
19
角量子数与电子亚层、轨道形状的对应关系
角量子数 亚层符号 轨道形状
鲍林原子轨道能级图★
08:28
29
08:28
30
E4s E4p E4d E4f
08:28
31
08:28
32
从鲍林近似能级图可以看出,各轨道能级次序如下:
1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f< 5d<6p<7s<5f<6d<7p
08:28
能量相同的轨道称为简并轨道(或等价轨道), 如:3px、3py、3pz 互相称为等价轨道。
08:28
23
l=2,m=-2,-1,0,+1,+2 五个取值,说明d 轨道在空间有5个不同取向 的原子轨道:
dz2 、dxy 、dxz 、dx2 y2 、d yz
08:28
24
根据n、l、m三个量子数的取值范围,可以 确定每个电子层中原子轨道的数目。
理奖 量子概念是1900年普朗克首先提出的,到今天已经一百多年 了。期间,经过玻尔、德布罗意、玻恩、海森柏、薛定谔、 狄拉克、爱因斯坦等许多物理大师的创新努力,到20世纪30 年代,初步建立了一套完整的量子力学理论
08:28
4
§4-1 氢原子光谱和玻尔理论
基础化学第八版第四章(ppt)

• 一般由具有足够浓度和适当比例的共 轭酸碱对的两种物质组成。共轭酸称 为抗碱成分,共轭碱称为抗酸成分。
• 组成缓冲溶液的共轭酸碱对的两种物 质合称为缓冲系(buffer system)或缓冲 对(buffer pair)。
第一节 缓冲溶液及缓冲机制
组成示意图
共轭酸
HAc
NH4Cl H2PO4-
V (B-)
pH
pKa
lg V (HB)
第二节 缓冲溶液pH的计算
3.缓冲溶液pH计算公式的意义
pH
pKa
lg
[B- ] [HB]
① 缓冲溶液的pH主要取决于Ka。温度对Ka有影响。
共轭碱
NaAc
NH3·H2O HPO42-
抗碱成分
缓冲系
抗酸成分
第一节 缓冲溶液及缓冲机制
常见的缓冲系
缓冲系
HAc-NaAc
H2CO3-NaHCO3 H3PO4-NaH2PO4
Tris·HCl -Tris
H2C8H4O4- KHC8H4O4 NH4Cl - NH3
CH3NH3+Cl - CH3NH2 NaH2PO4- Na2HPO4 Na2HPO4- Na3PO4
质子转移平衡
HAc+H2O
H2CO3+ H2O
H3PO4+H2O Tris·H++H2O
H2C8H4O4+H2O NH4++H2O
CH3NH3++H2O H2PO4-+H2O HPO42-+H2O
Ac-+H3O+ HCO3-+H3O+ H2PO4-+H3O+
高中化学新人教版选择性必修1 第4章 第1节 第2课时 化学电源 课件(69张)
课前 ·新知导学
课堂 ·素养初培
辨析 ·易错易混
小练 ·素养达成
课后提能训练
化学 选择性必修1 新人教版
第四章 化学反应与电能
正误判断。(对的打“√”,错的打“×”)
(1)碱性锌锰电池、铅酸蓄电池、锂离子电池都属于二次电池。
()
(2)二次电池充电时,化学能转化为电能。
()
(3)二次电池充电时发生的反应不能自发进行。
课前 ·新知导学
课堂 ·素养初培
辨析 ·易错易混
小练 ·素养达成
课后提能训练
化学 选择性必修1 新人教版
(2)二次电池(以铅酸蓄电池为例)。 ①构造:
第四章 化学反应与电能
课前 ·新知导学
课堂 ·素养初培
辨析 ·易错易混
小练 ·素养达成
课后提能训练
化学 选择性必修1 新人教版
第四章 化学反应与电能
课前 ·新知导学
课堂 ·素养初培
辨析 ·易错易混
小练 ·素养达成
课后提能训练
化学 选择性必修1 新人教版
第四章 化学反应与电能
(2)给出总反应式,写电极反应式。 如果给定的是总反应式,可分析此反应中的氧化反应或还原反应 (即分析有关元素的化合价变化情况),先写出反应相对较简单的一极的 电极反应式,另一极的电极反应式可用总反应式减去已写出的电极反应 式,即得结果。
课前 ·新知导学
课堂 ·素养初培
辨析 ·易错易混
小练 ·素养达成
课后提能训练
化学 选择性必修1 新人教版
第四章 化学反应与电能
学法指导
1.实物感知——查找生活中见到的化学电源,认识其结构和实际应 用,增强生活离不开化学电源的认识 2.以氧化还原反应知识为基础,运用双线桥法,深刻认识重要化学 电源的工作原理
生物化学试题 08 (4)
8.具有催化活性的核算称为。
9.三羧酸循环的限速酶是。
10.原核细胞蛋白质合成中第一个被掺入的氨基酸是。
11.乙酰CoA进一步氧化需要生物素和作辅助因子。
12.E.coli参与错配修复的是DNA聚合酶。
13.tRNA基因启动子最重要的特征是。
14.真核生物中,负责合成5SrRNA是RNA聚合酶。
中山大学2003年研究生入学考试生物化学试题
一、填空题
1.糖肽的两种主要连接键为和。
2.淀粉与碘反应呈紫蓝色,而糖原遇碘呈色。
3.蛋白质二级结构主要有和两类。
4.蛋白质分子是由氨基酸通过肽键连接成多肽链,而DNA分子由核苷酸通过键连接成多核苷酸。
5.氨基酸的共有代谢途径有和。
6.假设tRNA上的反密码子是GGC,它可识别的密码子为GCC和。
5.尿素是蛋白质的变性剂,高浓度尿素可拆开蛋白质分子中的二硫键。
4.对于提纯的DNA样品,测得OD260/OD280<1.8则表明样品中由RNA残留。
7.由于酶反应的速度较快,因而酶反应的温度系数高于一般化学反应的温度系数。
5.一般的PCR反应不能扩增单链DNA。
9.目前发现的修饰核苷酸大多存在于tRNA分子中。
15.分子伴侣通常具有酶活性。
16.真核mRNA上的加尾信号序列是。
17.能互补和杂交于某一些基因产物,并能抑制其功能的RNA分子称。
二、判断正误题。Βιβλιοθήκη 1.糖链的合成无模板,糖基顺序由基因编码的转移酶决定。
2.自然界常见的不饱和脂肪酸多具有反式结构。
3.同工酶各自对同一底物的米氏常数相同或相似。
3.汤圆合成的关键酶是磷酸化酶。
高中化学第四章非金属及其化合物4.4.1氨名师制作优质课件新人教版必修
市消防中心接到报案后立即制定方案,出动上百 名消防队员,十余量消防车……
通过今天的学习,我们要解决以下几 个问题:
1、为什么在液氨泄漏时附近会寒气逼 人? 2、消防队员为什么用水吸收弥漫在空 气中的大量氨气? 3、被围困在污染区的居民怎样做才 能保证不吸入氨气?
一、物理性质
无色 有刺激性气味气体 0.771 g/L 比空气小 -33.5℃(易液化,利用液氨气化吸收
NH3+HNO3=NH4NO3 (白烟) 2NH3+H2SO4=(NH4)2SO4
与 挥 发 性 的 酸 反 应 有 白 烟
能不能用浓硫酸干燥氨气?如果不能 可以用哪种物质来干燥氨气?
从氧化还原角度分析
1、氨气中氮元素的化合价是多少? -3 2、氨气具有什么性质?
还原性
3、NH3与氧气的反应:
4NH3+5O2 △ = 4NO+6H2O
(4)收集装置:向下排空气法 (5)验满: a:湿润的红色石蕊试纸变 蓝(唯一的一种碱性气体)
b:蘸有浓HCl的玻璃棒接 近试管口产生白烟。
——重要的化工原料 三、氨的用途
制纤维、塑料、氨基酸 等(有机合成工业)
制铵盐、 制纯碱
氨
制尿素
制硝酸
用做制冷剂
学以致用
1、为什么在液氨泄漏时附近会寒气逼 人? 2、消防队员为什么用水吸收弥漫在空 气中的大量氨气? 3、被围困在污染区的居民怎样做才 能保证不吸入氨气?
催化剂
氨的催化氧化(接触氧化) 工业制硝酸的基础
红热的铂丝
NH3
O2
无色气体
余气吸收
红棕色气体
三、NH3的制法
1、NH3的工业制法
高温、高压
电荷转移复合物的研究与应用
电荷转移复合物的发展趋势
迄今为止,人们对电荷转移复合物的研究还不算很系 统和很全面,只有更加深刻的探讨电荷转移复合物的结构和形 成机制,才能运用电荷转移理论解释人们无法理解的化学难 题,比如说研究一些有机反应历程,酶反应的模型以及许多疾 病的发病机理等都是很有意义的;才能更好地将电荷转移复合 物应用于其他学科。 电荷转移复合物将来会在隐形材料,光敏型材料,电 致发光材料,医药科学等方面还有很大的发展潜力。 在今后几年中,预计会围绕电荷转移复合材料以下几 个方面会展开研究:从有机光电活性材料与无机光电材料本质 上的异同点出发,建立或发展有机光电复合材料的电荷转移能 带理论;基于结构与性能相关性的研究,通过制备新的电荷转 移复合材料,进一步优化材料性能;
电荷转移复合物的基础理论
电荷转移复合物的测定方法 (3)在X射线光电子能谱中,电荷转移复合物的形成前后构 成复合物的两个中心原子周围的电子云分布的变化,使内层电 子受到的外层电子的屏蔽作用也发生这相应的变化。因此,这 两中心原子内壳电子的结合能位移发生变化。X射线光电子能谱 法的化学位移的变化程度的大小,反映出给体与受体之间的电 荷转移程度。 (4)核磁共振谱法主要通过测定质子分裂和化学位移不 同,来测定电荷转移复合物生成。即在形成电荷转移复合物之 后由于给体分子和受体分子周围的化学环境的改变,使得复合 物的核磁共振谱图与给体,受体分子有了比较明显的差异。
电荷转移复合物的应用
电荷转移复合物在有机发光材料中的应用
电荷转移复合物的发光机理 首先我们先了解一下发光的定义,发光是物质内部不 经过热的阶段而以某种方式吸收能量,并直接转换为有选择性 的特征辐射的现象。主要包括三个过程:激发,能量运输和发 光。在处理有机电荷转移发光材料时,人们更关心处于溶液和 固态的能量传递。能量传递之间,损失能量的一方是能量给体 (D),获得能量的一方是能量受体(A)。能量传递又可分为 辐射传递和非辐射传递两类。处于激发态的给体(D*)先发射 一个光子,然后处于基态的受体(A)吸收一个光子后,被激发 到激发态,形成受体的激发态(A*)。由于辐射能量转移不需 要给体和受体之间的相互作用,所以可以实现比较远距离的能 量传递。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
当把2~<120151~0~025个50 容器作为125一00 个5>01批~001量00 时:51000~~150000
30 50
15 20
50~100
30
500~1000
25
>100
50 图4.2 车厢中的10采0样0~布5点0示00意图 30
>5000
35
填空题
1. 固体废物按化学性质可分为( )和( ); 按它的危害状况可分为( )和( )。
当车数不多于该批废物规定的份样数时:
当车数多于该批废物规定的份样数时:
每车应采份样数=规定份样数/车数
车中采样点的布设最:少容器数=最少份样数/容器
车数/辆 数批所量需大最小少采样车最数少/辆份样个数
对于一批若干容器盛装的<废10 物:/(液体m3,固体t5) /份
10~25
<5
10 5
当把容一器个个数容/个器作所需为最一少采个样批容器2量5个~数时50/个: 5~10 20 10
按化学性质:有机物和无机物;
分
类
按形状:固体和泥状;
ቤተ መጻሕፍቲ ባይዱ
方
法
按危害状况:危险废物(有害废物)和一般废物;
按来源:矿业、工业固体废物、城市垃圾 (包括下水道污泥)、农业和放射性固体废物 等。
二、危险废物的定义和鉴别
指在国家危险废
物名录中,或根据国
务院环境保护部门规
定的危险废物鉴别标
准认定的具有危险性 (1)引起或严重导致人类
危险废物的特性:以下时对钢c.能制和品水每形年成的爆腐炸蚀性深混度合大物于;d.
易燃性 腐蚀性
0.64cm的和烟废水雾物混;。e合.有产引生发毒源性或气加体热、时蒸能汽爆或
反应性 放射性 浸出毒性
震和或爆爆炸炸性;反f应.常引;温起j.根常小急据压鼠性其下(毒它易大性法爆鼠:规炸)指 定义的爆炸品在。48h内死亡半数
急性毒性
以上者。
其他毒放射性性:含有天然放射性元素的废物,比放射性大
于浸1出×1毒0-性7B:q按/kg规者定;的含浸有出人方工法放进射行性浸元取素,的当废浸物出或液比中放有
一种射或性一大种于以露上天有水害源成限分制的浓浓度度的超1过0~表140.01倍所(示半鉴衰别期标>准60的天物) 质。者。
表4.1 有色金属工业固体废物浸出毒性鉴别标准
40~50 50~100 3
15 1700
20~40 100~5002
份样20 800
10~20 <10
500~10010
25 300
1000~50.050
样品制备
30
125
>5000 图 4.1 采样3示5意图
(五) 采样方法 1.现场采样
采样间隔≤
批量/ t 规定的份样数
2.运输车及容器采样
序号 1 2 3 4 5 6 7 8 9 10
项目 汞及其无机化合物
镉及其化合物 砷及其无机化合物
六价铬化合物 铅及其无机化合物
铜及其化合物 锌及其化合物 镍及其化合物 铍及其化合物
氟化物
浸出液的最高允许浓度/ (mg·L-1) 0.05(按Hg计) 0.3(按Cd计) 1.5(按As) 1.5(按Cr6+计) 3.0(按Pb) 50(按Cu) 50(按Zn) 25(按Ni) 0.1(按Be计) 50(按F计)
的废物。
和动植物死亡率增加;
(2)引起各种疾病的增加;
危险废物
(3)降低对疾病的抵抗力; (4)在处理、贮存、运送、
处置或其他管理不当时,对人
体健康或环境会造成现实的或
潜在的危害。
易燃腐性蚀:性含:含闪水点废低物于,6或0℃本身不含水
的变液化但 pH体具加≥,有入12经着定.5摩火量的发擦倾水废生或向后物剧反吸的其,烈应湿固浸或变性和体出最化:自。液低;a.发的无温b.的p爆和度H震水为≤时剧525或就烈℃很反易应;
一、样品的采集
第二节 固体废物样品的采集和制备 ((((一二三四))))采采份份样 样 样 样工 数 量具最150>0大0~1~15粒10050应粒随填度0/(采度即写/液m批份份确采采am体.样量5<样定集样根~m5最大1;份份记据30份,小固样样录b固样153份.体采内5量,。体0根量样t样衬);组废据和量铲塑尖成c物固最份采批 份./、 料头k根总批体少样量样样g具的钢1据样量废份5/铲0份采盖采锹采,大物样容样采样、样17并小的数量60铲样袋钢方00认确最00容桶。尖法0真定大量或镐,份/、样mL
第四章 固体废物监测
第一节 固体废物概述 第二节 固体废物样品的采集和制备 第三节 有害特性的监测方法 第四节 生活垃圾和卫生保健机构废弃物的监测 第五节 有害物质的毒理学研究方法
第一节 固体废物概述
一、固体废物的定义和分类
固体废物:生产、建设、日常生活和其他 活动中产生的污染环境的固态、半固态废弃物 质。
填空题
1. 测定样品水分时,对于无机物:称取样品20g左右于 2. ()℃下干燥,恒重至±0.1g,测定水分含量;对
于有 3. 机物:样品于( )℃下干燥24h,测定水分含量。 4. 2. 测定样品腐蚀性时,对粉、粒、块状物料,称取
制备 5. 好的样品( )置于1 L塑料瓶中,加入新鲜蒸馏水
250 6. mL,使固液比为( )。 7. 3. 生活垃圾主要包括:生活垃圾、()、()、()
2. 危险固体废物特性主要包括( )、()、 ()、()、()、()。
3. 易燃性指闪点低于( )的液体。
4. 固体废物的腐蚀性是指含水废物,或本身 不含水但加入定量水后浸出液的pH≤()或 pH≥()的废物。
5. 含有天然放射性元素的废物,比放射性活 度大于()者称为放射性废物。
单项选择题
1.对环境影响最大的固体废物是()。 A. 城市垃圾 B. 工业废物 C.建筑垃圾 D. 有害固体废物 2.下列物质的特性中,不属于危险性废物特性的是()。 A.易燃性 B.腐蚀性 C.反应性 D. 可生物降解性 3.下列固体废物中,按照来源进行分类的有()。 A. 有机废物 B. 工业废物 C.有害废物 D. 危险废物 B. 4.下列是固体废物加入定量水后浸出液的pH值,具有
