正交实验法优选注射用单磷酸阿糖腺苷的配伍条件
注射用单磷酸阿糖腺苷使用说明书精编版

……………………………………………………………医药资料推荐…………………………………………………注射用单磷酸阿糖腺苷使用说明书【药品名称】通用名称:注射用单磷酸阿糖腺苷英文名称:Vidarabine Monophosphate for Injection【成份】单磷酸阿糖腺苷【性状】本品为白色或类白色的冷冻干燥灭菌粉末。
【适应症】用于治疗疱疹病毒感染所致的口炎、皮炎、脑炎及巨细胞病毒感染。
【规格】100mg【用法与用量】临用前,每瓶加2ml灭菌生理盐水溶解后肌内注射或缓慢静脉注射,或遵医嘱。
成人按体重一次5~10mg/kg,儿童按体重一次5mg/kg,一日一次。
用药过程中密切注意不良反应的发生并及时处理。
【不良反应】可见注射部位疼痛。
极少情况下,有出现神经肌肉疼痛及关节疼痛,偶有见血小板减少、白细胞减少或骨髓巨细胞增多现象,停药后可自行恢复,为可逆性,必要时可对症治疗。
不良反应程度与给药量和疗程成正相关。
【注意事项】如注射部位疼痛,必要时可加盐酸利多卡因注射液解除疼痛症状。
【孕妇及哺乳期妇女用药】孕妇慎用。
【药物相互作用】不可与含钙的输液配伍。
不宜与血液、血浆及蛋白质输液剂配伍。
别嘌呤醇可加重本品对神经系统的毒性,不宜与别嘌呤醇并用。
与干扰素同用,可加重不良反应。
【药物过量】一般剂量低于每日每kg体重10mg用量时,所产生的副作用轻微或不明显。
当超过每日每kg体重10mg用量时,可见食欲不振、头晕、耳鸣、全身乏力、恶心等,上述反映与治疗本身的因果关系尚未确定。
【药理毒理】本品为抗脱氧核糖核酸(DNA)病毒药,其药理作用是与病毒的脱氧核糖核酸聚合酶结合,使其活性降低而抑制DNA合成。
单磷酸阿糖腺苷进入细胞后,经过磷酸化生成阿糖腺苷二磷酸(Ara-ADP)和阿糖腺苷三磷酸(Ara-ATP)。
抗病毒活性主要由阿糖腺苷三磷酸(Ara-ATP)所引起,Ara-ATP与脱氧腺苷三磷酸(dATP)竞争地结合到病毒DNAP上,从而抑制了酶的活性及病毒DNA的合成,同时抑制病毒核苷酸还原酶的活性而抑制病毒DNA的合成,还能抑制病毒DNA末端脱氧核苷酰转移酶的活性,使Ara-A渗入到病毒的DNA中并连接在DNA链3′-OH位置的末端,抑制了病毒DNA的继续合成。
单磷酸阿糖腺苷

单磷酸阿糖腺苷Danlinsuan Atangxian’ganVidarabine MonophosphateC10H14N5O7P·H2O 365.26 本品为9-(β-D-阿拉伯呋喃糖)-腺膘呤5'-单磷酸酯。
按无水、无溶剂物计算,含C10H14N5O7P 应为98.0%~102.0%。
【性状】本品为白色或类白色针状结晶或结晶性粉末;无臭,味微酸。
本品在水中极微溶解,在甲醇、乙醇、乙醚中几乎不溶。
比旋度取本品约0.25g,精密称定,加水适量与0.5mol/L氢氧化钠溶液数滴,使溶解,并用0.5mol/L氢氧化钠溶液调节pH值至7.0,定量转移至25ml量瓶中,用水稀释至刻度,摇匀,依法测定(中国药典2015年版四部通则0621),比旋度为+14°至+18°。
【鉴别】(1)取本品约20mg,加6mol/L盐酸溶液2ml溶解后,加间苯三酚10mg,振摇,置水浴中加热,呈紫红色。
(2)取本品,加0.01mol/L盐酸溶液溶解并稀释制成每1ml中约含10μg的溶液,照紫外-可见分光光度法(中国药典2015年版四部通则0401)测定,在258nm的波长处有最大吸收,在230nm的波长处有最小吸收。
(3)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(4)取本品约0.1g,加无水碳酸钠1g,混匀,灼烧灰化,冷却后加水10ml振摇使溶解,滤过,滤液显磷酸盐的鉴别反应(中国药典2015年版四部通则0301)。
【检查】酸度取本品0.20g,加水20ml使溶解,取上层饱和溶液,依法测定(中国药典2015年版四部通则0631),pH值应为2.5~3.5。
碱性溶液的澄清度与颜色取本品0.50g,加1mol/L氢氧化钠溶液10ml溶解后,依法检查(中国药典2015年版四部通则0901第一法和0902第一法),溶液应澄清无色;如显色,与黄色或黄绿色3号标准比色液比较,不得更深。
注射用单磷酸阿糖腺苷说明书

【用法用量】临用前,每瓶加2ml灭菌生理盐水溶解后肌肉注射,缓慢静脉注射或遵医嘱。成人按体重一次5~10mg/kg,一日一次。用药过程中密切注意不良反应的发生并及时处理。
【不良反应】可见注射部位疼痛。极少情况下,有出现神经肌肉疼痛及关节疼痛,偶见血小板减少或骨髓巨细胞增多现象,停药后可自行恢复,为可逆性,必要时可对症治疗。不良反应程序与给药量和疗程成正相关。
【成份】本品主要成份为单磷酸阿糖腺苷,其化学名称为:9-(β-D-阿拉伯呋喃糖)-腺嘌呤5`-单磷酸酯-水合物。
其结构式为:
分子式:C10H14N5O7P·H2O
分子量:365.26
辅料:甘露醇、氢氧化钠。
【性状】本品为白色或类白色的疏松块状物或粉末。有引湿性。
【适应症】用于治疗疱疹病毒感染所致的口炎、皮炎、脑炎及巨细胞病毒感染。
【禁忌】未进行该项实验且无可靠参考文献。
【注意事项】如注射部位疼痛,必要时可加盐酸利多卡因注射液解除疼痛症状。
【孕妇及哺乳期妇女用药】孕妇慎用。
【儿童用药】未进行该项实验且无可靠参考文献。
【老年用药】未进行该项实验且无可靠参考文献。
【药物相互作用】1.不可与含钙的输液配伍。
2.不宜与血液、血浆及蛋白质输液剂配伍。
【贮藏】遮光,密封,在干燥处保存。
【包装】管制注射剂玻璃瓶;药用氯化丁基橡胶塞;0.1g×瓶/盒。
【有效期】24个月。
【执行标准】
【批准文号】
【生产企业】
企业名称:
生产地址:
邮政编码:
电话号码:
传真号码:
Байду номын сангаас
【药代动力学】本品静脉滴注或肌肉注射后可被血液和组织中腺苷脱氨酶代谢为阿糖次黄嘌呤(Ara-HX),使血药浓度很快下降。本品达到最高血药浓度的时间,肌肉注射为3小时,静脉滴注为0.5小时;半衰期为3.5小时。本品在各组织中的分布不同,在肝、肾、脾脏中浓度最高,骨骼肌、脑内浓度低,脑脊液内的浓度为血浆浓度的35~50%。约60~80%的单磷酸阿糖腺苷以阿糖次黄嘌呤(Ara-HX)的形式从尿中排泄。
2013年1月注射用单磷酸阿糖腺苷临床应用调查与分析

注射用单磷酸阿糖腺苷临床应用调查与分析2013年1月份随着医疗机构阳光用药活动的深入开展,我院发现临床较多使用单磷酸阿糖腺苷替代利巴韦林治疗病毒感染类疾病,因此结合阳光用药活动精神,本次开展对注射用单磷酸阿糖腺苷的临床用药分析。
单磷酸阿糖腺苷又名阿糖腺苷(MCDEX-2006版),为抗脱氧核糖核酸(DNA)病毒药,其药理作用是与病毒的脱氧核糖核酸聚合酶结合,使其活性降低而抑制病毒DNA的继续合成。
其适应症主要用于治疗疱疹病毒感染等所致的口炎、皮炎、脑炎及巨细胞病毒感染。
但现时该药的禁忌项目尚不明确,对于儿童用药和老年用药方面的研究资料同样处于尚不明确状态。
1. 资料与方法1.1 资料与方法:用药监测分析主要通过对开用该药的门诊处方进行点评着手。
本次抽查了我院门诊1月份处方688张,发现使用注射用单磷酸阿糖腺苷的处方63张,使用率为9.2%,其中用于10岁以下儿童的占45人,使用率高达71%。
1.2 使用分布情况表2 临床诊断情况2. 结果2.1 数据结果:以上抽查数据表明儿科和急诊对于注射用单磷酸阿糖腺苷的使用率较高,而且多用于小儿,该药大多被用于上、下呼吸道感染患者身上。
2.2 用药分析2.2.1 超说明书适应症用药:本次抽查处方中,用于上呼吸道感染的患者有30人、下呼吸道感染患者22人。
实际上,上、下呼吸道感染大多由鼻病毒、冠状病毒、流感病毒、副流感病毒、腺病毒等病毒,而这些病毒大多为RNA病毒。
从单磷酸阿糖腺苷的药用机制方面考虑,该药主要通过与病毒的脱氧核糖核酸聚合酶结合,使其活性降低而抑制病毒DNA的合成而发挥作用,对于此类RNA的病毒几乎是不起作用。
单磷酸阿糖腺苷其适应症主要用于治疗疱疹病毒感染等所致的口炎、皮炎、脑炎及巨细胞病毒感染,对于疱疹病毒作用甚强,因此用于上、下呼吸呼吸道感染病人属于超说明书范围用药。
2.2.2药品的不良反应重视程度欠佳:本次抽查数据中,用于10岁以下小儿(尤以0-5岁内小儿居多)占45人。
注射用单磷酸阿糖腺苷国家标准

注射用单磷酸阿糖腺苷Zhusheyong Danlinsuan Atangxian’ganVidarabine Monophosphate for Injection本品为单磷酸阿糖腺苷的无菌冻干品。
按平均装量计算,含单磷酸阿糖腺苷(C10H14N5O7P·H2O)应为标示量的90.0%~110.0%。
【性状】本品为白色或类白色的疏松块状物或粉末;有引湿性。
【鉴别】(1)取本品适量(约相当于单磷酸阿糖腺苷20mg),加6mol/L盐酸溶液2ml 溶解后,加间苯三酚10mg,振摇,置水浴中加热,呈紫红色。
(2)取本品,加0.01mol/L盐酸溶液溶解并稀释制成每1ml中约含单磷酸阿糖腺苷10μg 的溶液,照紫外-可见分光光度法(中国药典2015年版四部通则ⅣA)测定,在258nm的波长处有最大吸收,在230nm的波长处有最小吸收。
(3)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(4)取本品适量(约相当于单磷酸阿糖腺苷0.1g),加无水碳酸钠1g,混匀,灼烧灰化,冷却后加水10ml振摇使溶解,滤过,滤液显磷酸盐的鉴别反应(中国药典2015年版四部通则Ⅲ)。
【检查】酸碱度取本品,加水溶解并稀释制成每1ml中含单磷酸阿糖腺苷4mg的溶液,依法测定(中国药典2015年版四部通则0631),pH值应为6.5~8.0。
溶液的澄清度与颜色取本品1瓶,加水溶解并稀释制成每1ml中含单磷酸阿糖腺苷50mg的溶液,依法检查(中国药典2015年版四部通则0901第一法和0902第一法),溶液应澄清无色;如显色,与黄色或黄绿色3号标准比色液比较,不得更深。
干燥失重取本品,以五氧化二磷为干燥剂,在40℃减压干燥至恒重,减失重量不得过5.0%(中国药典2015年版四部通则0831)。
有关物质取本品,精密称定,加0.01mol/L盐酸溶液溶解并定量稀释制成每1ml中约含0.15mg的溶液,作为供试品溶液;精密量取适量,用0.01mol/L盐酸溶液稀释制成每1ml 中约含0.3μg和0.15μg的溶液,分别作为对照溶液和灵敏度溶液;另取阿糖腺苷对照品、腺嘌呤对照品适量,精密称定,加0.01mol/L盐酸溶液溶解并定量稀释制成每1ml中约含阿糖腺苷与腺嘌呤各0.75μg的溶液,作为对照品溶液。
注射用单磷酸阿糖腺苷的冻干工艺研究
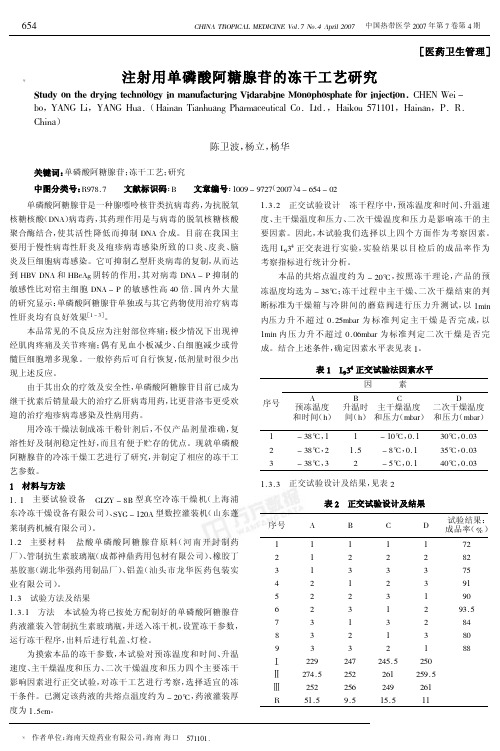
药液灌装入管制抗生素玻璃瓶, 并送入冻干机, 设置冻干参数, 运行冻干程序, 出料后进行轧盖、 灯检。 为摸索本品的冻干参数, 本试验对预冻温度和时间、 升温 速度、 主干燥温度和压力、 二次干燥温度和压力四个主要冻干 影响因素进行正交试验, 对冻干工艺进行考察, 选择适宜的冻 干条件。已测定该药液的共熔点温度约为 ( GAP , 药液灌装厚 度为 @E>98。
。因此, 在产品预冻
阶段必须保证产品冻牢, 主干燥阶段必须控制好隔板温度, 在 升华段制品温度不能超过其共熔点温度。 通过正交试验确定本品的冻干参数为预冻温度为 ( %)* 。
!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
(上接第 65% 页)
此, 有关主管部门和医院管理者应拟合国家整体和谐的科学发 展观长效管理思路, 构建以 “患者为中心” 的管理理念, 树立为 患者减轻病患、 保障健康的服务宗旨。根据当前我国医疗卫生 的发展特点, 敢下猛药, 敢触及部门利益, 以寻求各种执行操作 制度的创新, 并针对国家医院管理年的建设热点, 不断完善医 疗机构的 “生存、 服务、 发展” 的思路, 并进一步拓展生存能力, 开发稳定的医疗服务集约群体, 扶持基层医疗服务水平, 构建 和谐祥和医患关系的平安医院和平安社会, 以更好地为患者服 务, 为自身的生存和发展铺基础。 参考文献:
[.]黄勃 7 单磷酸阿糖腺苷抗乙型肝炎病毒的疗效观察 [ 8] - 四川医学, (.#) : #,,,, #. ..,# 9 ..,%[#]邰 立 慧 7 单 磷 酸 阿 糖 腺 苷 治 疗 慢 性 乙 肝 的 近 期 疗 效 观 察 [ 8] (%) : - :;<=314> ?@A3B1C 8;<241C, #,,%, %. ##,[%]周莉, 于岩岩, 王勤环 7 单磷酸阿糖腺苷联合胸腺治疗慢性乙型肝 炎疗效观察 [ 8] (.) : - 临床肝胆病杂志, #,,%, .D %5 9 %6[’]李艳萍 - 冻干技术研究进展 [ 8] - 微生 物 学 免疫 学 进 展, .DD’, ## (’) : ’) 9 5.收稿日期: #,,6 ( .# ( .’
我院注射用单磷酸阿糖腺苷用药分析

我院注射用单磷酸阿糖腺苷用药分析宋 瑞,卞光奇,陈晓东(泗县人民医院药剂科,安徽泗县234300)摘要:目的 调查我院2016年2月份出院患者注射用单磷酸阿糖腺苷的使用情况,促进临床合理用药。
方法 利用我院合理用药信息系统对该药的科室分布、出院诊断、患者年龄分布作统计分析。
结果 我院新生儿科患者使用最多;该药主要用于呼吸道感染疾病;临床使用较多的患者为小于3岁的儿童;本院不合理使用注射用单磷酸阿糖腺苷的最突出表现为超适应症用药。
结论 我院应针对单磷酸阿糖腺苷的临床用药加强监管,尤其要确保儿童合理、安全用药。
关键词:注射用单磷酸阿糖腺苷;用药分析;合理用药中图分类号:R969 4 文献标识码:B 文章编号:1006 3765(2021) 02 0188 02 注射用单磷酸阿糖腺苷作为一种抗脱氧核糖核酸(DNA)类病毒药物,其作用机制表现为能与病毒的DNA聚合酶结合,从而抑制合成病毒的脱氧核糖核酸。
主要适应症为治疗巨细胞病毒感染及疱疹病毒感染所致的脑炎、口炎等。
查阅相关说明书及文献资料发现,单磷酸阿糖腺苷只对疱疹病毒、巨细胞病毒和乙肝病毒有效,但其对疱疹性病毒的疗效与阿昔洛韦比较也不占优势,对于RNA病毒感染的有效性没有充分证据证明。
注射用单磷酸阿糖腺苷不良反应报告数量近年来增长趋势明显〔1〕,为规范我院药品的合理使用,降低患者用药风险,现对我院使用注射用单磷酸阿糖腺苷住院患者病历进行统计、分析与评价,并将结果进行汇总。
1 资料与方法1 1 资料来源 利用我院合理用药软件系统抽取2016年2月份所有使用注射用单磷酸阿糖腺苷的患者的出院归档病历,合计60份。
1 2 方法 通过对每份使用注射用单磷酸阿糖腺苷病历的住院号、使用科室、姓名、年龄、诊断、单次剂量和频次逐项进行登记,根据药品说明书及相关文献资料,点评注射用单磷酸阿糖腺苷的用药合理性。
2 结果2 1 使用科室情况 经统计,我院单磷酸阿糖腺苷用药情况,新生儿科患者应用最多(见表1)。
注射用单磷酸阿糖腺苷无菌检查方法适用性研究

注射用单磷酸阿糖腺苷无菌检查方法适用性研究佘凡;王自义;高翔;李秋菲【摘要】目的建立注射用单磷酸阿糖腺苷无菌检查方法标准.方法按照2015年版《中国药典》规定,采用薄膜过滤法,对14家企业生产的注射用单磷酸阿糖腺苷进行无菌方法适用性研究.结果确定了规格为0.1g注射用单磷酸阿糖腺苷的无菌检查方法.14家企业(共111批次)无菌检验方法均为:取样品60支,采用薄膜过滤法,用pH 7.0氯化钠-蛋白胨缓冲液冲洗,每次100 mL,共冲洗2次.结论通过对14家企业生产的注射用单磷酸阿糖腺苷的方法验证资料进行整理、归纳、分析、试验,最终确定严谨统一的无菌检查方法.%Objective To set up the standards for the sterility test of adenine arabinoside monophosphate for injection.Methods According to Chinese pharmacopoeia (2015),the sterility tests on adenine arabinoside monophosphate for injection from 14 producers were performed by membrane-filtration procedure.Results The sterility test on 0.1 g adenine arabinoside monophosphate for injection was confirmed.The sterility tests of all 14 producers (111 batches) were carried out as follows:60 samples were filtered by membranefiltration procedure,and washed twice by pH 7.0 sodium chloride peptone buffer,100 mL each time.Conclusions A strict and unified sterility test has been confirmedby reorganizing,concluding,analyzing and testing of the data on the adenine arabinoside monophosphate for injection from the 14 producers.【期刊名称】《安徽医药》【年(卷),期】2017(021)012【总页数】5页(P2164-2168)【关键词】注射用单磷酸阿糖腺苷;无菌检查法;方法适用性【作者】佘凡;王自义;高翔;李秋菲【作者单位】杨凌示范区药品检验监测评价中心,陕西杨凌712100;陕西省医疗器械质量监督研究院,陕西西安712046;陕西省食品药品监督检验研究院,陕西西安710065;陕西省食品药品监督检验研究院,陕西西安710065【正文语种】中文注射用单磷酸阿糖腺苷常用于治疗疱疹病毒感染所致的口炎、皮炎、脑炎,也用于治疗免疫抑制患者的带状疱疹和水痘感染,但对巨细胞病毒无效。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
·1221·
样品溶液按中国药典 2010 年版二部微粒检测法中 的光阻法进行不溶性微粒测定 , 每个样品重复测 定5次取平均值。 2.6 样 品 溶 液 pH 稳 定 性 测 定 按照中国药典 2010年版(一部)附录VII G pH测定法检查“2.3”项
中国现代应用药学 2015 年 10 月第 32 卷第 10 期
2.8 2.8.1
。
有关注射用单磷酸阿糖腺苷与溶媒配伍后稳 定性研究目前主要集中于温度、放置时间对稳定 性的影响
[3-4]
,而忽视了溶媒种类、溶媒体积、光
照条件对稳定性的影响。此外,当多因素共同作 用时,其稳定性是否会产生新的变化,也未见相 关报道。本实验采用正交试验,选择温度、光照、 放置时间、溶媒、溶媒用量 5 个影响因素,以单
ABSTRACT: OBJECTIVE To investigate multiple factors on the compatibility stability of Vidarabine Monophosphate for Injection mixed with different solvents. METHODS L18(35) of orthogonal design was used with five factors: temperature, illumination, storage time, solvent and amount of solvent. With the content of vidarabine monophosphate, pH value changes of the compatibility solution and the insoluble particles as indexes, the content of vidarabine monophosphate in the mixture was determined by HPLC, the change of pH value before and after compatibility determined by pHs-2C type precision acidity meter, the insoluble particles were observed by GWJ-4 type particle analyzer. RESULTS There were no significant changes in appearance and character of the mixture in the inspection time. The temperature and time showed significant effects on the contents of vidarabine monophosphate in the mixture, and illumination could influence the number of insoluble particles. The solvent and amount of solvent had no significant influence on all indexes. CONCLUSION The optimal compatibility conditions as follows: temperature of 25 ℃, under the incandescent lights, compatibility time of 4 h, and 100 mL 0.9% sodium chloride injections as the solvent. KEY WORDS: Vidarabine Monophosphate for Injection; compatibility conditions; compatible stability
作者简介: 王会品,女,主管药师
·1220·
Tel: 13938222761
E-mail: 147689768@
Chin J Mod Appl Pharm, 2015 October, Vol.32 No.10
中国现代应用药学 2015 年 10 月第 32 卷第 10 期
定研究院,批号:140710-200401,纯度:98%); 注射用单磷酸阿糖腺苷 ( 广东先强药业,批号: 140806/1,规格:0.1 g);5%葡萄糖注射液(国内某 厂家,规格:100,250,500 mL);10%葡萄糖注 射液(国内某厂家, 规格: 100, 250, 500 mL); 0.9% 氯化钠注射液(国内某厂家,规格:100,250,500 mL)。试剂均为分析纯,水为超纯水。 2 2.1 方法与结果 实验用水制备 取注射用水,用0.45 µm微孔滤膜过滤,弃去 初滤液,收集续滤液得实验用水。经检测符合中 国药典2010年版微粒检查用水有关规定。 2.2 试验用具准备 于层流净化台上将实验用具用实验用水冲洗 至洁净,备用。 2.3 样品溶液制备 在层流净化台上进行配制。按表1、2正交试验 设计要求,精取注射用单磷酸阿糖腺苷置量瓶中, 分别加0.9%氯化钠注射液、5%葡萄糖注射液、10% 葡萄糖注射液至刻度,摇匀,根据表2试验方案安 排试验,每号试验做3次,共制备54个样品溶液。 2.4 外观 取洁净的20 mL具塞纳氏比色管若干支,分别 加入“2.3”项下样品溶液各15 mL,用未加药的小 儿电解质补给注射液作对照,在正交实验表中的 各时间点分别检查外观变化。结果表明,配伍液 的外观、性状在各考察时间均无明显变化,各配 伍液外观均澄清透明,无颜色、气体、沉淀、浑 浊产生,与未加药的小儿电解质补给注射液相比 也无差异。 2.5 不溶性微粒 取各配伍液按中国药典 2010 年版二部微粒检 测法中的光阻法,用GWJ-4 型智能微粒检测仪检 查微粒。 2.5.1 空白试验 取试验用注射用单磷酸阿糖腺 苷和不同溶媒各3份,测定其不溶性微粒,取平均 值。结果表明本次试验所用药液均符合规定。 2.5.2 样品溶液微粒测定 取“2.3”项毒药, 其药理作用是与病毒的脱氧核糖核酸聚合酶结 合,使其活性降低而抑制 DNA 合成。单磷酸阿糖 腺苷为广谱的抗病毒药,临床主要用于治疗慢性 乙型肝炎和其他病毒性感染如带状疱疹、单纯疱 疹、生殖器疱疹等,此外在手足口病及儿童水痘 方面也有一定的疗效
[1-2]
磷酸阿糖腺苷含量、 配伍液的 pH 值变化及不溶性 微粒数为检测指标,优选合理的配伍条件,为临 床安全、合理用药提供理论依据。 1 仪器与试药 LC-2010A 高效液相色谱仪,LC Solution 色 谱工作站(日本岛津公司); Agilent 8453紫外可见分 光光度计(美国Agilent公司);XS205 电子天平(瑞 士梅特勒 -托利多公司 ); pHs-2C 型精密酸度计 (上 海雷磁仪器厂);DK-8D型电热恒温水槽(上海一恒 科技有限公司); VS-840-1(2)型单人净化工作台(苏 州净化设备有限公司);狮鼎 SHB循环水式多用真 空泵 (郑州长城工贸有限公司 ); GWJ-4 型智能微 粒检测仪(天大天发科技有限公司)。 单磷酸阿糖腺苷对照品(中国药品生物制品检
Optimize the Compatibility Condition of Vidarabine Monophosphate for lnjection by Orthogonal Test WANG Huipin(Pharmacy of the Third Hospital of Zhengzhou, Zhengzhou 450004, China)
1
配制单磷酸阿糖腺苷低
(400 µg·mL )、中(500 µg·mL1)、高(600 µg·mL1) 系列浓度的对照品溶液, 重复进样 20 µL(n=9), 考 察其仪器精密度。结果低、中、高浓度的单磷酸 阿糖腺苷峰面积的 RSD 分别为:0.92%,0.51%, 0.19%。 2.7.5 稳定性试验
正交实验法优选注射用单磷酸阿糖腺苷的配伍条件
王会品(郑州市第三人民医院药剂科,郑州
摘要:目的
450004)
考察多因素对注射用单磷酸阿糖腺苷与不同溶媒配伍后稳定性的影响。方法
5
选择温度、光照、放置时间、
溶媒、溶媒用量 5 个影响因素,采用 L18(3 )正交试验表,以单磷酸阿糖腺苷含量、配伍液的 pH 值变化及不溶性微粒数 为检测指标,采用高效液相色谱法测定配伍液中单磷酸阿糖腺苷的含量,pHs-2C 型精密酸度计测定配伍前后 pH 值的变 化,GWJ-4 型智能微粒检测仪测定溶液中微粒数。结果 考察指标均无显著性影响。结论 射配伍放置 4 h。 关键词:注射用单磷酸阿糖腺苷;配伍条件;配伍稳定性 中图分类号:R978.7 文献标志码:B DOI: 10.13748/ki.issn1007-7693.2015.10.015 文章编号:1007-7693(2015)10-1220-04 配伍液的外观、性状在考察时间内均无明显变化。温度、放置 时间对配伍液中单磷酸阿糖腺苷的含量有显著性影响;光照对溶液中微粒的含量有显著性影响;溶媒及溶媒用量对所有 注射用单磷酸阿糖腺苷合理配伍条件为 25 ℃、白炽灯光照下与 100 mL 0.9%氯化钠注
[5]
下各样品溶液的pH,及其混合后0 h的pH,每个样 本连测3次,取平均值,并进行比较,计算其差值。 2.7 2.7.1 含量测定[3] 色谱条件 流动相:水(含6.8 g磷酸二氢钾
与15 mL四丁基氢氧化铵10%加至1 000 mL)-甲醇 (85∶15);柱温:室温;流速:1.0 mL·min1;进 样量:20 µL。 2.7.2 测定波长的选择 称取单磷酸阿糖腺苷对 照品适量,加流动相稀释后,在 200~400 nm 内扫 描, 结果单磷酸阿糖腺苷在 258 nm 处有最大吸收。 2.7.3 标准曲线的绘制 精密称取单磷酸阿糖腺 苷对照品100 mg于10 mL量瓶中加流动相至刻度。 分别取上述对照品溶液 0.5, 4, 5, 6, 8, 10 mL 于100 mL量瓶中加流动相至刻度,配成系列浓度 的单磷酸阿糖腺苷的对照溶液。 按“2.6.1”项下的色 谱条件分别进样测定,以峰面积A为纵坐标,浓度 C 为 横 坐 标 , 进 行 线 性 回 归 , 得 回 归 方 程 为 A= 6.79×105C325 , r=0.999 8(n=6) ,结果表明单磷 酸阿糖腺苷在 50~1 000 µg·mL1 内呈良好的线性 关系。 2.7.4 仪器精密度试验
